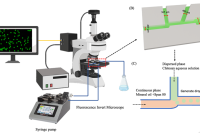
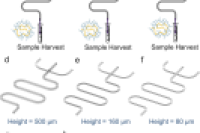
一种阶梯式T型结微流控反应器,旨在解决高粘度非牛顿流体在制备壳聚糖微球时难以精确控制粒径和均匀性的难题。
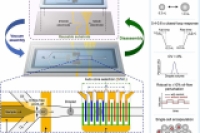
仁济大学研究人员开发了一种名为 EWOD-SAVE 的新型微流控芯片,通过结合电润湿(EWOD)技术与电容反馈控制,实现了对液滴体积的精确调节。
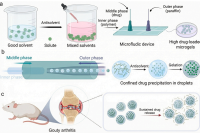
微凝胶是局部药物递送的理想载体,但疏水性药物与亲水性网络之间的兼容性较差,限制了其载药量并导致药物释放不可控。
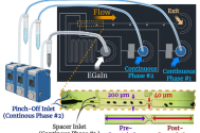
液态金属(如共晶镓铟合金 EGaIn)兼具高电导率、流动性与生物相容性,但由于表面自发的氧化膜生长和不稳定的流动行为,其应用受到了限制。
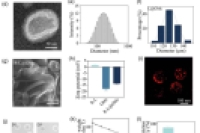
苏州大学附属第二医院骨外科陆政峰主任医师联合多单位,开发了一种负载人参皂苷Rg1与趋化因子SDF1α的脂质体锚定水凝胶微球(R-L@S-GMs),通过时空受控的药物释放来调节早期炎症微环境并招募内源性干细胞,从而显著促进了脊髓损伤后的神经再生与功能修复。
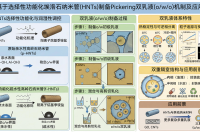
Pickering乳液以固体微/纳米粒子替代传统表面活性剂,具备制备简便、稳定性高、生物相容性好的优势。

总结了丝素蛋白的提取方法与结构特征,同时梳理了丝素蛋白纳米粒的制备、改性策略、理化性质及应用场景。
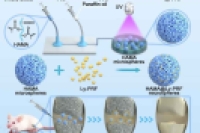
该研究受透明质酸微球仿生结构与冻干富血小板纤维蛋白中多种生长因子的启发,采用微流控技术构建了负载冻干富血小板纤维蛋白的甲基丙烯酰化透明质酸微球(HAMA@Ly-PRF 微球)。
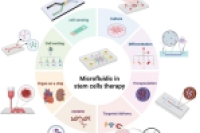
再生医学领域愈发依赖间充质干细胞(MSCs)、诱导多能干细胞(iPSCs)及工程化细胞构建体,来实现受损组织的修复与功能重建。
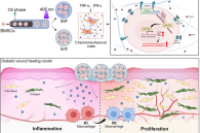
糖尿病溃疡是糖尿病的严重并发症,为非创伤性下肢截肢的首要原因,其核心治疗难点在于伤口微环境存在慢性低级别炎症、血管生成受损、上皮再生缺陷,其中巨噬细胞 M1/M2 极化失衡是炎症期紊乱的关键。
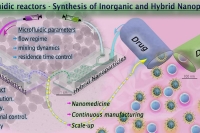
无机纳米颗粒凭借其独特的理化性质,能够实现成像、治疗与多功能药物递送,在纳米医学的发展进程中始终占据重要地位。
基因治疗通过外源性核酸调控基因表达,核酸的易降解性要求高效递送载体,脂质纳米颗粒(LNPs)和聚合物纳米颗粒(PNPs)是主流方向,其中PNPs具备化学稳定、热耐受性好、储存条件温和、可功能化修饰的优势,是LNPs的理想替代。
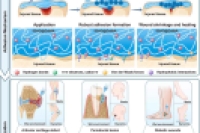
临床治疗中,牙周炎骨缺损、关节软骨损伤、糖尿病皮肤溃疡等湿组织缺损修复,一直是再生医学的棘手问题 —— 动态富液环境下生物支架黏附不稳,易被唾液、滑液、伤口渗出液冲脱,药物和细胞递送效率大打折扣,最终影响组织修复效果。
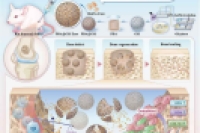
该研究开发了一种由仿生预处理骨髓间充质干细胞外泌体(BioPre-Exos)与聚多巴胺修饰的可注射多孔甲基丙烯酰化明胶(GelMA)微球(PDA@GM)组成的协同骨再生体系,旨在解决临界尺寸骨缺损修复中内源性自愈能力不足、外泌体生物活性低且递送效率差的临床难题。
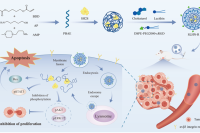
该研究构建了一种脂质杂化纳米粒(SLHN)递送系统,用于靶向输送SH2超亲体蛋白(SH2S)治疗乳腺癌,显著提升其体内稳定性、肿瘤靶向性与治疗效果。
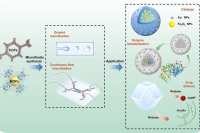
重点阐述了依托微流控技术实现MOFs/COFs精准制备与结构定制的突破性进展。
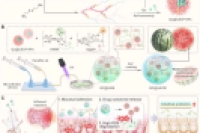
开发了一种名为QC@HACM的创新型“西瓜样”微/纳复合递药系统,旨在通过多维度干预策略实现溃疡性结肠炎(UC)的高效治疗。
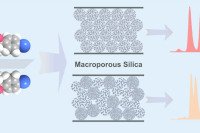
多糖功能化大孔二氧化硅微球是高效液相色谱中应用最广泛的手性固定相之一。
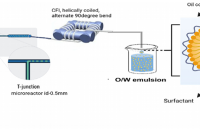
以微流控技术为核心,开发出适用于航天领域的壳聚糖包覆褪黑素载药水包油纳米乳剂,成功解决了液态药物在太空模拟环境中的稳定性难题,同时实现了药物的可控缓释,为航天制药的研发提供了全新的微流控解决方案,也为极端地面环境的药物制备拓宽了思路。
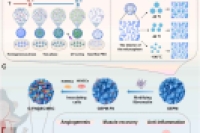
本研究开发了一种仿生分级多孔微球(GEPM-FN),该微球不仅支持高质量的细胞培养与扩增,还可作为重症肢体缺血(CLI)治疗的递送载体。