研究背景
1、临界尺寸骨缺损因内在自愈能力不足,易引发骨不连、运动功能障碍,成为临床骨科的重大难题;基于生物活性支架的组织工程策略是骨再生的重要方向,BMSC来源外泌体介导的无细胞治疗因低免疫原性、无致瘤风险成为研究热点。
2、现有研究存在两大核心瓶颈:一是传统外泌体多通过2D单层培养+单因子预处理获得,无法模拟骨髓的低氧梯度(生理氧分压1%~4%)和3D细胞–细胞/细胞–基质相互作用,外泌体成血管、成骨活性不足;二是常规水凝胶递送系统刚性高、可注射性差,无法适配不规则骨缺损,且外泌体依赖被动扩散释放,易出现突释现象,降低长期治疗效果。
3、研究切入点:构建3%低氧+3DGelMA微球的仿生预处理体系提升外泌体活性,结合PDA修饰的可注射多孔GelMA微球实现外泌体的高效负载和缓释,形成协同骨再生系统。

近期,浙江大学医学院附属邵逸夫医院徐文斌副教授、诸进晋博士等人,通过微流控技术构建了聚多巴胺改性的可注射多孔甲基丙烯酰化明胶微球,用于负载经3%低氧联合三维微球培养预处理的骨髓间充质干细胞外泌体。该复合系统在体外可显著促进干细胞迁移、成骨分化、血管形成及巨噬细胞抗炎极化,并在大鼠股骨缺损模型中实现了高效的血管化骨再生。相关研究以“Injectable Porous Microspheres Loaded With Biomimetic Preconditioned Bone Marrow Mesenchymal Stem Cell‐Derived Exosomes for Vascularized Bone Regeneration”为题目,发表于期刊《Advanced Science》。
本文要点:
1、该研究开发了一种由仿生预处理骨髓间充质干细胞外泌体(BioPre-Exos)与聚多巴胺修饰的可注射多孔甲基丙烯酰化明胶(GelMA)微球(PDA@GM)组成的协同骨再生体系,旨在解决临界尺寸骨缺损修复中内源性自愈能力不足、外泌体生物活性低且递送效率差的临床难题。
2、研究以3%低氧结合3D GelMA微球培养构建仿生骨髓微环境,预处理骨髓间充质干细胞(BMSCs)以获得生物活性显著提升的BioPre-Exos;同时通过微流控技术制备PDA@GM微球,其兼具可注射性、良好的生物相容性,还能实现外泌体的高效负载与持续控释,避免传统递送系统的突释问题。
3、体外实验证实,该复合体系(PDA@GM-BioPre-Exos)能显著促进BMSCs迁移与成骨分化、增强人脐静脉内皮细胞血管生成能力,并诱导巨噬细胞向抗炎M2型极化,营造利于骨再生的微环境;体内大鼠股骨髁缺损模型实验表明,该体系可大幅提高缺损区新生血管密度和骨体积分数,显著改善新生骨的结构与力学性能,实现高效的血管化骨再生。
4、研究还验证了PDA@GM微球无细胞毒性和全身组织损伤,具备优异的体内外生物相容性。不过该研究仍存在局限性,仅在啮齿动物模型中验证了效果,后续需在大动物模型中进一步验证,并解析外泌体发挥作用的具体组分与分子机制,为其临床转化奠定基础。
5、该无细胞仿生协同递送体系为临界尺寸骨缺损的临床治疗提供了新策略,也为再生医学领域先进生物材料的设计提供了新思路。
该研究构建的PDA@GM-BioPre-Exos复合系统的核心创新点体现在哪些方面?
一是外泌体预处理的仿生创新,首次采用3%低氧(匹配骨髓1%~4%生理氧分压)结合3DGelMA微球培养的双因素仿生策略,模拟骨髓微环境,显著提升BMSC外泌体的成骨、成血管和免疫调节活性,克服了传统2D培养+单因子预处理的局限性;
二是递送系统的性能创新,通过PDA修饰可注射多孔GelMA微球,实现外泌体的高吸附效率和14天持续缓释,解决了常规递送系统外泌体突释、清除快的问题,且微球多孔、可注射,适配不规则骨缺损的微创治疗;
三是治疗策略的协同创新,构建了无细胞仿生协同递送系统,将微球的物理支架支撑(细胞浸润、营养交换)与外泌体的生物活性调控(成骨、成血管、抗炎)相结合,实现了骨再生的多维度协同调控,突破了单一成分治疗的效能瓶颈。
该骨再生系统走向临床应用还需要解决哪些关键问题?
一是动物模型的临床转化验证,需在羊、猪等大动物模型中构建更贴近临床的骨缺损模型(如长段骨干皮质骨缺损、骨质疏松性骨缺损、感染性骨缺损),评估系统的修复效果、长期生物安全性和体内降解规律,验证其在大尺寸、复杂病理条件下的骨再生效能;
二是分子机制的精准解析,需明确BioPre-Exos中介导成骨、成血管和免疫调节的具体功能成分(如特异性miRNA、蛋白、脂质)及下游信号通路,为外泌体的定向改造和效能提升提供分子靶点,实现系统的精准优化;
三是制备工艺的临床应用优化,需优化GelMA微球的微流控制备工艺,实现规模化、标准化生产,同时调控PDA@GM的降解速率、外泌体的负载量和缓释速率,适配人体不同部位骨缺损的再生需求,此外还需开展临床试验前的药代动力学、毒理学研究,满足临床应用的质量控制要求。
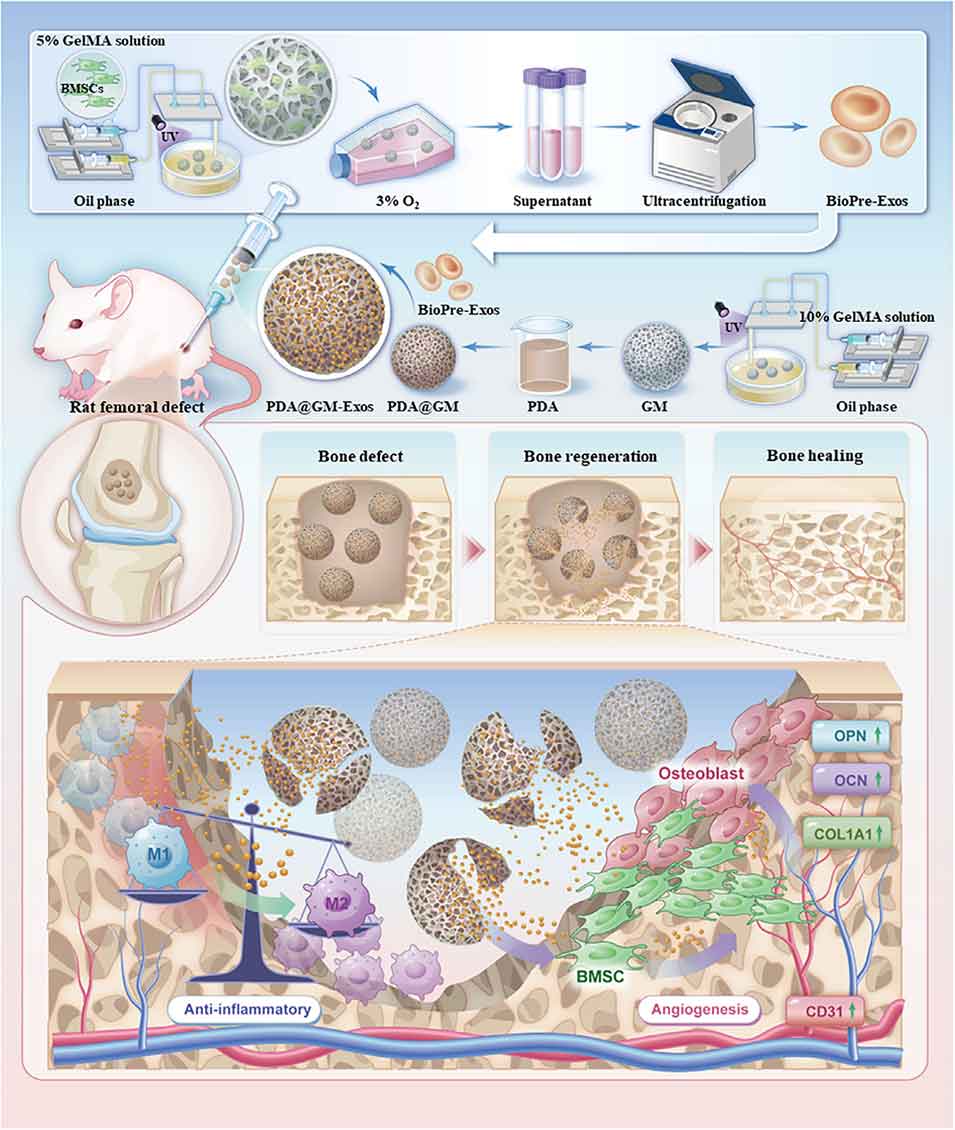
图1. 负载仿生预处理外泌体的可注射聚多巴胺修饰GelMA微球用于血管化骨再生的示意图
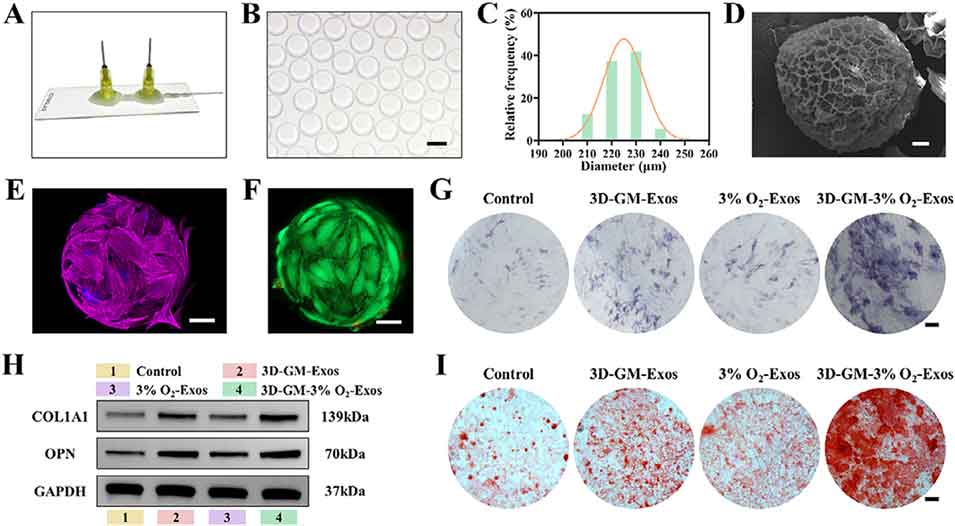
图2. 5% GelMA微球的制备、表征及细胞实验结果。
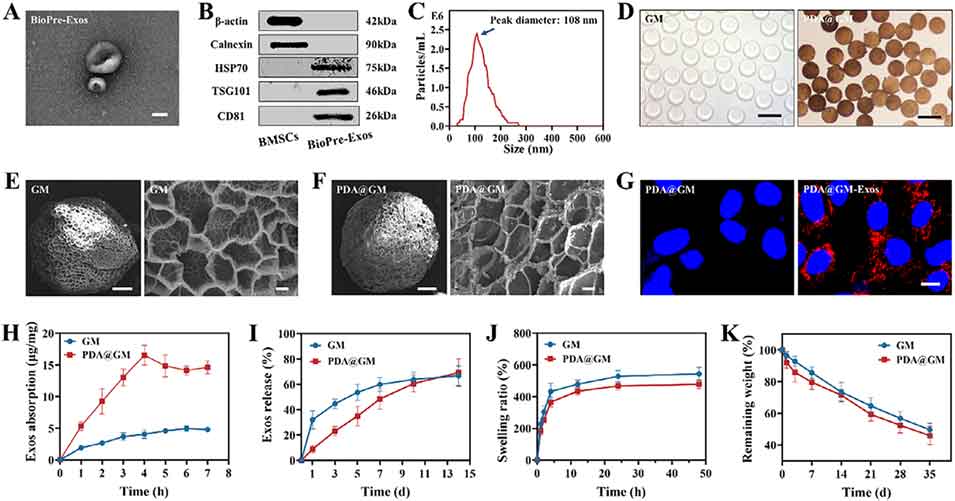
图3. 仿生预处理外泌体的鉴定及PDA@GM复合体系的性能表征。
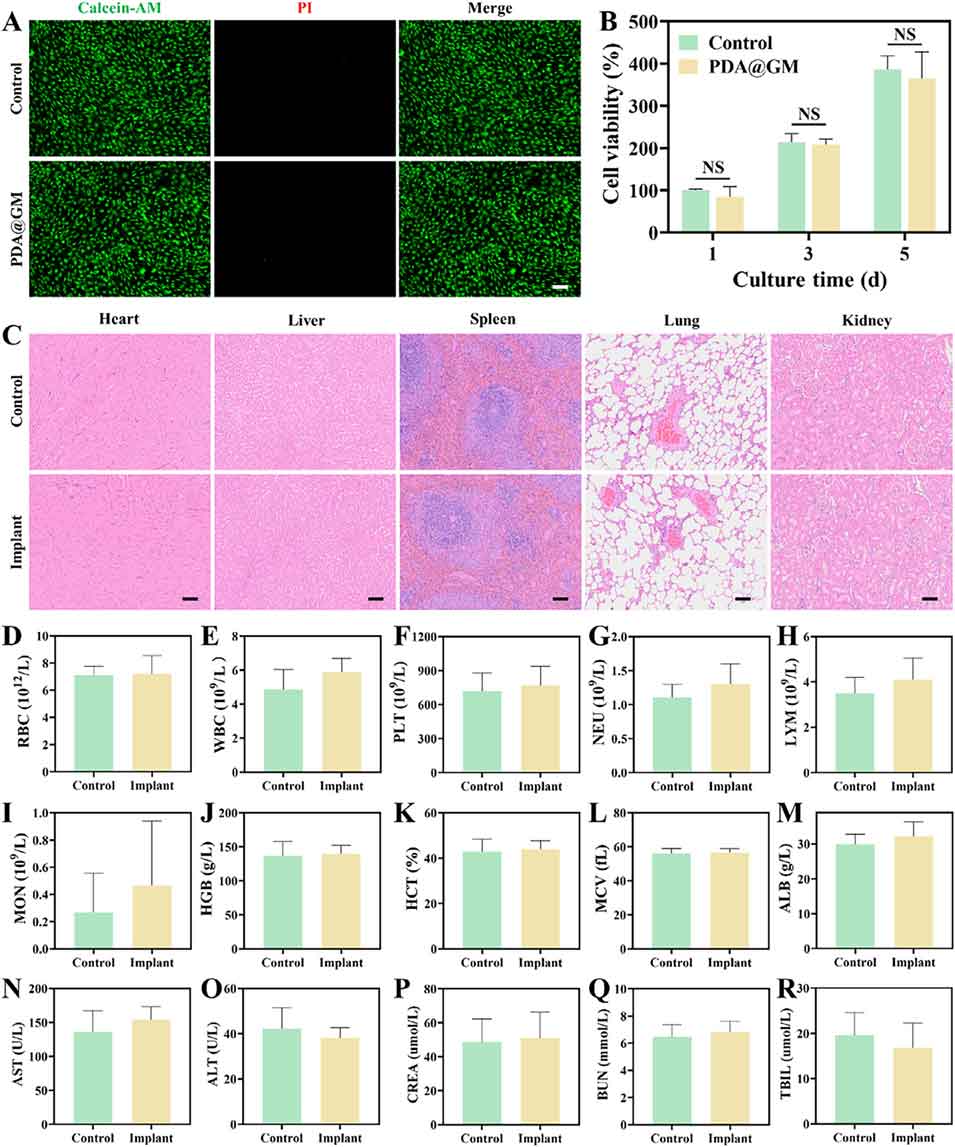
图4. PDA@GM微球的体内外生物相容性评价。
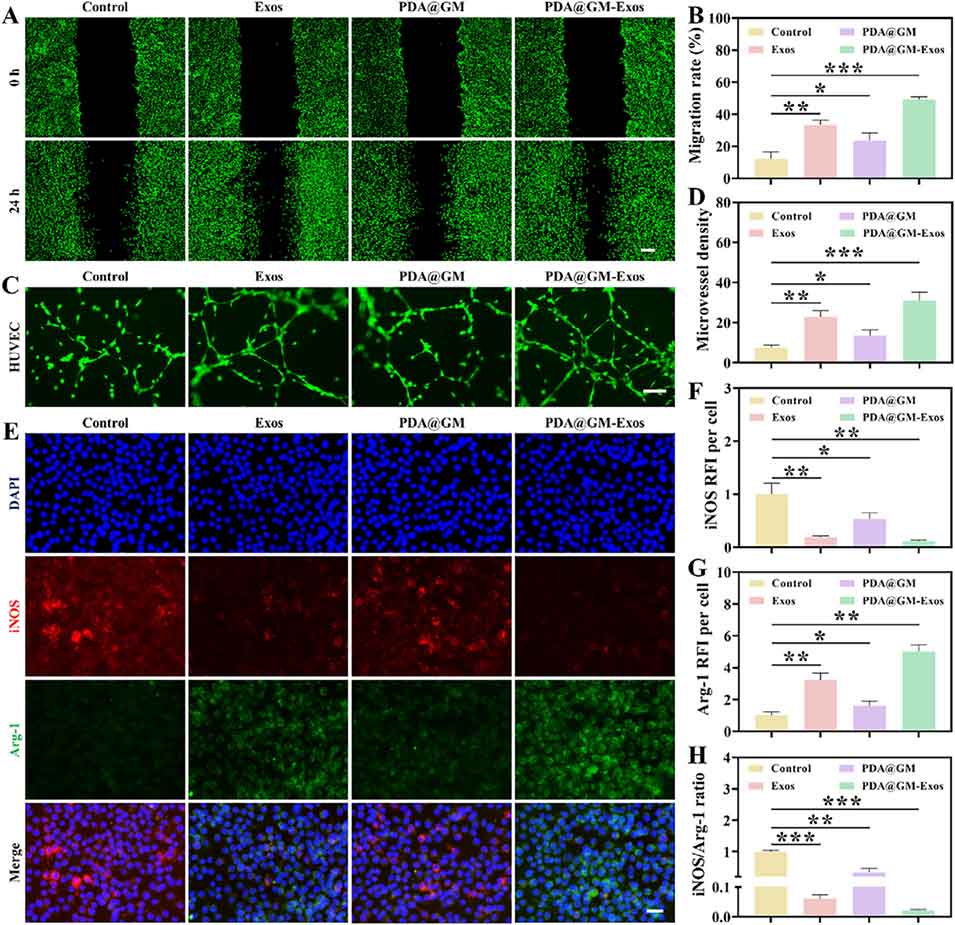
图5. PDA@GM-仿生预处理外泌体复合体系的体外多功能作用效果。
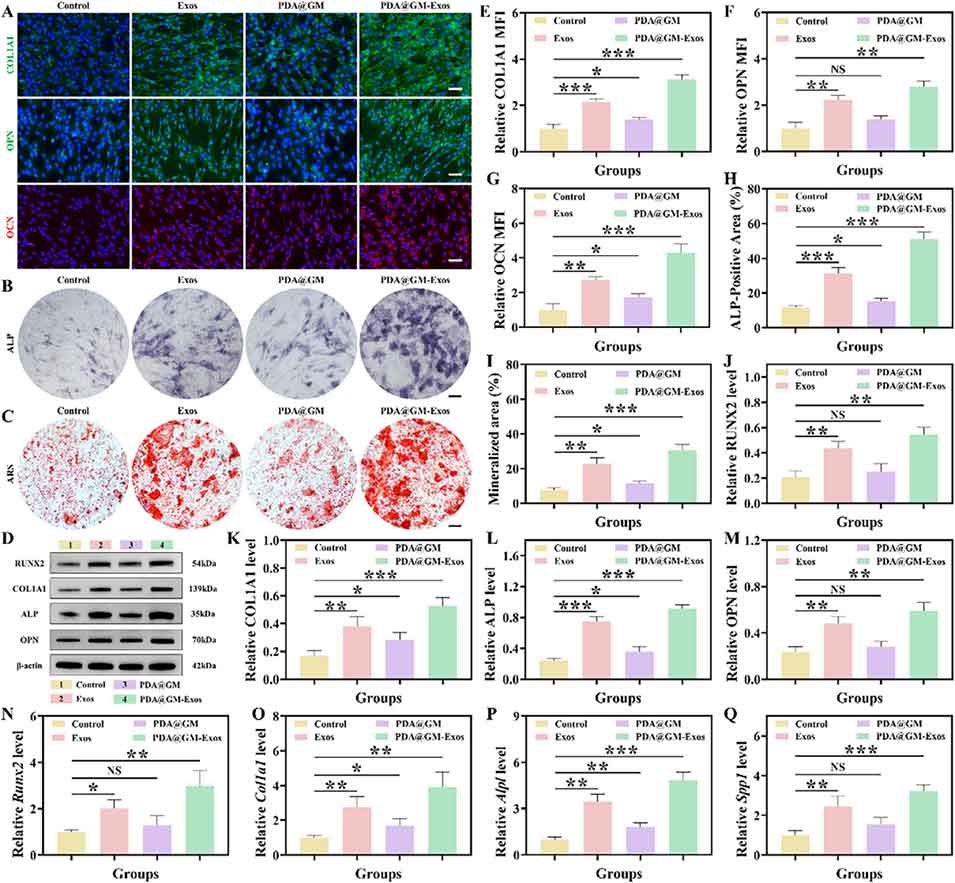
图6. PDA@GM-仿生预处理外泌体复合体系调控骨髓间充质干细胞的体外成骨分化结果。
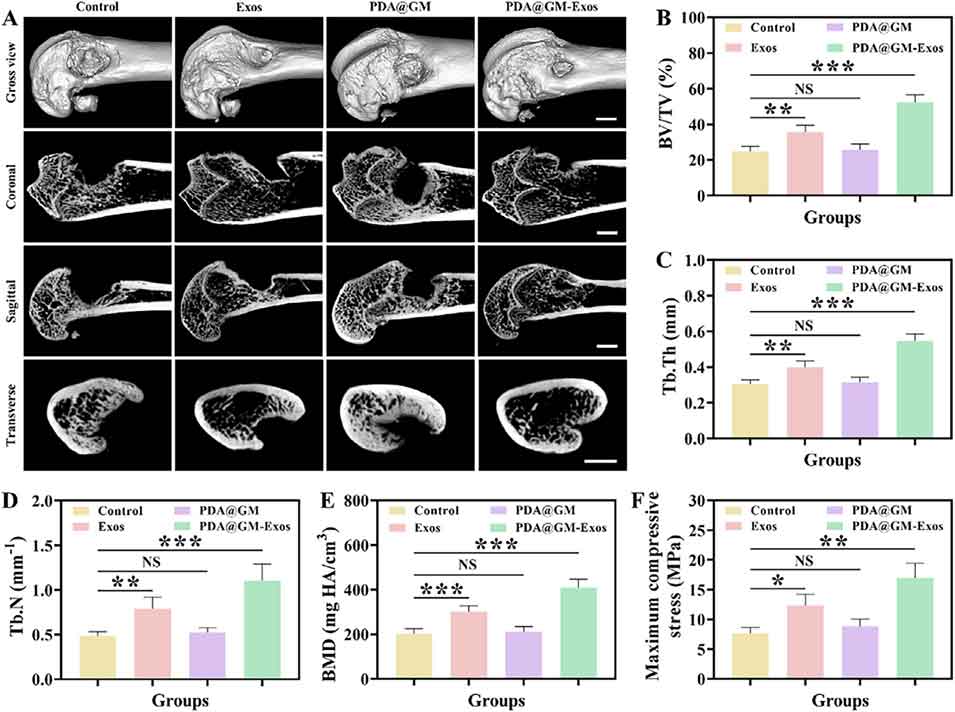
图7. 利用显微计算机断层扫描和生物力学检测对骨缺损修复效果的体内评价。
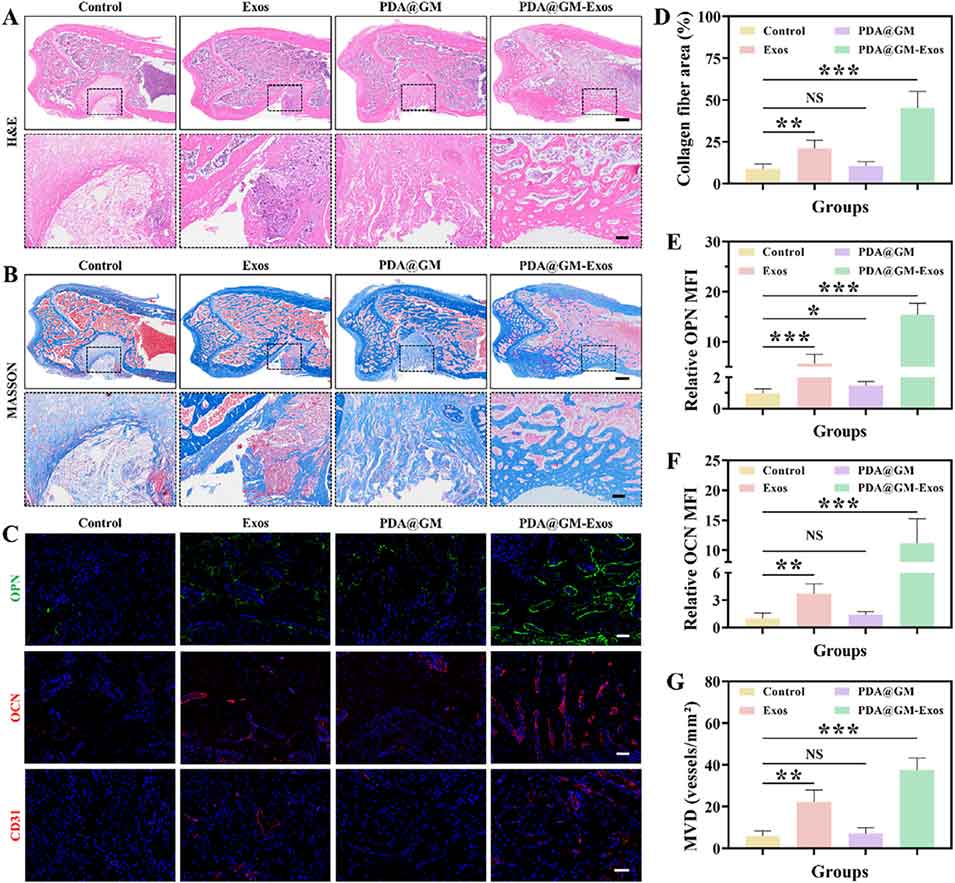
图8. 骨缺损修复的组织学及免疫荧光分析结果。
论文链接:https://doi.org/10.1002/advs.74987
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














