临床治疗中,牙周炎骨缺损、关节软骨损伤、糖尿病皮肤溃疡等湿组织缺损修复,一直是再生医学的棘手问题 —— 动态富液环境下生物支架黏附不稳,易被唾液、滑液、伤口渗出液冲脱,药物和细胞递送效率大打折扣,最终影响组织修复效果。

近日,重庆医科大学附属口腔医院张曦木教授团队受大鲵皮肤分泌物(SSAD)天然湿黏附机制启发,设计出SSAD@GelMA微球(SGM)这一新型多功能仿生水凝胶微球,解决了动态富液环境中生物支架与组织黏附不稳定、治疗递送效率低的临床难题,为湿组织修复提供了兼具强湿黏附、细胞/药物递送及细胞外基质(ECM)重塑功能的仿生平台,且验证了其在多种湿组织缺损修复中的临床潜力。相关研究以“A nature-derived, strong adhesive hydrogel microsphere for wet tissue repair: Multifunctional and clinical potential”为题目,发表在期刊《Bioactive Materials》上。
本文要点:
1、该研究受大鲵皮肤分泌物(SSAD)天然湿黏附机制启发,通过微流控技术制备出SSAD@GelMA微球(SGM)这一新型多功能仿生水凝胶微球,经配方优化确定30%SSAD为最优比例。
2、表征证实,SGM具有均匀多孔结构、良好溶胀性,通过氢键、范德华力、π-π堆叠等多重界面作用实现强湿黏附,同时具备持续的药物释放能力,可高效封装并递送细胞,且能促进细胞铺展与迁移。转录组测序等实验表明,SGM可显著上调ECM相关基因表达,促进胶原合成与ECM重塑,为组织修复奠定基础。
3、体外黏附实验中,SGM在模拟唾液、滑液、伤口渗出液的流体剪切应力及动态力学刺激下,于牙周、软骨、皮肤湿组织表面的黏附保留率与黏附强度远高于纯GelMA微球(GM)。
4、体内动物实验进一步验证,SGM负载药物/细胞后,在大鼠牙周炎骨缺损、软骨缺损、糖尿病皮肤伤口模型中均展现出优异的修复效果:可抑制牙周骨吸收、促进新骨形成,实现透明软骨样组织再生并恢复关节功能,加速糖尿病伤口愈合、促进血管生成与胶原有序沉积。此外,生物安全性评估证实SSAD水解物无体内毒性,SGM生物相容性良好。
5、该研究的创新点在于融合大鲵天然生物黏附成分与水凝胶微球载体,实现了黏附性与生物活性的协同,突破了传统水凝胶微球湿环境黏附差的局限,且SGM为可注射型,易整合入现有临床治疗流程。
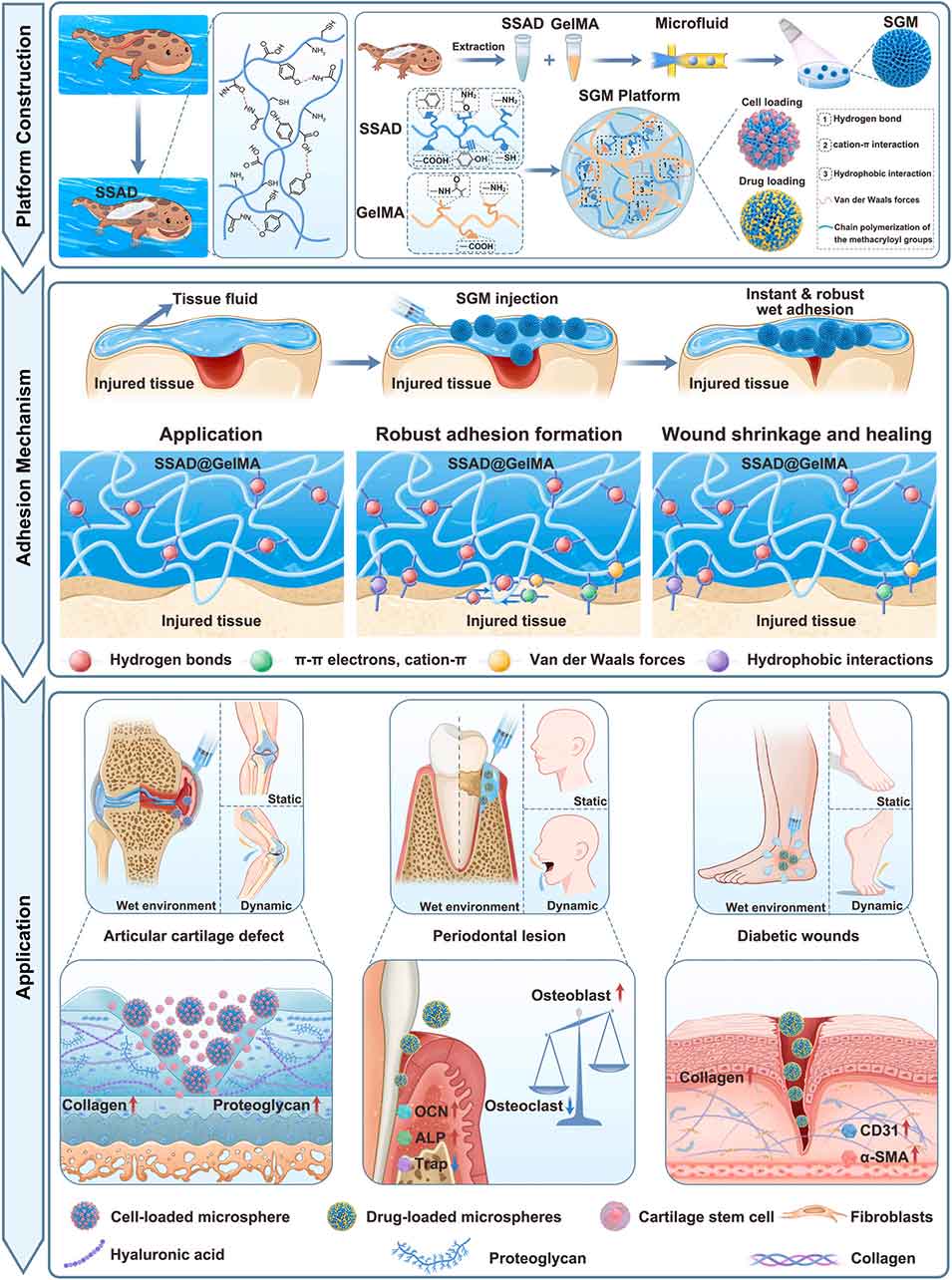
示意图1 大鲵皮肤分泌物来源的可注射水凝胶微球,通过多重相互作用力实现独特的湿黏附特性,可在动态生理环境中实现牢固的组织黏附。这类生物黏附微球是用于局部递送治疗性细胞和药物的多功能平台。临床前研究证实,其在多种组织修复模型中均展现出显著的再生潜力,包括牙周炎诱导的骨丢失、关节软骨缺损以及慢性糖尿病伤口。
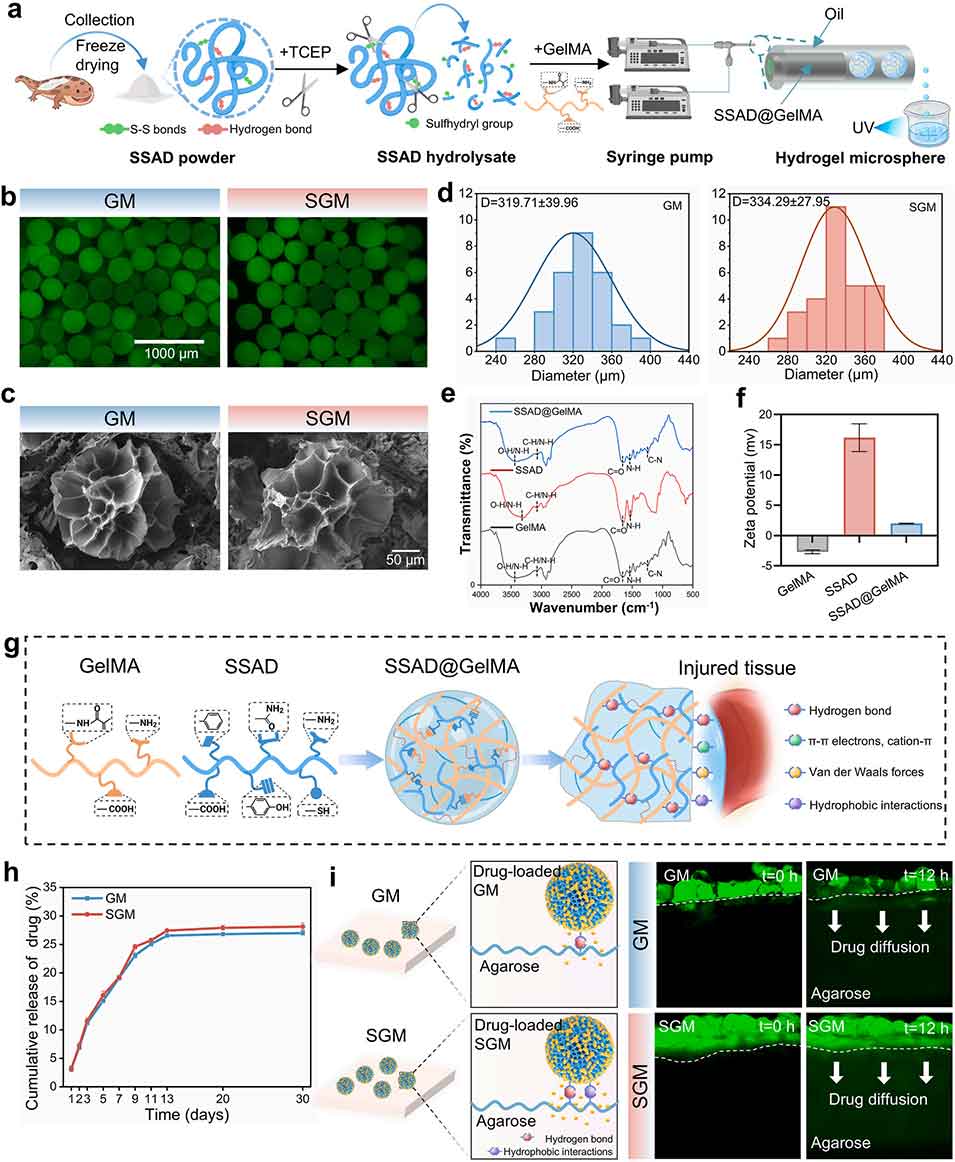
图1 SGM 的制备与表征。a) SGM 的制备流程示意图;b) 微球球形形貌的显微镜图像;c) 冻干微球多孔结构的扫描电子显微镜(SEM)照片;d) 微球的粒径分布定量分析;e) 傅里叶变换红外(FTIR)光谱分析,证实 GelMA 与 SSAD 成功结合且特征官能团得以保留;f) 采用 Zeta 电位检测的微球表面电荷表征;g) 微球的黏附机制示意图,涉及氢键、疏水作用、范德华力及阳离子 -π 作用等协同界面相互作用;h) 微球药物释放动力学对比,显示其具备长效药物递送特征;i) GM 与 SGM 在琼脂糖上的黏附效果及后续药物释放情况,荧光显微镜下观察载药微球的组织穿透性。
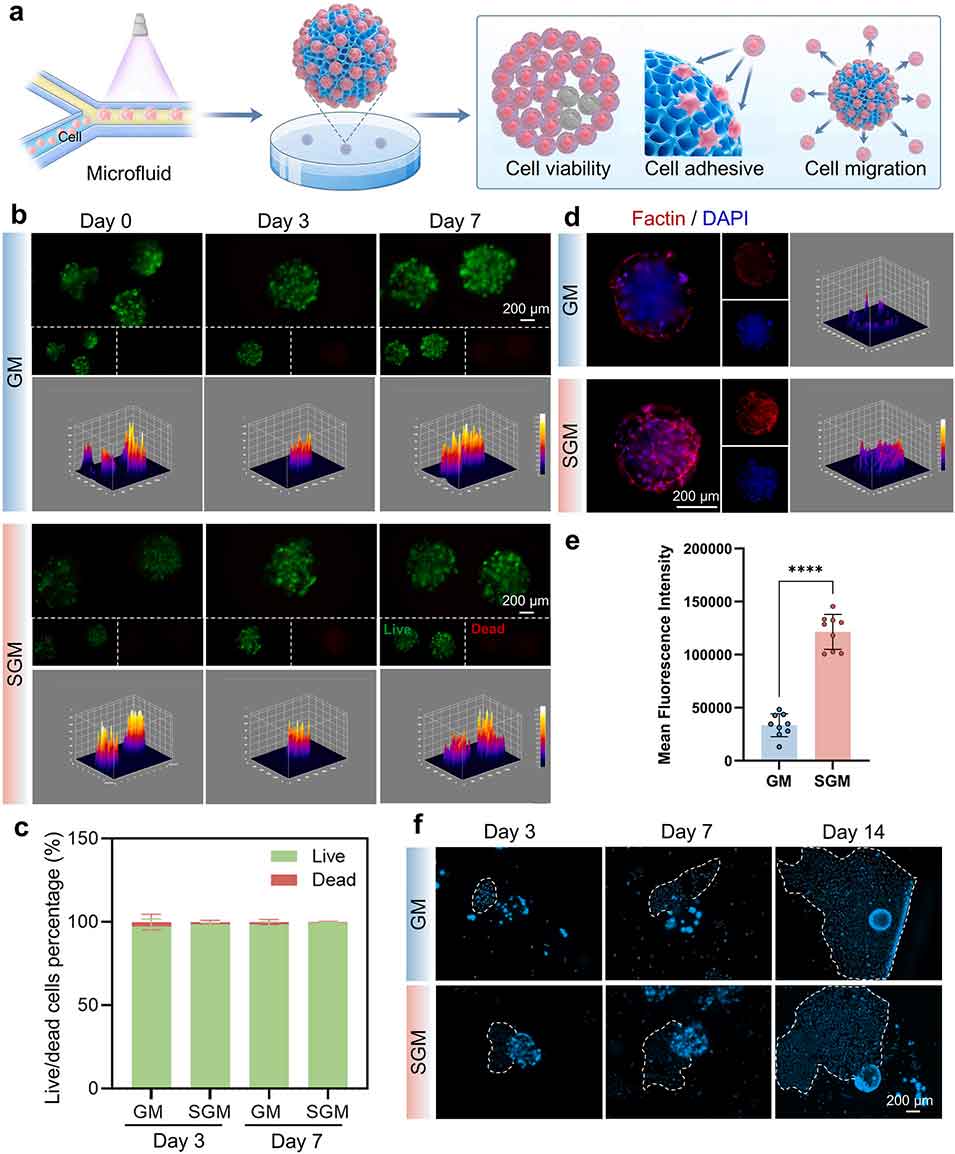
图2 载细胞微球的功能表征。a) 载细胞微球的制备流程示意图;b) 微球包封细胞后第 0、3、7 天的活/死细胞染色存活率检测(绿色:活细胞;红色:死细胞);c) 活/死细胞占比定量结果;d) F - 肌动蛋白细胞骨架染色(红色)与细胞核形态染色(蓝色)及对应的半定量分析;e) 细胞骨架染色的平均荧光强度定量;f) 包封细胞在第 3、7、14 天的迁移能力随时间变化检测结果(*P<0.05,**P<0.01,***P<0.001)。
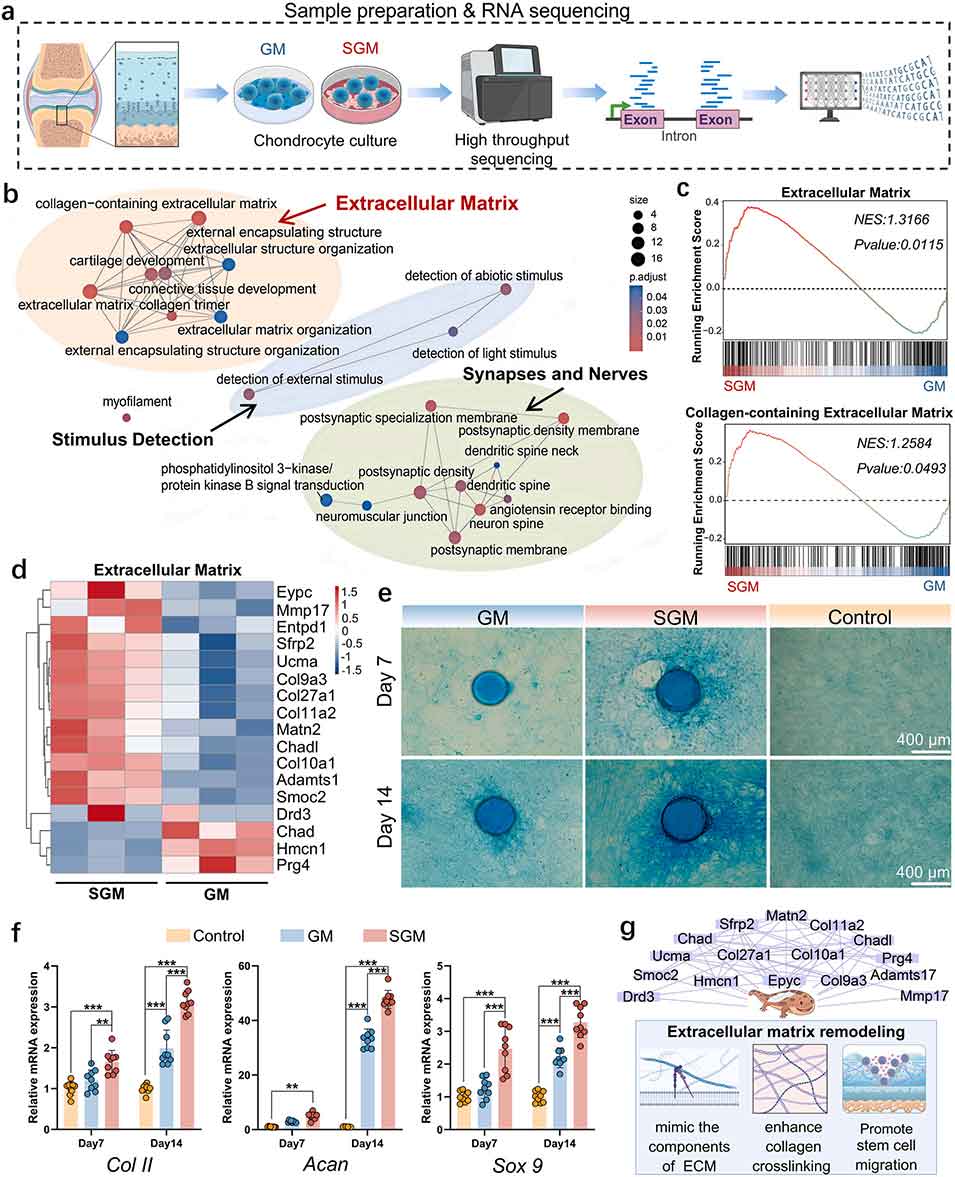
图 3 SGM 介导的细胞外基质重塑的转录组学与功能验证 a) 实验流程示意图;b) 基因本体论(GO)富集网络图谱;c) 细胞外基质相关基因的基因集富集分析(GSEA)结果;d) 细胞外基质相关差异表达基因的热图;e) 蛋白聚糖的阿利新蓝染色结果;f) 软骨形成相关细胞外基质基因的实时定量聚合酶链式反应(RT-qPCR)检测结果;g) SSAD 调控细胞外基质重塑的机制示意图。*P<0.05,**P<0.01,***P<0.001。
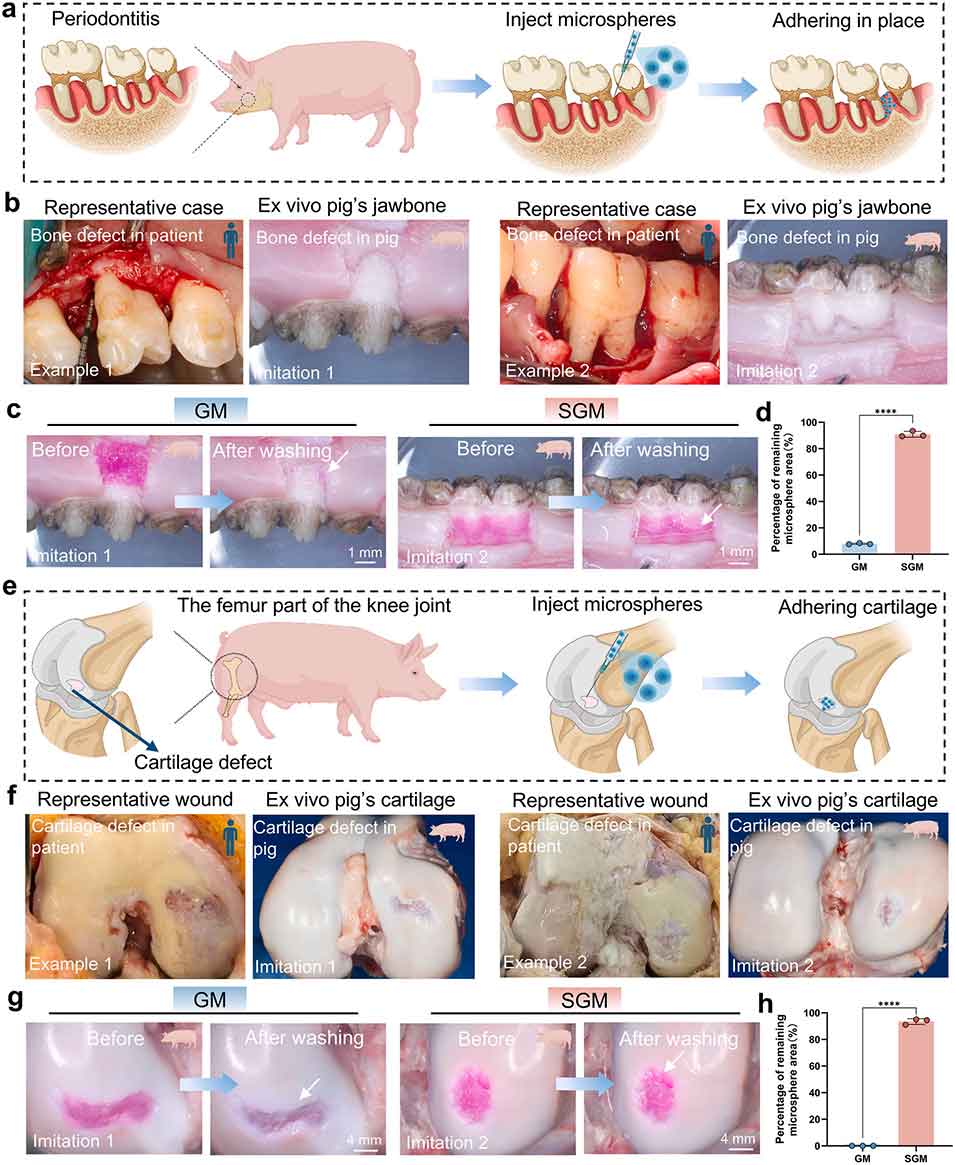
图4 模拟生理环境下 SGM 的湿黏附性。a) 流体动力学挑战实验示意图,模拟唾液或龈沟液对牙槽骨表面微球的冲刷作用;b) 人类牙周炎临床图像及猪牙槽骨的牙周缺损模拟模型;c) 恒流冲洗条件下 SGM 在猪软骨表面的保留情况;d) 微球保留率的定量分析;e) 流体动力学挑战实验示意图,模拟滑液对软骨表面微球的冲刷作用;f) 人类骨关节炎临床图像及猪膝关节的骨软骨缺损等效模拟模型;g) 恒流冲洗条件下 SGM 在猪软骨表面的保留情况;h) 微球保留率的定量分析。*P<0.05,**P<0.01,***P<0.001,****P<0.0001。
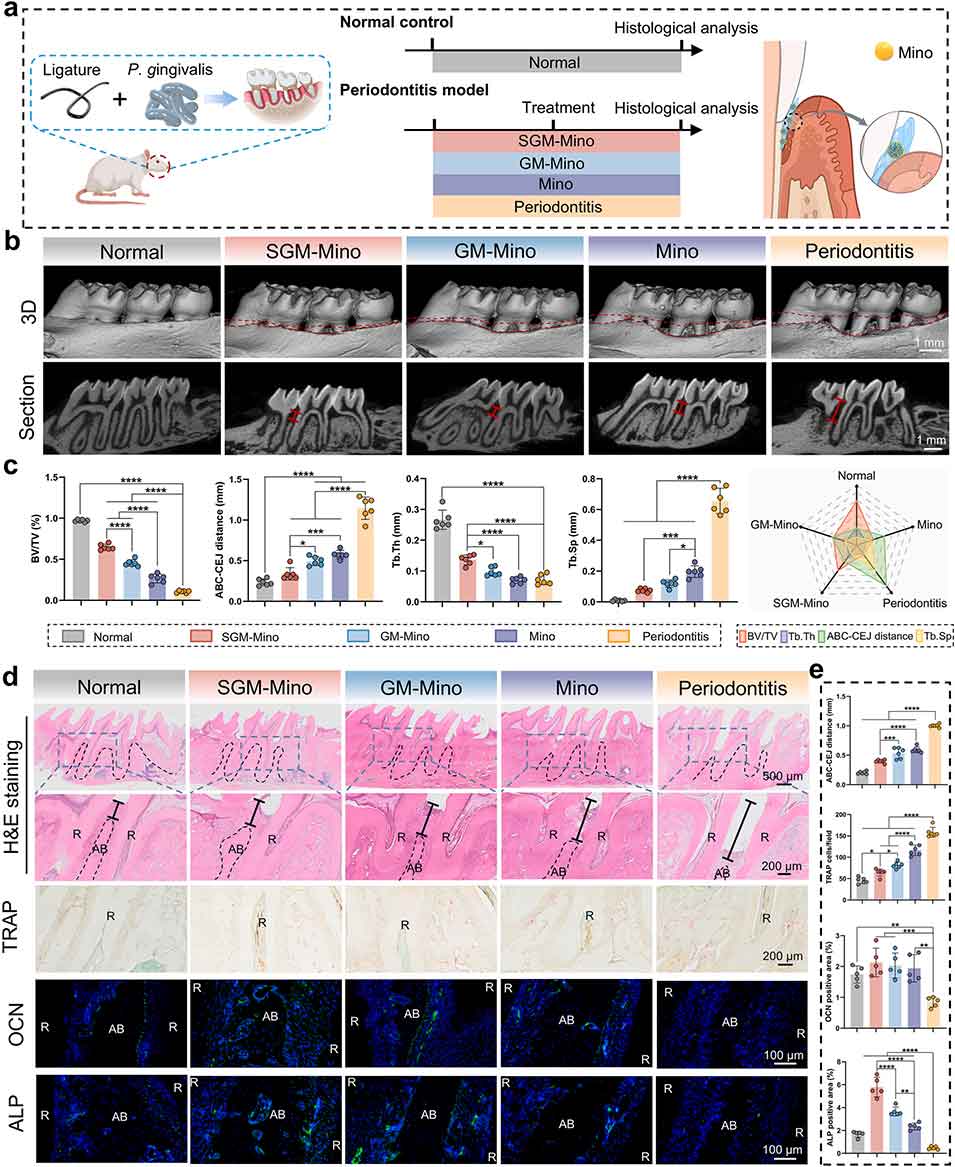
图5 SGM 在大鼠牙周炎模型中的治疗效果。a) 实验流程示意图;b) 显微计算机断层扫描(micro-CT)三维重建的代表性图像;c) 骨组织参数的微 CT 定量结果:骨体积分数(BV/TV)、牙槽骨顶-釉牙骨质界距离(ABC-CEJ)、骨小梁厚度(Tb.Th)及骨小梁间距(Tb.Sp),雷达图汇总各组整体表现;d) 组织学与免疫荧光分析结果(AB:牙槽骨;R:牙根);e) 苏木精-伊红(H&E)染色的 ABC-CEJ 距离定量、抗酒石酸酸性磷酸酶(TRAP)染色的破骨细胞占比定量,以及骨钙素(OCN)、碱性磷酸酶(ALP)阳性面积的半定量结果。*P<0.05,**P<0.01,***P<0.001,****P<0.0001。
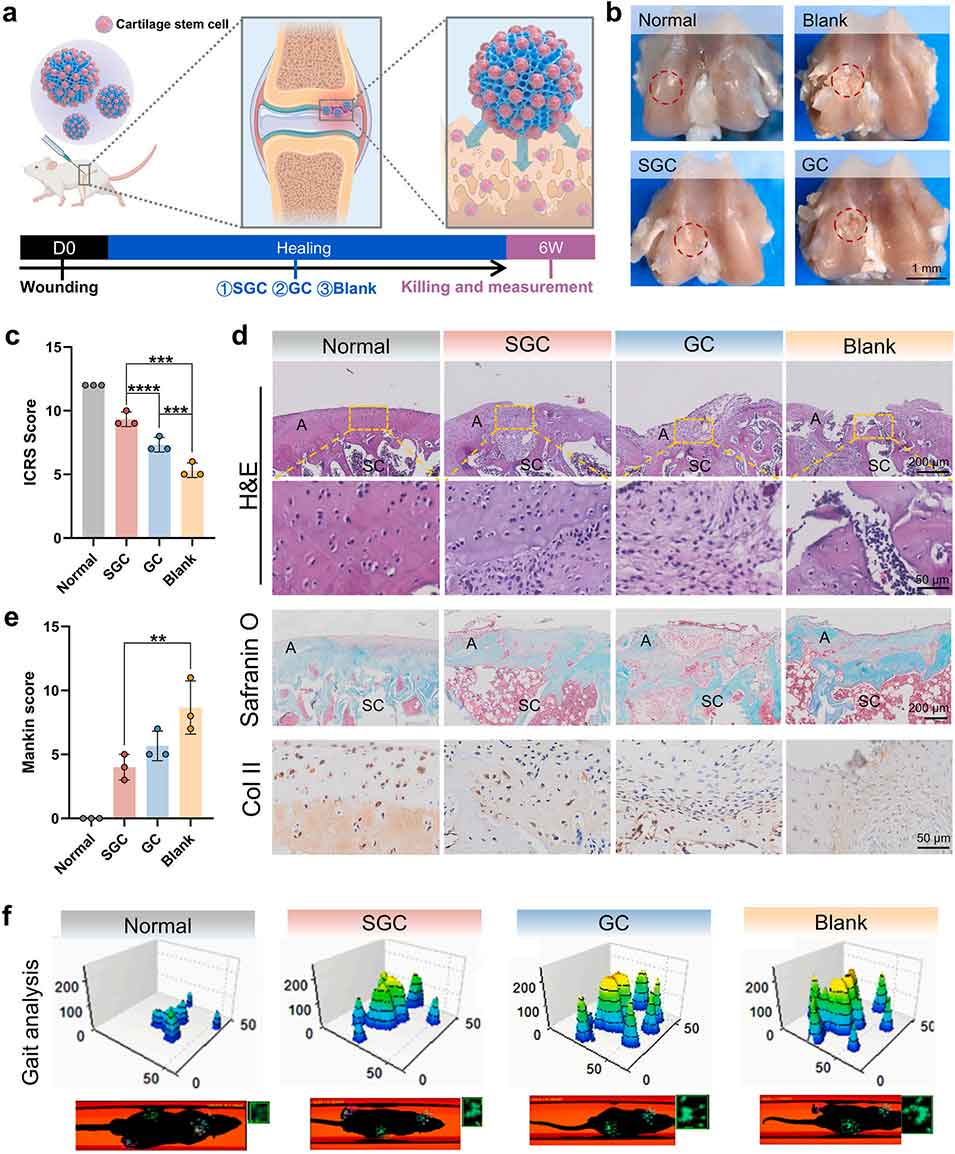
图6 SGM 在大鼠软骨缺损模型中的体内治疗效果。a) 动物实验流程示意图;b) 术后 6 周各组软骨缺损的数码照片;c) 国际软骨修复协会(ICRS)评分结果;d) 各组标本的 H&E 染色、番红 O - 固绿染色及 II 型胶原(Col II)免疫组化染色结果(A:关节软骨;SC:软骨下骨);e) 各组的曼金(Mankin)评分结果;f) 上图:三维步态压力分布图谱(X 轴:足印长度;Y 轴:足印宽度;Z 轴:足印最大接触强度),下图:术后 6 周的足部峰值接触压力定量结果。*P<0.05,**P<0.01,***P<0.001,****P<0.0001。
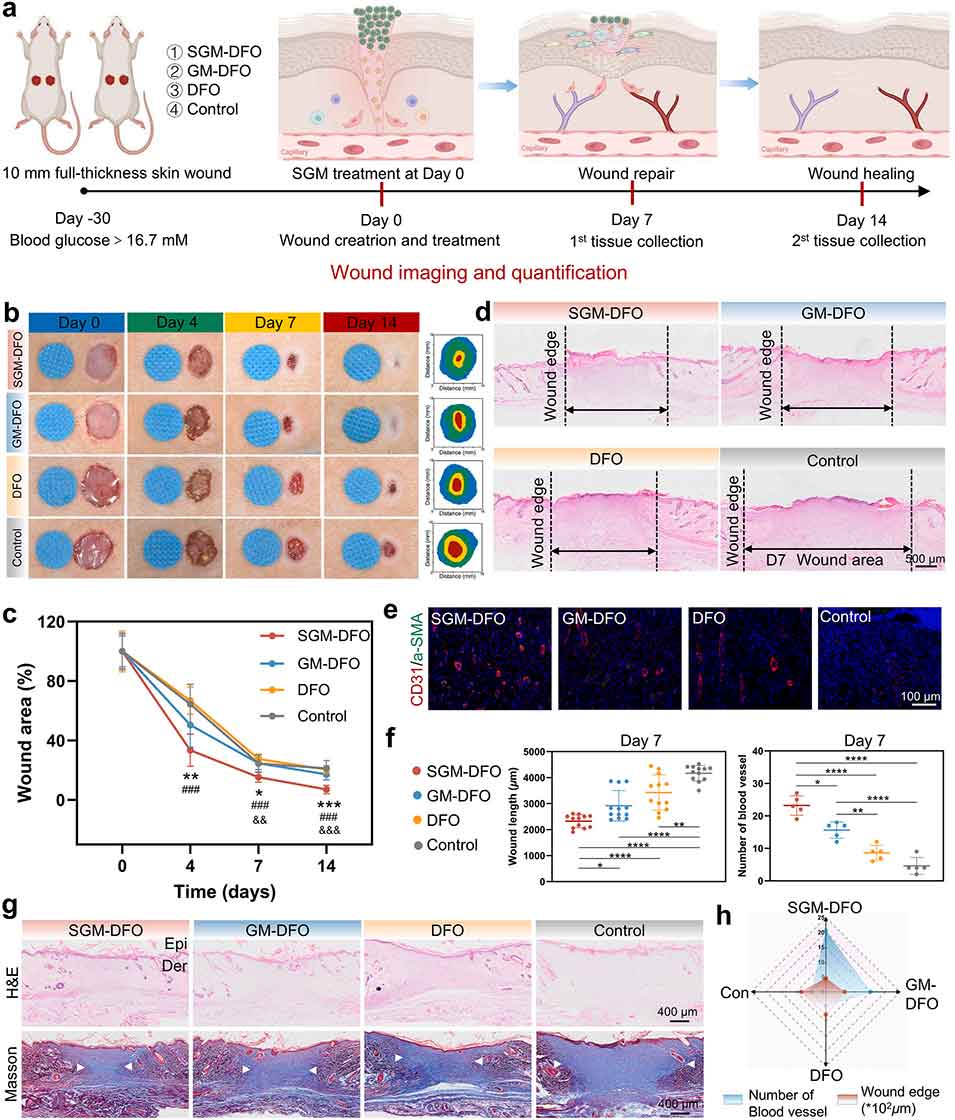
图7 SGM 在糖尿病皮肤伤口模型中的治疗效果。a) 实验流程示意图;b) 各组伤口愈合过程的数码照片;c) 14 天内相对伤口面积的定量结果(*:与对照组比较;#:与去铁胺(DFO)组比较;&:与 GM-DFO 组比较);d) 伤口造模后第 7 天各组的 H&E 染色结果;e) 内皮标志物 CD31(红色)与平滑肌标志物 α-SMA(绿色)的免疫荧光(IF)染色结果;f) 伤口长度及血管数量的定量结果;g) 造模后第 14 天各组的 H&E 染色与马松(Masson)三色染色结果;h) 基于伤口面积和微血管密度的各组表现对比雷达图。*P<0.05,**P<0.01,***P<0.001,****P<0.0001。
结论
该研究开创了一种仿生工程策略,成功攻克了动态湿性组织环境中治疗因子易流失这一关键难题。研究团队模拟大鲵皮肤分泌物的湿性黏附机制,设计出SSAD@GelMA微球(SGM),这一多功能材料平台集湿性黏附、载药能力与生物活性于一体。实验证实,SGM能在软骨、骨、皮肤软组织等多种组织表面实现稳固的界面结合,可抵御机械力导致的脱落与液体冲刷作用,同时在生理应力下保持结构完整性。除实现物理层面的稳定滞留外,大鲵皮肤分泌物本身的生物活性还能激活细胞迁移与基质重塑过程,与所递送的治疗因子产生协同作用,放大机体的内源性修复能力。该研究搭建起天然生物黏附机制与精准再生医学之间的桥梁,为复杂的富液型组织缺损治疗,提供了一种通用性强、具备临床转化潜力的解决方案。
论文链接:https://doi.org/10.1016/j.bioactmat.2026.01.033
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














