糖尿病溃疡是糖尿病的严重并发症,为非创伤性下肢截肢的首要原因,其核心治疗难点在于伤口微环境存在慢性低级别炎症、血管生成受损、上皮再生缺陷,其中巨噬细胞 M1/M2 极化失衡是炎症期紊乱的关键;间充质基质细胞(MSCs)凭借旁分泌的免疫调节和组织再生能力成为糖尿病伤口治疗的潜在策略,其治疗效果依赖炎症微环境的激活,但细胞外基质(ECM)的力学线索与炎症生化信号的协同作用机制尚未明确,且缺乏精准调控 MSCs 分泌组的生物材料平台。

近期,中山大学药学院(深圳)贾小芳副教授团队开发出基于微流控技术制备的甲基丙烯酰化明胶(GelMA)水凝胶微球体系,可实现间充质基质细胞与炎症细胞因子 TNF-α、IFN-γ 的共包封。借助软基质力学信号与炎症生化线索的协同作用,该体系通过 FAK-YAP 依赖通路介导间充质基质细胞的机械敏感激活,进而提升其免疫调节与组织再生能力。在糖尿病慢性伤口小鼠模型中的实验结果表明,该体系能显著加速伤口闭合、促进血管新生,并重塑伤口局部的免疫稳态。相关研究以“Synergistic Chemomechanical Cues within Mesenchymal Stromal Cell-Laden Hydrogel Microspheres for Accelerated Diabetic Wound Healing”为题目,发表在期刊《ACS Applied Materials & Interfaces》上。
本文要点:
1、该研究开发了一种基于微流控技术的甲基丙烯酰化明胶(GelMA)水凝胶微球系统,将间充质基质细胞(MSCs)与炎症细胞因子(TNF-α、IFN-γ)共包封,通过调控局部化学-机械微环境编程 MSC 分泌组,实现糖尿病慢性伤口的加速愈合,为慢性炎症疾病治疗提供了新型机械医学策略。
2、研究首先制备了刚度可调的软、硬两种 GelMA 微球(杨氏模量分别为 2.45 kPa、8.37 kPa),验证了软微球可通过细胞-基质相互作用,促进包封 MSC 的铺展和机械感知,激活黏着斑激酶(FAK)和 Yes 相关蛋白(YAP)介导的机械转导通路。
3、体外实验发现,软基质与炎症细胞因子的协同作用,能显著上调 MSC 的抗炎/免疫调节基因(TSG6、IDO 等)和再生相关生长因子基因(VEGF、TGFβ1 等)表达,其分泌的条件培养基可促进成纤维细胞迁移和血管内皮细胞血管生成,并有效调控巨噬细胞从促炎 M1 表型向促再生 M2 表型极化。
4、在 1 型糖尿病小鼠伤口模型中,经 TNF-α/IFN-γ 预激活的 MSC 负载软 GelMA 微球局部给药后,显著加速了伤口闭合(术后 6 天闭合率超 50%,远高于对照组和无细胞微球组),同时促进了伤口再上皮化、胶原沉积和新生血管形成,还能在体内重编程巨噬细胞极化、恢复免疫稳态,解决了糖尿病伤口慢性炎症、血管生成受损的核心问题。
5、机制上,MSC 的机械敏感激活依赖于适宜的细胞骨架张力,以及 FAK-YAP 信号通路的协同调控;化学信号决定 MSC 应答的绝对强度,机械信号则作为关键 “增强因子” 优化其治疗表型。此外,该策略具有通用性,可扩展至不同来源的 MSC 和其他炎症细胞因子,不限于单一水凝胶材料。
6、研究证实,精准设计的化学-机械微环境能协同增强 MSC 的免疫调节和再生能力,该工程化细胞负载微球为糖尿病伤口愈合提供了高效治疗方案,也为编程细胞功能的机械医学研究奠定了基础。
研究者采用同轴微流控装置制备GelMA微球。内相为含有MSCs的GelMA预聚物溶液(7.5 wt%)+ 光引发剂LAP(0.25 wt%),外相为含有0.5% Span 80的石蜡油。通过调节油相与水相的流速比(油:水 = 20:1),可控制微球直径(约229 ± 4 μm)。
力学性能的调控主要通过改变GelMA的甲基丙烯酰化程度(DOM)实现:高DOM(~60%)对应硬微球(Stiff),低DOM(~20%)对应软微球(Soft)。具体通过控制甲基丙烯酸酐的添加量(高:0.3 mL;低:0.09 mL)在碳酸钠-碳酸氢钠缓冲液中反应3小时,并经透析、冻干获得。
该水凝胶微球系统在糖尿病伤口治疗中的核心优势主要体现在以下五个方面:
1、力学微环境匹配
软微球(~2.5 kPa)模拟天然细胞外基质的低刚度特征,促进MSCs铺展、粘着斑形成和YAP核转位,从而最大化免疫调节和再生基因表达(如TSG6上调8.9倍)。
避免硬基质(~8.4 kPa)引起的过高细胞张力,后者反而抑制TSG6等关键因子的表达(倒U型力学响应)。
2、协同化学-力学编程
微球可同时封装MSCs和炎症因子(TNF-α/IFN-γ),并在体内持续释放(3天内约20%保留),实现局部、持久的“力学+化学”协同刺激,显著增强MSCs的旁分泌功能。
3、可注射性与原位修复
微球直径可控(~229 μm),可通过注射器实现微创递送,填充不规则创面。
良好的生物相容性(活率 >90%)和至少7天的体内结构稳定性,覆盖伤口愈合的关键炎症-增殖过渡期。
4、促进血管新生与免疫重塑
软微球负载的MSCs条件培养基显著促进HUVECs管腔形成(总长度和分支点增加)和L929细胞迁移。
在糖尿病小鼠模型中,该微球系统将伤口局部巨噬细胞从M1(促炎)极化为M2(促再生),同时增加CD31⁺血管密度和胶原沉积,加速伤口闭合(第6天闭合率 >50% vs 对照组 ~20%)。
5、普适性平台
该制备策略可推广至其他水凝胶材料、不同MSC来源(如UC-MSC、iMSC)及其他炎症因子(如IL-1β、LPS),为慢性炎症性疾病提供通用型力学-化学编程平台。
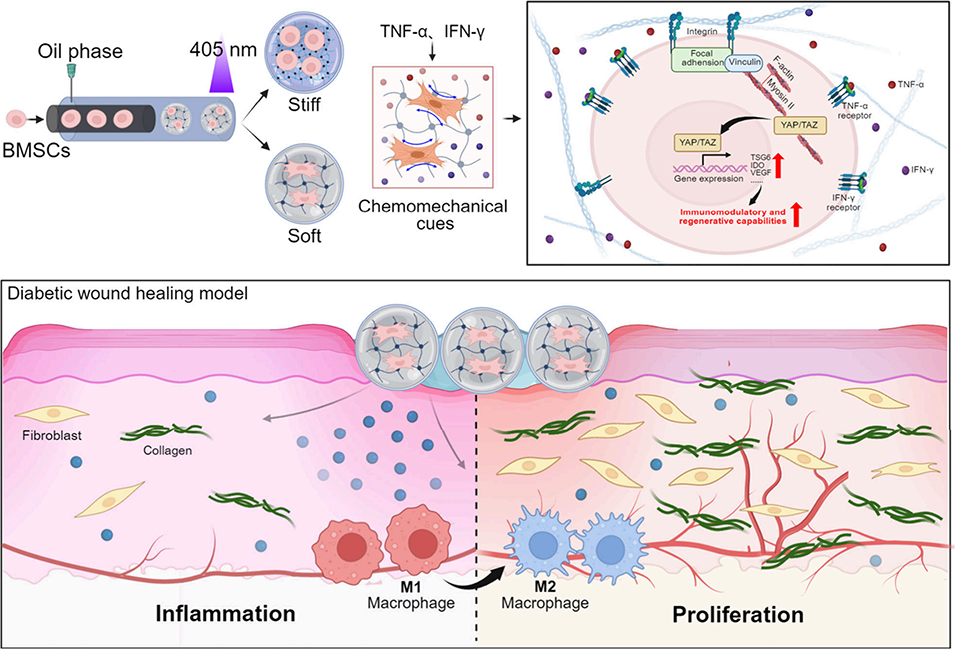
图1. 甲基丙烯酰化明胶微球包封间充质基质细胞,与炎症细胞因子协同调控间充质基质细胞分泌组以加速糖尿病伤口愈合的示意图。间充质基质细胞被包封于不同刚度的甲基丙烯酰化明胶微球中,该微球通过微流控技术制备。研究表明,包封在软质水凝胶微球中的间充质基质细胞可通过旁分泌信号发挥免疫调节、促血管生成和促细胞迁移作用,而软质水凝胶微球能为细胞提供特异性化学-机械微环境。
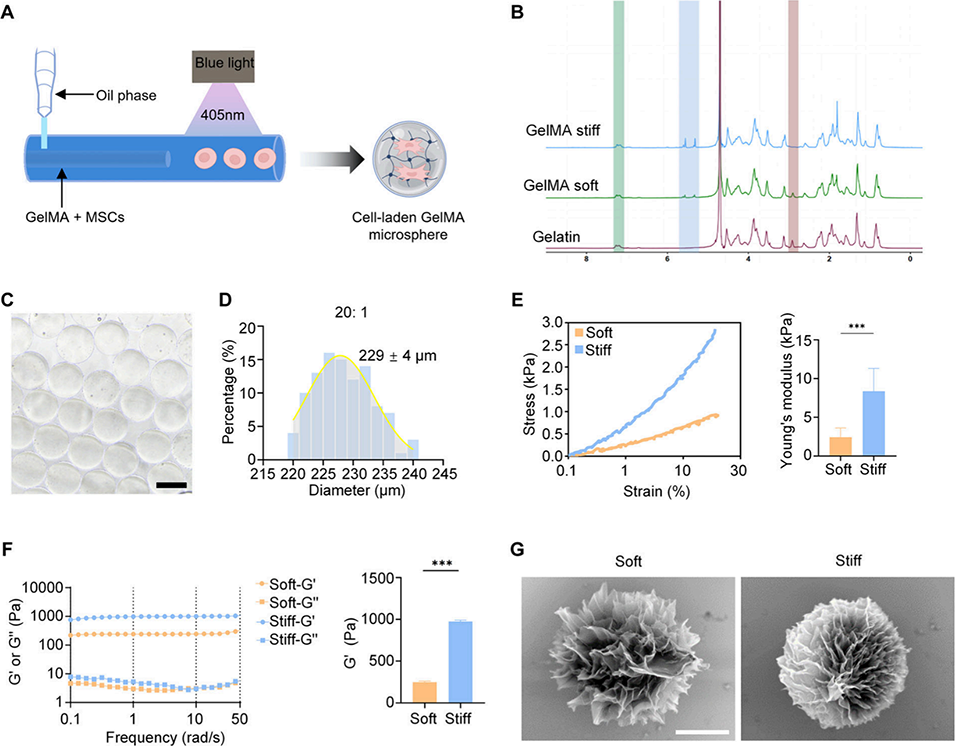
图2. 甲基丙烯酰化明胶微球的制备与表征。A)制备载细胞甲基丙烯酰化明胶微球所用的同轴微流控装置示意图;B)明胶以及甲基丙烯酰化度为 60%(硬质)和 20%(软质)的甲基丙烯酰化明胶的氢核磁共振谱图;C)油相与水相流速比为 20:1 时,甲基丙烯酰化明胶微球的明场显微镜图像;D)上述条件下水凝胶微球的粒径分布(n=108);E)采用微型材料试验机测定的甲基丙烯酰化明胶微球的应力-应变曲线与杨氏模量(n=7,***p<0.001,学生 t 检验);F)流变仪测定的甲基丙烯酰化明胶的频率扫描曲线(左)和流变学分析结果(右);G)不同刚度甲基丙烯酰化明胶微球的代表性扫描电镜图像(比例尺:50μm)。
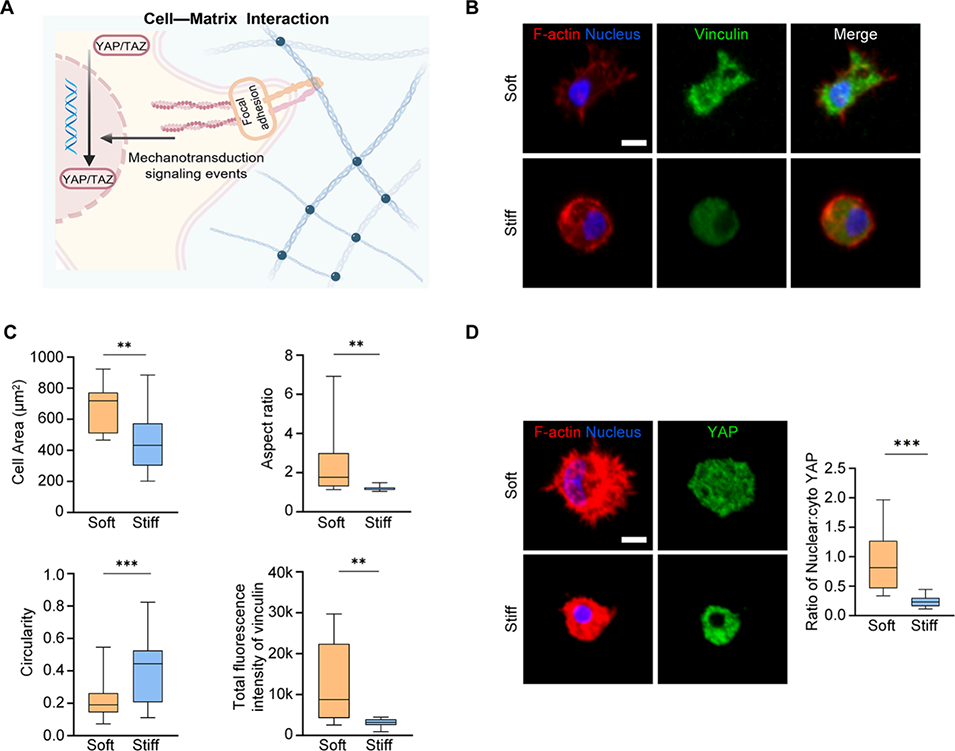
图3. 软质甲基丙烯酰化明胶微球促进包封间充质基质细胞的铺展与机械感知。A)细胞感知甲基丙烯酰化明胶微球的机械信号,触发一系列机械转导信号事件并最终影响 Yes 相关蛋白核转位的示意图;B)包封在不同刚度甲基丙烯酰化明胶微球中间充质基质细胞的 F - 肌动蛋白和纽蛋白代表性荧光图像;C)不同刚度水凝胶微球中间充质基质细胞的铺展面积、长宽比、圆形度及纽蛋白总荧光强度的统计分析(n=15-20);D)水凝胶微球中间充质基质细胞中 Yes 相关蛋白的代表性荧光图像(左)及细胞核/细胞质中 Yes 相关蛋白比值的定量分析(右,n=11)。B、D 比例尺:10μm。
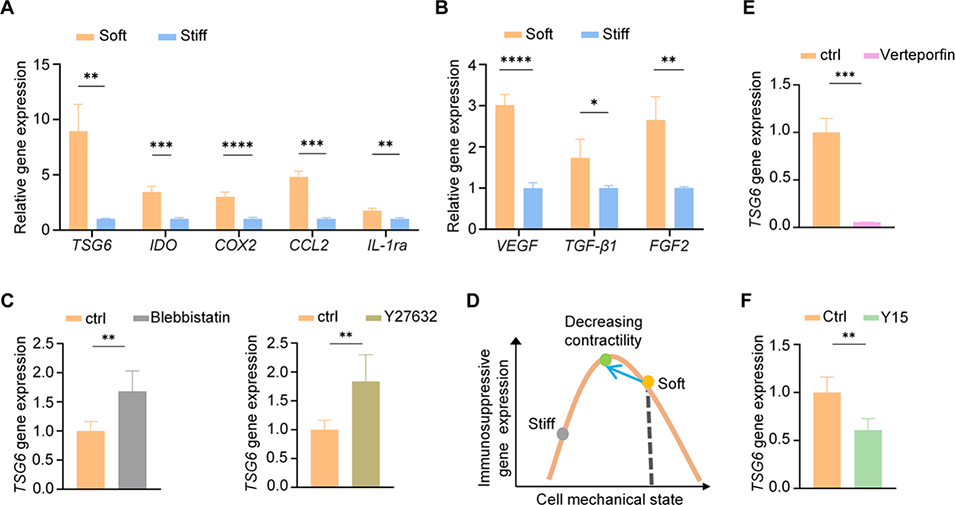
图4. 炎症因子通过调控适宜的细胞骨架张力和 Yes 相关蛋白的核定位,实现对间充质基质细胞的机械敏感激活。A、B)炎症环境下,包封在甲基丙烯酰化明胶微球中的间充质基质细胞其抗炎相关基因(A)和再生相关基因(B)的相对表达量荧光定量 PCR 分析;C)软质水凝胶微球经布雷他汀(左)和 Y27632(右)抑制剂处理后,肿瘤坏死因子刺激基因 6 的表达情况;D)在软质甲基丙烯酰化明胶微球中,利用布雷他汀或 Y27632 抑制剂降低细胞收缩性,可上调免疫抑制相关基因的表达;E、F)软质甲基丙烯酰化明胶微球中的间充质基质细胞在维替泊芬(E)和 Y15(F)抑制剂作用下,肿瘤坏死因子刺激基因 6 的表达情况。A、B、C、E、F 均为 n=4,*p<0.05,**p<0.01,***p<0.001,学生 t 检验。
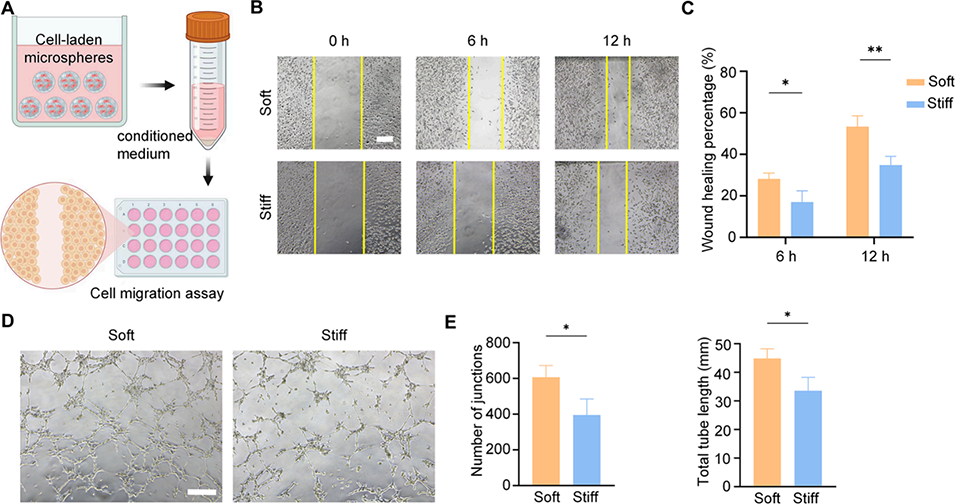
图5. 经肿瘤坏死因子 -α/ 干扰素 -γ 处理的、包封于软质甲基丙烯酰化明胶微球的间充质基质细胞可促进细胞迁移和血管生成。A)收集条件培养基用于细胞迁移实验的示意图;B)细胞在 0h、6h、12h 时的迁移代表性图像(比例尺:200μm);C)6h 和 12h 时细胞划痕区域的闭合率(n=3,*p<0.05,**p<0.01,学生 t 检验);D)人脐静脉内皮细胞管状结构形成的代表性明场图像(比例尺:200μm);E)对形成的管状结构进行定量分析,统计连接节点数(左)和总长度(右,n=3,*p<0.05,学生 t 检验)。
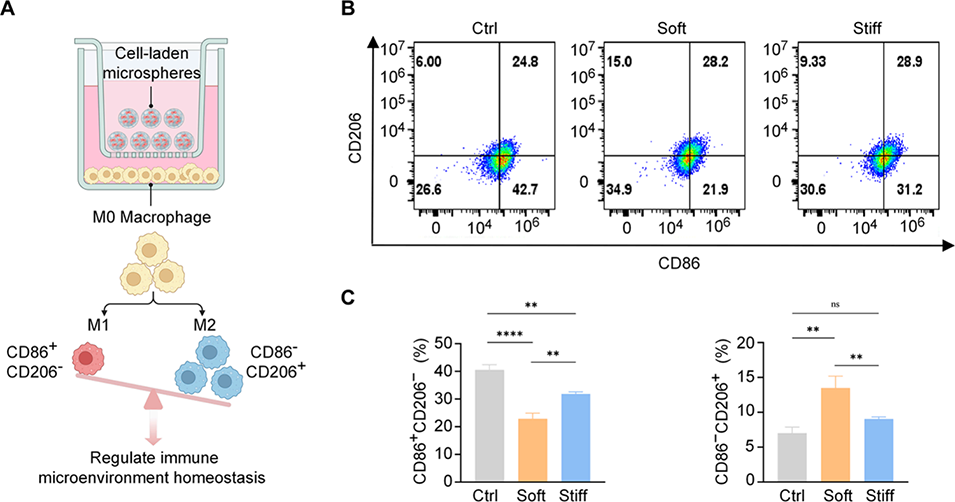
图6. 经肿瘤坏死因子 -α/ 干扰素 -γ 处理的、包封于软质甲基丙烯酰化明胶微球的间充质基质细胞可促进巨噬细胞极化。A)利用 Transwell 小室构建的共培养体系示意图;B)与不同刚度甲基丙烯酰化明胶微球包封的间充质基质细胞共培养后,RAW264.7 细胞中 CD206 和 CD86 表达的流式细胞术分析;C)M1 型(CD86+CD206-)(左)和 M2 型(CD86-CD206+)(右)巨噬细胞的占比(n=3,**p<0.01,***p<0.001,单因素方差分析)。
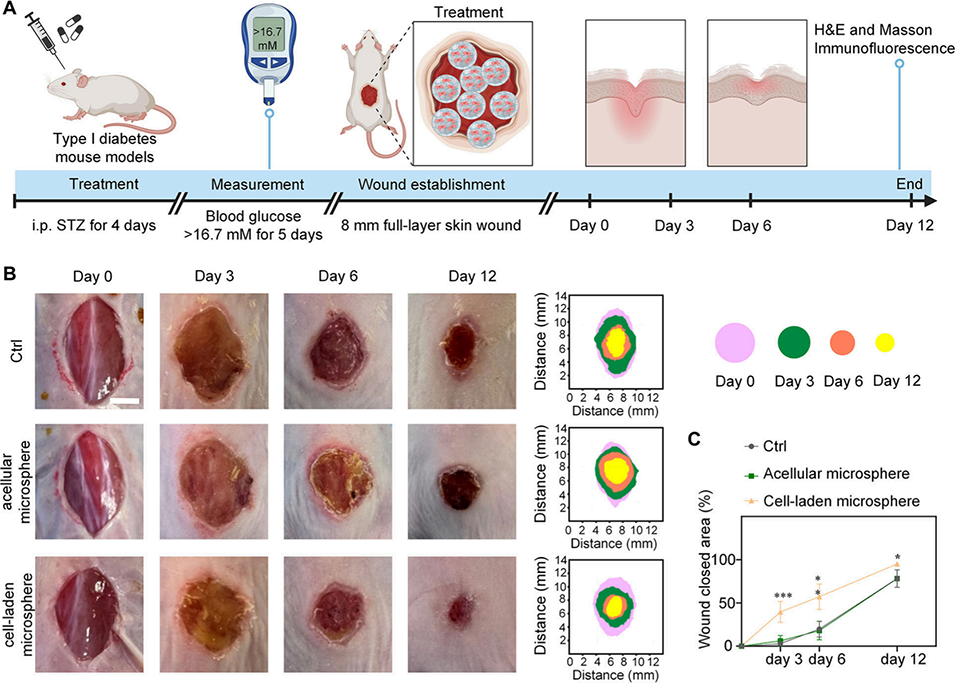
图7. 载细胞水凝胶微球经穴位给药可促进糖尿病小鼠皮肤伤口的加速修复。A)动物实验流程示意图;B)磷酸盐缓冲液对照组、无细胞微球组和载细胞微球组在 0、3、6、12 天伤口愈合过程的代表性图像(左)和示意图(右,比例尺:5mm);C)伤口愈合面积的定量分析折线图(n=3,*p<0.05,**p<0.01,***p<0.001,单因素方差分析)。
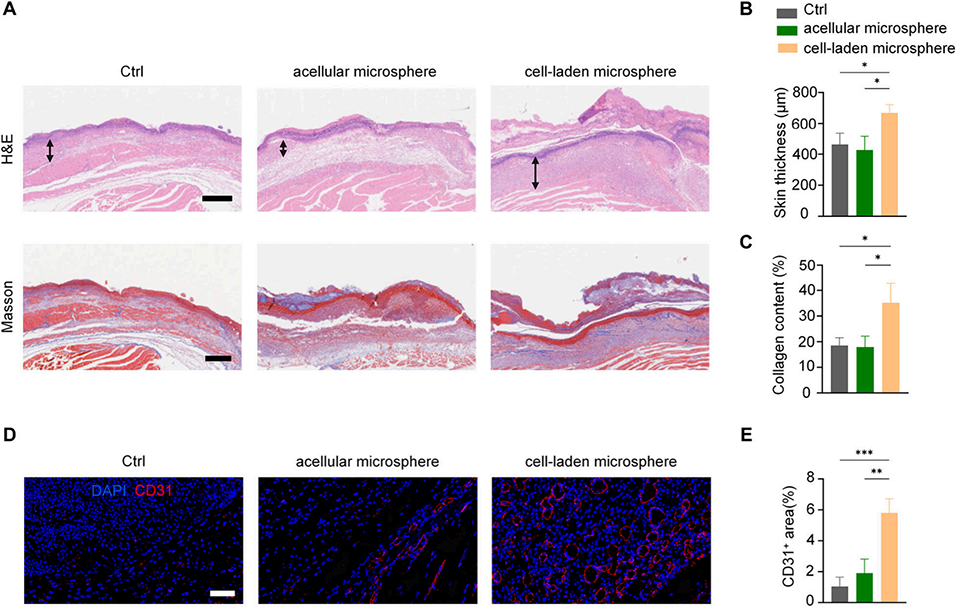
图8. 负载肿瘤坏死因子 -α/ 干扰素 -γ 的载细胞甲基丙烯酰化明胶微球促进糖尿病伤口的再上皮化和新生血管形成。A)各组伤口组织的苏木精-伊红染色(上)和马松染色(下)代表性图像,黑色箭头指示新生真皮厚度(比例尺:500μm);B)各组真皮厚度的定量分析;C)各组胶原含量的定量分析;D)CD31 免疫荧光染色图像(比例尺:50μm);E)CD31 阳性血管密度的定量分析。B、C、E 均为 n=3,*p<0.05,**p<0.01,***p<0.001,单因素方差分析。
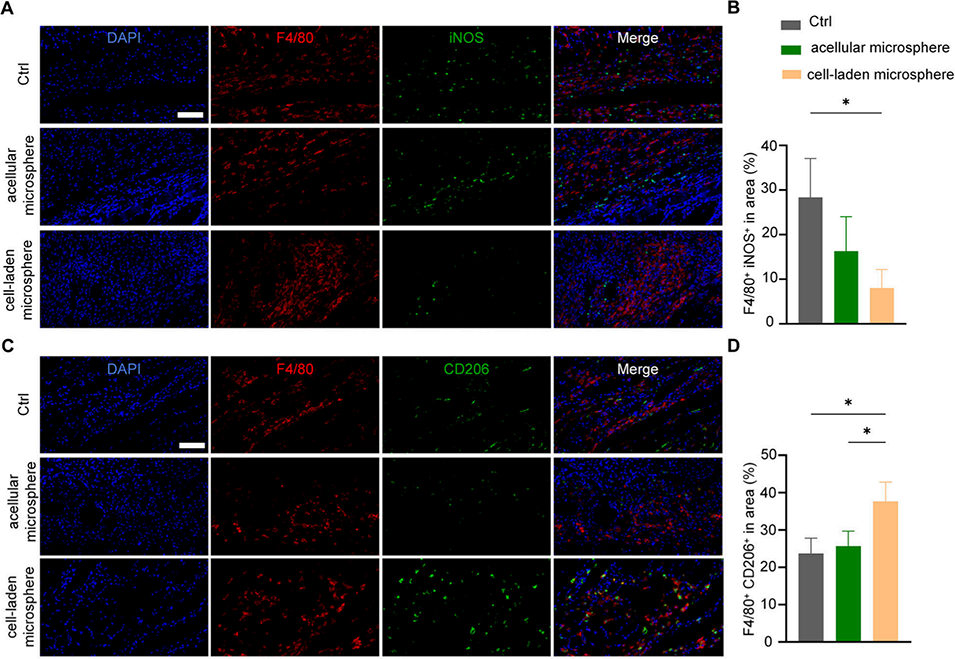
图9. 负载肿瘤坏死因子 -α/ 干扰素 -γ 的载细胞甲基丙烯酰化明胶微球促进糖尿病伤口中 M2 型巨噬细胞极化。A)伤口组织中 M1 型巨噬细胞的免疫荧光图像:F4/80(红色)和 CD86(绿色,比例尺:50μm);B)区域内 F4/80+iNOS+ 细胞的占比;C)伤口组织中 M2 型巨噬细胞的免疫荧光图像:F4/80(红色)和 CD206(绿色,比例尺:50μm);D)区域内 F4/80+CD206+ 细胞的占比。B、D 均为 n=3,*p<0.05,单因素方差分析。
论文链接:https://doi.org/10.1021/acsami.6c01199
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














