
导读:
近期,苏州大学附属第二医院骨外科陆政峰主任医师联合多单位,开发了一种负载人参皂苷Rg1与趋化因子SDF1α的脂质体锚定水凝胶微球(R-L@S-GMs),通过时空受控的药物释放来调节早期炎症微环境并招募内源性干细胞,从而显著促进了脊髓损伤后的神经再生与功能修复。相关研究以“Injectable Liposome-Anchored Hydrogel Microspheres Promote Spinal Cord Injury Repair by Modulating the Inflammatory Microenvironment and Recruiting Endogenous Stem Cells”为题目,发表在期刊《Small Structures》上。
本文要点:
1. 研究背景与挑战
脊髓损伤(SCI)的难点:损伤后的早期局部炎症反应会导致骨髓间充质干细胞(BMSCs)功能障碍,并抑制内源性修复机制,导致神经元坏死和胶质瘢痕形成。
治疗策略:理想的治疗需要同时控制急性期的“细胞因子风暴”,并为后期的神经再生创造有利的微环境。
2. 复合材料(R-L@S-GMs)的设计与制备
核心组分:
R-L(阳离子脂质体):封装了具有抗炎和神经保护作用的中药单体人参皂苷 Rg1。
S-GMs(GelMA微球):通过微流控技术制备,负载了干细胞趋化因子 SDF1α。
结合机制:脂质体通过自发的希夫碱反应(Schiff base reaction)和静电吸附作用锚定在甲基丙烯酸酐化明胶(GelMA)微球表面。
3. 时空受控的药物释放
顺序释放:该系统实现了药物的梯次释放。Rg1 在前 7 天快速释放(累计达 8%),用于抑制早期炎症;而 SDF1α 释放更缓慢且持久(28 天累计达 79.37%),用于后期招募干细胞。
生物降解:复合微球在 4 周内均匀降解,其多孔结构有助于药物负载和细胞迁移。
4. 生物学功能与疗效
抗炎调节(急性期):
体外:有效诱导巨噬细胞向 M2 型极化,显著增加抗炎细胞因子(如 IL-10)的分泌。
体内:抑制局部和全身的急性炎症反应。
促进神经再生(亚急性/慢性期):
招募与分化:通过 SDF1α/CXCR4 轴招募内源性 BMSCs,并利用 Rg1 促进其向神经元方向分化。
抑制瘢痕与血管再生:显著减少胶质瘢痕形成(如降低 GFAP 和 NG2 表达),并促进血管新生(如增加 CD31 和 VWF 表达)。
功能恢复:在大鼠实验中,接受 R-L@S-GMs 治疗的组别在 BBB 评分和斜板试验(IPT)中表现出最显著的后肢运动功能改善。
5. 结论
该研究成功构建了一个双功能支架,实现了早期炎症控制与后期神经修复的协调,为脊髓损伤的微创治疗提供了一种极具潜力的临床方案。
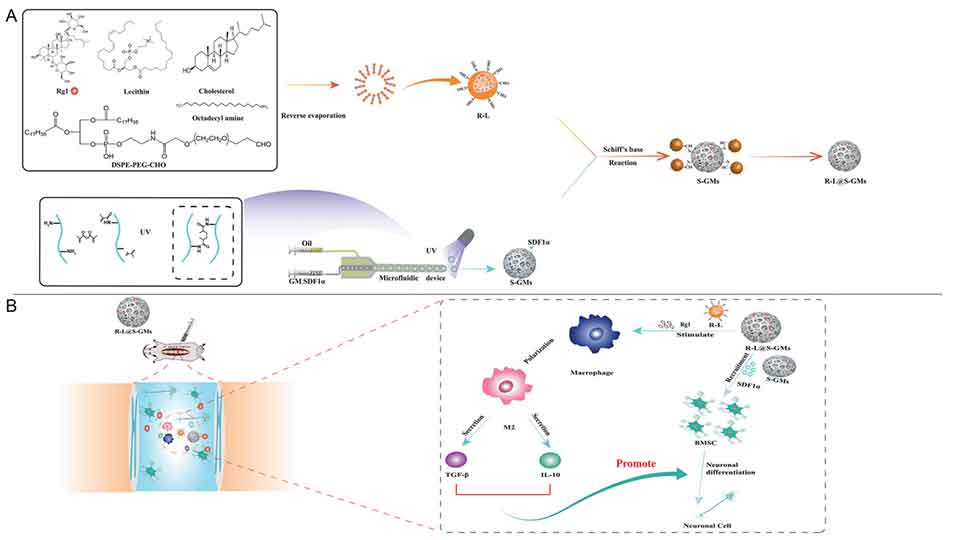
图1 复合材料 L@GMs 的构建及作用机制。 (A) 用于治疗脊髓损伤的仿生 L@GMs 构建方案图,以及 (B) 其炎症调节和神经再生效果的示意图。
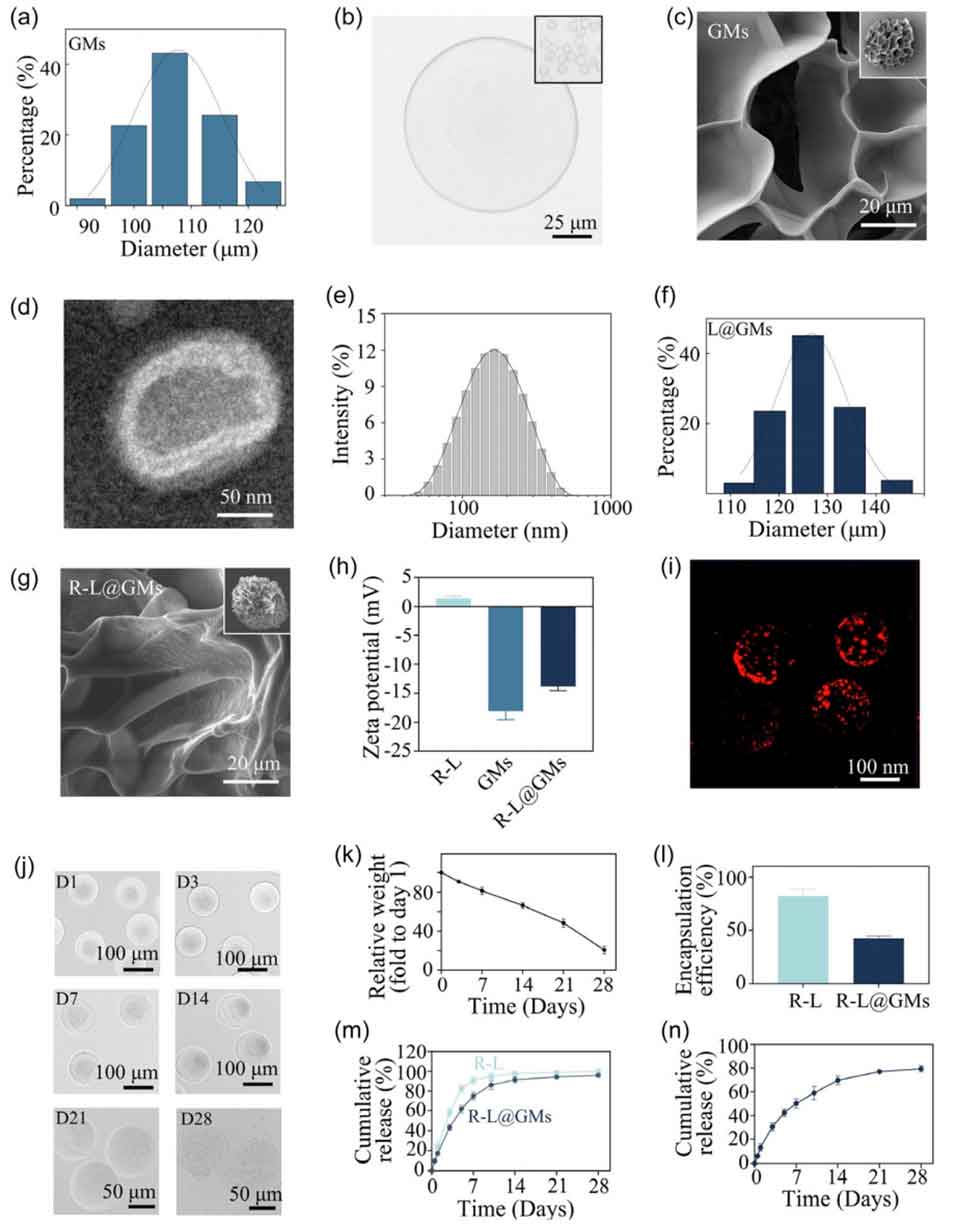
图2 复合材料 L@GMs 的物理表征。 (a) GMs 的粒径分布。(b) GMs 的显微镜图像。(c) GMs 的扫描电镜(SEM)图像。(d) 脂质体的透射电镜(TEM)图像。(e) 通过动态光散射(DLS)测量的脂质体尺寸分布。(f) L@GMs 的粒径分布。(g) 附着在 GMs 表面的脂质体的扫描电镜图像。(h) 脂质体、GMs 和 L@GMs 的表面电荷(Zeta 电位)。(i) L@GMs 的激光共聚焦扫描显微镜(LSCM)图像,附着在 GMs 表面的脂质体用 DiI 染料标记。(j) 显示 L@GMs 在 4 周内形态变化的显微镜图像。(k) L@GMs 的降解曲线。(l) Rg1 在脂质体和 L@GMs 中的包封率。(m) Rg1 从脂质体和 L@GMs 中的体外释放曲线。(n) SDF1α 从 L@GMs 中的体外释放曲线。n = 3。
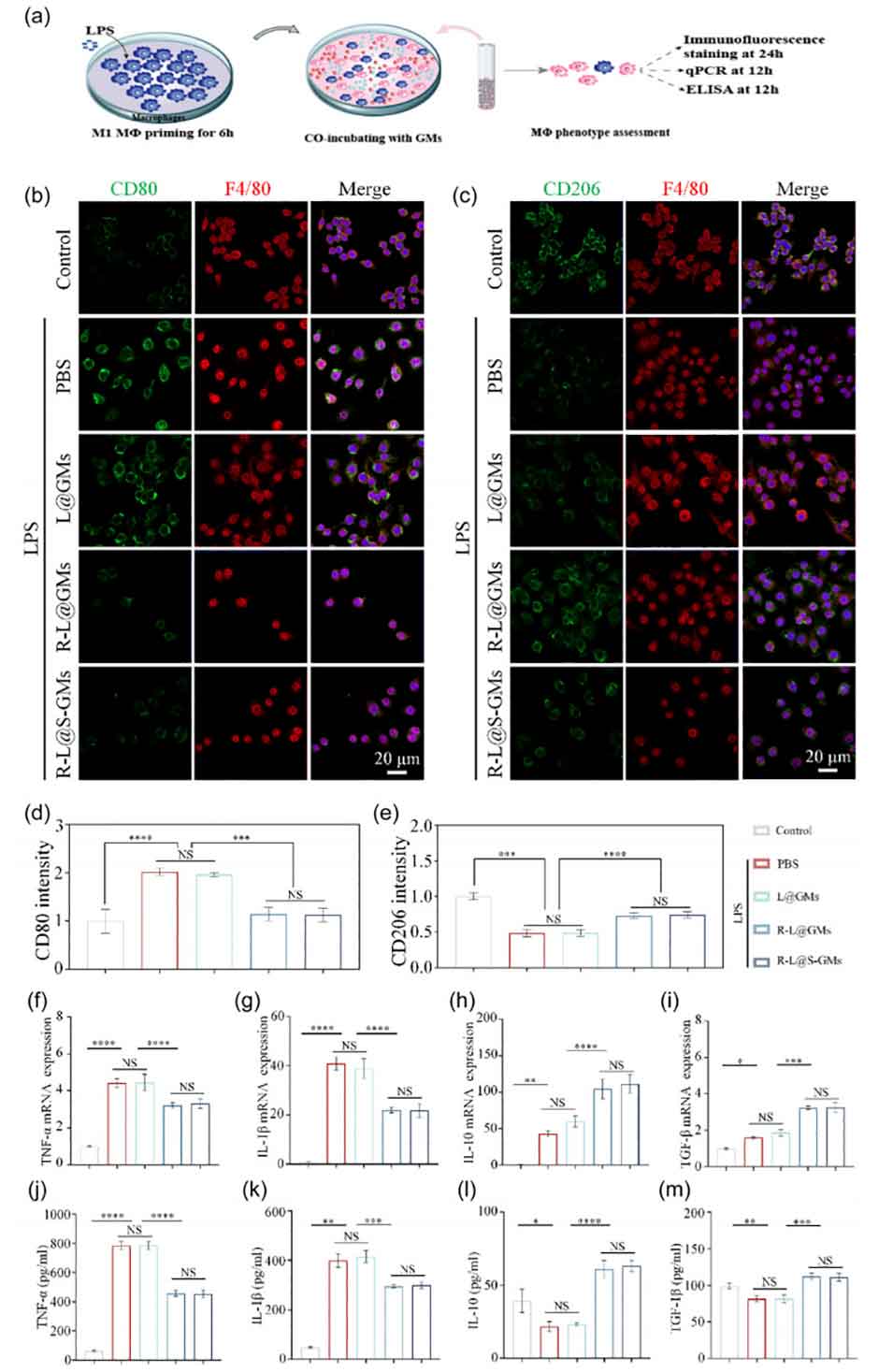
图3 Raw264.7 分泌的极化和炎症因子。 (a) Raw264.7 体外极化示意图。(b) 巨噬细胞标记物 F4/80(红色)和 M1 型巨噬细胞标记物 CD80(绿色)的免疫荧光染色。(c) 巨噬细胞标记物 F4/80(红色)和 M2 型巨噬细胞标记物 CD206(绿色)的免疫荧光染色。(d) M1 型巨噬细胞标记物 CD80 的荧光半定量分析。(e) M2 型巨噬细胞标记物 CD206 的荧光半定量分析。(f–i) TNF-α、IL-1β、IL-10、TGF-β 的 mRNA 表达分析。(j–m) 通过 ELISA 检测 Raw264.7 分泌的炎症因子 TNF-α、IL-1β、IL-10、TGF-β。n = 3,当空白组与其他组对比时:*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001,NS 表示无显著差异。
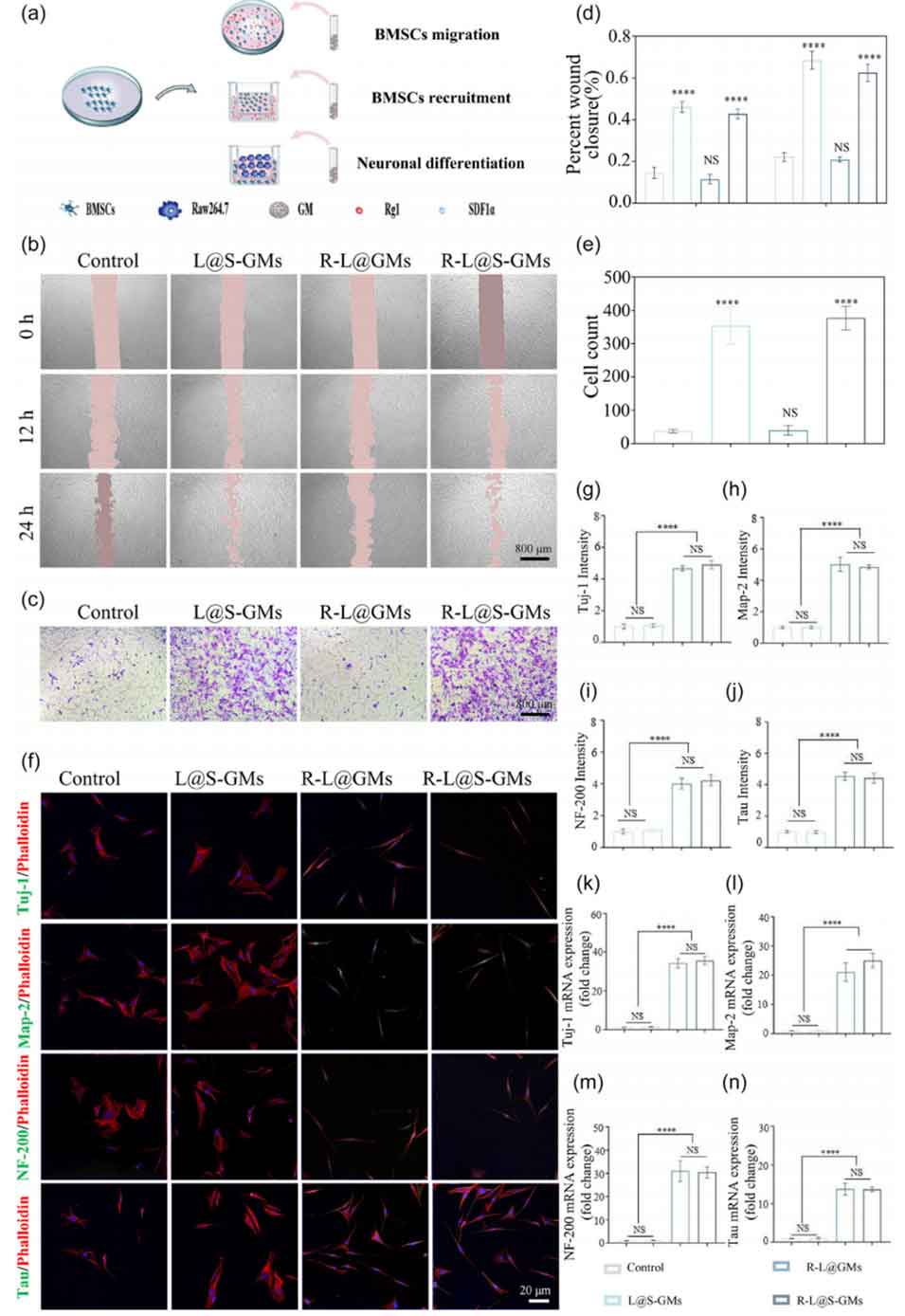
图4 L@GMs 促进细胞迁移、招募及向神经元分化。 (a) L@GM 在体外促进骨髓间充质干细胞(BMSCs)迁移、招募和向神经元分化的示意图。(b) 分别在 0、12 和 24 小时处划痕线的代表性光学显微镜图像。(c) 显示从上室迁移的细胞的代表性光学显微镜图像。(d) 通过 Image J 分析的伤口愈合百分比。(e) 培养 24 小时后迁移细胞的数量。(f) Tuj-1、Map-2、NF-200 和 Tau 的免疫荧光染色图像,以及 (g–j) 相应的荧光半定量分析。(k–n) Tuj-1、Map-2、NF-200 和 Tau 的 mRNA 表达分析。n = 3,当空白组与其他组对比时:****p < 0.0001,NS 表示无显著差异。
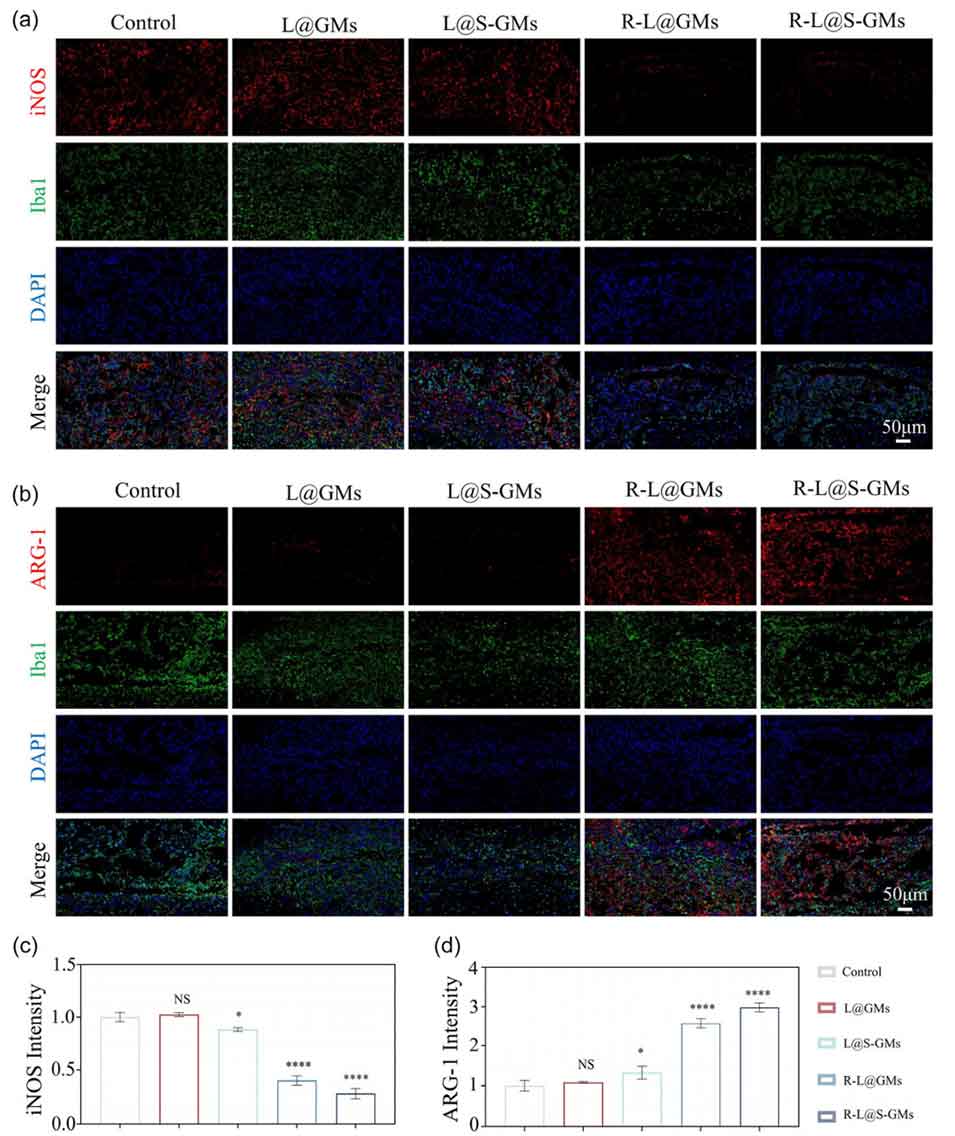
图5 体内术后 7 天免疫细胞的表型鉴定。 (a) 巨噬细胞标记物 Iba1(绿色)和 M1 型巨噬细胞标记物 iNOS(红色)的免疫荧光染色,以及 (c) 其光密度定量分析。(b) 巨噬细胞标记物 Iba1(绿色)和 M2 型巨噬细胞标记物 ARG-1(红色)的免疫荧光染色,以及 (d) 其光密度定量分析。n = 3,当空白组与其他组对比时:*p < 0.05, ***p < 0.001, ****p < 0.0001,NS 表示无显著差异。
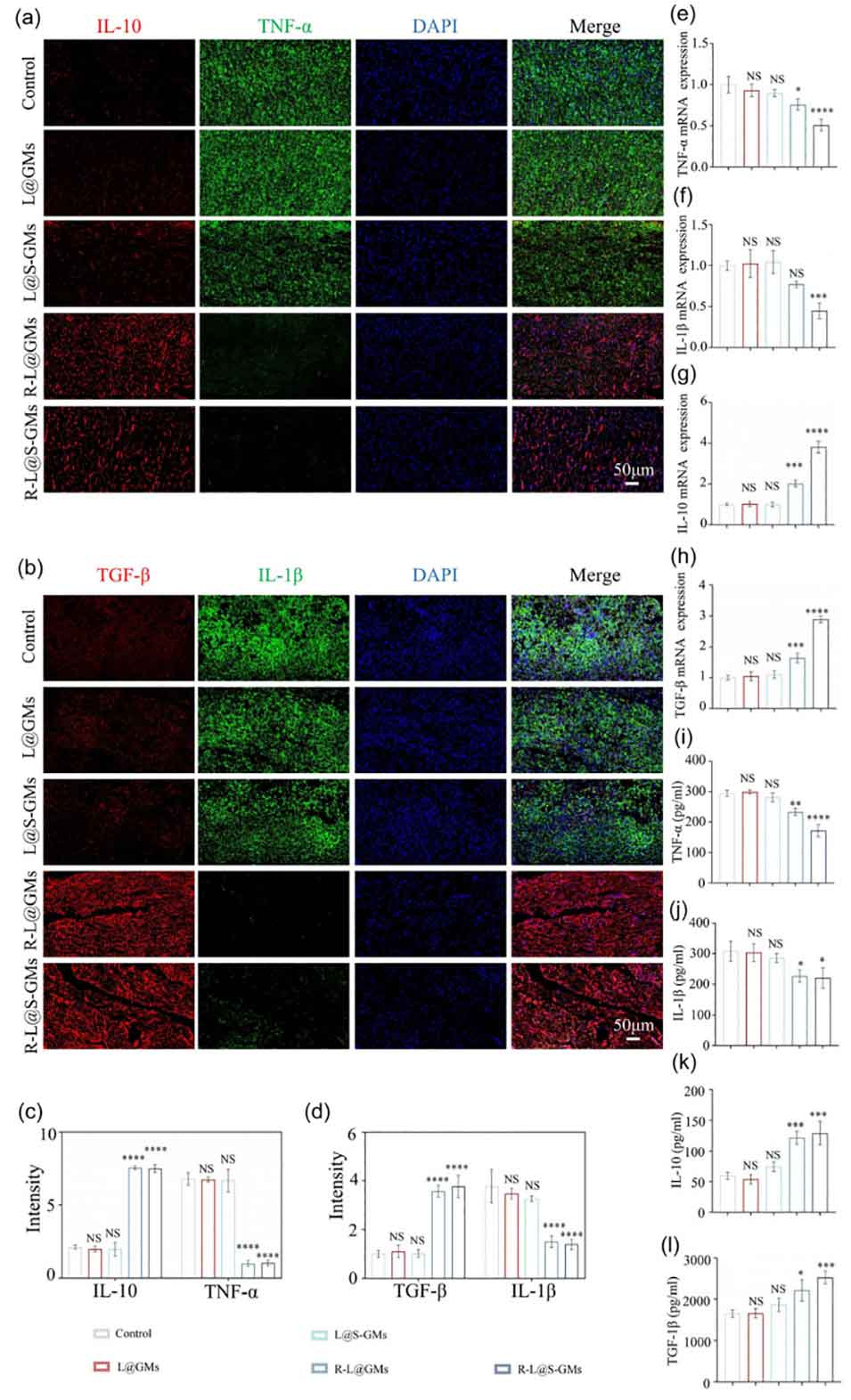
图6 术后 7 天炎症调节评估。 (a) IL-10、TNF-α 和 (b) TGF-β、IL-1β 的免疫荧光双标染色。对 (c) IL-10 和 TNF-α 免疫荧光,以及 (d) TGF-β 和 IL-1β 免疫荧光进行定量分析。通过 qRT-PCR 评估脊髓标本中 (e) TNF-α、(f) IL-1β、(g) IL-10 和 (h) TGF-β 的基因表达水平。通过 ELISA 评估血清中 (i) TNF-α、(j) IL-1β、(k) IL-10 和 (l) TGF-β 的水平。n = 3,当空白组与其他组对比时:*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001,NS 表示无显著差异。
0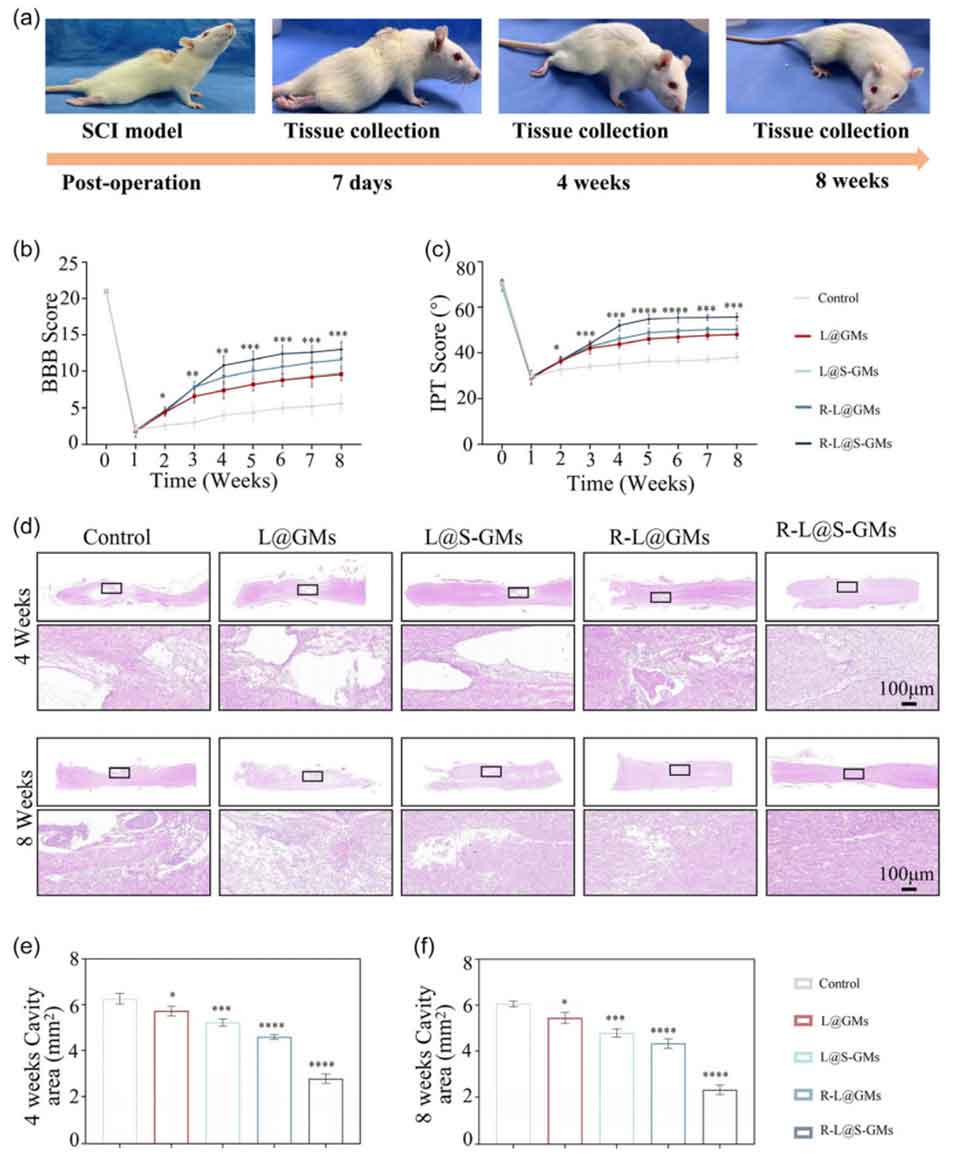
图7 脊髓标本 H&E 染色及运动功能评分。 (a) 动物实验和组织收集时间轴照片。(b) 通过 BBB 评分和 (c) 大鼠倾斜板试验(IPT)评分评估下肢运动功能恢复情况。(d) 分别在术后 4 周和 8 周对大鼠脊髓进行 H&E 染色。计算术后 (e) 4 周和 (f) 8 周的脊髓空洞面积。n = 3,当空白组与其他组对比时:*p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。
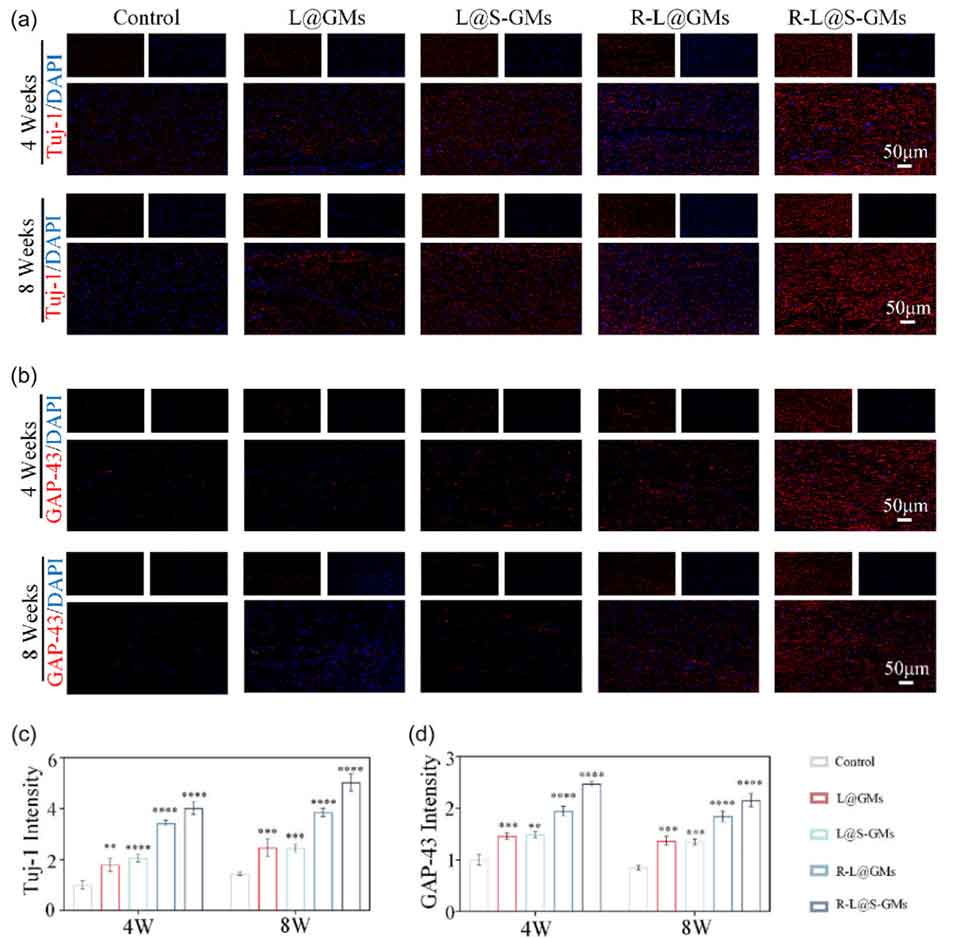
图8 神经元细胞和轴突的免疫荧光染色。 (a) 神经元细胞的免疫荧光染色,以及 (c) 使用 Tuj-1 光密度进行的定量分析。(b) 轴突的免疫荧光染色,以及 (d) 使用 GAP-43 光密度进行的定量分析。n = 3,当空白组与其他组对比时:**p < 0.01, ***p < 0.001, ****p < 0.0001。
论文链接:https://doi.org/10.1002/sstr.202500875
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














