
导读:
微凝胶是局部药物递送的理想载体,但疏水性药物与亲水性网络之间的兼容性较差,限制了其载药量并导致药物释放不可控。近期,华中科技大学李威教授课题组提出利用微流控辅助受限反溶剂沉淀技术,将疏水性药物高效包裹进亲水性微凝胶的新策略。该方法通过在微流控液滴内部触发快速的溶剂交换,使药物在聚合物凝胶化前实现原位重结晶,从而克服了疏水药物与亲水网络不兼容导致的载药量低和爆发释放等难题。实验证实,这种工艺不仅能将载药量提升至传统方法的五倍以上,还能通过结晶滞留效应实现药物的持续释放。
研究团队进一步开发了色氨酸接枝壳聚糖基质以增强药物-基质相互作用,在小鼠模型中成功缓解了痛风性关节炎的炎症症状并促进了关节功能恢复。总之,这项研究为治疗炎症和退行性疾病提供了一个通用的、高载药量且长效的局部递药平台。相关成果以“Confined antisolvent precipitation enables efficient drug encapsulation in microgels for effective gouty arthritis therapy”为题目,发表在期刊《Chemical Engineering Journal》上。
本文要点:
1. 核心技术策略
受限反溶剂沉淀:利用三通道微流控系统,使溶解在有机溶剂中的疏水性药物在与水相聚合物溶液接触时,在微滴内部发生快速过饱和、成核和原位结晶。
同步成胶捕获:药物结晶发生后,微滴随之发生凝胶化,将药物晶体封存在聚合物网络中,形成“药物晶体保留效应”。
2. 性能优势
高载药量与高效率:与传统方法相比,该策略使微凝胶的载药量提高了5倍以上。
延缓释放:药物以晶体形式存在,必须先溶解才能扩散,从而有效减缓了初始突释并延长了释放时间。
广泛适用性:该方法适用于多种快速成胶的亲水性聚合物系统(如天然的脱乙酰壳聚糖和合成的聚乙二醇二丙烯酸酯)以及多种疏水性药物。
3. 基质改性优化
研究开发了色氨酸接枝的脱乙酰壳聚糖 (CST)作为基质,通过 π-π 堆积和疏水相互作用进一步增强药物与基质的结合。
这种改性显著延长了姜黄素 (CUR) 的释放时间,在体外可持续释放超过3天。
4. 治疗应用与效果
痛风性关节炎治疗:在小鼠模型中,载姜黄素微凝胶 (CUR@CST) 展现出卓越的疗效。
免疫调节:能够诱导巨噬细胞向抗炎的 M2 型极化,有效降低促炎细胞因子(如 IL-1β、TNF-α和 IL-6)水平,并抑制活性氧 (ROS) 产生。
功能恢复:治疗显著减轻了关节肿胀,降低了血清尿酸水平,并实现了关节功能的恢复(如步态改善)。
5. 结论
该研究建立了一个通用的平台,用于制造高载药量、长效的微凝胶,为治疗炎症性和退行性疾病(如痛风性关节炎)提供了新的策略。
受限反溶剂沉淀策略之所以能将疏水性药物的载药量提高5倍以上,主要归因于其独特的物理化学机制和微流控技术的精确控制。具体如下:
1. 克服热力学不相容性
疏水性药物与亲水性聚合物网络(如脱乙酰壳聚糖或 PEGDA)在分子水平上具有天然的不相容性,缺乏氢键或 π-π 堆积等相互作用。在传统方法中,这种不相容性会导致药物分子在成胶过程中逃逸出微滴,或被限制在微滴表面,导致载药量极低。而该策略通过诱导药物原位结晶,将溶解态的药物转化为固态晶体,从而避开了分子层面的不相容性障碍。
2. 利用“药物晶体保留效应” (Drug Crystalline Retention Effect)
在该微流控系统中,溶解在有机溶剂(如 DMSO)中的药物在与水相聚合物溶液接触时,会由于溶解度骤降而发生快速过饱和、成核和沉淀。
快速捕获:这种沉淀发生在微凝胶完全成胶之前。
防止扩散:相比于分子态药物容易向外部油相扩散或逃逸,形成的药物晶体体积较大且处于固态,被机械地“锁”在正在形成的聚合物网络中。
3. 微环境的受限控制
与传统的本体沉淀法相比,微流控液滴提供了一个受限的微环境:
抑制无序生长:在微小的液滴内部,药物的成核速度极快,但液滴边界限制了晶体的无序生长和聚集,确保了药物能均匀分布在微凝胶内部。
高度单分散性:微流控技术确保了每个液滴的大小和成分分布高度一致,从而实现了极高的封装效率和批次间的稳定性。
4. 同步沉淀与成胶过程
传统方法往往无法精确控制药物封装与凝胶化的时间点。而该三通道微流控系统实现了沉淀与成胶的精确同步:
在液滴形成的一瞬间触发反溶剂效应(沉淀),随后紧接着发生光聚合或化学交联(成胶)。
实验对比显示,如果不使用这种反溶剂效应(如对照组 PEGDA(D),其内外相均使用同种溶剂),药物会在成胶前扩散流失,导致载药量极低。
总体而言,这一策略通过在微滴内将药物“由液转固”并快速用聚合物网络“封锁”,有效地解决了疏水药物在亲水基质中载药难的问题,在多种药物(如 FEN、IBU、MPS 和 CUR)中均验证了这种平均 5 倍以上的性能提升。
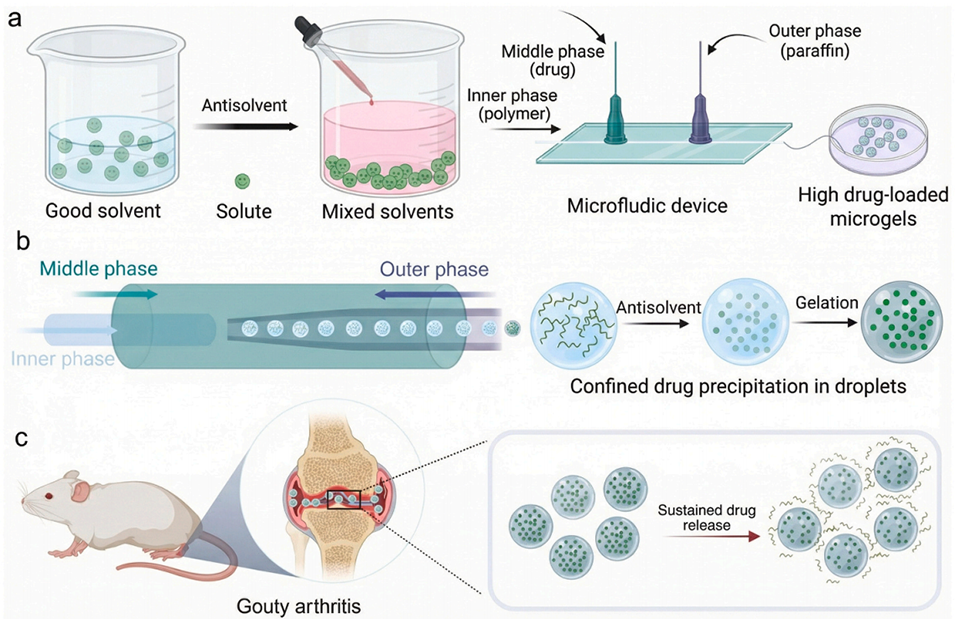
Scheme 1:微流控辅助受限反溶剂沉淀策略制备高载药微凝胶及其在痛风性关节炎中的治疗应用示意图。(a) 良溶剂与不良溶剂间溶质溶解度差异原理,以及用于液滴生成以制备载药微凝胶的微流控装置结构;(b) 反溶剂效应诱导疏水药物在乳液液滴内析出,在微凝胶基质中形成药物晶体;(c) 将高载药微凝胶注射至炎症关节,通过结晶滞留效应实现药物长效释放,进而获得优异治疗效果。
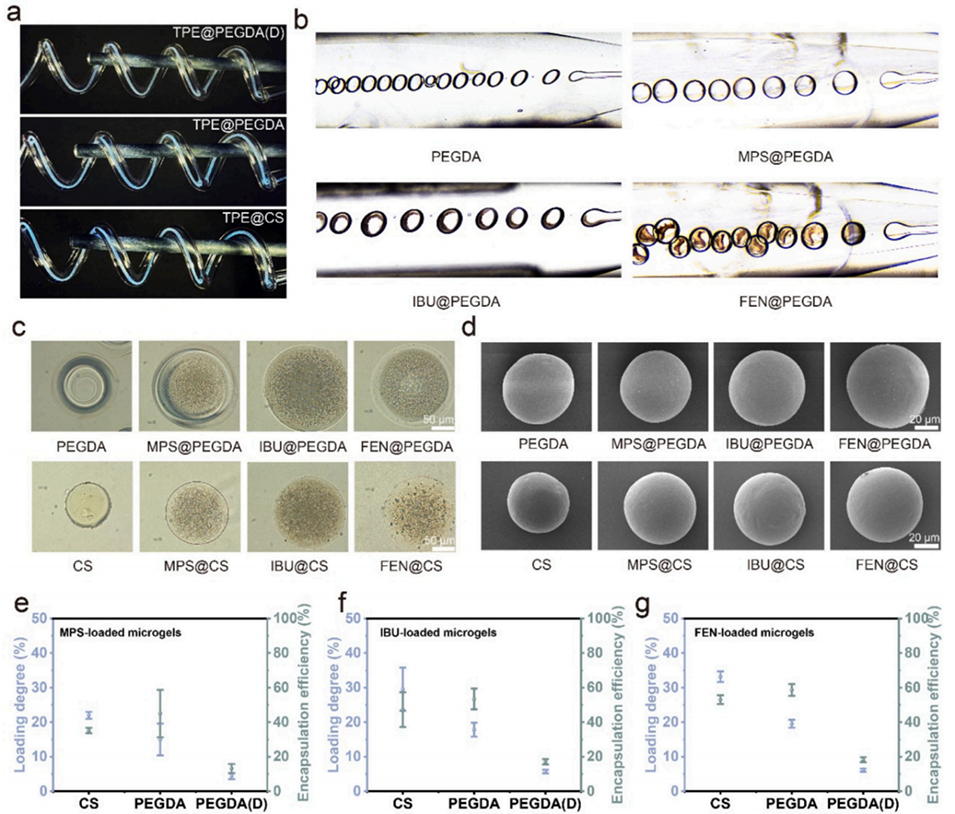
图1 疏水药物载药微凝胶的制备与表征。(a) 基于微流控体系,通过反溶剂效应验证疏水四苯乙烯(TPE)分子在聚乙二醇二丙烯酸酯(PEGDA)微凝胶内的析出行为;(b) 含 PEGDA 与多种疏水药物(甲泼尼龙 MPS、布洛芬 IBU、非诺贝特 FEN)的单分散乳液液滴光学显微镜图;(c) 微凝胶光学显微镜图;(d) 微凝胶扫描电子显微镜(SEM)图;(e–g) 分别负载 (e) 甲泼尼龙、(f) 布洛芬、(g) 非诺贝特的微凝胶载药量与包封率(n=3)。
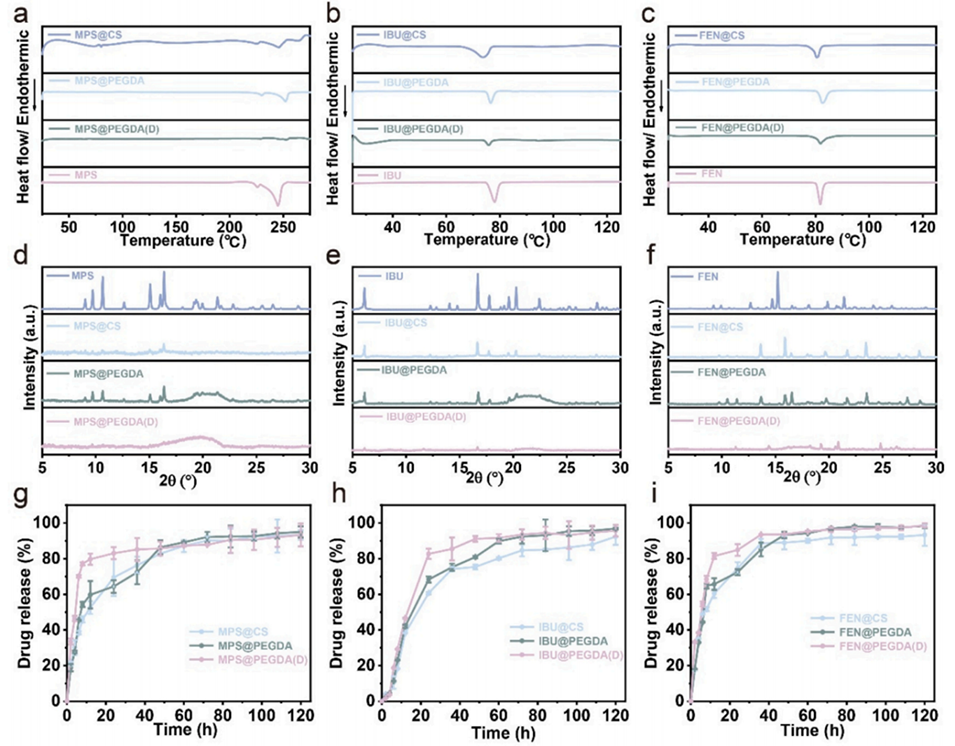
图2 载药微凝胶的理化性质与释放曲线。(a) 甲泼尼龙及甲泼尼龙载药微凝胶、(b) 布洛芬及布洛芬载药微凝胶、(c) 非诺贝特及非诺贝特载药微凝胶的差示扫描量热(DSC)曲线;(d) 甲泼尼龙及甲泼尼龙载药微凝胶、(e) 布洛芬及布洛芬载药微凝胶、(f) 非诺贝特及非诺贝特载药微凝胶的 X 射线衍射图谱;(g–i) 微凝胶在磷酸盐缓冲液(PBS)中的药物累积释放曲线(n=3)。
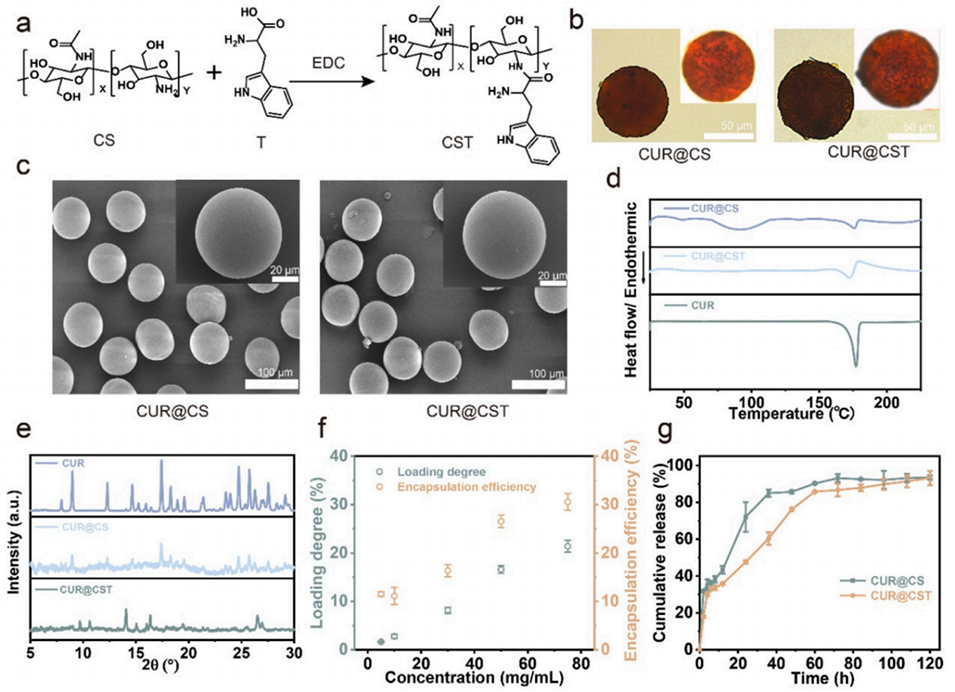
图3 姜黄素载药微凝胶的理化性质与释放曲线。(a) 疏水改性壳聚糖(CST)的合成路线;(b) 姜黄素 @壳聚糖(CUR@CS)与姜黄素 @疏水改性壳聚糖(CUR@CST)微凝胶光学图;(c) CUR@CS 与 CUR@CST 微凝胶扫描电子显微镜图;(d) 姜黄素及姜黄素载药微凝胶的差示扫描量热曲线与 (e) X 射线衍射图谱;(f) 不同药物浓度下 CST 微凝胶的载药量与包封率(n=3);(g) 姜黄素载药微凝胶的体外释放曲线(n=3)。
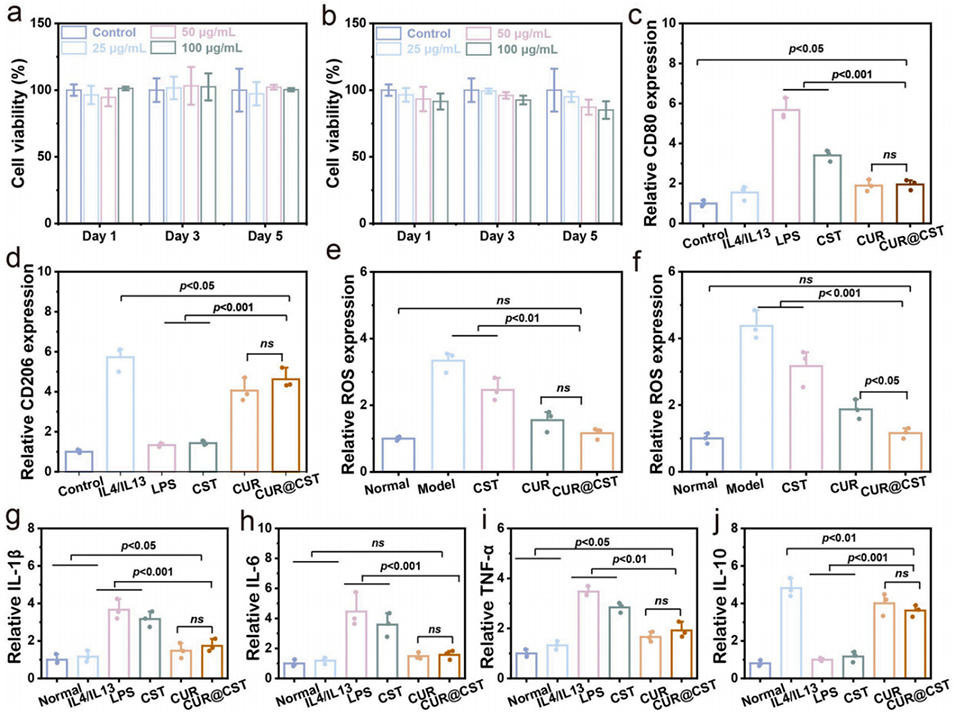
图4 CUR@CST 微凝胶对脂多糖(LPS)诱导巨噬细胞的抗炎作用。(a) 不同浓度 CST、(b) 不同浓度 CUR@CST 微凝胶与巨噬细胞共培养 1、3、5 天的细胞存活率;共培养 1 天后,巨噬细胞 (c) M1 型标志物 CD80、(d) M2 型标志物 CD206 的相对表达量;处理 (e) 1 天、(f) 3 天后细胞内活性氧(ROS)水平;酶联免疫吸附测定(ELISA)检测培养上清中 (g) 白细胞介素 - 1β(IL-1β)、(h) 白细胞介素 - 6(IL-6)、(i) 肿瘤坏死因子 -α(TNF-α)、(j) 白细胞介素 - 10(IL-10)的细胞因子水平(n=3)。数据以相对分泌量表示,归一化为正常组(设为 1)。
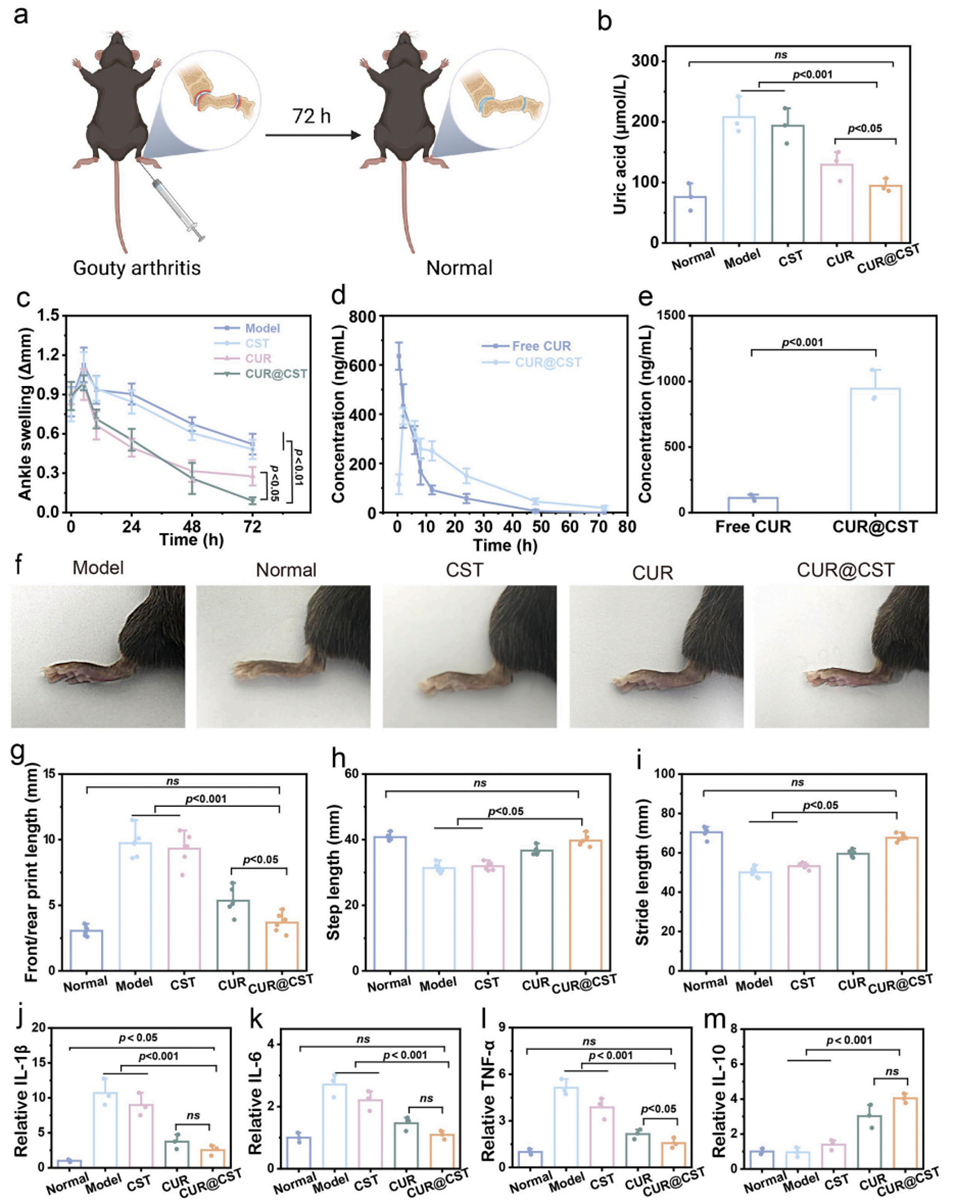
图5 CUR@CST 微凝胶在单钠尿酸盐(MSU)诱导的小鼠痛风性关节炎模型中的治疗效果评价。(a) 治疗方案示意图;(b) 治疗后血清尿酸水平;(c) 72 小时内踝关节肿胀程度定量分析;注射后 72 小时,(d) 血清药物浓度与 (e) 关节局部药物浓度;(f) 治疗 3 天后小鼠踝关节代表性照片;治疗 3 天后小鼠 (g) 前后爪印长度、(h) 步幅长度、(i) 步长;实时荧光定量 PCR(qPCR)检测踝关节组织中 (j) 白细胞介素 - 1β、(k) 白细胞介素 - 6、(l) 肿瘤坏死因子 -α、(m) 白细胞介素 - 10 的 mRNA 相对表达量(n=3)。
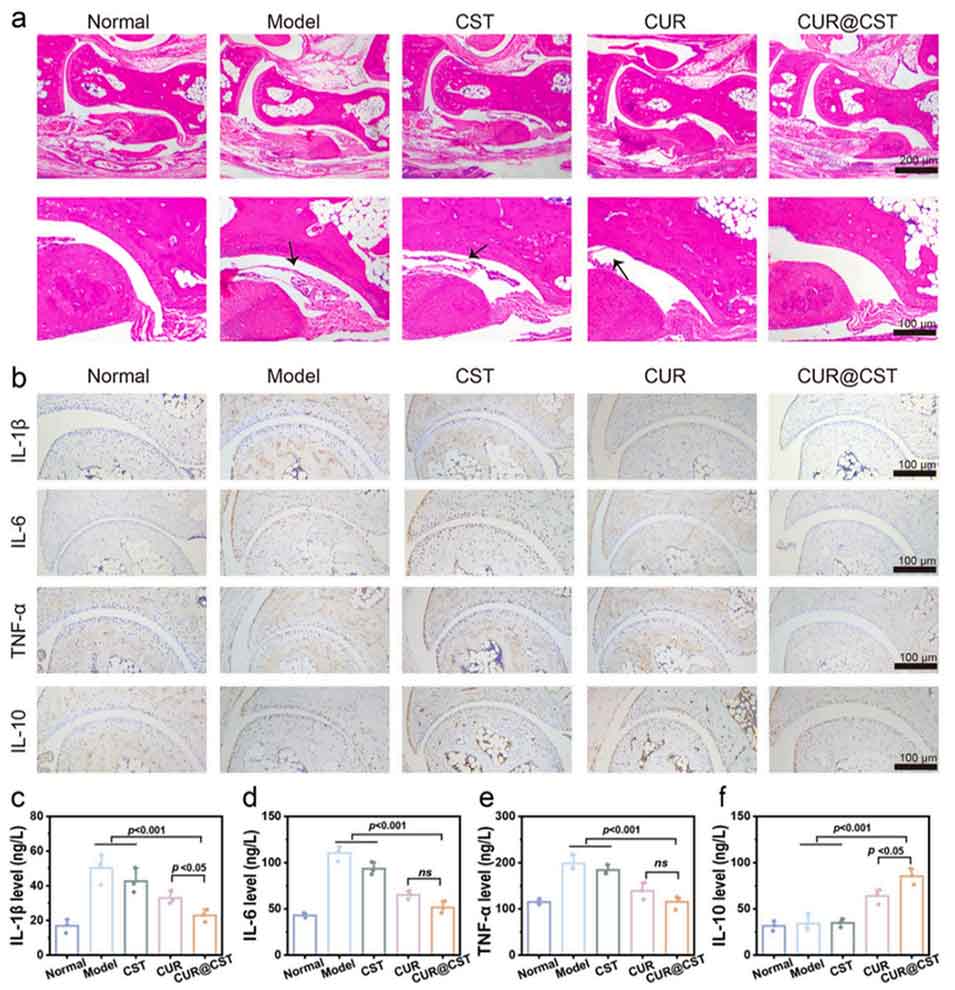
图6 治疗后踝关节组织学与细胞因子分析。(a) 治疗 3 天后踝关节组织代表性苏木精 - 伊红(H&E)染色图(箭头指示炎性细胞浸润);(b) 治疗后踝关节组织中肿瘤坏死因子 -α、白细胞介素 - 1β、白细胞介素 - 10、白细胞介素 - 6 的免疫组化染色图;酶联免疫吸附测定(ELISA)检测血清中 (c) 白细胞介素 - 1、(d) 白细胞介素 - 6、(e) 肿瘤坏死因子 -α、(f) 白细胞介素 - 10 水平(n=3)。
论文链接:https://doi.org/10.1016/j.cej.2026.173300
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














