溃疡性结肠炎(UC)是反复发作的难治性炎症性肠病,核心病理特征为肠道黏膜屏障损伤、免疫紊乱、肠道菌群失衡,伴随活性氧(ROS)过量堆积引发的持续氧化应激;临床常用5-氨基水杨酸、糖皮质激素、生物制剂等药物,存在全身毒性、靶向性差、长期使用副作用显著等缺陷,因此亟需开发兼具口服稳定性、结肠靶向性、多靶点调控能力的新型递送系统。

近期,中国药科大学邓大伟教授团队受“西瓜籽与西瓜”的概念启发,开发了一种名为QC@HACM的创新型“西瓜样”微/纳复合递药系统,旨在通过多维度干预策略实现溃疡性结肠炎(UC)的高效治疗。该治疗体系由两大核心部分构成:外部起保护作用的HACM水凝胶外壳,以及内部发挥治疗作用的Qu@CSCP纳米粒内核;二者协同构建了兼具优异结肠靶向能力与多级释药性能的递药平台。相关研究以“A Watermelon-Like Micro/Nano Hierarchical Delivery Platform for Ulcerative Colitis by Regulating Redox Homeostasis and Remodeling Gut Microbiota”为题目,发表在期刊《Advanced Healthcare Materials》上。
研究亮点:
首创西瓜状微纳分级核-壳仿生递送系统,适配溃疡性结肠炎口服靶向治疗。
采用微流控一步法制备,实现载体高单分散性与结构精准可控。
构建双重靶向+氧化响应释药机制,大幅提升炎症结肠药物富集与滞留。
实现抗氧化、抗炎、黏膜修复、菌群重塑多维度协同治疗。
天然多糖载体搭载天然活性成分,生物相容性优异、毒副作用低。
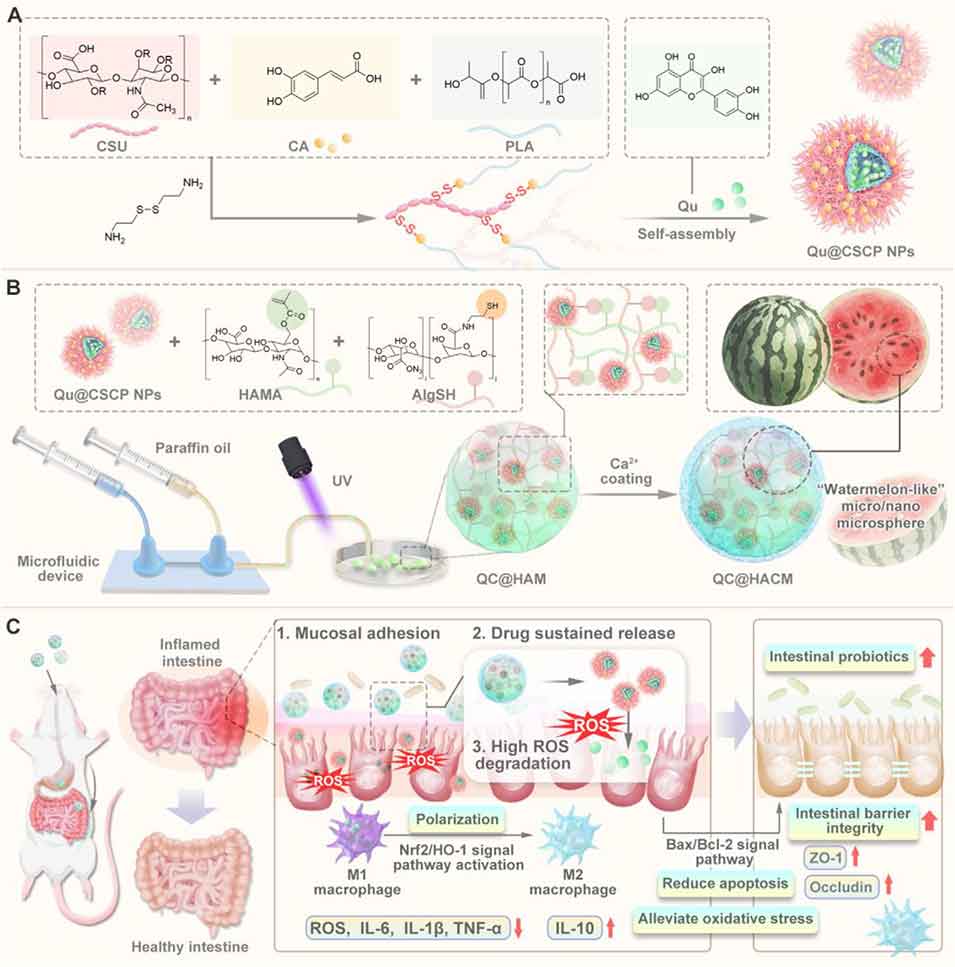
方案1 用于溃疡性结肠炎(UC)联合治疗的 “西瓜样” 分级靶向微球示意图。(A) Qu@CSCP 纳米平台的制备流程;(B) 微/纳复合水凝胶微球(QC@HACM)的制备过程;(C) 口服 QC@HACM 通过清除活性氧、发挥抗炎作用、抑制细胞凋亡、修复肠道屏障功能及调控肠道菌群,实现 UC 靶向治疗的作用机制。
受“西瓜籽与西瓜”的结构启发,该研究设计了一种具有“西瓜样”构型的仿生微/纳多功能水凝胶微球体系,专为溃疡性结肠炎(UC)的靶向抗炎治疗与协同分步释药而构建(方案1)。
该分级结构微球通过微流控技术高效制备,具有典型的核壳结构。如方案1A、1B所示,“西瓜样”外壳由透明质酸(HA)与海藻酸钙(Alg/Ca)经序贯矿化形成的微球构成,而核心的“西瓜籽”则为抗氧化纳米颗粒Qu@CSCP——该纳米颗粒通过将抗氧化剂槲皮素(Qu)负载于硫酸软骨素(CSU)与咖啡酸(CA)构建的载体基质中制得。海藻酸盐中的钙离子交联可增强水凝胶网络的机械强度,从而为Qu@CSCP纳米颗粒提供保护,保障其在胃部降解环境中仍能维持长效生物活性。CSU是一种在生理pH条件下带有负电硫酸基团的天然多糖,可与炎症微环境中大量存在的阳离子物质发生静电结合;其丰富的功能基团还可实现表面修饰,是极具潜力的靶向给药载体平台。
在葡聚糖硫酸钠(DSS)诱导的UC小鼠模型中,最终制备得到的微/纳多功能水凝胶微球(QC@HACM)展现出与“西瓜籽-西瓜壳”结构相契合的分级靶向能力(方案1C)。该微球外壳整合了两大创新作用机制:一是透明质酸介导的CD44受体主动靶向作用,二是巯基-黏蛋白二硫键锚定作用。这种双靶向策略显著提升了Qu@CSCP纳米颗粒在结肠部位的滞留效果。此外,HACM水凝胶基质还具有生物黏附的“创可贴”效应,可增强黏膜黏附能力,恢复紧密连接相关蛋白的表达,重塑肠道菌群屏障功能。
Qu@CSCP纳米颗粒在病灶部位释放后,可通过调控多条信号通路,清除UC病灶处的活性氧(ROS),抑制肠上皮细胞凋亡,恢复肠道屏障的机械完整性,并促进巨噬细胞向M2型极化,进而调控肠道氧化还原稳态。总体而言,QC@HACM通过微/纳组分的功能整合与协同调控,在DSS诱导的UC模型中实现了显著的治疗效果。
综上,该研究提出了一种“西瓜样”仿生微/纳递药系统,构建了以多维度调控与分级释药协同整合为核心的天然产物递送新策略,为实现UC的高效、长效治疗提供了极具前景的应用范式。
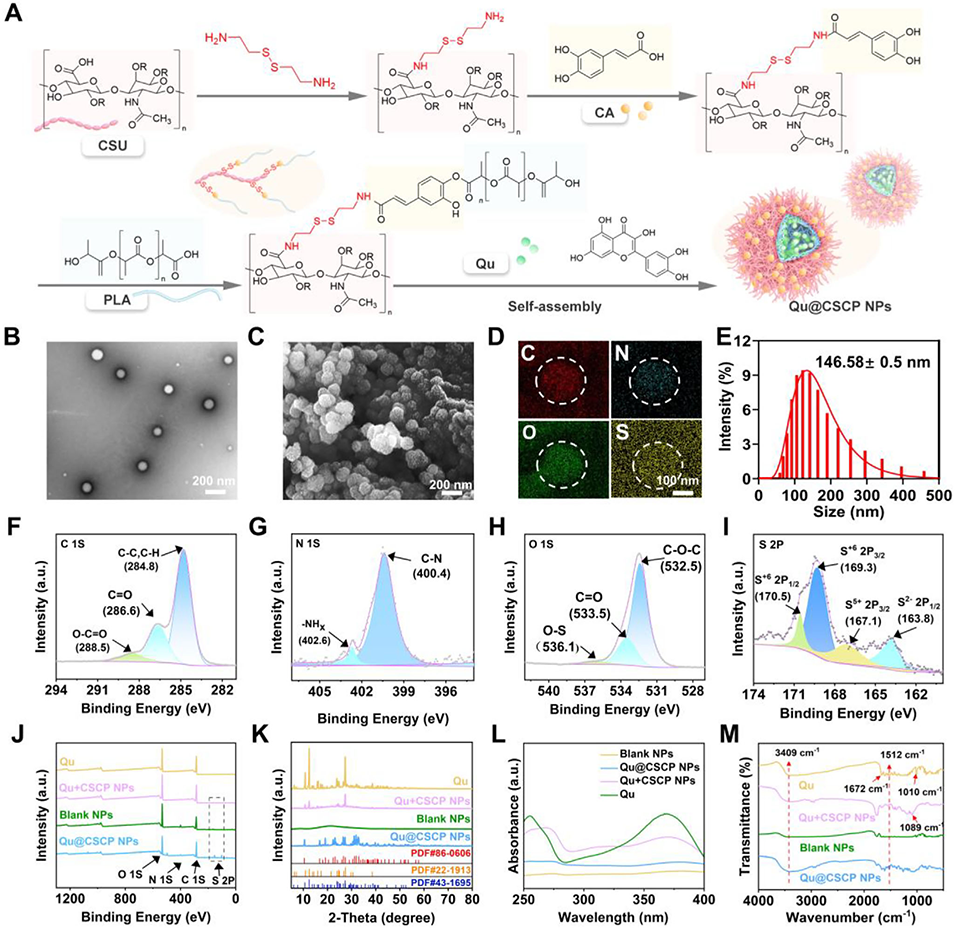
图1 Qu@CSCP 纳米粒的合成与表征。(A) Qu@CSCP 的合成路线;(B,C) Qu@CSCP 的透射电子显微镜(TEM)与扫描电子显微镜(SEM)图像;(D) Qu@CSCP 的 X 射线能谱(EDS)元素 Mapping 图;(E) Qu@CSCP 的粒径分布;(F-I) Qu@CSCP 的 C 1s、N 1s、O 1s、S 2p 轨道 X 射线光电子能谱(XPS),(J) Qu@CSCP 的 XPS 全谱;(K-M) Qu@CSCP 的结构与组成表征:(K) X 射线衍射(XRD)图谱、(L) 紫外-可见吸收光谱、(M) 傅里叶变换红外光谱(FTIR)(n=3)。
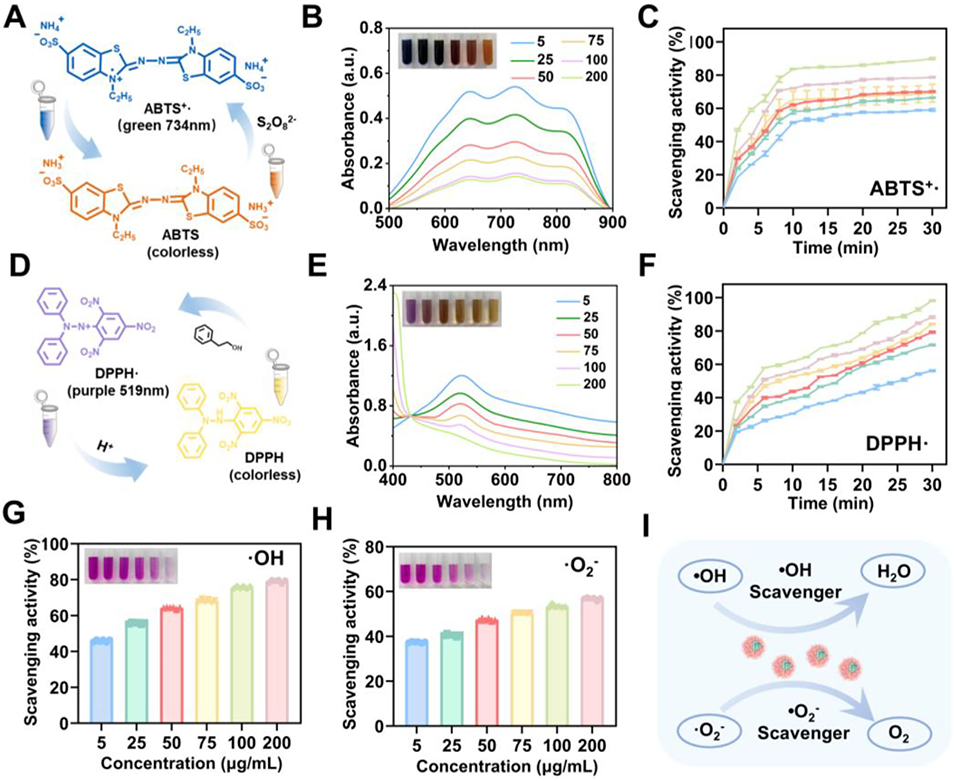
图2 Qu@CSCP 纳米粒的抗氧化能力。(A,D) Qu@CSCP 清除 ABTS+・(A) 与 DPPH・(D) 自由基的原理示意图;(B,E) 不同浓度 Qu@CSCP 处理后,ABTS+・(B) 与 DPPH・(E) 溶液的紫外-可见吸收光谱,插图为对应溶液的颜色变化,反映自由基清除程度;(C,F) 不同浓度 Qu@CSCP 在 pH 7.4 磷酸盐缓冲液(PBS)中清除 ABTS+・(C) 与 DPPH・(F) 的动力学曲线(n=3);(G,H) 不同浓度 Qu@CSCP 对羟基自由基(・OH)和超氧阴离子自由基(・O₂⁻)的清除能力;(I) Qu@CSCP 的抗氧化作用机制示意图(n=3)。
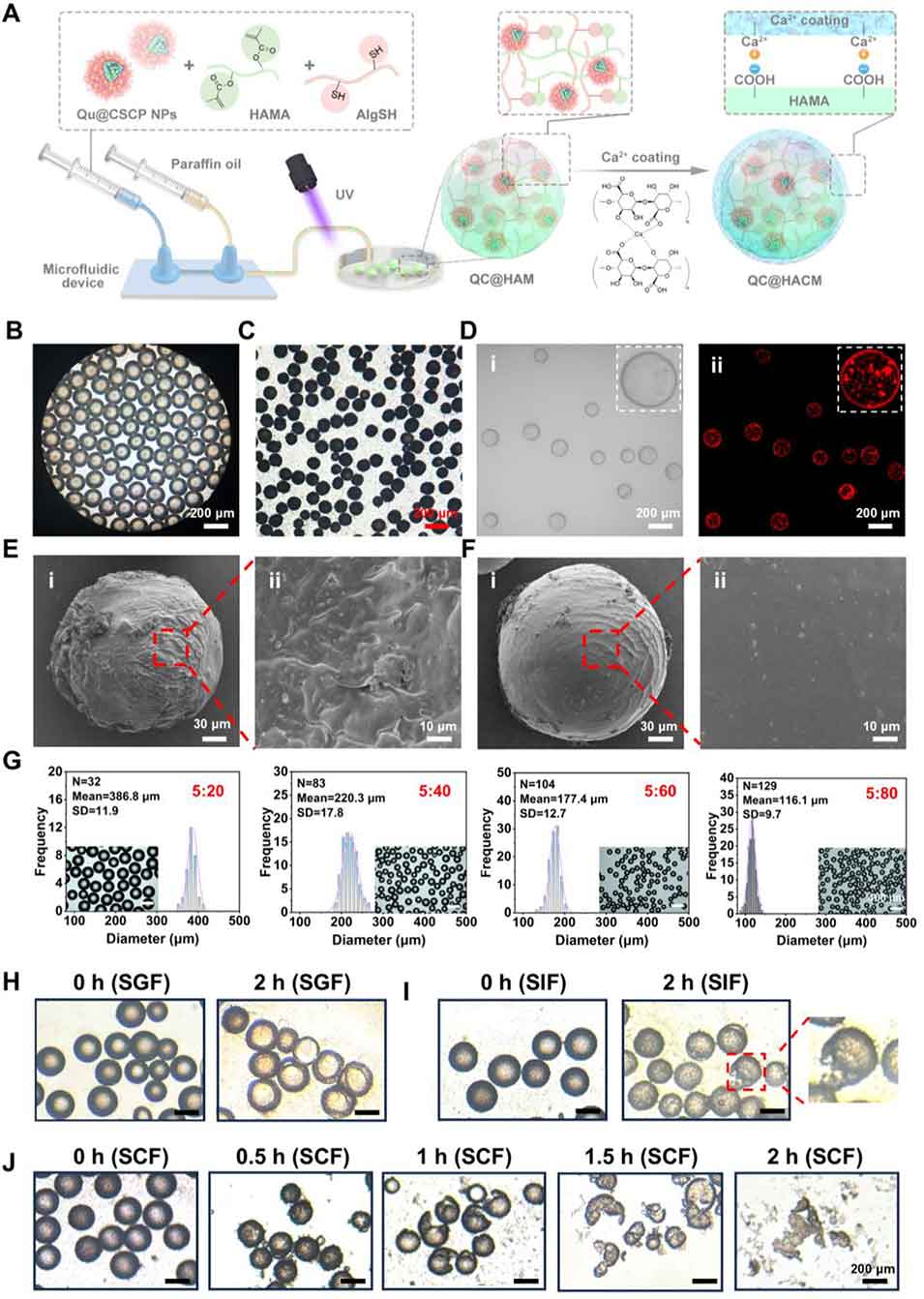
图3 微/纳复合水凝胶微球的制备与表征。(A) QC@HACM 的制备流程示意图;(B) QC@HACM 微球的光学显微镜图像;(C) 凝胶化后 QC@HACM 的显微镜图像;(D) QC@HACM 微球的激光共聚焦扫描显微镜(CLSM)图像;(E,F) 不同放大倍数下 QC@HAM 与 QC@HACM 微球的 SEM 图像,左右图比例尺分别为 30 µm 和 10 µm;(G) 明场显微镜下,不同内/外水相流速制备的 QC@HACM 的粒径统计分布及对应光学图像(n=3);(H-J) QC@HACM 分散于模拟胃液(SGF)(H)、模拟肠液(SIF)(I)、模拟结肠液(SCF)(J) 后的明场显微镜形貌观察结果。
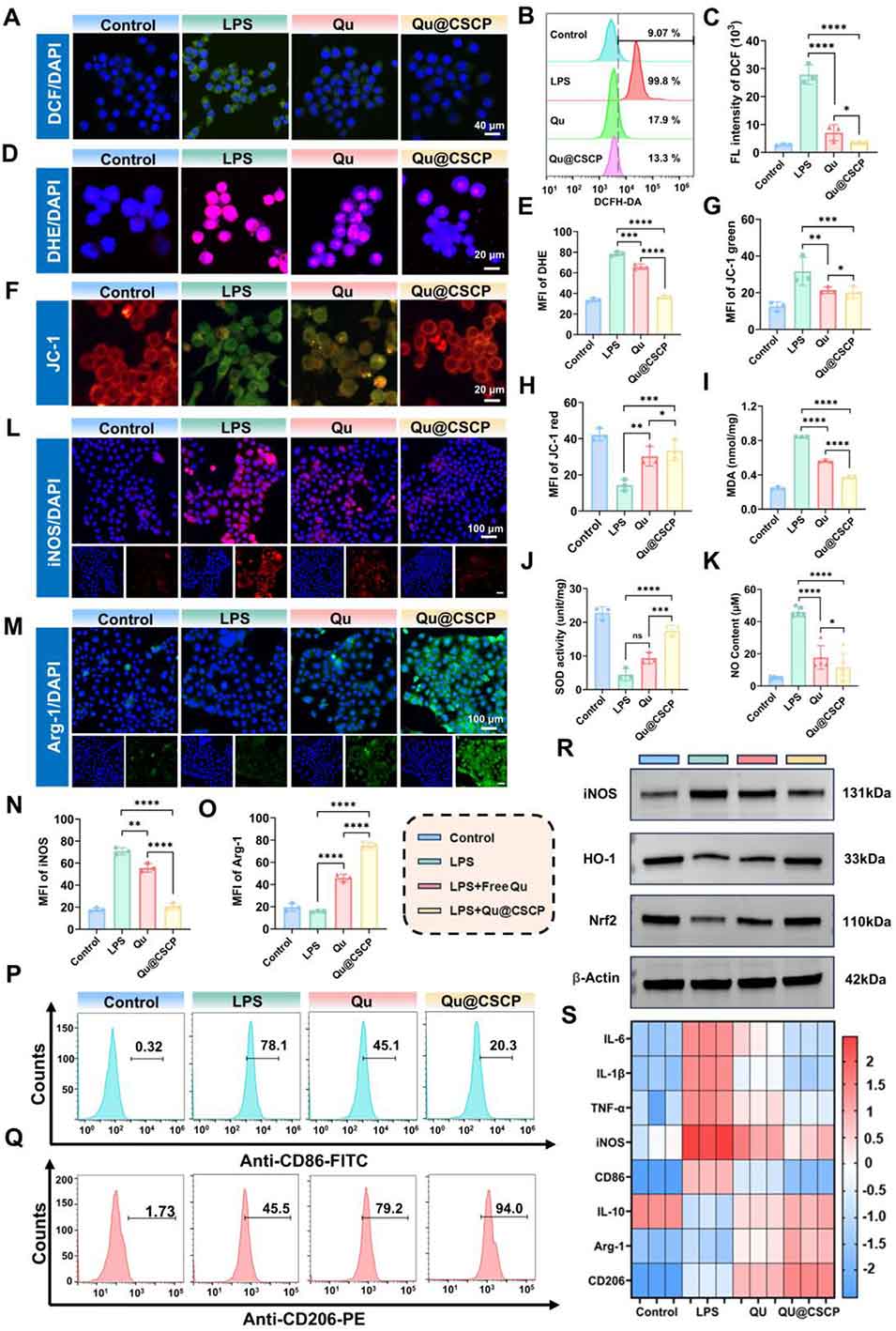
图4 Qu@CSCP 的体外抗氧化与抗炎活性。(A) 不同处理条件下,经 DCFH-DA 染色的 RAW 264.7 细胞的代表性共聚焦荧光图像;(B,C) 不同处理后 RAW 264.7 细胞内活性氧水平的流式细胞术分析结果;(D,E) 不同处理下,经二氢乙啶(DHE)染色的 RAW 264.7 细胞的荧光图像及半定量分析结果;(F-H) 不同处理后 RAW 264.7 细胞线粒体膜电位的 JC-1 染色图像及对应半定量分析结果;(I-K) 不同处理下 RAW 264.7 细胞中丙二醛(MDA)含量、超氧化物歧化酶(SOD)活性、一氧化氮(NO)水平的定量检测结果;(L-O) 不同处理后 RAW 264.7 细胞中 iNOS 与 Arg-1 表达的免疫荧光图像及半定量分析结果;(P,Q) 不同处理后 RAW 264.7 细胞中 M1 型(CD86⁺)、M2 型(CD206⁺)巨噬细胞比例的流式细胞术分析结果;(R) 不同处理后 RAW 264.7 细胞中 iNOS、HO-1、Nrf2 蛋白表达的蛋白免疫印迹(WB)分析结果;(S) 不同处理下 RAW 264.7 细胞中,促炎因子/标志物(IL-6、IL-1β、TNF-α、iNOS、CD86)与抗炎因子/标志物(IL-10、Arg-1、CD206)的 mRNA 相对表达水平热图。所有数据以均值 ± 标准差表示(n=3);*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
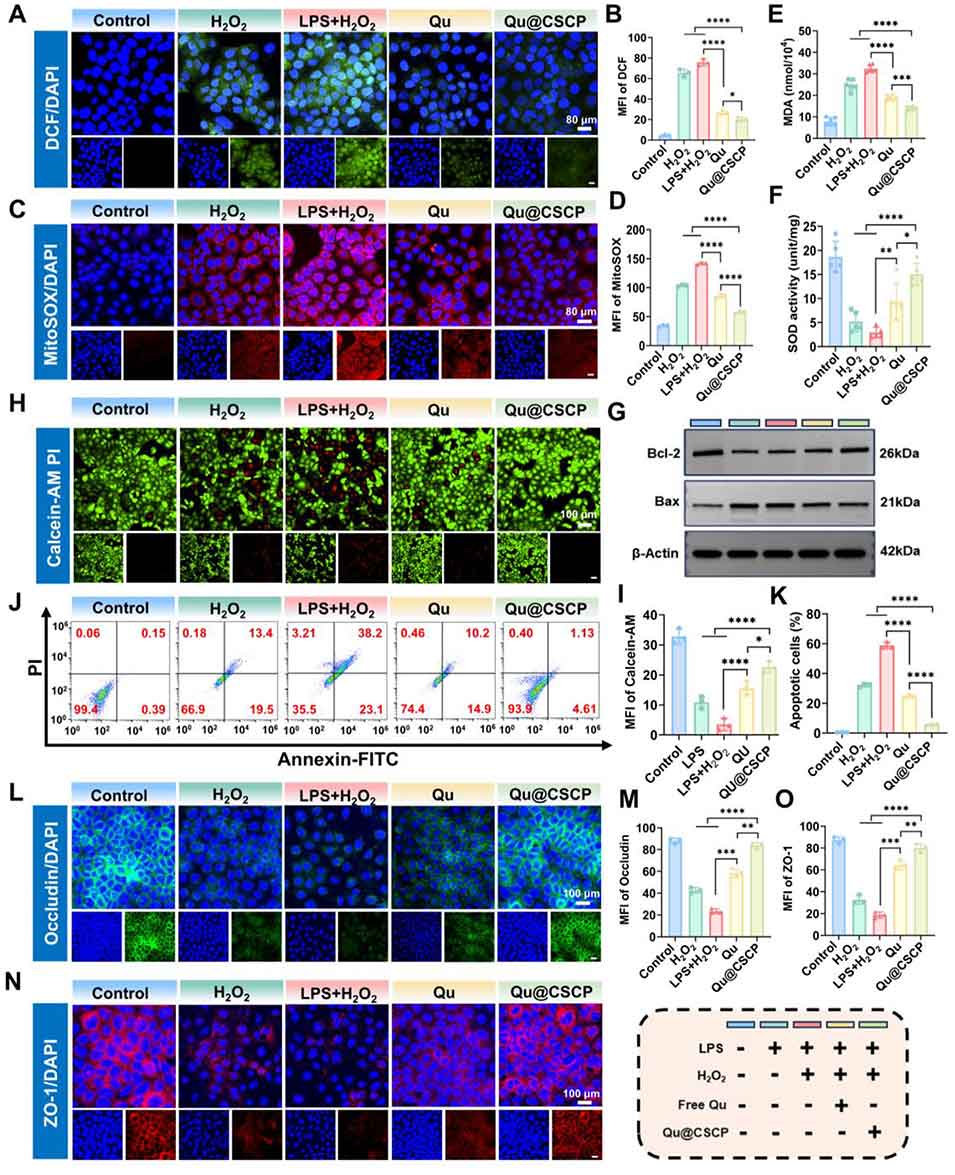
图5 Qu@CSCP 抑制细胞凋亡并促进肠上皮细胞修复。(A,B) 经 LPS 或 LPS+H₂O₂刺激的 Caco-2 细胞,经 DCFH-DA 染色后的代表性荧光图像、及胞内活性氧水平的定量分析结果;(C,D) 相同处理条件下,细胞线粒体超氧阴离子水平的荧光成像及半定量分析结果;(E,F) 不同处理下 Caco-2 细胞中 MDA 含量与 SOD 活性的定量检测结果;(G) 不同组别 Caco-2 细胞中 Bax、Bcl-2 蛋白表达的 WB 分析结果;(H-K) 经 LPS 或 LPS+H₂O₂处理后,Caco-2 细胞的钙黄绿素 - AM/PI(Calcein-AM/PI)活死染色荧光图像、及 Annexin V-FITC/PI 染色的流式细胞术凋亡定量结果;(L-O) 不同处理后 Caco-2 细胞中 Occludin 与 ZO-1 表达的免疫荧光图像及半定量分析结果。所有数据以均值 ± 标准差表示(n=3);*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
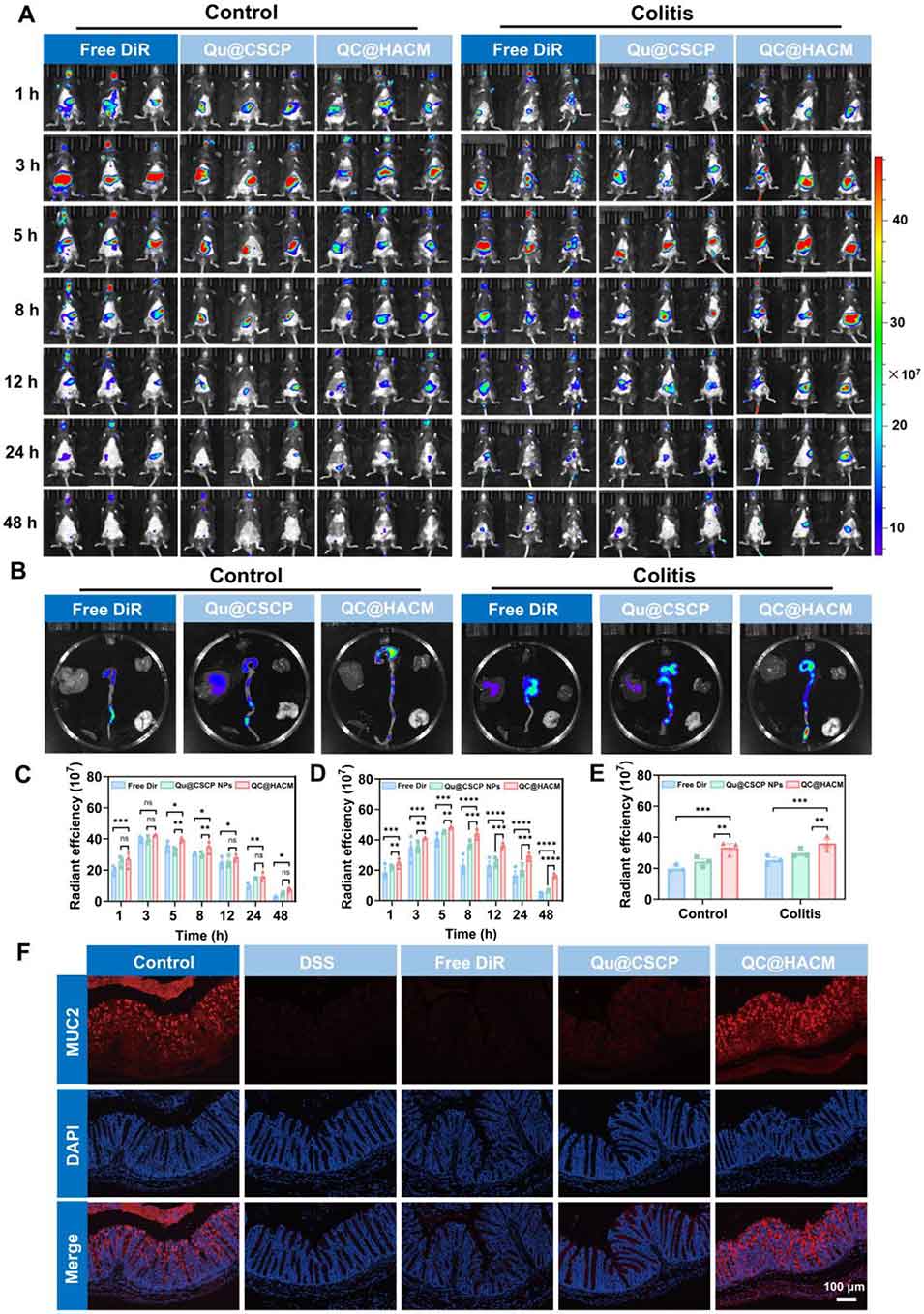
图6 QC@HACM 在炎症结肠中的双靶向与滞留能力。(A) 口服不同制剂后,正常小鼠与 DSS 结肠炎小鼠的时间序列体内荧光成像图;(B) 口服给药 48 h 后,离体结肠与主要脏器的荧光图像;(C) 不同制剂处理后,健康小鼠体内多个时间点的荧光定量检测结果;(D) 口服给药后不同时间点,结肠炎小鼠体内荧光强度的统计直方图;(E) 给药 48 h 后,正常小鼠与结肠炎小鼠结肠内荧光强度的定量分析结果;(F) 不同制剂处理的结肠炎小鼠结肠组织的免疫荧光染色结果。所有数据以均值 ± 标准差表示(n=3);*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
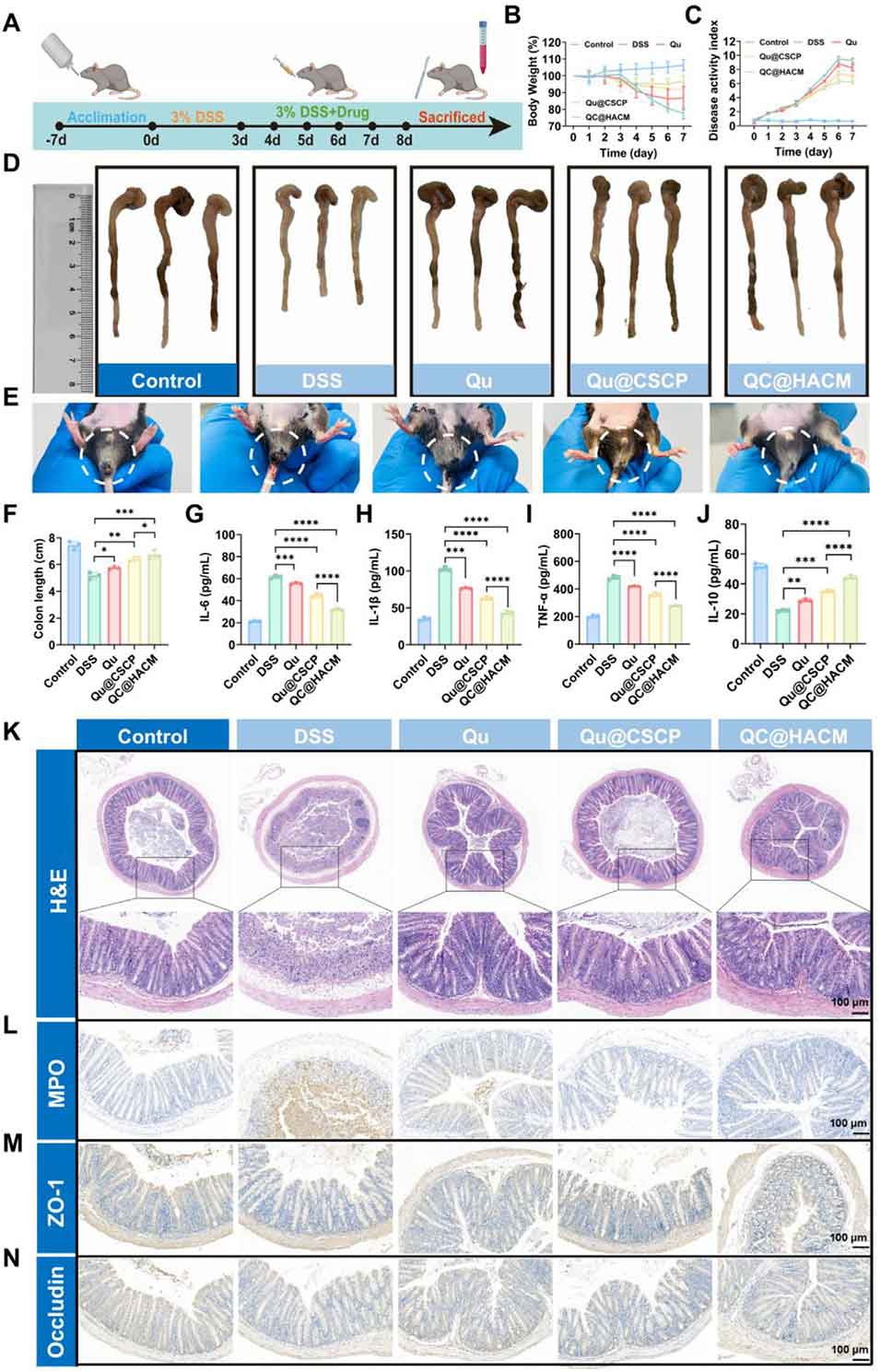
图7 QC@HACM 缓解 DSS 诱导结肠炎的炎症症状。(A) DSS 诱导结肠炎小鼠的治疗方案示意图;(B,C) 整个治疗周期内,不同组别小鼠的体重变化与疾病活动指数(DAI)评分变化;(D,E) 口服不同制剂后,小鼠结肠与肛周区域的大体照片;(F) 治疗后小鼠结肠长度的测量与统计分析结果;(G-J) 不同实验组小鼠结肠组织中,促炎细胞因子(IL-6、IL-1β、TNF-α)与抗炎细胞因子(IL-10)的定量分析结果;(K) 各组小鼠结肠组织的代表性苏木精-伊红(H&E)染色病理切片;(L) 小鼠结肠组织中髓过氧化物酶(MPO)的代表性免疫组化图像;(M,N) 不同处理组小鼠结肠组织中,紧密连接蛋白 ZO-1 与 Occludin 表达的免疫组化染色结果。所有数据以均值 ± 标准差表示(n=3);*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
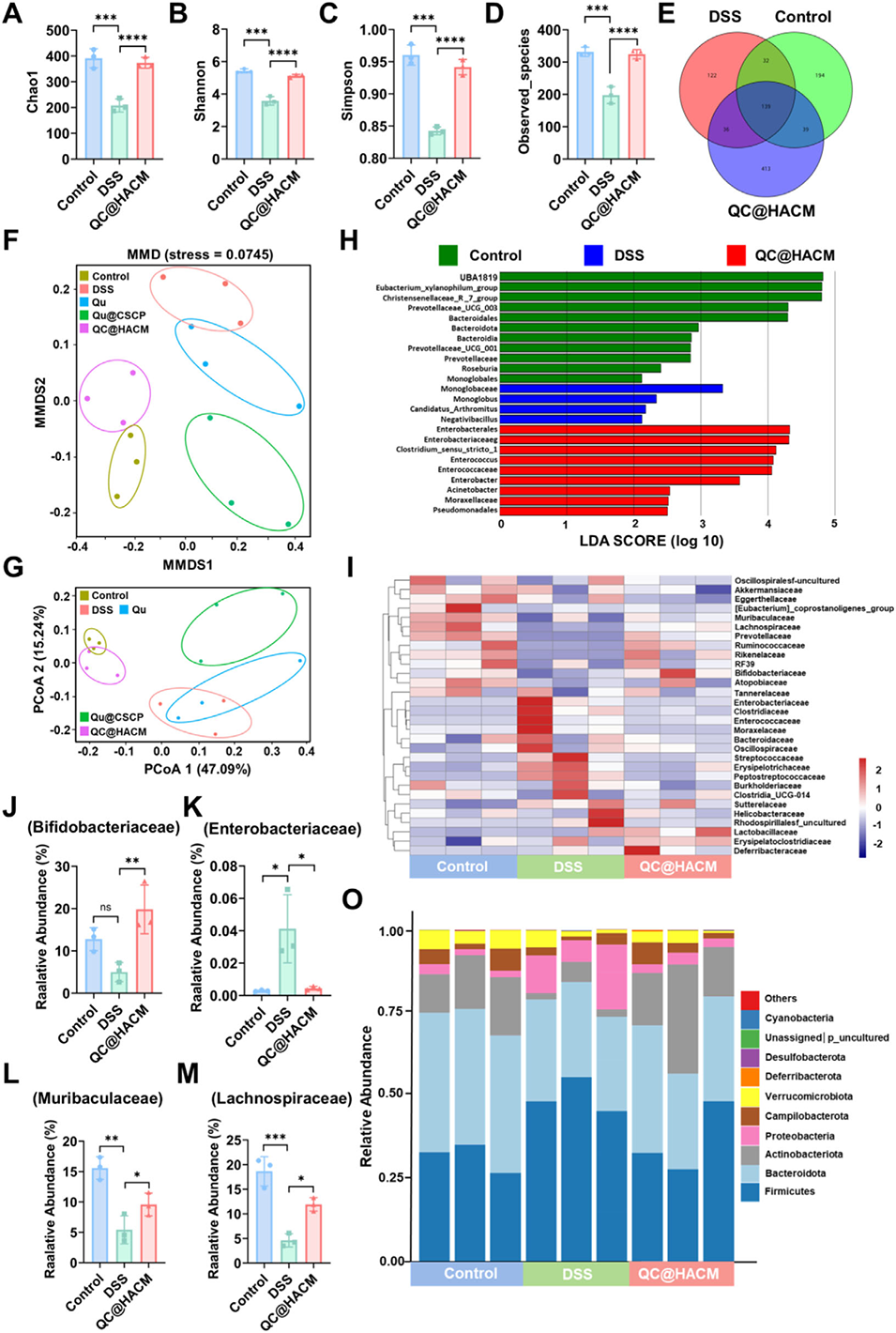
图8 QC@HACM 恢复 DSS 诱导溃疡性结肠炎(UC)小鼠的肠道菌群稳态。(A-D) 基于 Chao1 指数 (A)、Shannon 指数 (B)、Simpson 多样性指数 (C)、Observed-species 指数 (D) 评估的肠道菌群 α 多样性;(E) 对照组、DSS 模型组、QC@HACM 处理组之间共有与特有微生物物种的韦恩图;(F,G) 基于物种组成的非度量多维尺度分析(NMDS)与主坐标分析(PCoA)图,展示粪便菌群的 β 多样性;(H) 基于线性判别分析(LDA)的柱状图,识别对 QC@HACM 处理产生显著响应的微生物类群;(I) 科水平肠道菌群相对丰度热图,展示各组间的菌群组成变化,重点标注类群包括:双歧杆菌科 (J)、肠杆菌科 (K)、鼠杆菌科 (L)、毛螺菌科 (M);(O) 门水平相对丰度柱状图,展示不同处理组间微生物群落的组成差异。所有数据以均值 ± 标准差表示(n=3);*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
论文链接:https://doi.org/10.1002/adhm.202505873
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














