
导读:
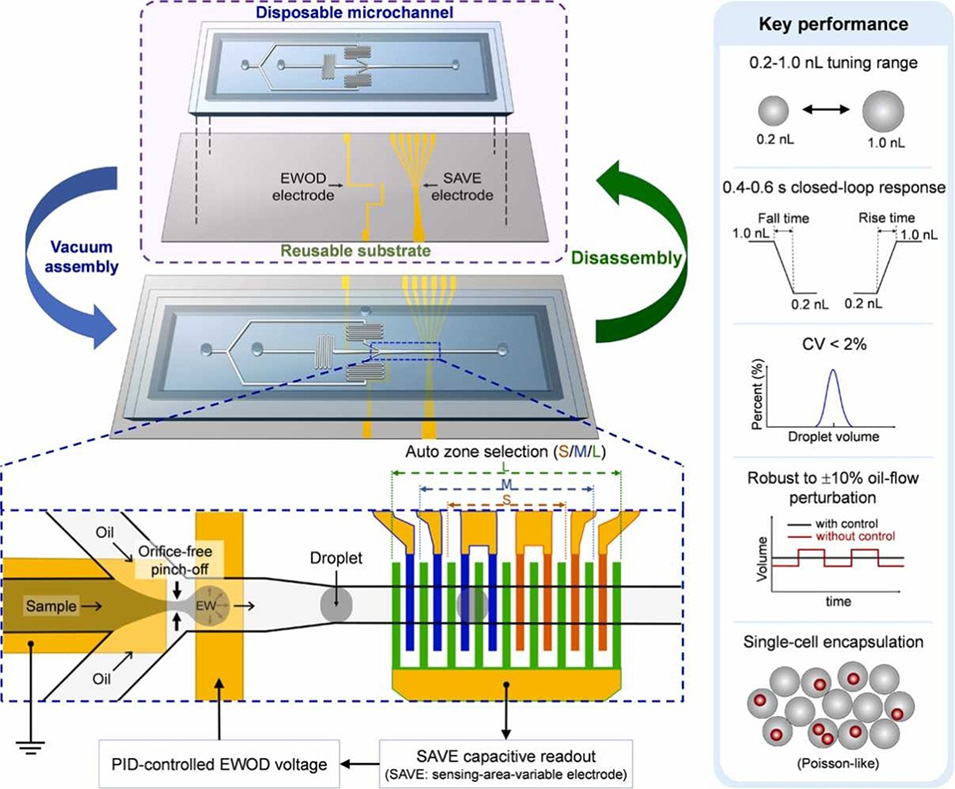
仁济大学研究人员开发了一种名为 EWOD-SAVE 的新型微流控芯片,通过结合电润湿(EWOD)技术与电容反馈控制,实现了对液滴体积的精确调节。该设备采用一次性微通道卡槽与可重复使用的电极基底相结合的设计,既降低了成本,又具备高性能的电子传感功能。通过集成可变传感面积电极(SAVE),系统能够实时监测液滴大小,并利用闭环反馈算法在亚秒级时间内做出响应,确保液滴体积在 0.2 至 1.0 nL 范围内保持极高的均一性。实验证明,该平台在流速波动下仍能稳定运行,并成功应用于遵循泊松分布的单细胞包裹任务。这种无需传统微孔结构的架构为即时检测(POCT)、数字 PCR 和高通量单细胞分析提供了一种自动化且极具性价比的解决方案。相关研究以“Electrowetting-actuated droplet microfluidic cartridge with capacitive feedback for wide-range droplet-size control”为题目,发表在期刊《Sensors and Actuators B: Chemical》上。
本文要点:
1. 核心架构:一次性与可重复使用的结合
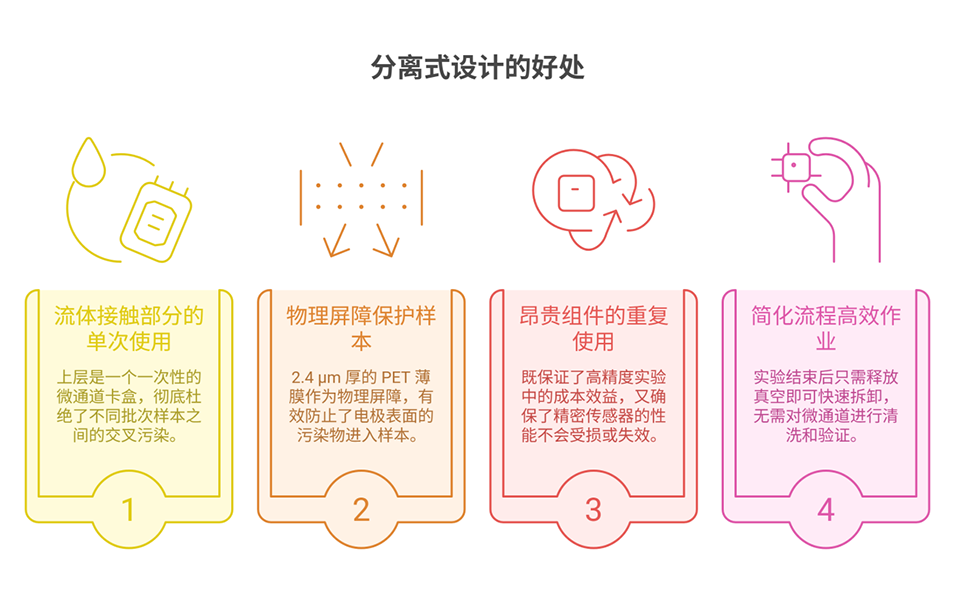
分离式设计:系统由一个一次性的微通道卡盒(上层)和一个可重复使用的驱动/传感基底(下层)组成。
组装方式:两者通过真空抽吸进行对齐和组装,使用后释放真空即可快速拆卸,兼顾了成本效益和使用的便捷性。
材料构成:上层卡盒采用 PDMS 与 4 μm 厚的 PET 薄膜结合,下层基底则集成了电极阵列。
2. 关键技术:EWOD 驱动与 SAVE 传感
无孔(Orifice-free)液滴生成:利用介质上电润湿(EWOD)技术驱动液滴断裂。通过调节 EWOD 电压(100–400 Vpp)改变接触角,从而在不需要固定几何结构的情况下控制液滴体积。
可变传感面积电极(SAVE):该技术解决了液滴尺寸与传感电极失配的问题。系统包含三个自动切换的传感区域(Zone S, M, L),确保在2 至 1.0 nL 的宽体积范围内保持线性传感灵敏度。
3. 性能表现:实时反馈与高精度控制
亚秒级响应:系统集成 PID 闭环控制,其响应时间仅为4–0.6 秒,远快于传统基于压力或泵控制的方案(通常需数十秒)。
极高的稳定性与均匀性:在闭环控制下,液滴体积的变异系数(CV)低于 2%。即使在外部油相流速波动 ±10% 的情况下,仍能保持液滴体积和生成速率的恒定。
4. 应用验证:单细胞包封
符合泊松分布:研究人员使用 Jurkat 和 K562 细胞进行了包封实验,结果证实细胞在不同体积液滴中的分布规律符合泊松统计模型。
按需调节:系统可以根据目标细胞的丰度灵活调节液滴体积,从而优化单细胞包封的产率,这对于单细胞基因组学、药物筛选和数字 PCR(dPCR)等应用具有重要意义。
5. 总结与展望
该芯片通过无孔式 EWOD 液滴生成与自适应电容传感的结合,提供了一种自动化、低成本且可扩展的液滴操纵方案。紧凑的电子控制系统(基于 MCU)使其具备开发为即时检测(POCT)设备的潜力。
SAVE(可变传感面积电极)传感器的三个区域(Zone S、M 和 L)通过微控制器(MCU)的数字化调控实现自动切换,其核心机制如下:
1. 切换的判定依据
系统会实时监测传感器输出的信号电平。MCU 根据测量到的液滴信号强度(对应液滴体积),自动判断当前液滴尺寸是否超出了当前区域的线性检测范围,并决定是否需要切换到另一个传感区域。
2. 电气执行机制
传感器的切换是通过 MCU 控制电极开关(标为 S1 和 S2)的“开启”或“关闭”来实现的。不同的开关组合对应不同的有效传感面积:
Zone S(小量程区域):开关 S1和 S2 均处于 OFF(关闭) 状态。
Zone M(中量程区域):开关 S1为 ON(开启),开关 S2 为 OFF。
Zone L(大量程区域):开关 S1和 S2 均处于 ON 状态。
3. 稳定性保障:滞后阈值(Hysteresis)
为了防止液滴体积在两个区域的分界点附近波动时产生频繁的“颤振”切换(Chattering),系统在 S–M 和 M–L 的转换中应用了滞后阈值控制。
重叠区域保留原态:在两个区域的重叠部分,控制器会保留上一个传感状态,只有当信号电平越过特定的滞后边界时才会触发正式切换,从而确保了系统运行的稳定性。
4. 切换的目的
这种自动切换的设计确保了无论液滴大小如何(在 0.2 至 1.0 nL 范围内),传感器的有效感应面积始终与液滴体积相匹配。这使得系统在所有量程下都能保持恒定的电容转电压灵敏度(4.34 V/nL),从而实现高精度的线性读数和闭环反馈控制。
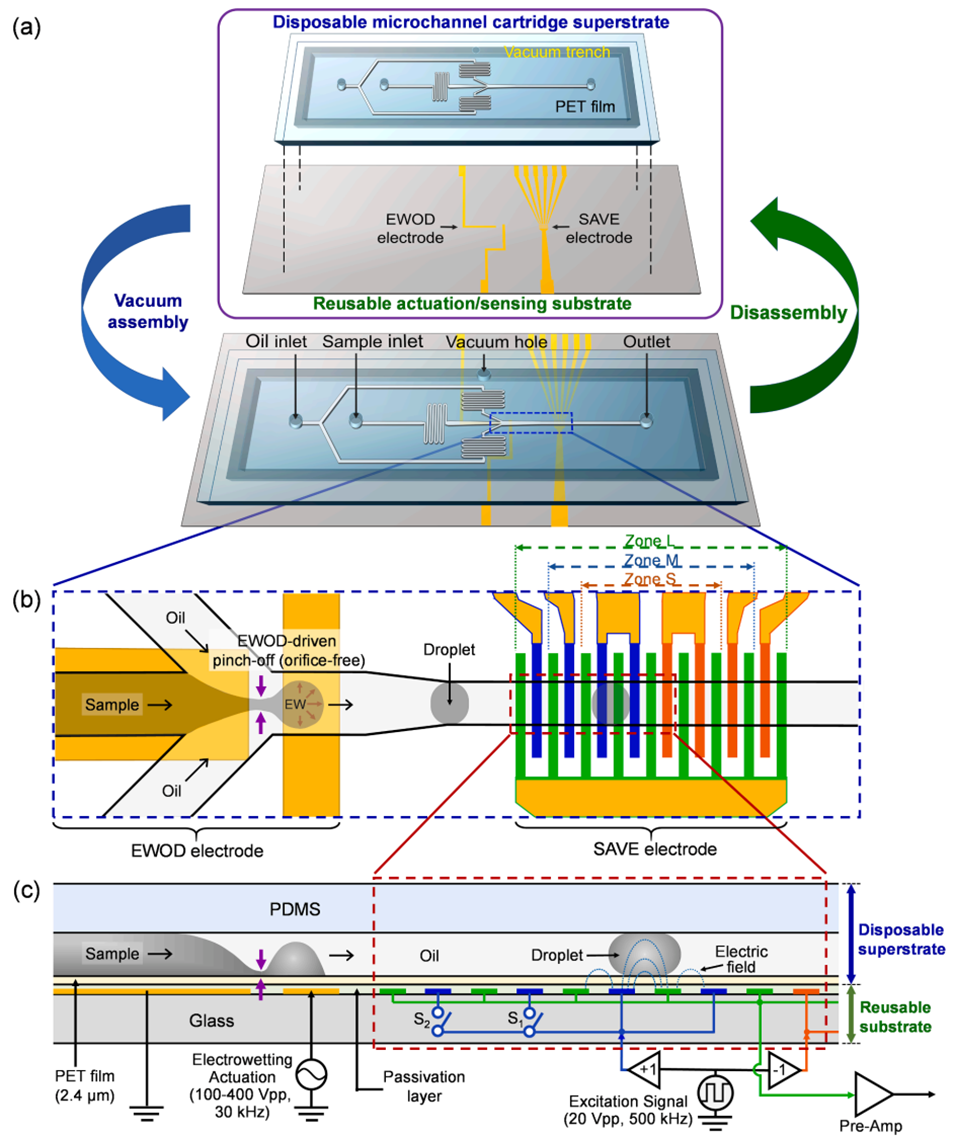
图1. EWOD-SAVE 芯片的架构与工作原理。 (a) 通过真空组装的一次性上层卡盒(由 2.4 μm 厚 PET 薄膜上的 PDMS 微通道组成)和集成了 EWOD 与 SAVE 电极的可重复使用基底;这两个部分可以反复结合与分离,以实现单次使用的操作方式。 (b) 汇合处的无孔式、EWOD 驱动的液滴断裂,以及下游的 SAVE 电极。SAVE 电极包含三个可自动选择的传感区域(区域 S、M 和 L),用于宽量程的液滴传感。 (c) 器件剖面图显示了 EWOD 驱动(100–400 Vpp, 30 kHz)和高频激励信号(20 Vpp, 500 kHz);液滴在 SAVE 电极处引起的电容变化被转换为电信号,并传输至前置放大器进行液滴尺寸检测。
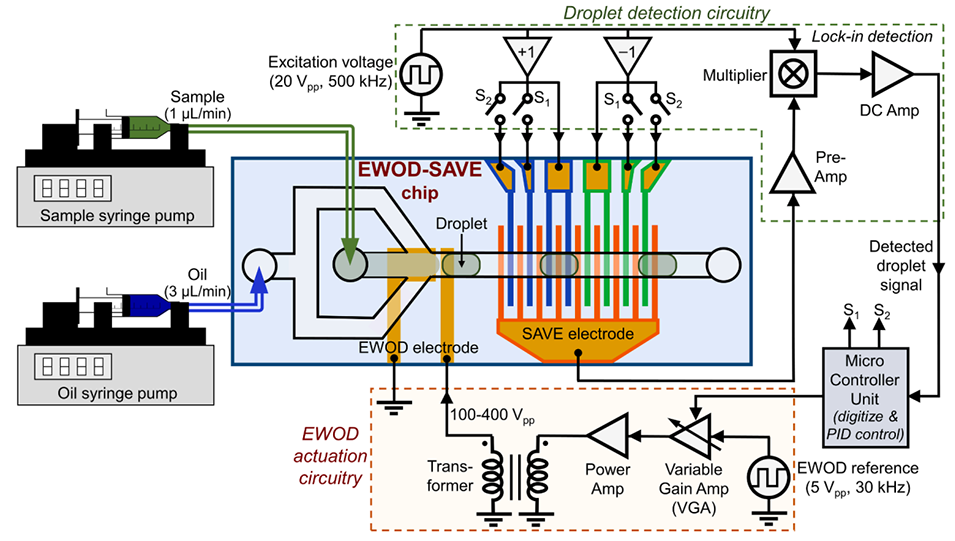
图2. 利用 EWOD-SAVE 芯片实现的液滴体积闭环控制。样品流(1 μL/min)和油相流(3 μL/min)由注射泵输送至流动聚焦汇合处,在此处通过片上 EWOD 电极生成液滴。下游液滴通过由激励信号(20 Vpp, 500 kHz)驱动的 SAVE 电极。液滴感应出的信号经前置放大和锁相检测电路解调后,由 MCU 进行数字化并转换为液滴体积。根据测量到的体积,MCU 选择合适的 SAVE 传感区域(S1/S2),并运行 PID 算法来更新可变增益放大器(VGA)的增益。VGA 与功率放大器和变压器协同工作,将低压 EWOD 参考信号(5 Vpp, 30 kHz)缩放至 EWOD 电极上的 100–400 Vpp,从而闭合反馈回路,实现对液滴尺寸的精确实时调节。
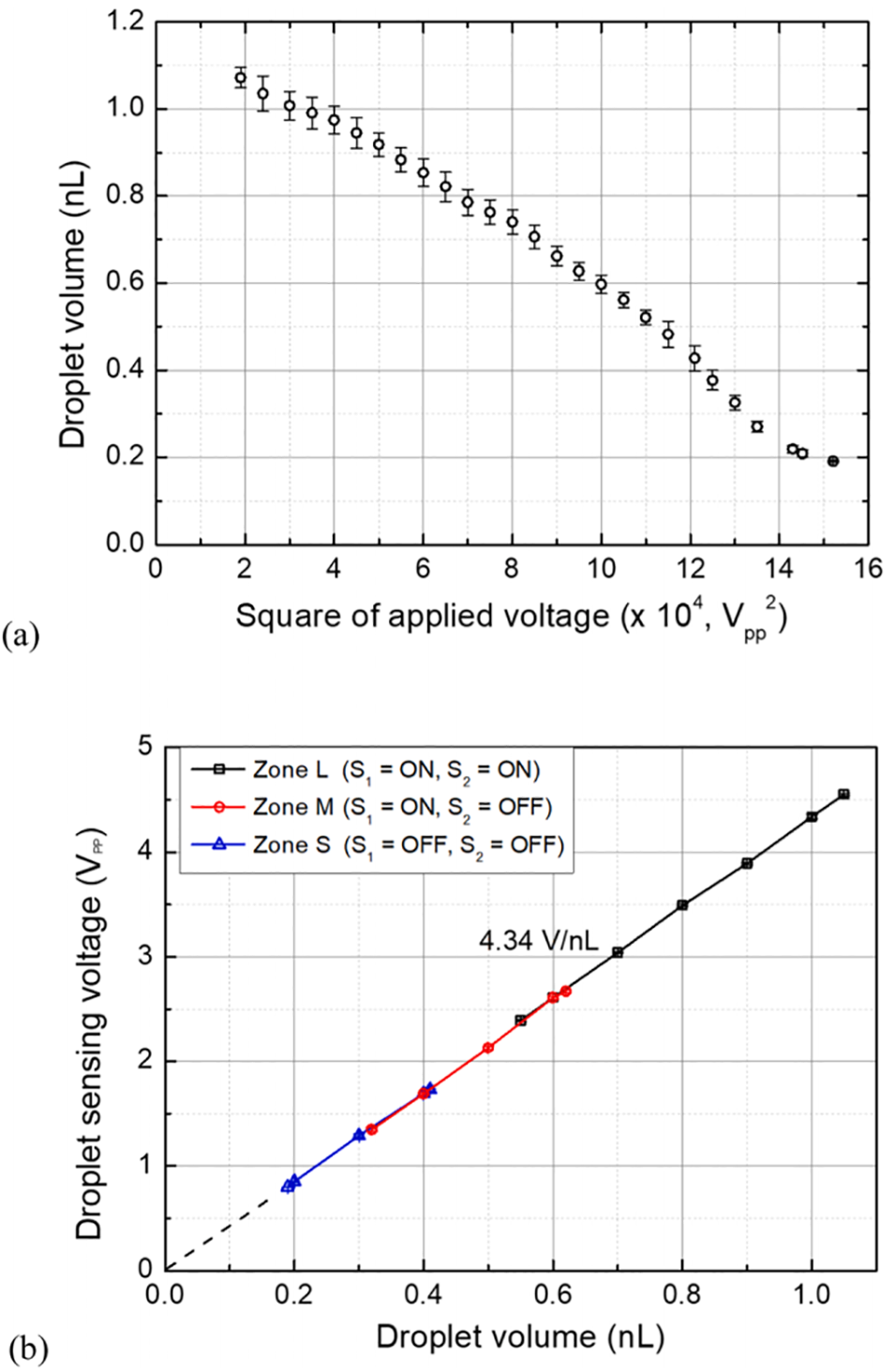
图3. EWOD-SAVE 芯片的重复性和灵敏度。 (a) 液滴体积与外加 EWOD 电压平方的关系。该结果通过使用五个相同的一次性微通道,在分散相和连续相流速分别固定为 1 和 3 μL/min 的条件下获得。误差条表示五次运行的标准差。 (b) 三种 SAVE 配置下液滴体积与液滴传感电压之间的关系。区域 S、M 和 L 分别对应 S1/S2 的状态:OFF/OFF、ON/OFF 和 ON/ON。线性回归显示所有区域的灵敏度均为恒定的 4.34 V/nL。控制器会自动选择合适的区域,以在 0.2–1.0 nL 的完整液滴体积范围内保持线性。
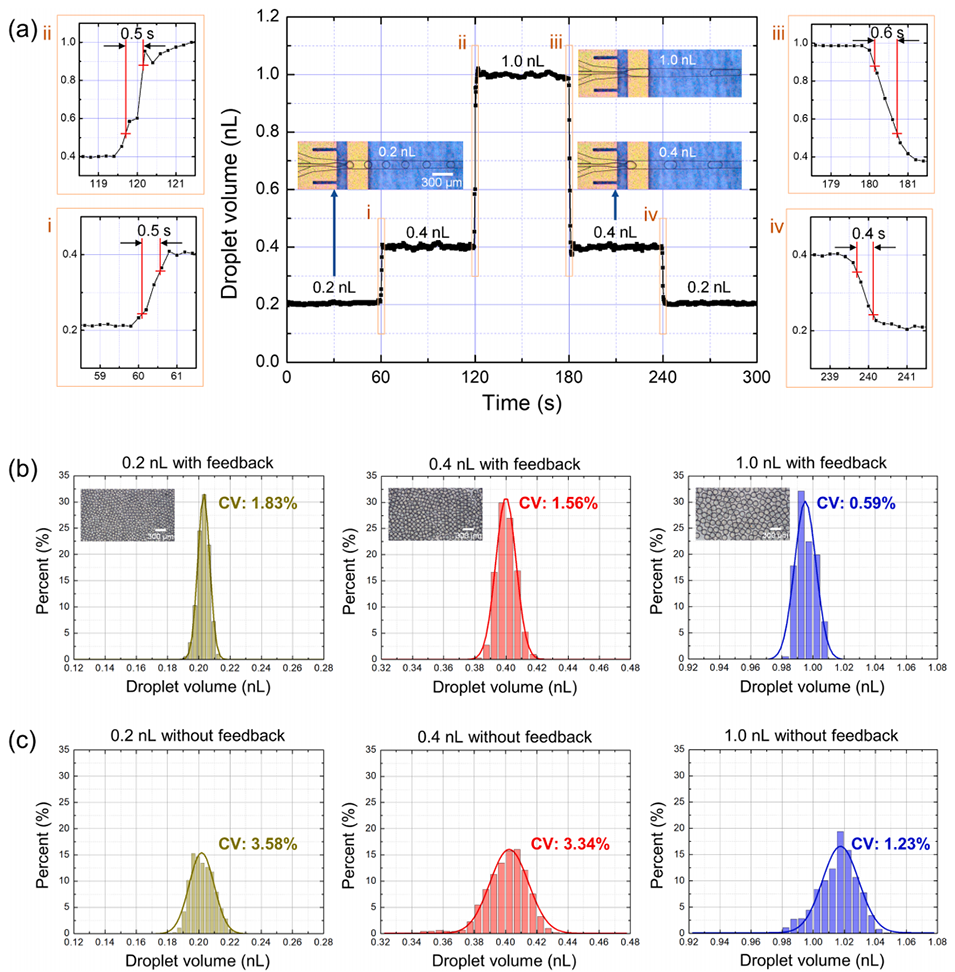
图4. 液滴体积的分步反馈控制。 (a) 当目标尺寸通过改变 EWOD 电压(140–390 Vpp)按序从 0.2 nL 切换至 0.4–1.0 nL 再返回 0.2 nL 时的液滴体积时间追踪图。插图 (i–iv) 显示了每次转换的放大视图,从中测得 20%–80% 的上升和下降时间为 0.4–0.6 秒;数据采集频率为 5 Hz。 (b, c) 在 (b) 开启和 (c) 关闭 EWOD-SAVE 反馈控制的情况下,针对每种目标尺寸(0.2、0.4 和 1.0 nL)获得的液滴体积直方图(每种条件包含 12,000 个数据点,采集时间超过 40 分钟)。 (b) 中的插图为反馈控制下生成的液滴代表性显微照片。所有实验中,样品流和油相流速均固定为 1 和 3 μL/min。
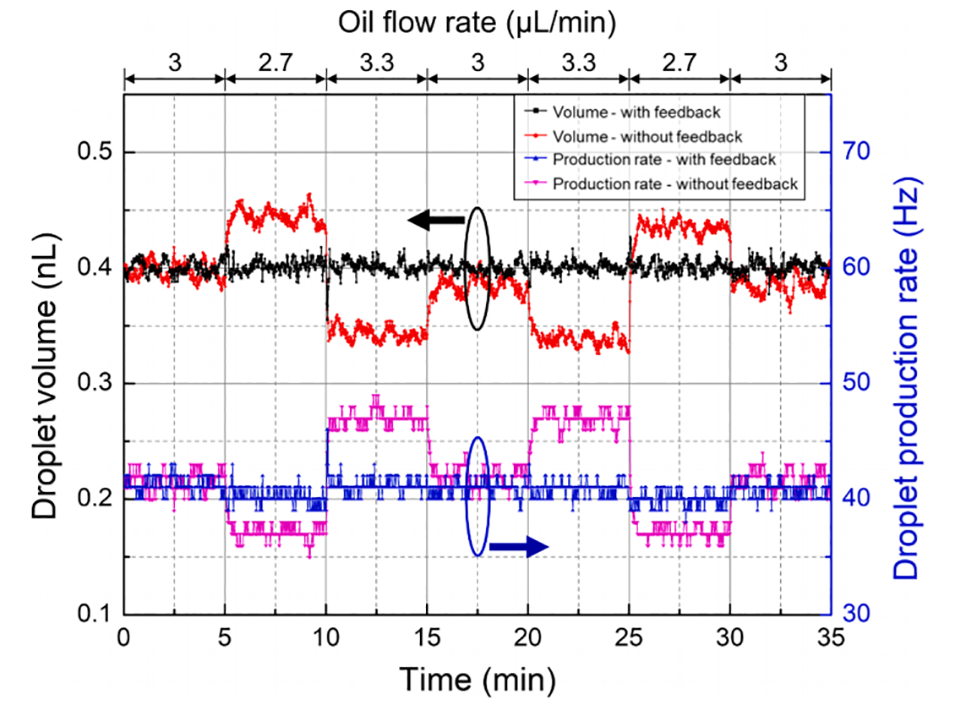
图5. 油相流波动下反馈控制对液滴体积和生成速率的影响。样品流速固定在 1 μL/min,目标液滴体积为 0.4 nL,而油相流速在 2.7 至 3.3 μL/min 之间周期性地发生 ±10% 的波动(顶轴)。在无反馈的情况下(红色和品红色曲线),液滴体积和生成速率都会随着流体扰动产生大幅波动。在开启 EWOD-SAVE 反馈的情况下(黑色和蓝色曲线),控制器通过调节 EWOD 驱动电压进行补偿,使液滴体积紧紧保持在 0.4 nL,并维持近乎恒定的生成速率(约 40 Hz)。这些结果证明 EWOD-SAVE 芯片即使在动态变化的流速条件下也能实现稳定的液滴生成。
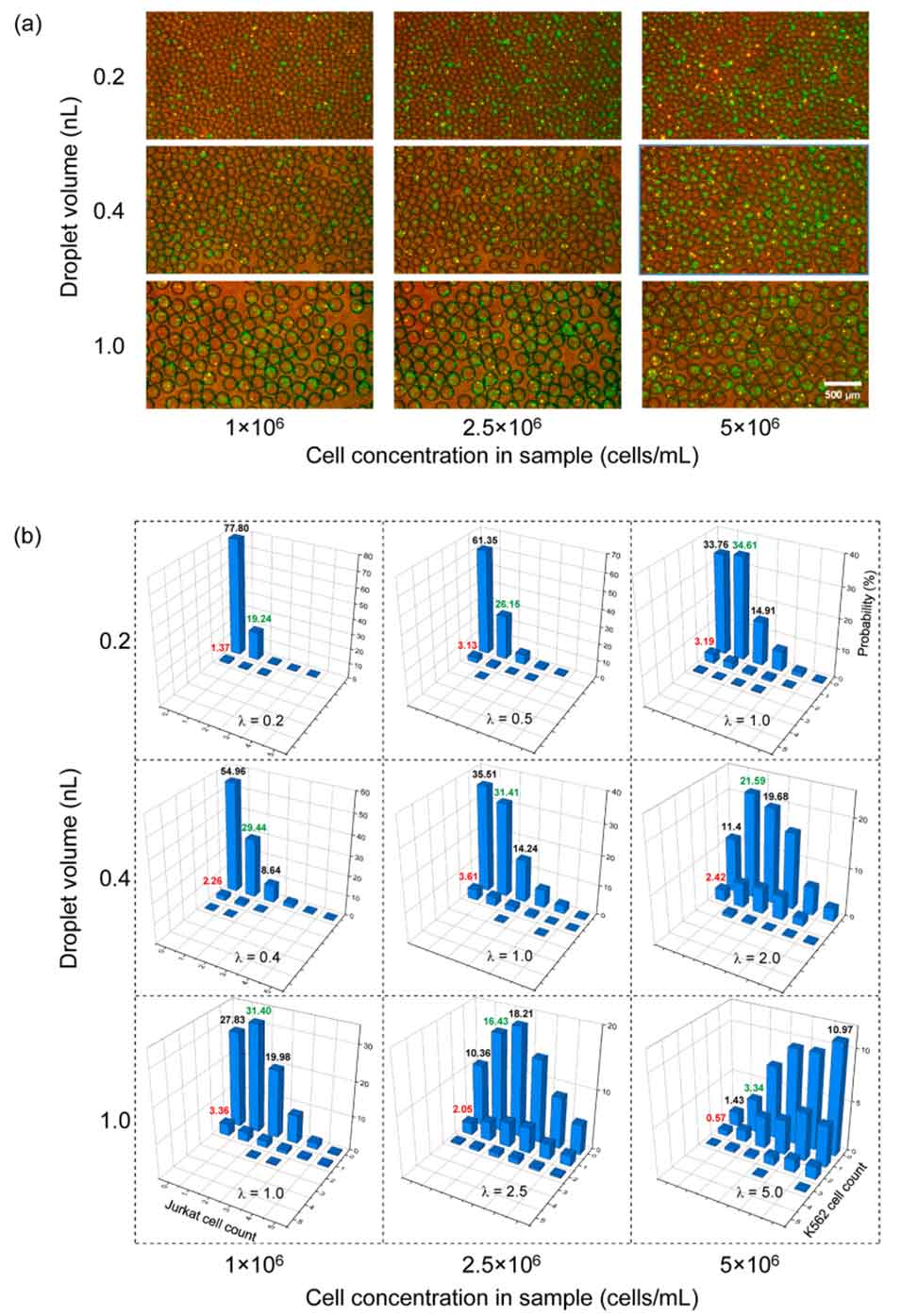
图6. 在 EWOD-SAVE 控制的液滴中进行细胞包封。 (a) 在三种初始细胞浓度(1×106、2.5×106 和 5×106 cells/mL)下,包封在 0.2、0.4 和 1.0 nL 体积液滴中的 Jurkat(绿色)和 K562(红色)细胞的荧光显微照片。比例尺:500 μm(适用于所有照片)。 (b) 不同液滴体积和细胞浓度下细胞占用情况(每滴液滴中 Jurkat 与 K562 细胞的数量)的 3D 直方图,说明了包封统计数据如何随 λ(每滴液滴的平均细胞数)的变化而变化。每种分布均基于 1000 个液滴量化而成。对应于单细胞占用的柱条已为 K562(红色)和 Jurkat(绿色)标出。所有图共用相同的 x 轴和 y 轴刻度;z 轴限值为了清晰起见独立缩放。
论文链接:https://doi.org/10.1016/j.snb.2026.139968
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
上一篇:微流控辅助受限反溶剂沉淀策略,破解亲水微凝胶封装疏水药物的载药量瓶颈
下一篇:暂无














