【研究背景】
1、重症肢体缺血(CLI)的临床问题:CLI由动脉粥样硬化/血栓导致肢体灌注不足,伴随微循环障碍、炎症,易引发静息痛、坏疽甚至截肢;传统血管介入/旁路手术仅能部分恢复血流,无法及时缓解缺血组织的氧化应激和炎症,难以逆转组织损伤。
2、细胞治疗的局限性:间充质干细胞(MSCs)是CLI细胞治疗的潜力细胞,但存在需大剂量细胞(数亿级)、治疗效果不一致、直接注射因剪切应力/无ECM支持导致细胞损伤/凋亡/滞留率低的问题。
3、细胞载体的研发需求:球形载体因比表面积大、适合微创注射成为研究热点,理想载体需仿生天然ECM的生化特征和纳米-微米多尺度多孔结构,但现有成孔技术(盐析、乳液模板、气体发泡)存在孔连通性差、可控性低、分布不均的缺陷,亟需优化成孔工艺。

【导读】
近日,中山大学生物医学工程学院刘杰教授、陈友副教授团队针对重症肢体缺血传统治疗的痛点与细胞治疗的局限性,开发出以小肠黏膜下层脱细胞外基质为核心的仿生可注射层级多孔微球载体。通过微流控技术、液-液相分离与冰模板法精准构建微球的层级多孔结构,结合纤连蛋白修饰优化生物活性,共载人脐带间充质干细胞和脐静脉内皮细胞形成协同细胞治疗体系,在体内外实验中均展现出优异的血管生成、肌肉再生与炎症调控效果,大幅提升了重症肢体缺血的治疗效率。相关研究以“Biomimetic injectable engineered hierarchical porous microspheres for enhanced synergistic cell therapy of critical limb ischemia”为题目,发表于期刊《Bioactive Materials》。
【研究亮点】
① 在脱细胞外基质体系中结合液-液相分离与冰模板法制备分级多孔微球,并阐明其成孔机制。
② 通过对成分、结构及界面信号的协同优化设计,构建细胞仿生微环境。
③ 利用共负载人脐静脉内皮细胞与脐带间充质干细胞的微球构建微组织,并借助转录组学解析其作用机制。
【主要内容】
本研究开发了一种仿生分级多孔微球(GEPM-FN),该微球不仅支持高质量的细胞培养与扩增,还可作为重症肢体缺血(CLI)治疗的递送载体。如示意图1所示,该微球以小肠黏膜下层脱细胞外基质(SIS-dECM)为主要成分,其保留了天然细胞外基质(ECM)的活性成分与结构,是理想的细胞仿生微环境。为提升其力学性能与加工性,研究引入甲基丙烯酰化明胶(GelMA)以增强机械强度并赋予其光交联能力,大幅提升了制备可控性。随后,通过聚乙二醇(PEO)的引入,结合微流控技术与液-液相分离原理,构建出孔隙均一的一级多孔结构;并系统探究了温度、相分离时间及材料配比对孔隙的可控调节作用,同时采用冰模板法构建二级孔隙。最后,通过修饰纤连蛋白(FN)增强生物活性,最终获得目标微球(GEPM-FN)。
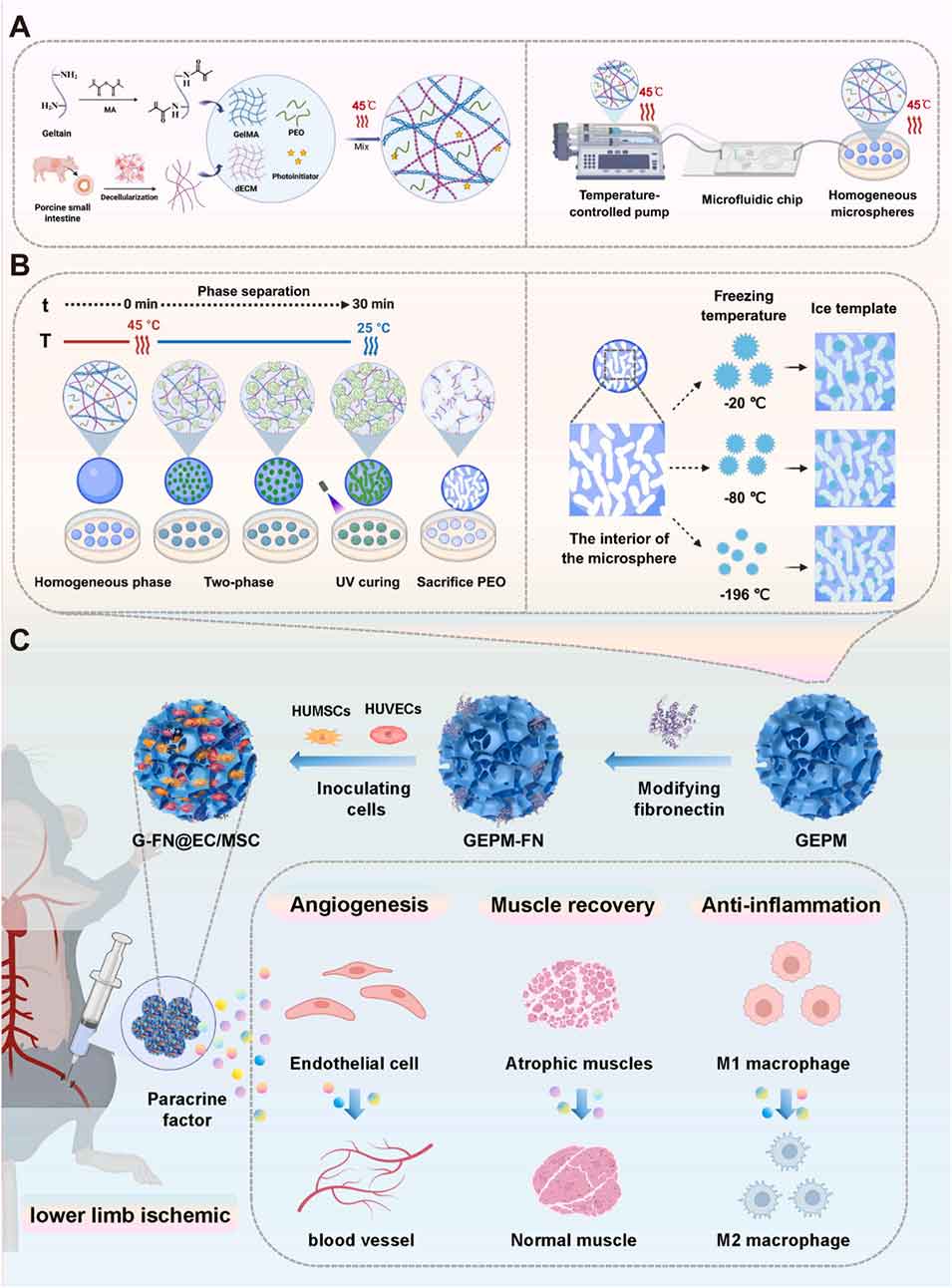
示意图1 仿生层级多孔微球共递送人脐静脉内皮细胞与人脐带间充质干细胞治疗重症肢体缺血。(A) 微球的组成及利用温控微流控装置的制备工艺;(B) 通过调控温度和时间,利用液-液相分离制备一级孔,结合不同温度的冰模板法形成二级孔;(C) 对仿生层级多孔微球进行纤连蛋白表面修饰,共载人脐静脉内皮细胞和人脐带间充质干细胞后注射至缺血部位,可显著促进血管生成、改善肌肉萎缩并抑制炎症反应。
GEPM-FN可实现高效细胞负载、三维浸润与增殖,并能有效保护细胞免受外界应力损伤。负载于GEPM-FN上的人脐带间充质干细胞(HUMSCs)可维持良好干性,包括三系分化能力与集落形成能力,同时旁分泌功能得到增强;而人脐静脉内皮细胞(HUVECs)在GEPM-FN上也表现出良好的黏附与增殖特性。
基于GEPM-FN优异的理化与生物学性能,研究人员将其作为载体,构建了HUVECs与HUMSCs的共培养递送体系(G-FN@EC/MSC),用于CLI治疗。两种细胞的协同作用有望解决单一细胞疗法的关键局限:内皮细胞(ECs)可快速形成血管网络以改善缺血状态,而间充质干细胞(MSCs)能分泌多种生长因子及免疫调节细胞因子,减轻缺血相关炎症并促进组织修复。体外实验证实,G-FN@EC/MSC可促进血管生成并诱导巨噬细胞M2型极化;研究还通过转录组测序(RNA-Seq)探究并分析了其治疗机制。在CLI小鼠模型中,G-FN@EC/MSC展现出最优的血管生成、肌肉组织修复及抗炎效果,凸显了多细胞协同治疗的优势。总体而言,该研究为仿生微球的可控构建及CLI的协同细胞治疗提供了新思路。
该研究的创新点主要体现在以下几个方面:
1、材料设计与构建创新:首次在脱细胞外基质(dECM)为主的三元体系中引入聚乙二醇(PEO)通过液-液相分离结合微流控技术实现对孔径与互联结构的精准调控并联合冰模板法构建了多级孔结构解决了传统多孔载体孔结构不可控、连通性差的问题。
2、工艺控制创新:在微流控制备过程中采用分段控温策略解决了微球生成时间差异导致的相分离不一致问题实现了结构高度均一的微球批量制备。
3、仿生功能整合:在保留dECM天然生物活性的基础上引入甲基丙烯酰化明胶(GelMA)改善力学性能与光交联可控性并通过纤连蛋白(FN)表面修饰增强细胞黏附与生物活性构建了生化-结构-界面多维仿生微环境。
4、细胞治疗策略创新:构建了人脐静脉内皮细胞(HUVECs)与人脐带间充质干细胞(HUMSCs)共载的协同治疗系统通过RNA-seq揭示了细胞间直接相互作用可激活MAPK、PI3K-Akt等关键信号通路协同促进血管生成与免疫调节。
5、应用性能优势:微球具备优异的细胞载量、深部细胞浸润能力、注射保护作用及长期冷冻保存稳定性在CLI动物模型中实现了94.23%的血流恢复显著优于单细胞治疗与载体单独使用组。
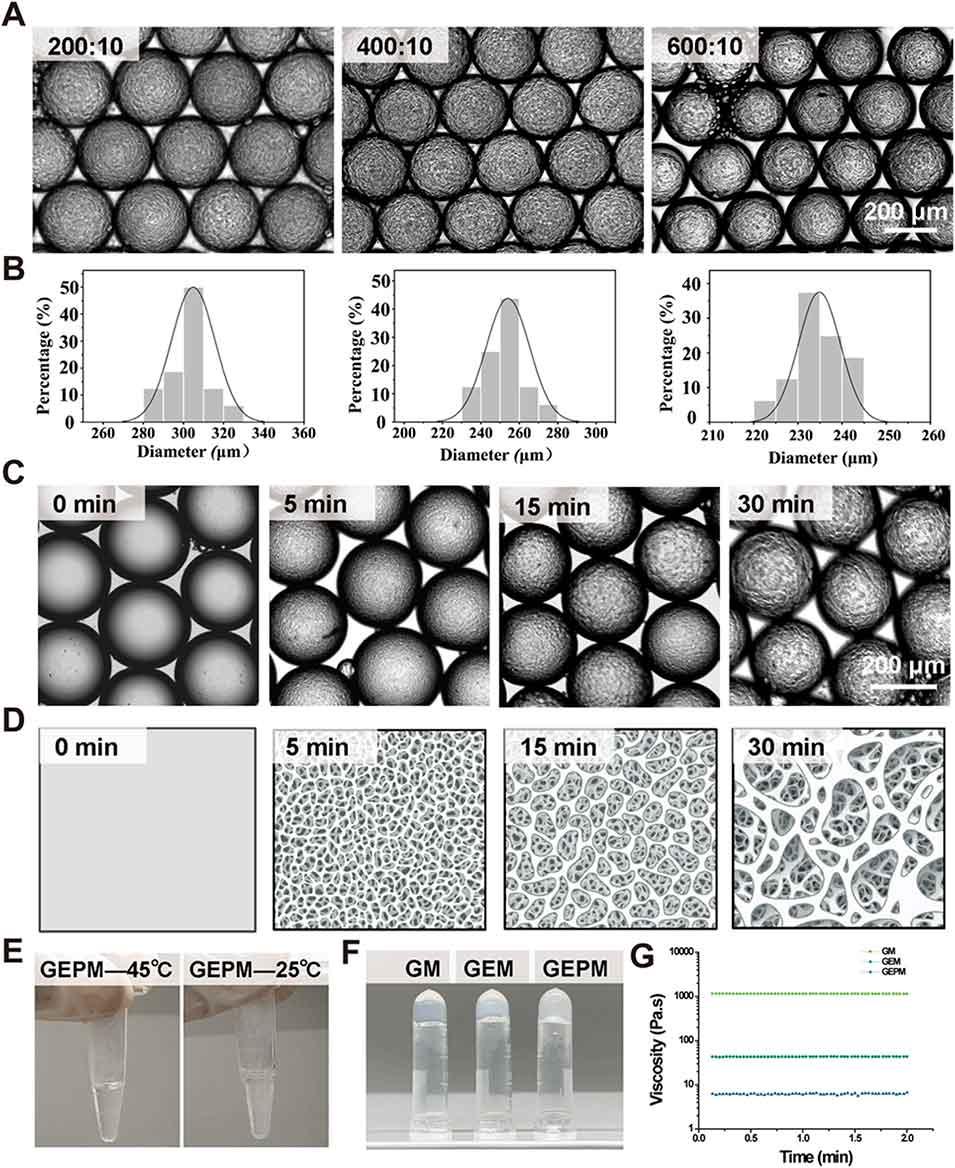
图1 微球的制备及其理化性质表征。(A) 通过调整油相与水相的流速比调控微球粒径,完成粒径筛选;(B) 不同流速比下制备的微球粒径统计直方图(n=50);(C) 25℃下微球发生相分离的代表性图像;(D) 微球内部微观相分离过程的示意图;(E) 不同温度下微球前驱体溶液的外观图;(F) 不同组成的水凝胶经紫外光交联后的外观图;(G) 黏度-时间曲线(n=3)。
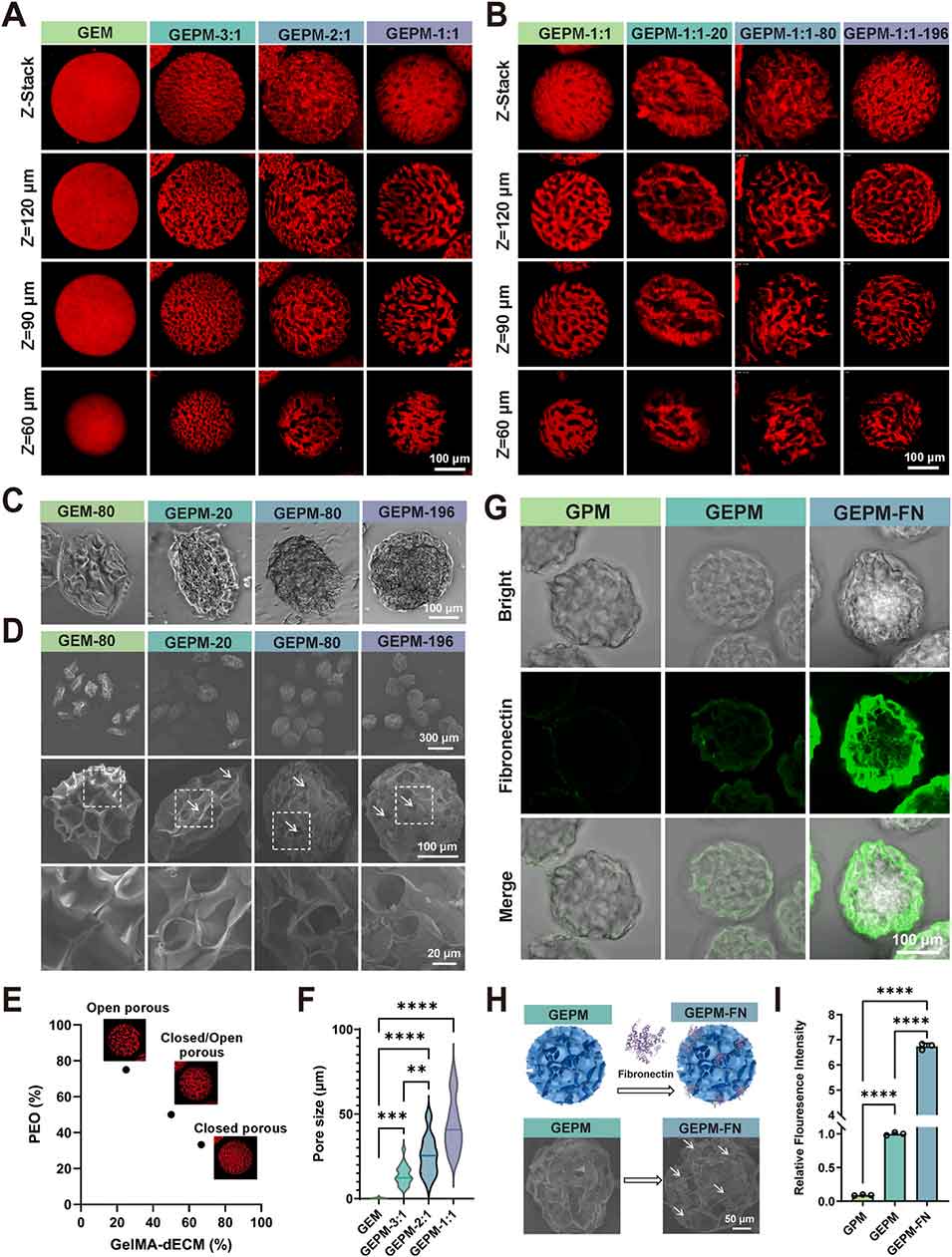
图2 层级多孔微球的构建及其表面修饰。(A) 激光共聚焦显微镜 Z 轴堆叠图像与重构图像,展示不同比例的脱细胞外基质/甲基丙烯酰化明胶与聚乙二醇混合制备的微球内部结构;(B) 未冷冻及在 - 20℃、-80℃、-196℃冷冻的 GEPM-1:1 微球的激光共聚焦显微镜 Z 轴堆叠图像与逐层扫描图像;(C) 光学显微镜下观察到的微球形态图像;(D) 扫描电子显微镜拍摄的微球表面形态图像,白色箭头指示相互连通的孔结构;(E) 不同脱细胞外基质/甲基丙烯酰化明胶与聚乙二醇比例制备的微球孔结构特征总结;(F) 上述微球孔径的统计分析(n=10 个样本,每个样本随机测量 3 次);(G) 微球内纤连蛋白的激光共聚焦显微镜表征图像;(H) 微球纤连蛋白修饰前后的示意图及代表性扫描电子显微镜图像;(I) 纤连蛋白荧光强度的定量分析(n=3)。数据以平均值 ± 标准差表示,采用单因素方差分析结合杜凯事后检验,*P<0.05,**P<0.01,***P<0.005,****P<0.001。
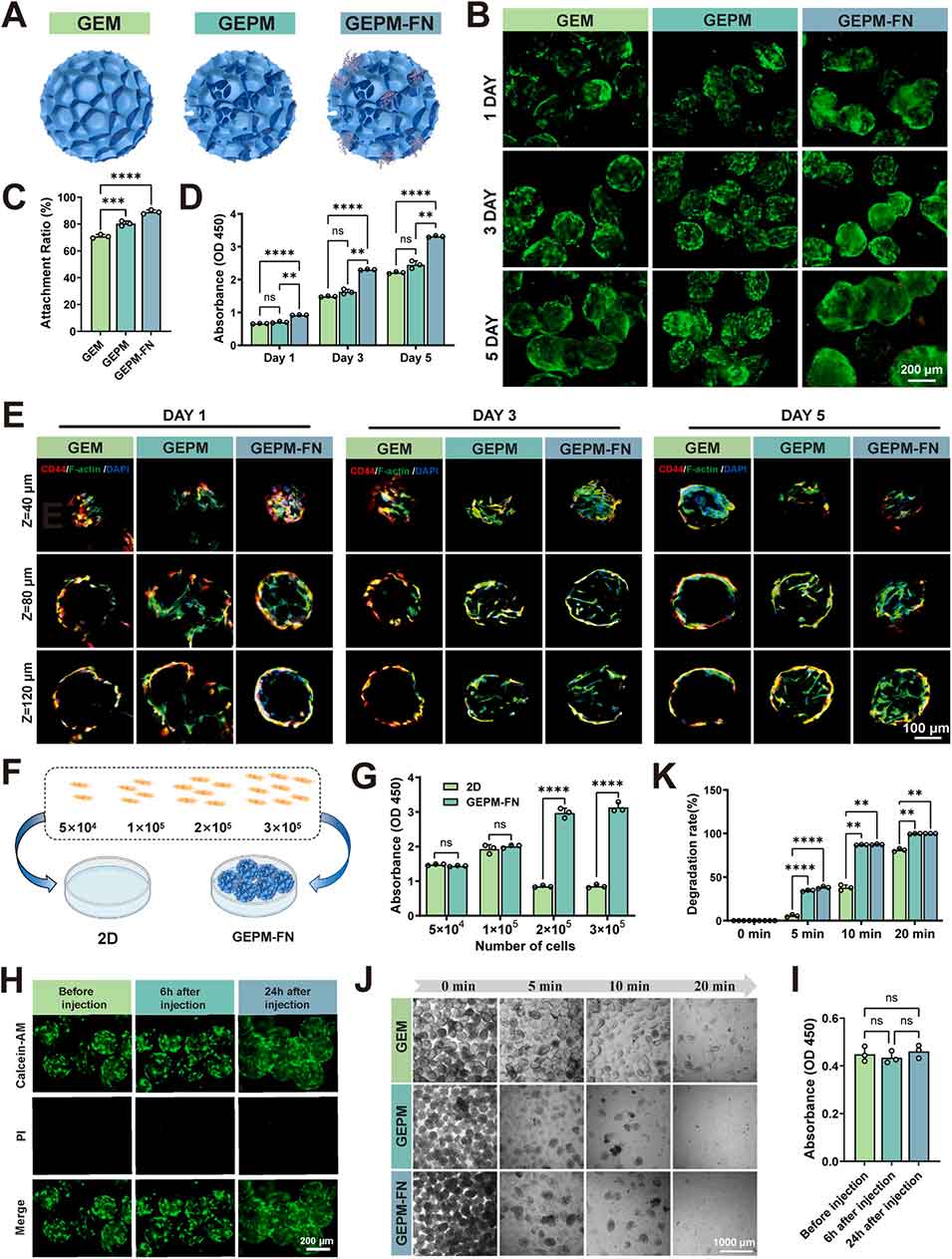
图3 GEPM-FN 促进细胞黏附与增殖,具备优异的细胞保护、载胞能力及降解性能。(A) 三种不同类型微球的示意图;(B) 活/死染色法检测三种微球上的细胞活力;(C) 三种微球表面的细胞黏附率(n=3);(D) CCK-8 法检测三种微球上的细胞增殖情况(n=3);(E) 激光共聚焦显微镜 Z 轴堆叠图像,展示三种微球内部的细胞浸润与生长情况;(F) 二维培养与 GEPM-FN 微球载胞能力的对比示意图;(G) CCK-8 法评价二维培养与 GEPM-FN 微球上的细胞活力(n=3);(H) GEPM-FN 微球注射前后的细胞活/死染色图像;(I) CCK-8 法检测 GEPM-FN 微球注射前后的细胞活力变化(n=3);(J) 三种微球在胶原酶作用下的降解过程(n=3);(K) 三种微球在胶原酶作用下的降解率(n=3)。数据以平均值 ± 标准差表示,图 3C、G、I 采用单因素方差分析结合杜凯事后检验,图 3D、K 采用双因素方差分析结合杜凯事后检验,*P<0.05,**P<0.01,***P<0.005,****P<0.001。
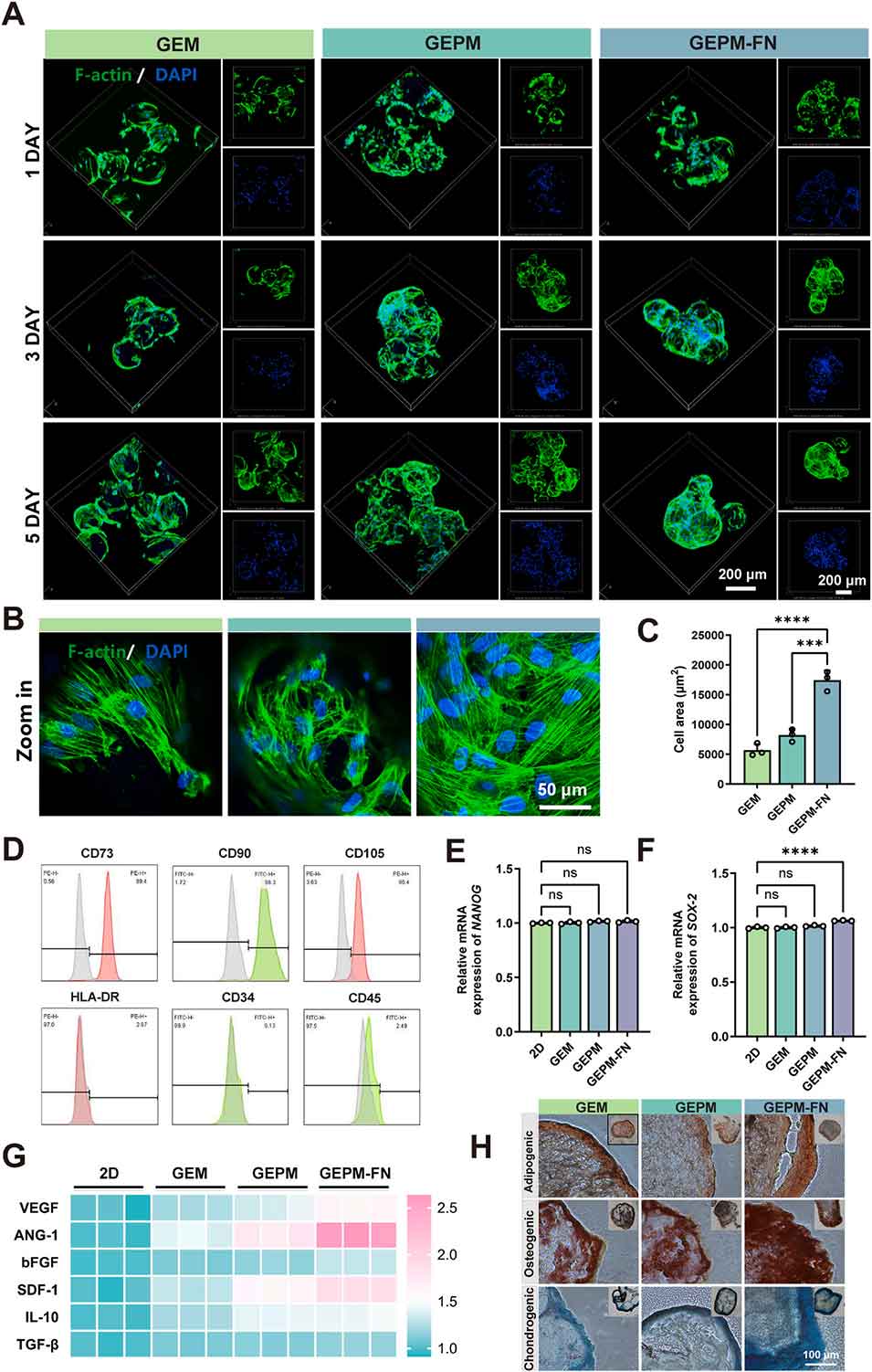
图4 GEPM-FN 上人脐带间充质干细胞的干性维持、旁分泌功能及三系分化能力的对比评价。(A) 三种微球上人脐带间充质干细胞经鬼笔环肽 / 4',6 - 二脒基 - 2 - 苯基吲哚染色后的激光共聚焦显微镜图像;(B) 三种不同微球顶端区域的代表性视野图像;(C) 细胞铺展面积的定量分析(n=3);(D) 流式细胞术分析 GEPM-FN 微球上人脐带间充质干细胞的干性表面标志物表达;(E) 不同培养条件下人脐带间充质干细胞的 NANOG 基因表达水平(n=3);(F) 不同培养条件下人脐带间充质干细胞的 SOX-2 基因表达水平(n=3);(G) 酶联免疫吸附试验定量检测不同培养条件下人脐带间充质干细胞分泌的旁分泌因子水平(n=3);(H) 三种微球上人脐带间充质干细胞的三系分化染色图像。数据以平均值 ± 标准差表示,采用单因素方差分析结合杜凯事后检验,*P<0.05,**P<0.01,***P<0.005,****P<0.001。
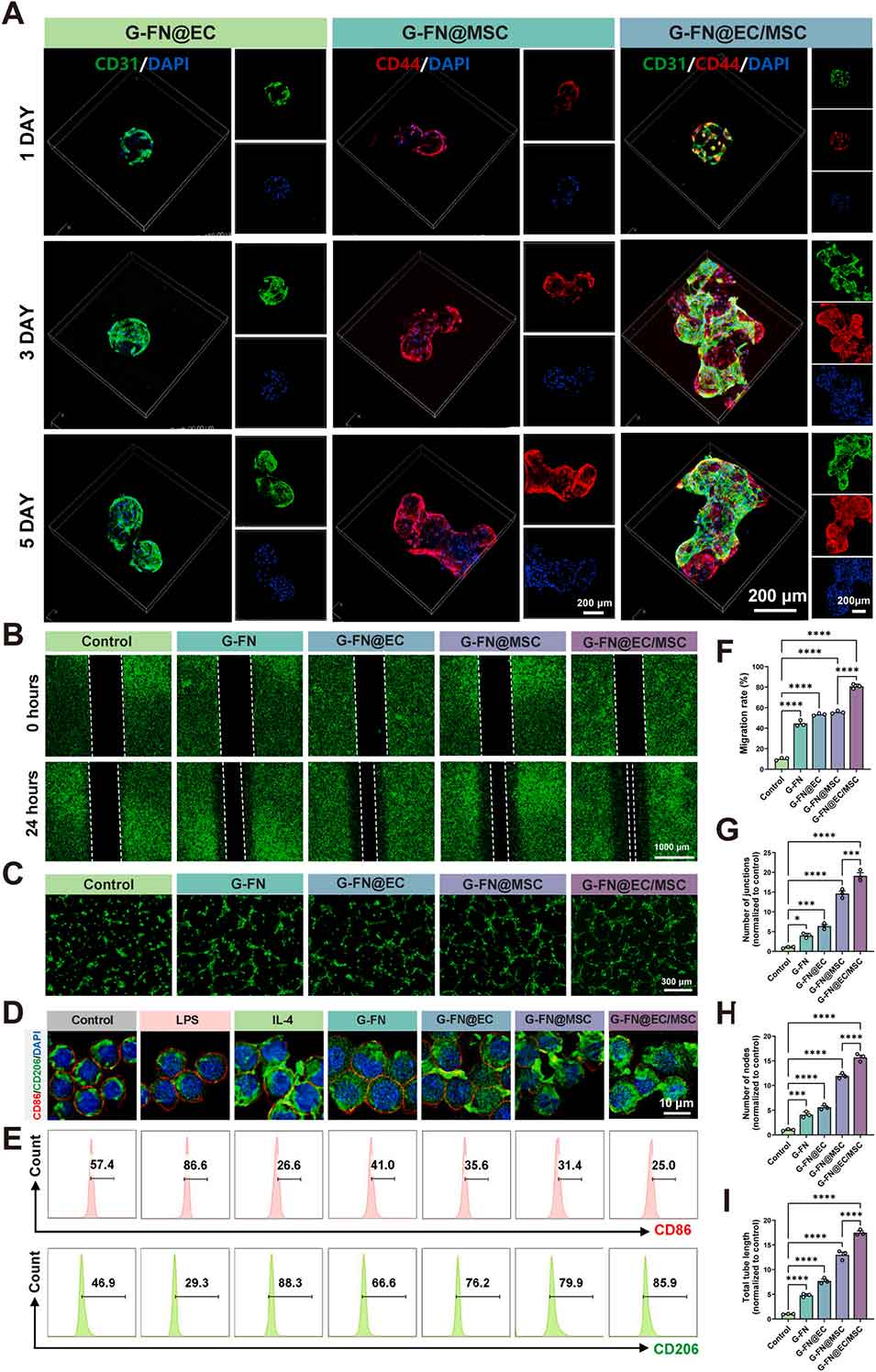
图5 G-FN@EC、G-FN@MSC 及 G-FN@EC/MSC 体外促血管生成和调控巨噬细胞极化的对比分析。(A) G-FN@EC、G-FN@MSC 及 G-FN@EC/MSC 在第 1、3、5 天的代表性激光共聚焦显微镜图像;(B) 划痕实验在 0 小时和 24 小时的代表性光学显微镜图像;(C) 体外血管生成实验的代表性光学显微镜图像;(D) 激光共聚焦显微镜图像展示 CD206(M2 型巨噬细胞)和 CD86(M1 型巨噬细胞)的表达;(E) 流式细胞术分析 CD206 和 CD86 的表达水平;(F) 划痕实验的定量分析(n=3);(G-I) 体外血管生成实验的定量分析(n=3)。数据以平均值 ± 标准差表示,采用单因素方差分析结合杜凯事后检验,*P<0.05,**P<0.01,***P<0.005,****P<0.001。
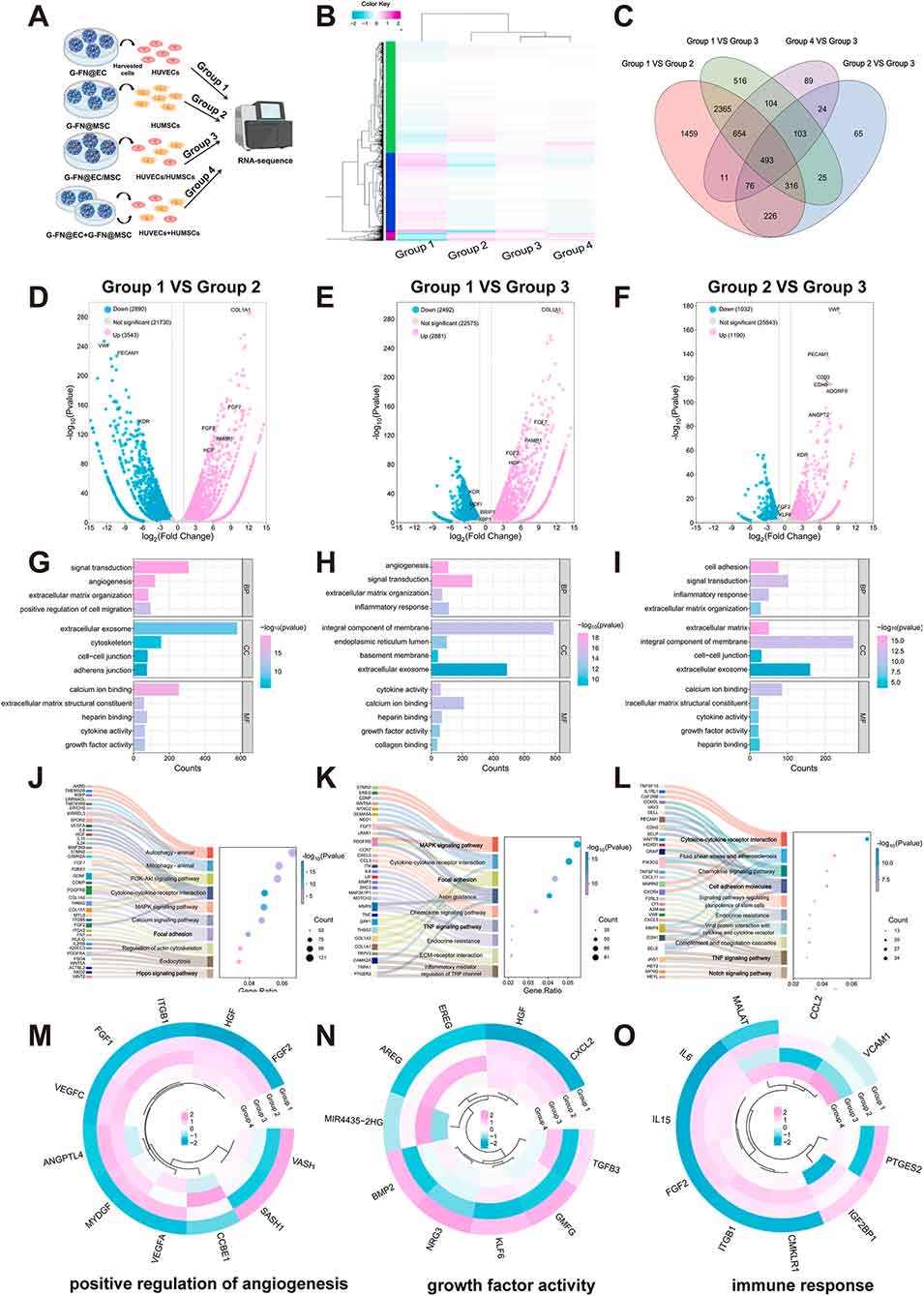
图6 转录组测序揭示不同细胞治疗方案的潜在机制。(A) 转录组测序实验组设计示意图;(B) 差异表达基因的表达水平热图;(C) 差异表达基因的韦恩图分析;(D-F) 差异表达基因的火山图;(G-I) 转录水平差异基因的基因本体(GO)富集分析;(J-L) 转录水平差异基因的京都基因与基因组百科全书(KEGG)通路富集分析;(M-O) 与重症肢体缺血治疗相关的基因本体术语的基因表达热图。
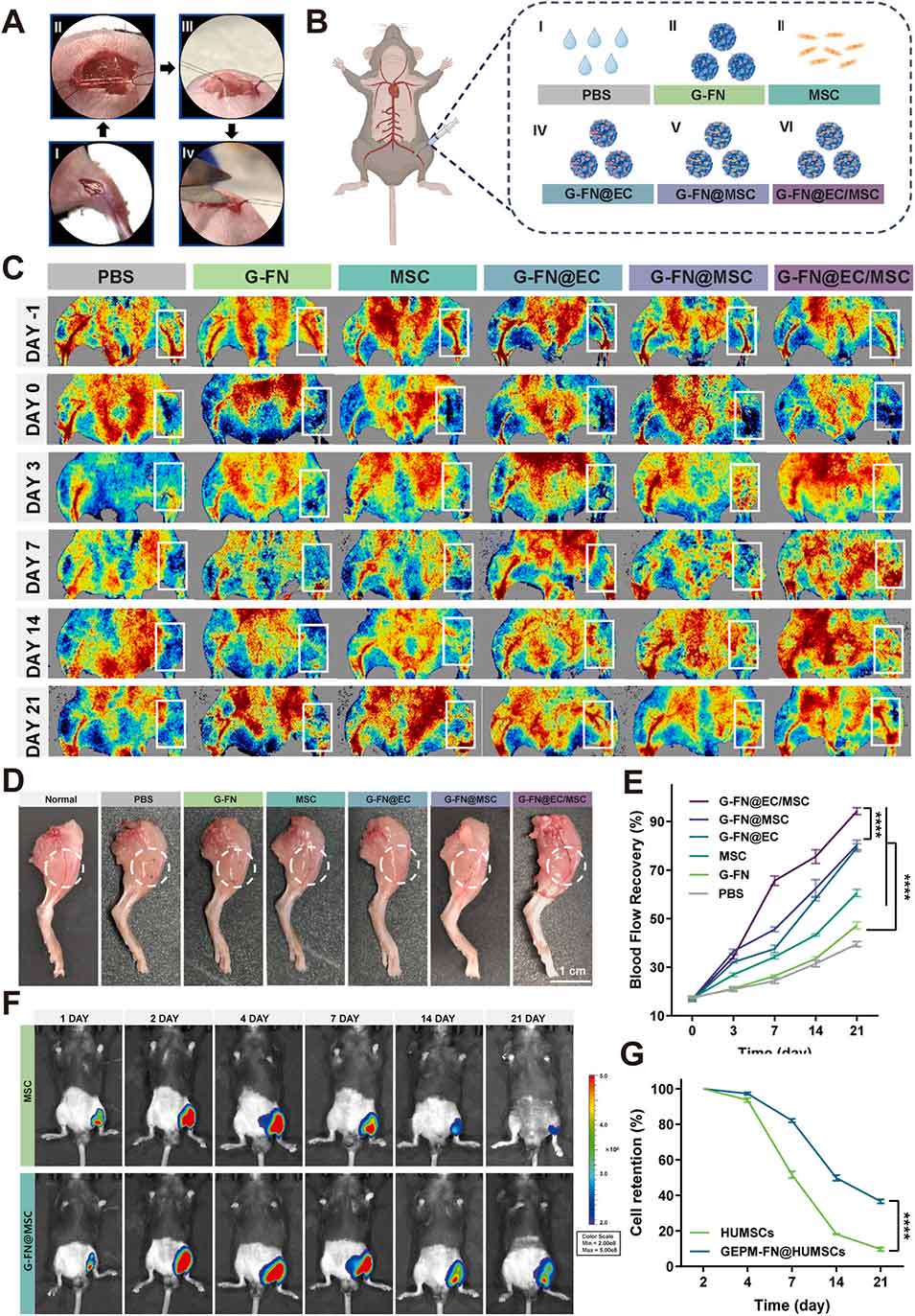
图7 不同细胞治疗方案在重症肢体缺血模型中的体内治疗效果评价。(A) 重症肢体缺血模型构建过程的代表性图像;(B) 重症肢体缺血治疗各组的实验设计;(C) 利用微循环血流成像系统动态监测不同治疗组后肢血流恢复情况,白色框选区域为关键感兴趣区;(D) 治疗 21 天后小鼠后肢解剖的代表性图像,白色虚线圆圈标记病灶区域;(E) 不同治疗组缺血区域的血流恢复曲线(n=5);(F) 直接注射与载体介导递送的体内细胞滞留情况对比;(G) 直接注射与载体介导递送的细胞滞留率定量分析(n=5)。数据以平均值 ± 标准差表示,采用双因素方差分析结合杜凯事后检验,*P<0.05,**P<0.01,***P<0.005,****P<0.001。
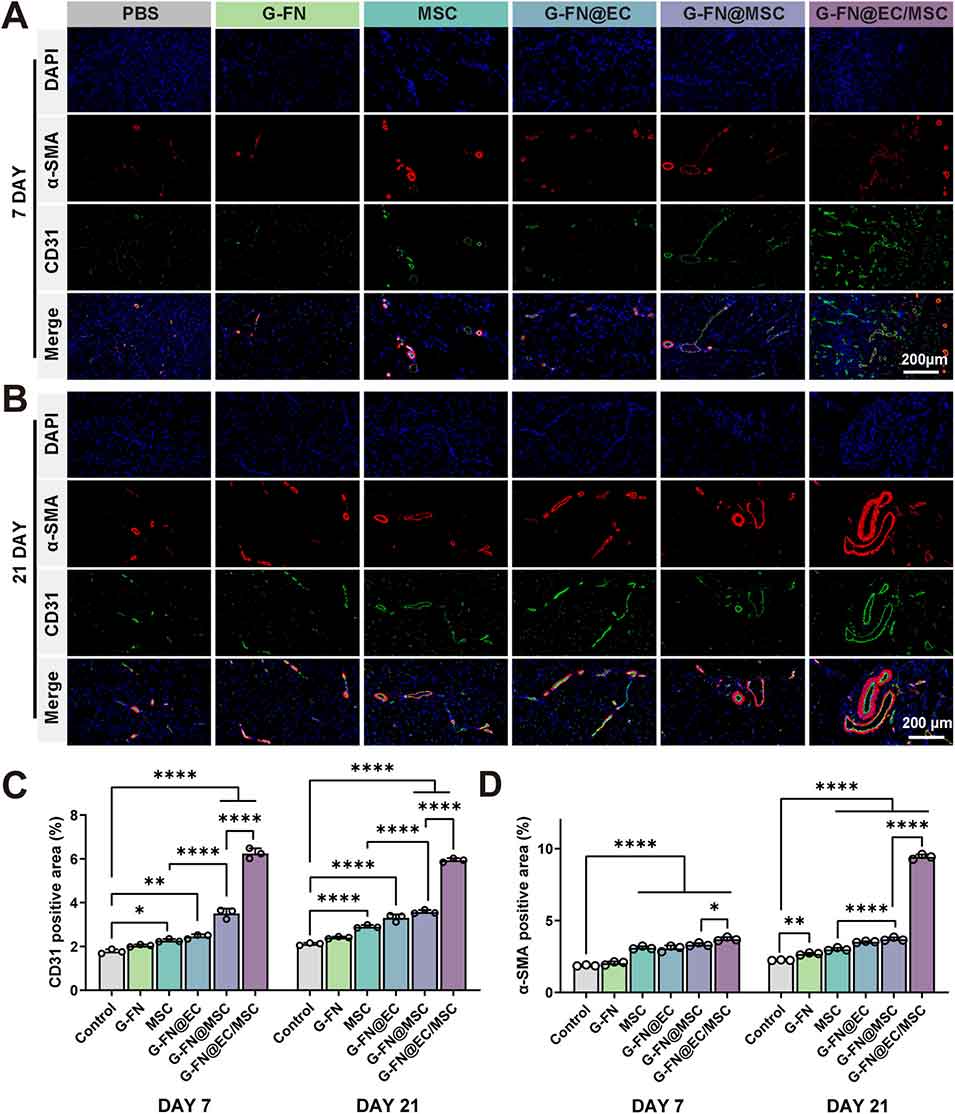
图8 治疗效果评价:缺血区域血管生成分析。(A) 治疗 7 天后,缺血部位骨骼肌经 α- 平滑肌肌动蛋白和血小板内皮细胞黏附分子免疫染色的血管生成评估图像;(B) 治疗 21 天后,缺血部位骨骼肌经 α- 平滑肌肌动蛋白和血小板内皮细胞黏附分子免疫染色的血管生成评估图像;(C) 治疗 7 天和 21 天后组织中 CD31 阳性区域的定量分析(n=3);(D) 治疗 7 天和 21 天后组织中 α- 平滑肌肌动蛋白阳性区域的定量分析(n=3)。数据以平均值 ± 标准差表示,采用单因素方差分析结合杜凯事后检验,*P<0.05,**P<0.01,***P<0.005,****P<0.001。
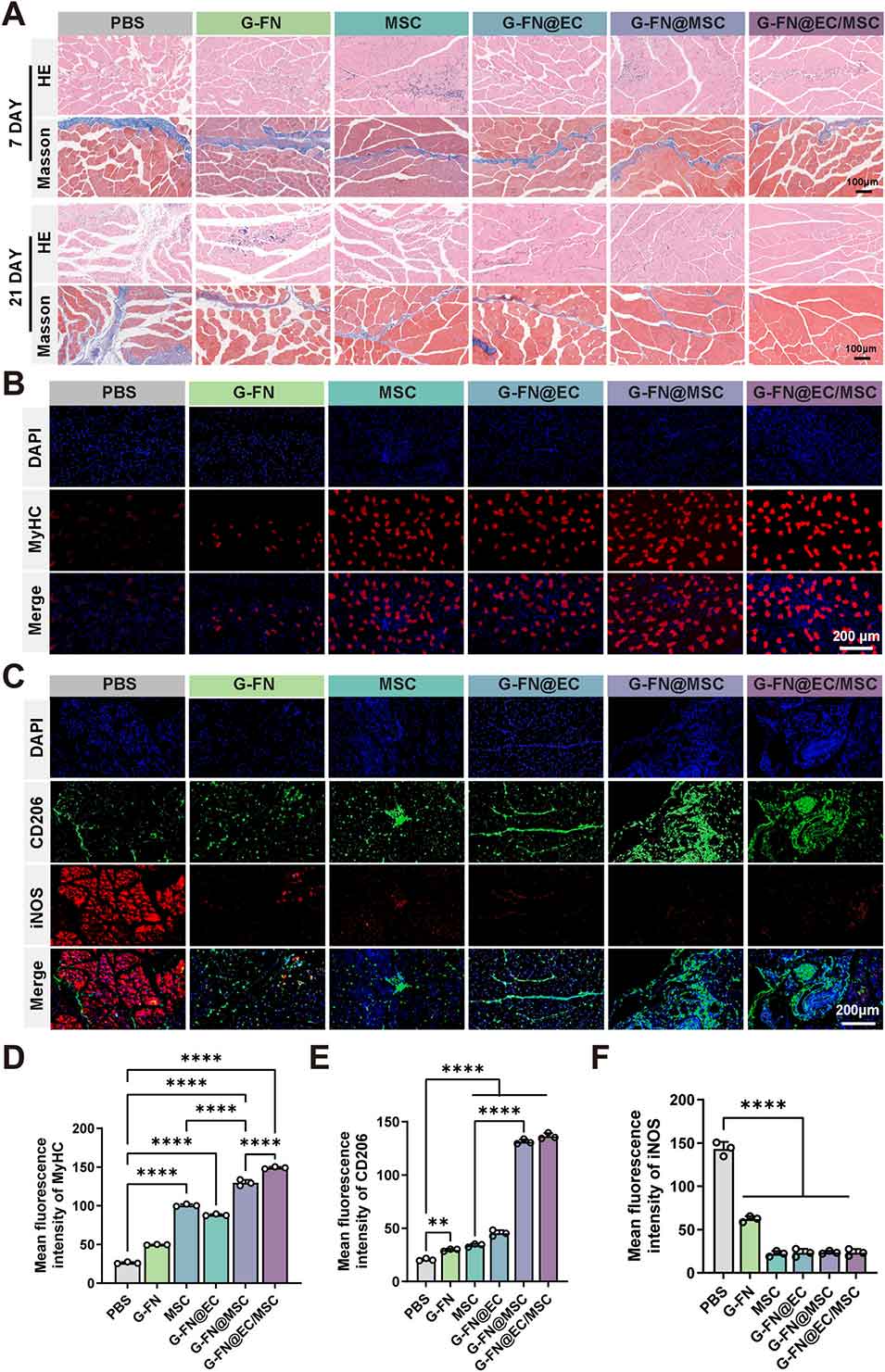
图9 缺血区域骨骼肌修复和炎症调控的治疗效果评价。(A) 治疗 7 天和 21 天后的苏木精-伊红染色及马松染色图像;(B) 治疗 21 天后,缺血骨骼肌经肌球蛋白重链免疫染色的肌肉修复评估图像;(C) 治疗 21 天后,缺血骨骼肌经 CD206 和诱导型一氧化氮合酶免疫染色的炎症调控评估图像;(D) 肌球蛋白重链平均荧光强度的定量分析(n=3);(E) CD206 平均荧光强度的定量分析(n=3);(F) 诱导型一氧化氮合酶平均荧光强度的定量分析(n=3)。数据以平均值 ± 标准差表示,采用单因素方差分析结合杜凯事后检验,*P<0.05,**P<0.01,***P<0.005,****P<0.001。
论文链接:https://doi.org/10.1016/j.bioactmat.2026.03.022
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














