导读:
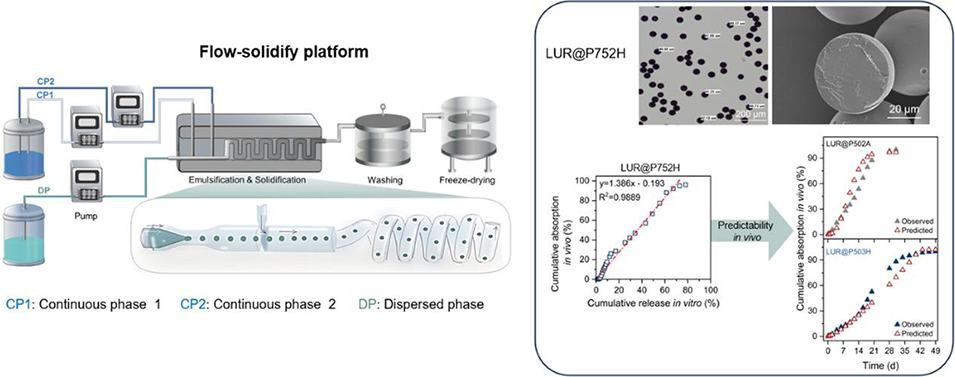
针对长效注射微球传统批量制备工艺存在的一致性差、难以建立可靠体外-体内相关性(IVIVC)的瓶颈问题,中国药科大学药学院刘东飞教授团队开发出一款端到端的连续流-固化制造平台,通过整合同轴毛细管可控乳化与双连续相超快速溶剂萃取固化两大核心模块,实现微球从液滴生成到固相成型的全程连续化、精准化控制。所得微球兼具结构均一、高药物负载率与优异的批次间一致性,为构建高预测性A级IVIVC模型奠定关键基础,也实现了可控制备工艺与可预测体内治疗效果的直接关联。相关研究以“Ultrafast solvent removal delivers high-loading of amorphous small-molecule drugs in polymeric microspheres with predictable in vivo performance”为题目,发表在期刊《Journal of Controlled Release》上。

本文亮点:
1、开发出一体化连续制备平台,实现可控液滴形成与超快固化的协同整合。
2、利用动力学捕获效应将药物稳定为无定形态,有效抑制药物结晶。
3、制得的微球兼具高载药量优势,且批次间一致性表现优异。
4、微球的均一结构为长效注射制剂搭建了可精准预测的体外-体内相关性模型。
完成装置组装、流体配制与输送系统调试后,平台进入连续化生产阶段,整个工艺为无间断的连续流程,从液滴生成到微球成型无需人工干预,后处理仅需简单的洗涤与冻干,具体步骤如下:
1、相液预热与脱气:将配制好的分散相(DP)与连续相(CP1/CP2)进行温和脱气处理,避免液滴生成过程中产生气泡,影响微球形貌;所有相液均在室温下输送,无需额外控温。
2、可控乳化液滴生成:通过无脉动活塞泵将CP1与DP分别输送至同轴毛细管乳化器。
DP从内毛细管100μm孔口流出,进入外毛细管的文丘里收缩区;
CP1从外毛细管环隙高速出流,通过流体剪切与共流聚焦作用,将DP剪切成单分散的有机液滴,液滴粒径由两相流速比精准调控。
3、超快速溶剂萃取与固化:生成的有机液滴随CP1流入下游的蛇形硅胶盘管,在盘管入口处通过独立通道引入CP2(次级连续相),实现双连续相对液滴的包裹与冲刷。
CP2的高速流入大幅提升了油-水界面的溶剂浓度梯度,触发超快速的溶剂萃取(二氯甲烷快速从有机液滴向水相扩散);
液滴在蛇形盘管内的停留时间约60min(由盘管总长度与总体积流速计算得出),此为溶剂完全萃取与微球固相成型的总时间,盘管的蛇形设计保证液滴与连续相的充分混合,溶剂去除更均匀。
4、产物连续收集:固相成型后的微球混悬液从蛇形盘管末端连续流出,收集至洁净容器中,整个收集过程无批次中断。
5、后处理步骤:收集的微球混悬液用去离子水多次洗涤,去除表面吸附的PVA与MgCl2,随后进行冷冻干燥,得到干燥的PLGA微球成品,用于后续理化表征与体内外实验。
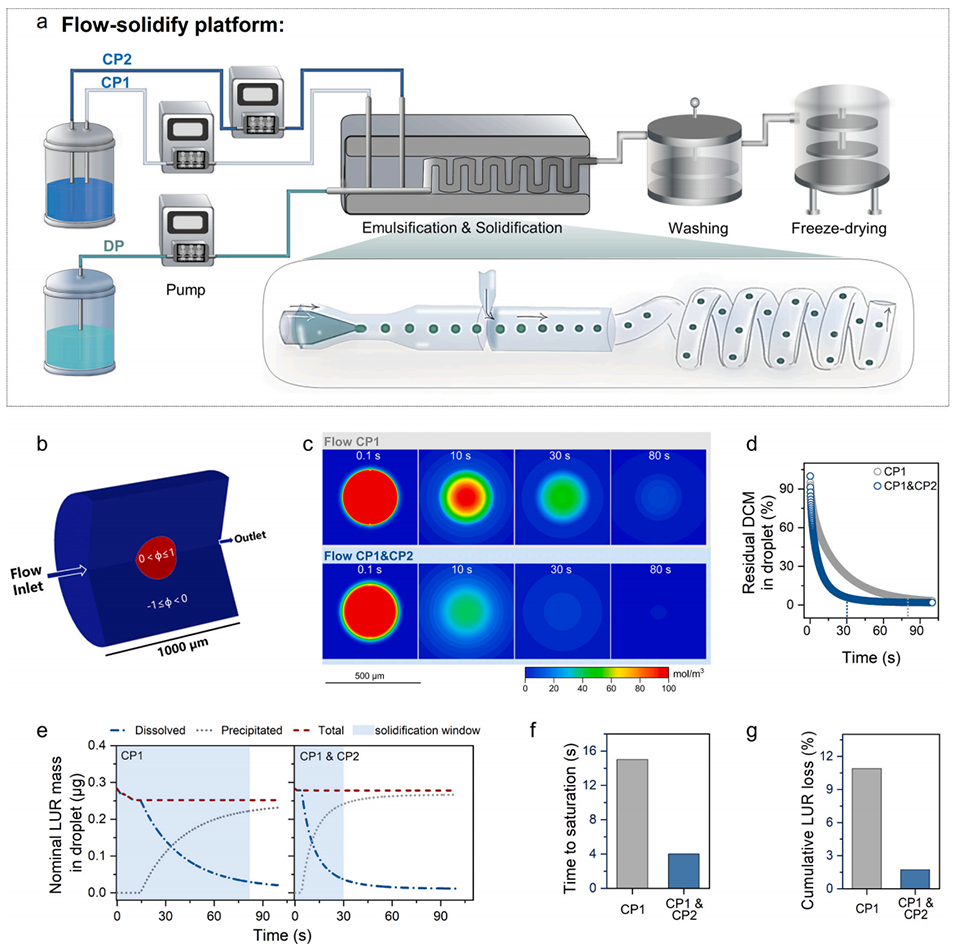
图1. 连续流-固化平台及液滴固化过程中的动力学捕获机制
该一体化平台整合了可控液滴形成与超快固化步骤,通过加速溶剂去除实现动力学捕获,将难溶性小分子药物以稳定的无定形固体分散体形式包封在PLGA聚合物微球中,增强了药物-聚合物相互作用并抑制药物结晶,最终制备的微球具备结构可控、载药量高、批次间一致性优异的特点,还大幅降低了残留溶剂含量,提升了工艺安全性。
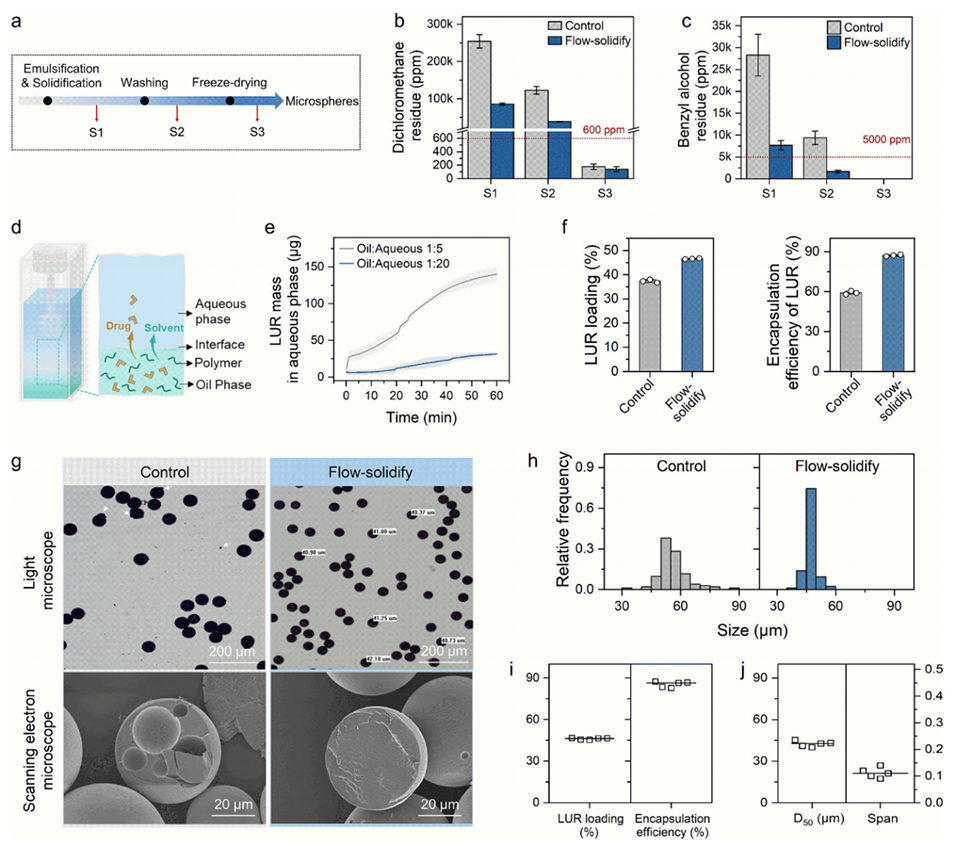
图2. 连续流-固化平台的动力学捕获效应验证及微球均一性提升效果
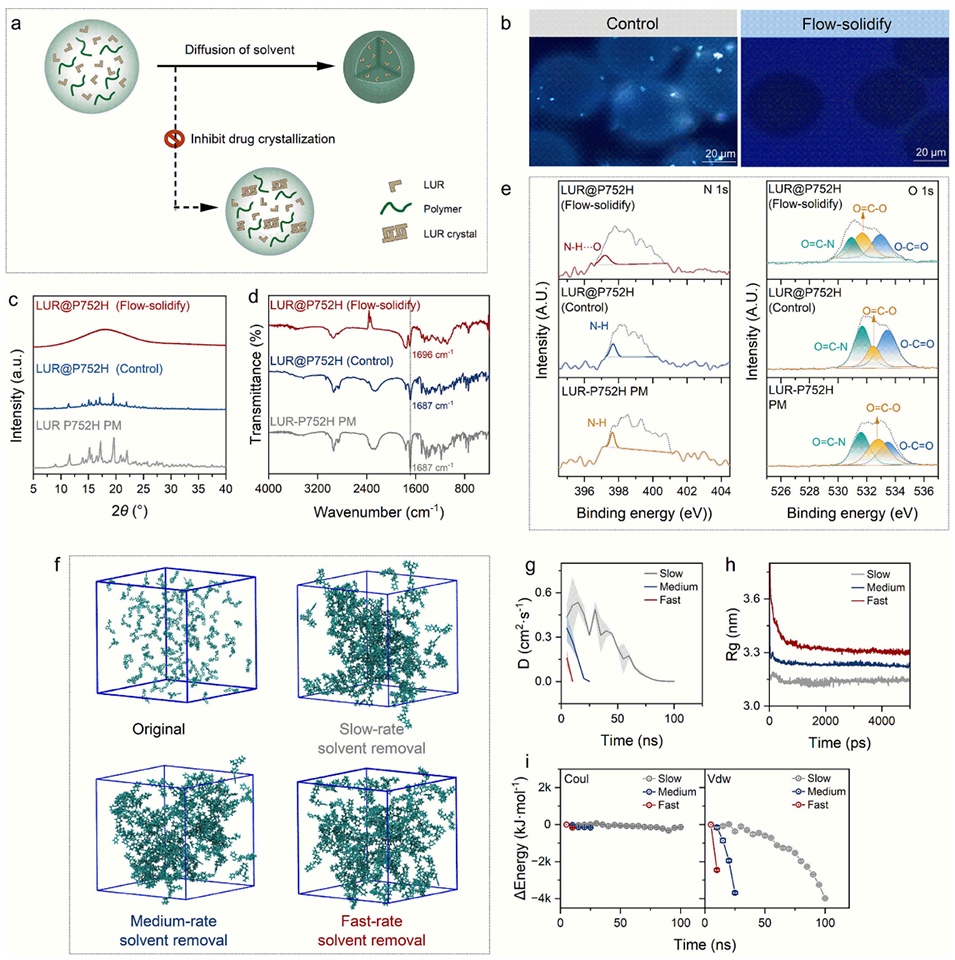
图3. 溶剂去除速率对盐酸鲁拉西酮分子堆积影响的实验与计算分析
研究以盐酸鲁拉西酮为模型药物,结合计算流体动力学模拟、分子动力学模拟和一系列实验表征,验证了超快溶剂去除能有效抑制药物结晶、强化药物-聚合物相互作用,且该平台具有良好的鲁棒性和通用性,可适配不同PLGA聚合物型号,还成功包封了孕酮、利培酮等不同理化性质的难溶性药物,均实现高载药量与高包封效率。
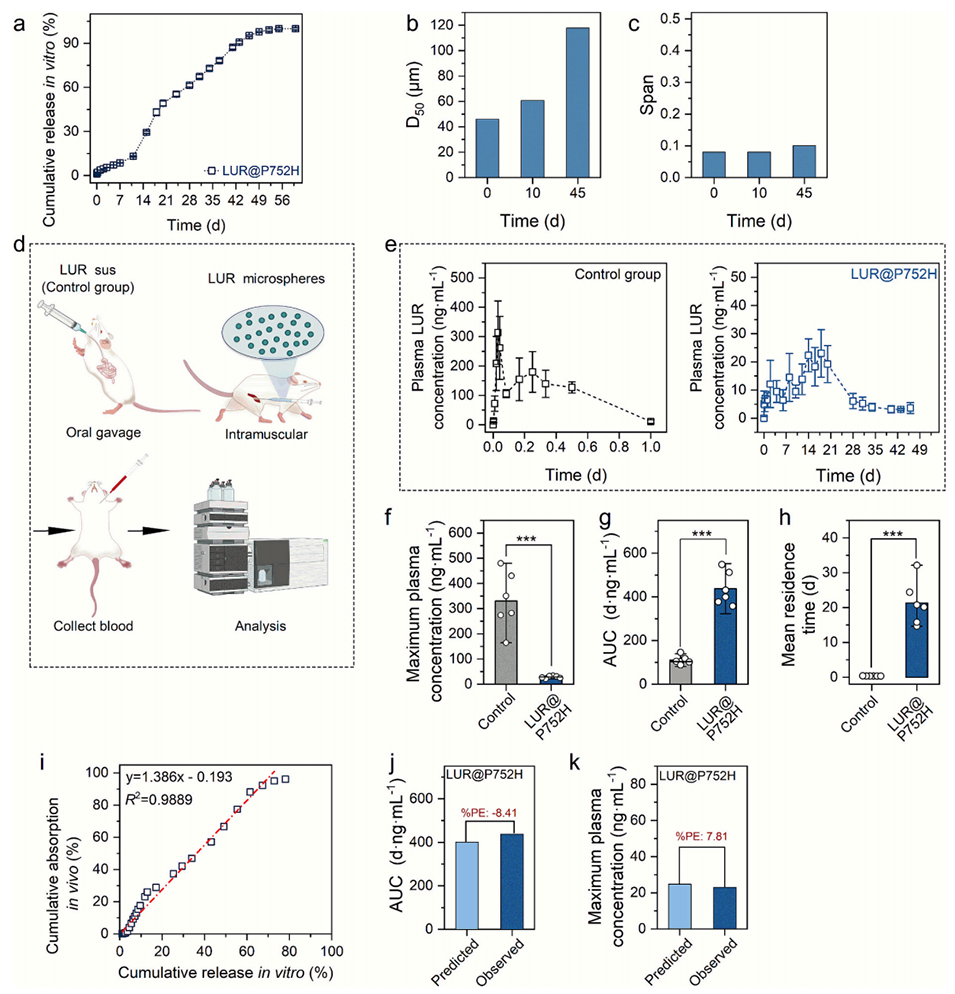
图4. 载盐酸鲁拉西酮的PLGA 752H微球的药代动力学评价及体外-体内相关性分析
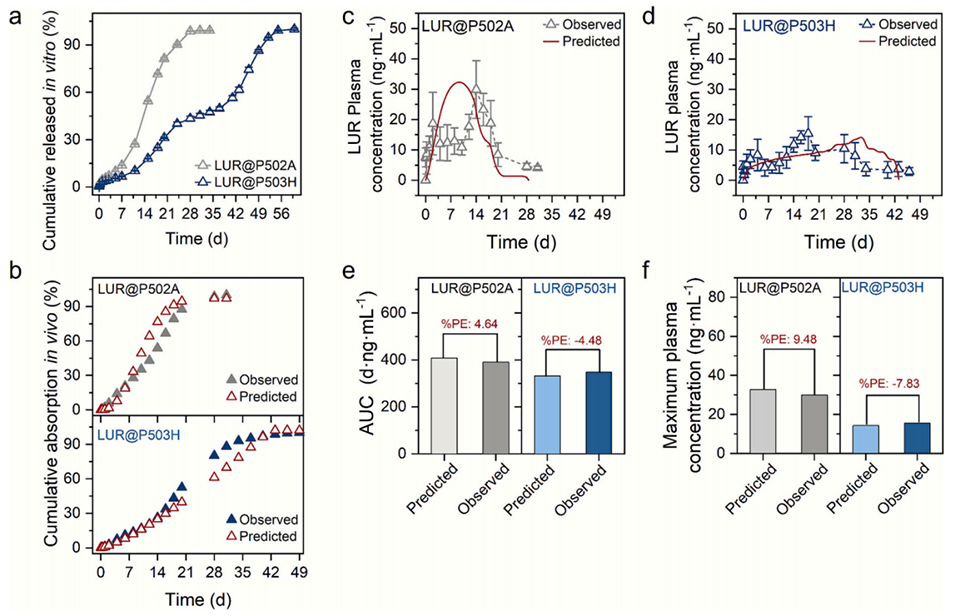
图5. 连续流-固化平台助力基于体外-体内相关性模型的体内药代动力学精准预测
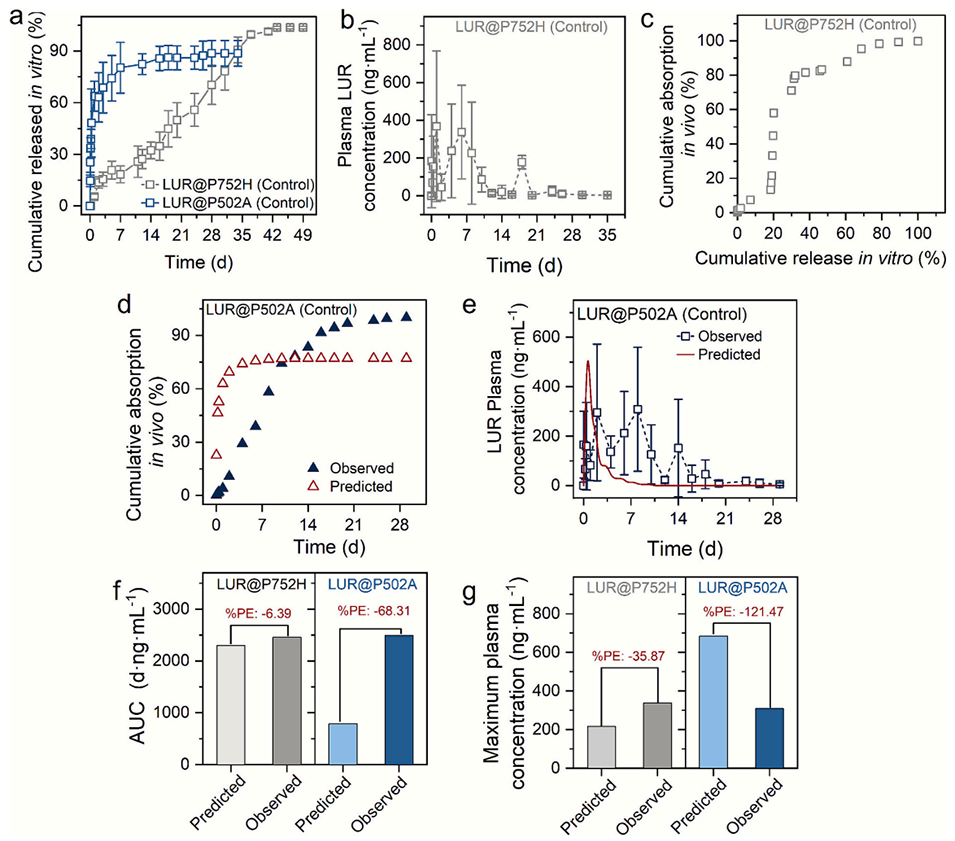
图6. 传统固化法制备微球的体外-体内相关性评价及预测效果
体外释放和体内药代动力学研究表明,该平台制备的微球突释效应低、释放长效可控,且能在大鼠体内维持稳定的血药浓度,显著提升药物暴露量和滞留时间。关键是利用其微球优异的结构均一性,建立了A级IVIVC模型(R²=0.9889),可仅通过体外释放数据精准预测不同配方的体内药代动力学曲线,关键参数(Cmax、AUC)预测误差均在±10%的严苛监管标准内;而传统工艺制备的微球因结构异质性,无法建立有效IVIVC,预测误差远超标准。
研究证实,该连续流-固化平台通过精准的工艺控制实现了微球结构的高度均一,搭建起工艺与性能的直接关联,解决了长效PLGA微球制备的核心痛点,不仅减少了对动物实验的依赖,还加速了难溶性小分子药物长效注射微球的研发与临床转化,同时该平台具备工业规模化潜力,契合质量源于设计和连续制造的制药行业发展趋势。
论文链接:https://doi.org/10.1016/j.jconrel.2026.114639
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














