金纳米颗粒(AuNP)具备优异的光学、吸光和产热性能,广泛应用于有机太阳能电池、导电材料、催化剂等领域;海胆状金纳米颗粒(AuNU)因表面电位不均,在近红外区存在最大吸收峰,可应用于活体筛查、光热治疗等医疗场景,但纳米级的AuNU易被吞噬、易团聚丧失光学性能,成为药物递送的核心痛点。

近期,京都大学团队利用喷墨混合系统(IMS)制备出含金纳米颗粒(AuNP)的壳聚糖微胶囊,对比优化了离子交联与反溶剂沉淀两种制备方法,还通过银离子介导合成了包封海胆状金纳米颗粒(AuNU)的壳聚糖微胶囊,实现了其近红外吸收波长的精准调控,同时提升了微胶囊的酸环境耐久性,有效解决了海胆状金纳米颗粒易被吞噬、易团聚的问题。相关研究以“Production of gold nanoparticle-containing chitosan microcapsules using an inkjet mixing system and control of the absorption wavelength”为题目,发表在期刊《Chemical Engineering Journal》上。
本文要点:
1、利用喷墨混合系统(IMS)通过离子交联法和反溶剂沉淀法制备了含金纳米颗粒(AuNP)的壳聚糖微胶囊,发现反溶剂沉淀法制备的AuNP粒径更小且分布更均一,但存在金包封效率低、酸环境耐久性差的问题,经磷钨酸(PTA)后续交联可显著提升其酸稳定性。
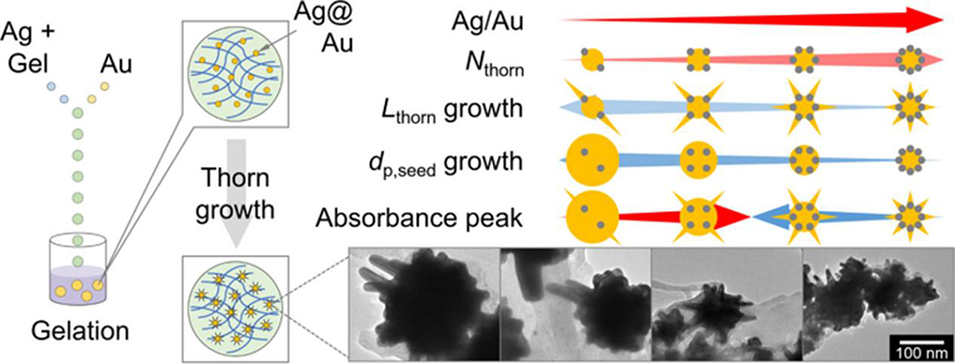
2、同时通过银离子介导,利用IMS成功合成了含海胆状金纳米颗粒(AuNU)的壳聚糖微胶囊,证实该微胶囊的吸收波长可通过调控种子颗粒表面银量(Ag/Au比)和刺生长阶段的金离子(HAuCl₄)浓度实现精准控制,其中金离子浓度升高使吸收峰波长单调增加,银量增加则让吸收峰波长先升后降(最佳Ag/Au比约0.6mol/mol)。
3、该微胶囊解决了AuNU在药物递送中易被吞噬、易团聚的核心问题,且酸稳定性适配结肠递送需求,虽IMS存在产率低的问题,但其高重现性使其适合高价值的药物递送领域,为AuNU在活体筛查、光热治疗等医疗领域的应用奠定了坚实基础。

图1. 喷墨混合系统(IMS)概念图

图2. 两种方法制备的微胶囊产物数码显微镜图像及收集瓶中产物外观:(a)离子交联法, (b)反溶剂沉淀法
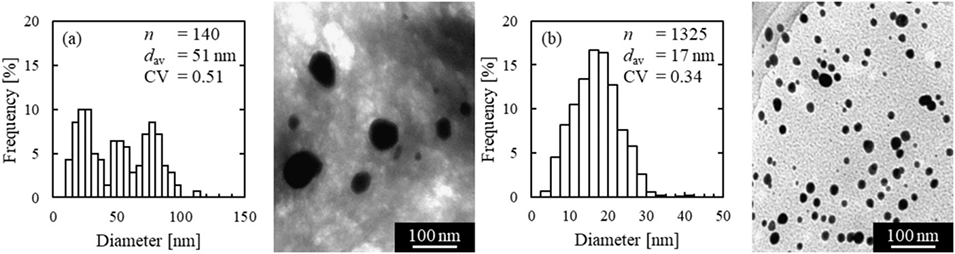
图3. 微胶囊内金纳米颗粒的粒径分布及透射电镜图像:(a)离子交联法,(b)反溶剂沉淀法。图中CV为变异系数

图4. 含金纳米颗粒的壳聚糖凝胶微胶囊在模拟胃液中浸泡24小时后的数码显微镜图像:(a)离子交联法,(b)反溶剂沉淀法 + 磷钨酸增强处理

图5. 种子颗粒与海胆状金纳米颗粒悬浮液的吸收光谱、颗粒的透射电镜图像及海胆状金纳米颗粒刺的高分辨透射电镜图像。
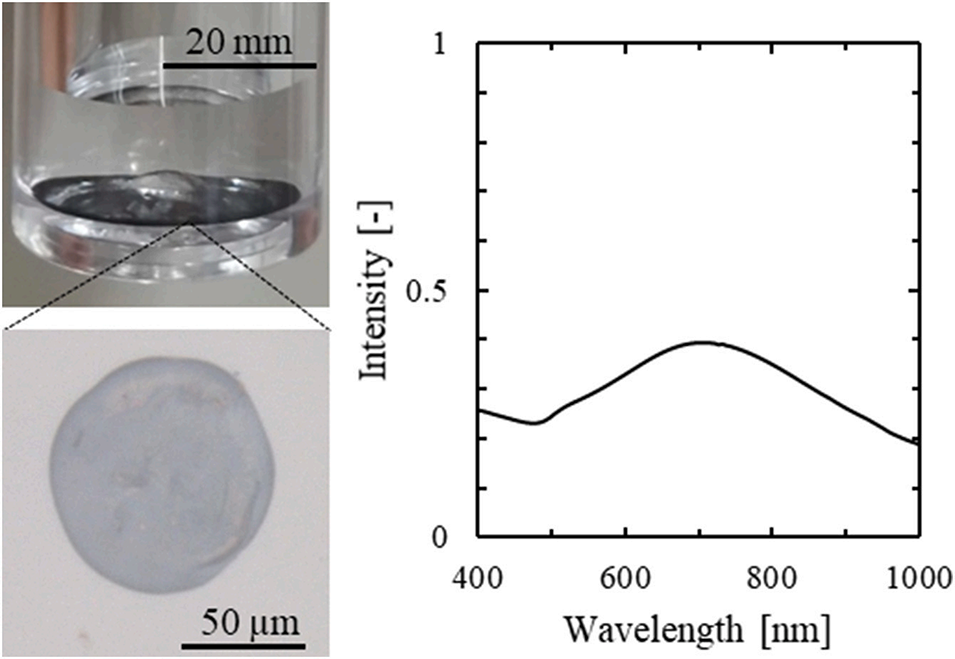
图6. 产物悬浮液外观、吸收光谱及微胶囊的数码显微镜图像。实验条件:喷射液滴为表1中的A3和B3溶液,收集液为含30 mM抗坏血酸与30 g/L磷钨酸的去离子水溶液,刺生长用氯金酸浓度为3 mM
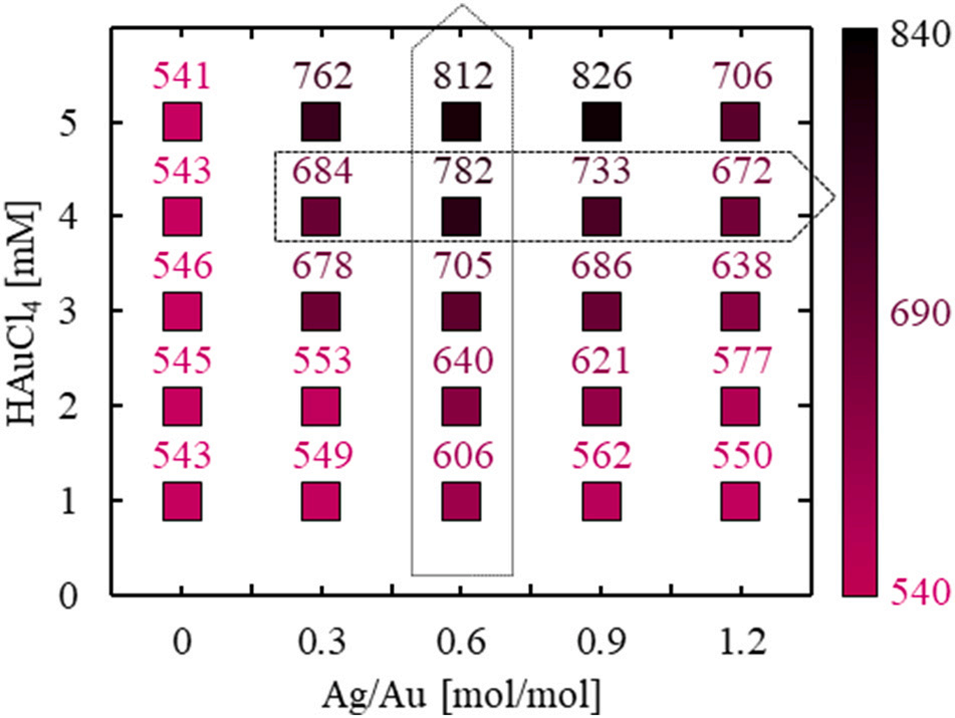
图7. 液滴碰撞时的银金摩尔比、刺生长阶段金离子浓度与吸收峰波长的关系。透射电镜图像对应图8中(a)虚线框、(b)虚线框区域,箭头为观察方向
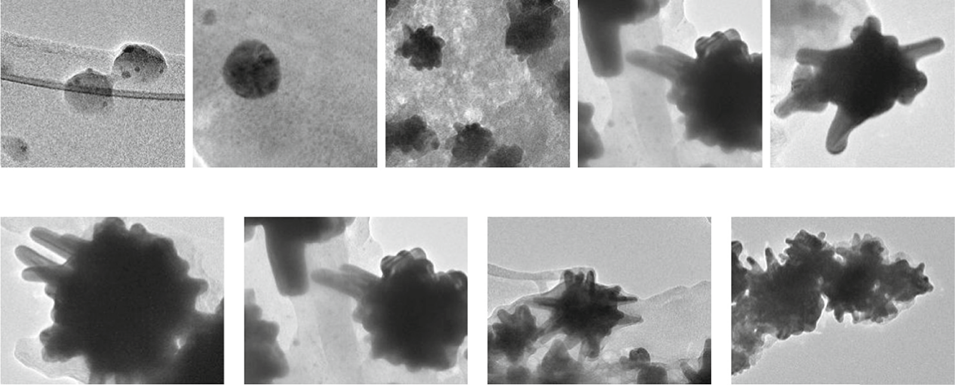
图8. 合成颗粒的透射电镜图像。(a)氯金酸浓度对刺生长的影响,银金摩尔比= 0.6 mol/mol(b)液滴碰撞时银金摩尔比对颗粒的影响,氯金酸浓度= 4 mM
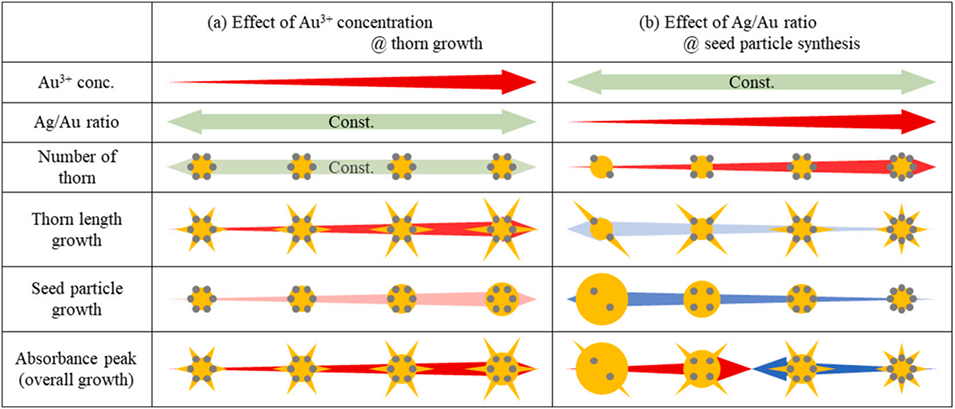
图9. 海胆状金纳米颗粒生长行为及吸收峰变化的概念图。(a)刺生长阶段金离子浓度的影响,(b)种子颗粒合成时银金摩尔比的影响
论文链接:https://doi.org/10.1016/j.cej.2026.174028
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














