围手术期神经认知障碍(PND)是老年手术患者(≥60 岁)的常见并发症,发生率高达40%-50%,这往往会延长患者住院时间、增加神经退行性疾病(如阿尔茨海默病)风险、提升死亡率并加重社会经济负担。目前PND的发病机制尚不明确,现有优化麻醉流程、抗炎等治疗手段效果有限或伴随明显副作用,因此亟需探索新靶点与治疗策略。

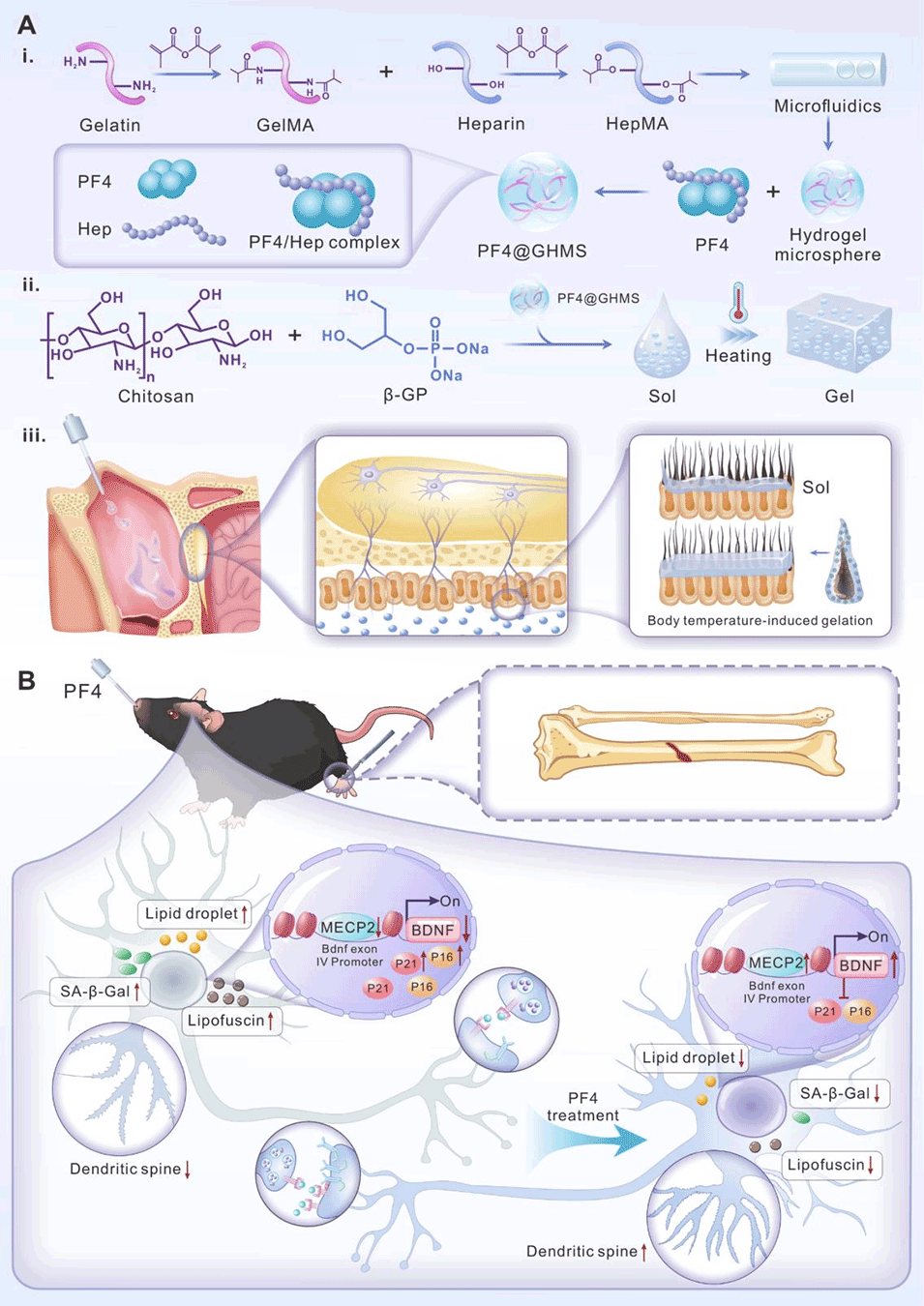
近期,同济大学医学院李成教授、高霄飞副研究员、Qiang Liu等人围绕老年患者PND展开研究,发现麻醉与手术会加重老年小鼠海马神经元衰老负荷,而血小板因子4(PF4)可通过激活Mecp2-BDNF通路减轻该负荷并改善认知,进而研发出PF4@GHMG复合微球水凝胶鼻脑递送系统实现PF4微创长效释放。相关研究以“Target anesthesia and surgery induced senescent cell via composite microsphere hydrogels as nose-to-brain amplifiers of platelet factor 4 delivery for neurocognitive dysfunction repair”为题目,发表于期刊《Biomaterials》。
本文要点:
1、本研究聚焦围手术期神经认知障碍(PND),旨在明确其发病机制并开发有效治疗方案。
2、研究发现,麻醉与手术会加重老年小鼠海马神经元衰老负荷,表现为衰老相关标志物(如P16、P21、SA-β-Gal)表达升高、脂褐素和脂滴积累及突触功能异常,进而导致认知障碍;而年轻小鼠因血小板因子4(PF4)代偿性升高更显著,未出现认知问题。
3、实验证实,腹腔注射PF4可通过上调Mecp2-BDNF通路,减轻老年手术小鼠神经元衰老负荷、改善突触可塑性与认知功能,且无明显毒副作用。
4、为优化给药方式,本研究利用微流控技术制备负载PF4的明胶甲基丙烯酸酯/肝素甲基丙烯酸酯微球(PF4@GHMS),并与壳聚糖(CS)基温敏水凝胶复合形成PF4@GHMG。
5、该复合水凝胶经鼻给药时,能在体温下凝胶化,延长鼻腔滞留时间、实现PF4持续释放,高效靶向脑部,显著提升老年手术小鼠颅内药物浓度,有效改善其认知功能,且局部和全身生物安全性良好。
6、综上,该研究揭示了细胞衰老在PND中的关键作用,提出以PF4为靶点、鼻用复合水凝胶为给药载体的治疗策略,为PND及其他衰老相关中枢神经系统疾病提供新方向。
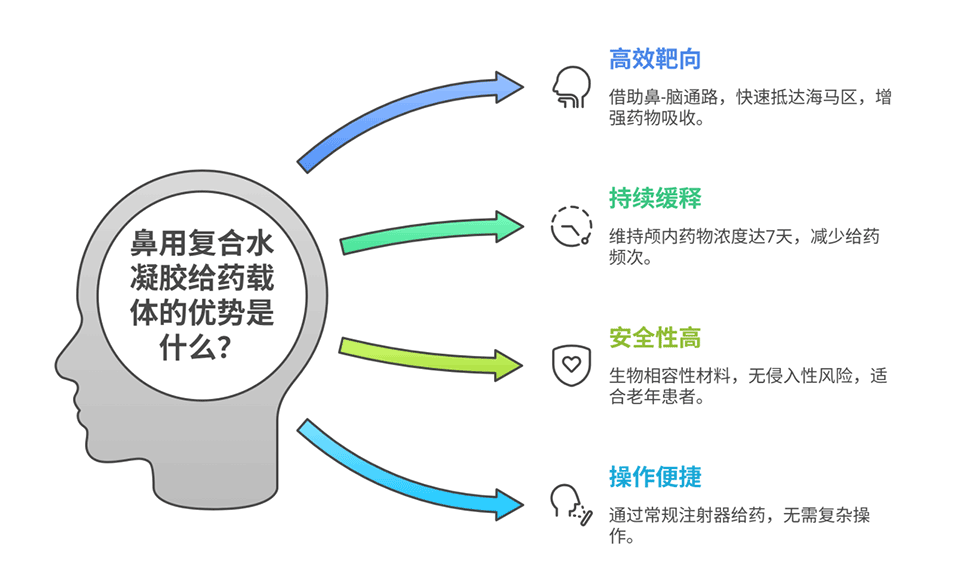
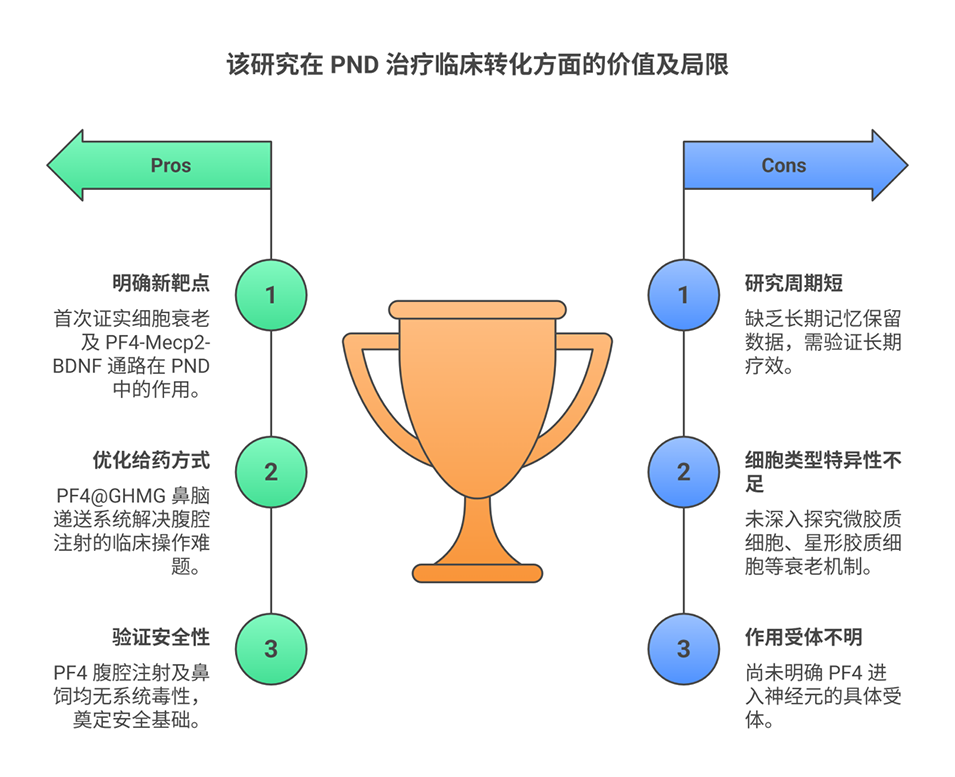
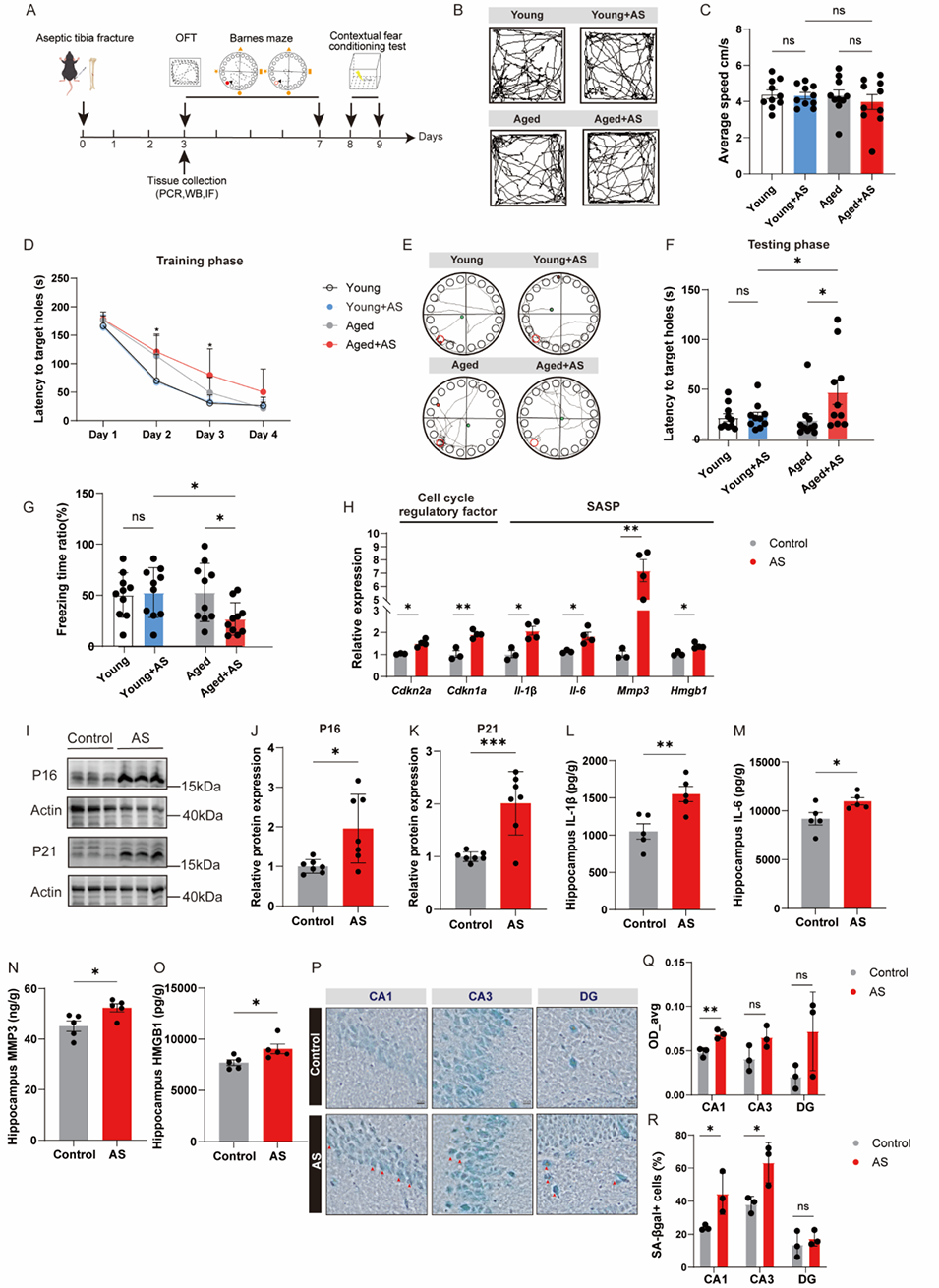
图1. 麻醉与手术上调衰老相关分泌表型(SASP)及周期蛋白依赖性激酶(CDK)抑制因子的表达,损害老年小鼠的学习记忆功能
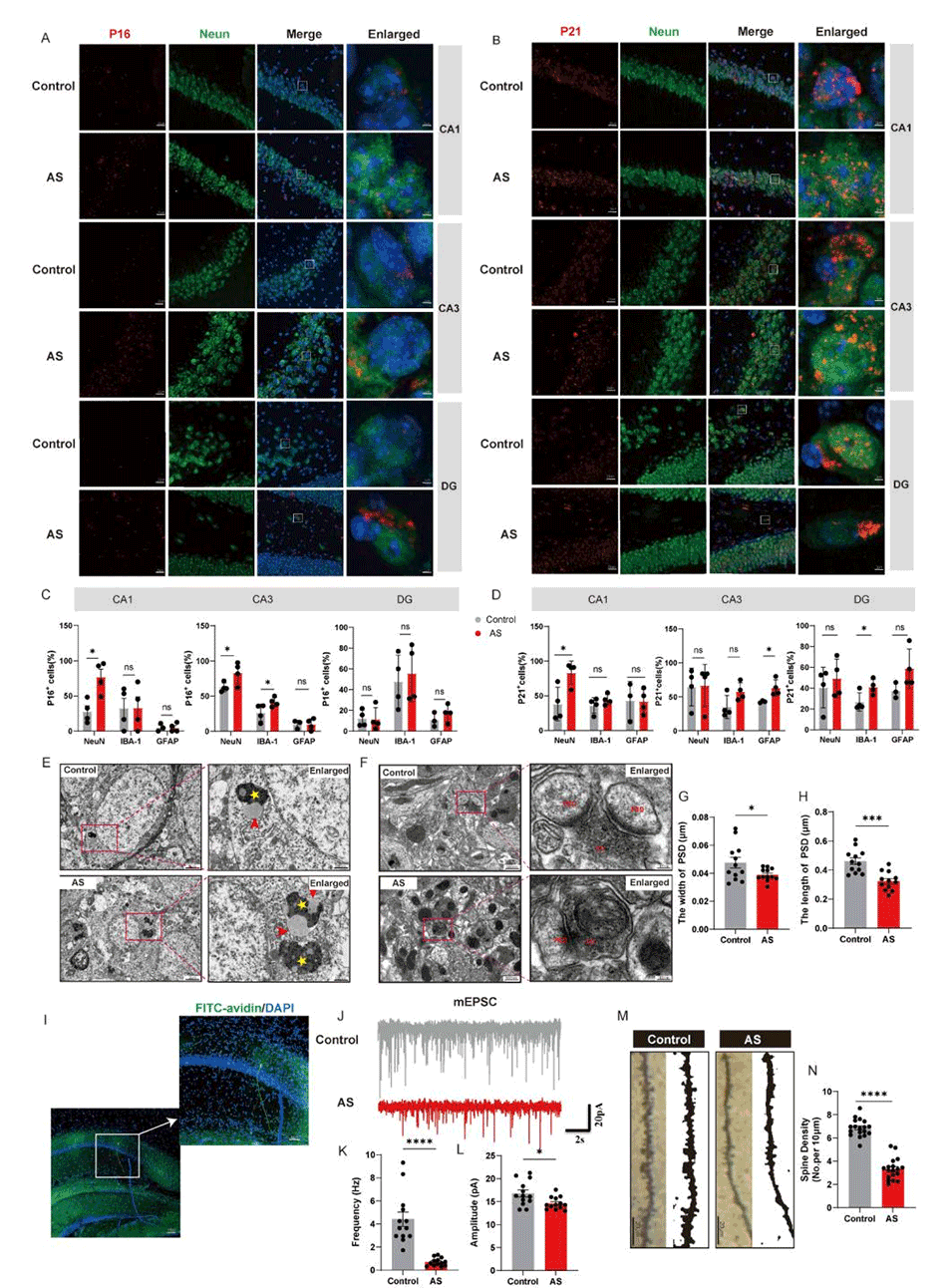
图2. 麻醉与手术加重神经元衰老样表型,破坏突触结构与功能
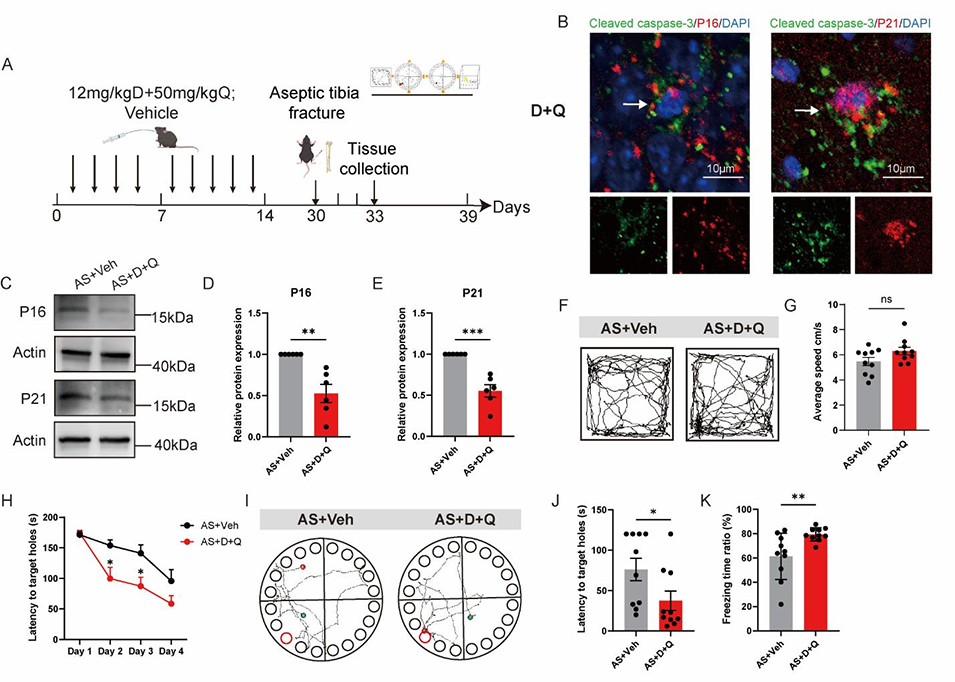
图3. 达沙替尼+槲皮素(D+Q)清除衰老细胞,改善麻醉/手术诱导的认知功能障碍
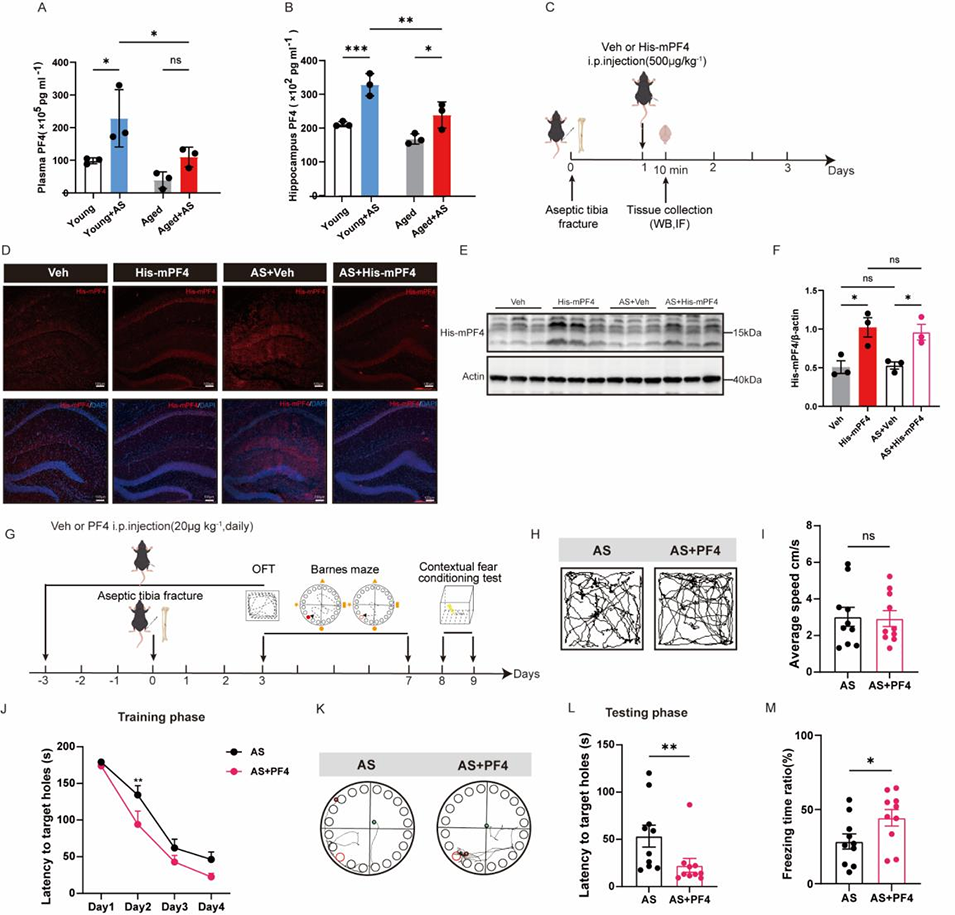
图4. 外周注射血小板因子4(PF4)升高海马区PF4浓度,缓解老年手术小鼠的神经认知衰退
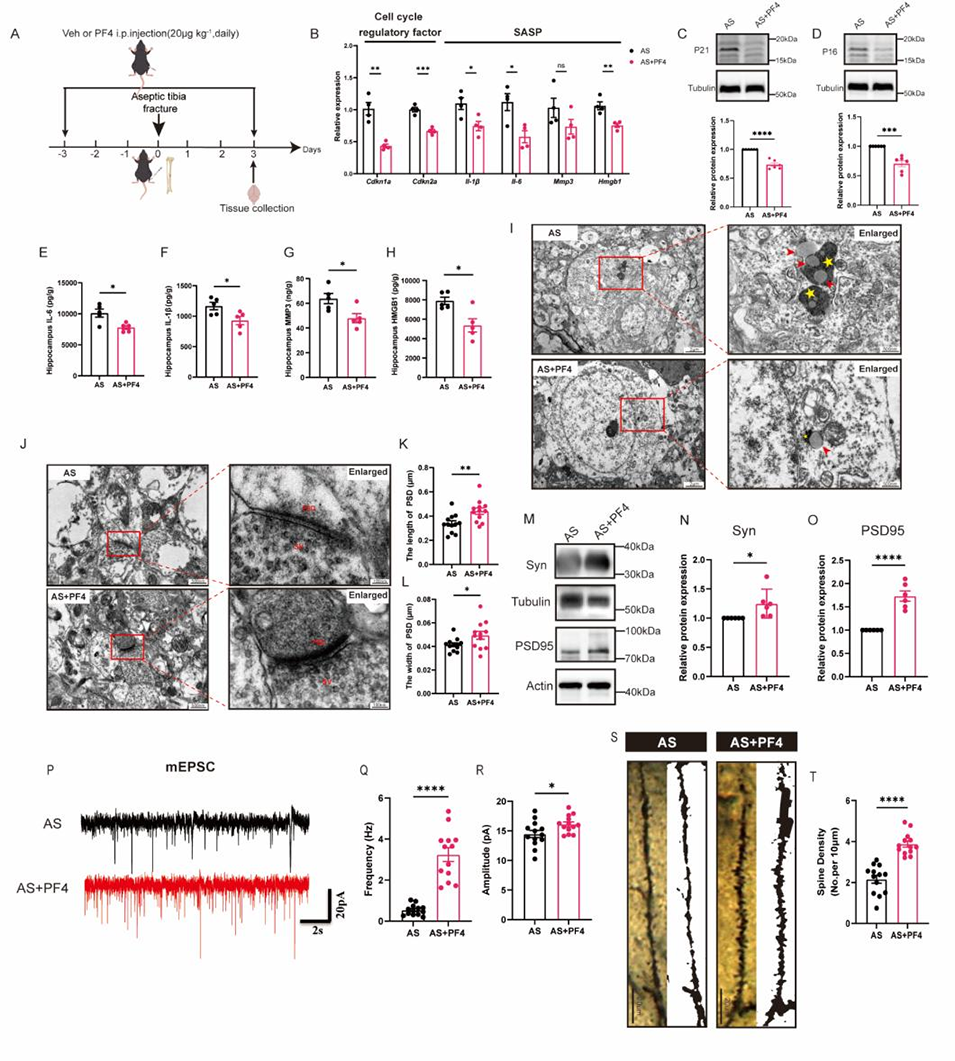
图5. 麻醉与手术前全身性给予PF4,减轻神经元衰老负荷并改善突触可塑性
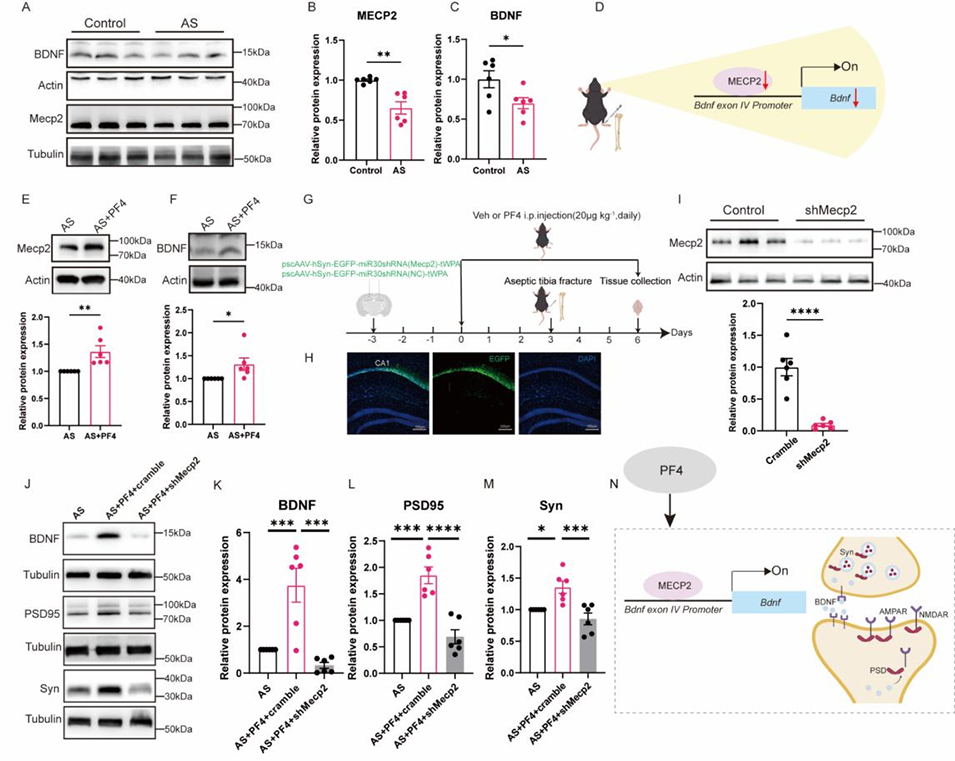
图6. 血小板因子4(PF4)通过Mecp2-BDNF通路介导认知功能改善
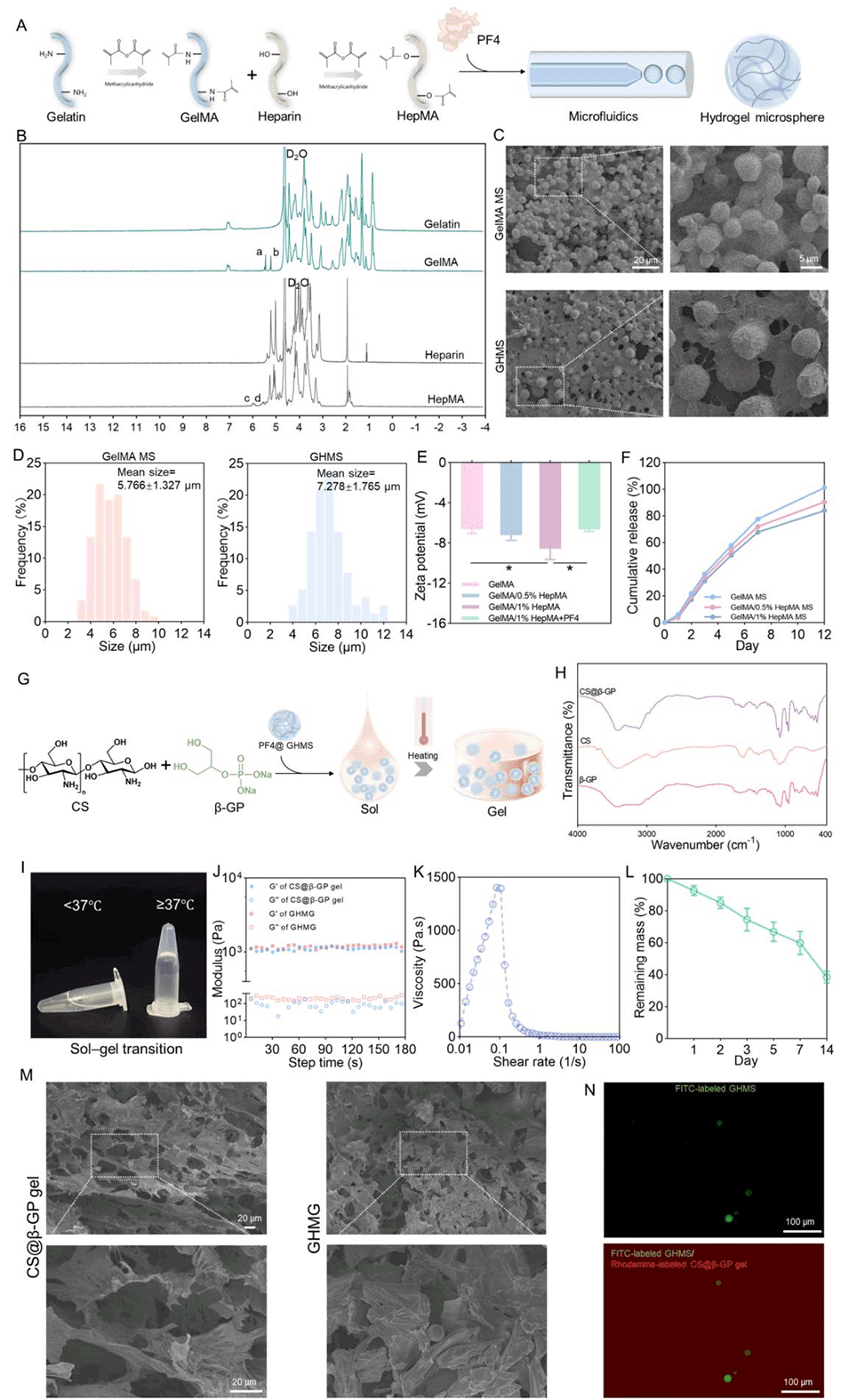
图7. 鼻用微球复合水凝胶的制备与表征
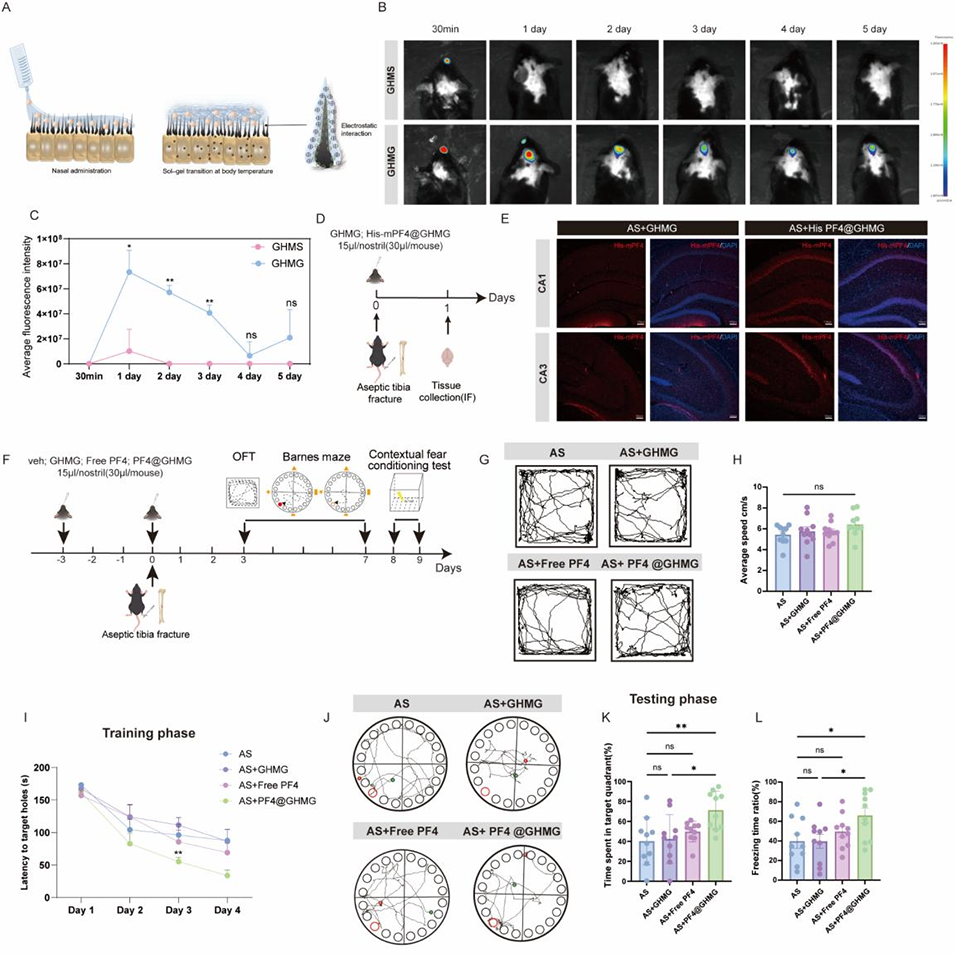
图8. 复合水凝胶(GHMG)的体内药物滞留效果及神经认知功能验证
论文链接:https://doi.org/10.1016/j.biomaterials.2025.123863
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














