
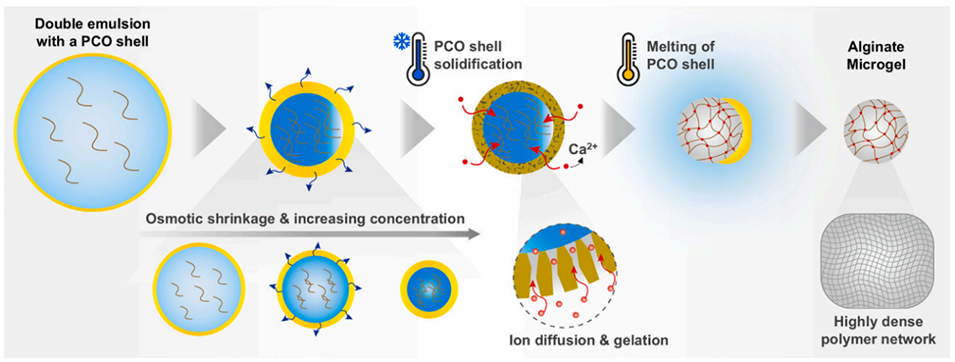
导读:
近期,有研究人员开发了一种结合相变油壳调控凝胶化与渗透收缩的微流控新方法,成功制备出具有高浓度、单分散性好且释放性能可控的海藻酸盐微凝胶。该方法通过热诱导油壳形成微裂纹以实现均匀离子交联,并利用渗透压使海藻酸盐预浓缩,显著提升了微凝胶的聚合物密度和屏障性能。相关研究以“Formation of high-concentration alginate microgels via double emulsion Shell-mediated gelation and osmotic shrinkage”为题目,发表在期刊《Journal of Colloid and Interface Science》上。
本文要点:
1、本研究开发了一种微流控双乳液模板法,通过相变油壳介导凝胶化与渗透收缩协同策略制备高浓度海藻酸盐微凝胶。
2、利用十六烷油相冷却固化形成微裂纹,引导钙离子定向扩散实现均匀交联;借助高渗环境使液滴收缩预浓缩藻酸盐,最终获得聚合物浓度高达10%的微凝胶。
3、该微凝胶具有单分散性好、形态规整、网络致密的特点,其分子渗透性可调并呈现pH响应性释放行为,为口服药物递送及生物封装提供了性能优越的新平台。

本研究开发的高密度海藻酸盐微凝胶,凭借其致密网络结构与低渗透性,在生物医药领域展现出以下应用潜力:
1、长效缓释药物制剂
利用其致密网络延缓药物扩散,装载多肽、蛋白质等易降解药物,实现长达数周至数月的持续释放,显著延长药效周期并减少给药频率。
2、免疫隔离细胞移植载体
凭借低渗透性有效阻挡宿主免疫细胞和抗体攻击,同时允许营养物质交换,为胰岛细胞、干细胞移植提供免疫豁免微环境,助力糖尿病或退行性疾病的细胞治疗。
3、肠道菌群精准调控制剂
作为高稳定性递送系统,保护益生菌或工程菌免受胃酸侵蚀,确保活菌高效递送至肠道定殖,用于炎症性肠病或菌群失调相关疾病的干预治疗。
4、植入式医用屏障材料
制成薄膜或涂层敷料,利用低渗透性物理阻隔细菌侵入或术后组织粘连,并可负载抗菌/抗粘连药物缓慢释放,促进创伤修复或减少手术并发症。
5、高稳定生物传感界面
封装酶、抗体等生物探针,其致密网络可排除生物样本中大分子杂质干扰,显著提升体外诊断灵敏度和体内植入传感器的长期稳定性与准确性。
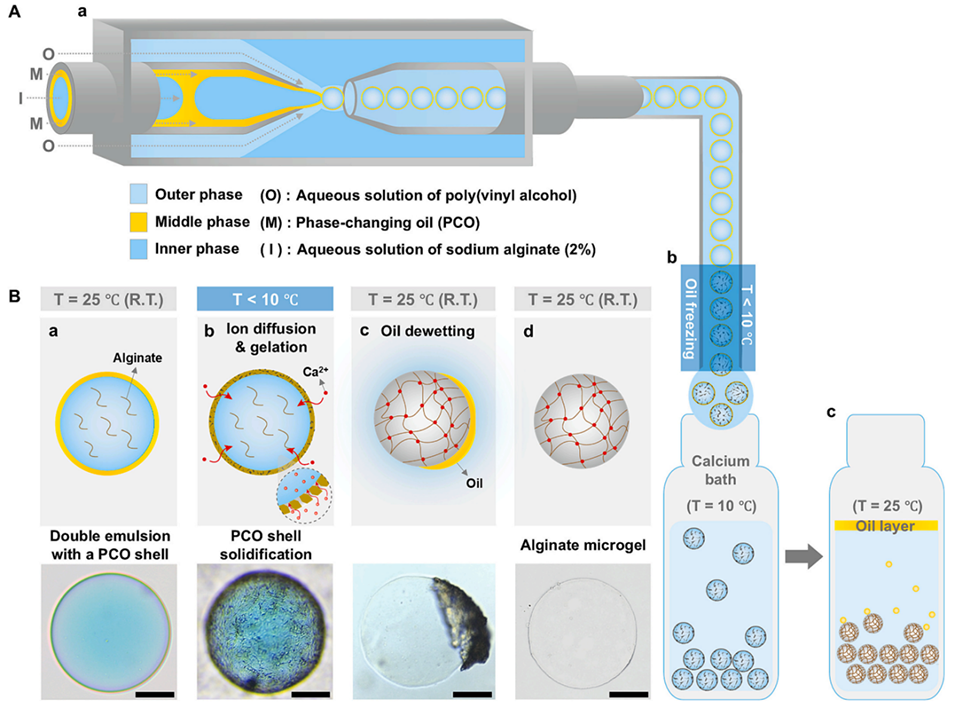
图1. 利用含相变油(PCO)壳的双乳液通过微流控技术制备海藻酸盐微凝胶。
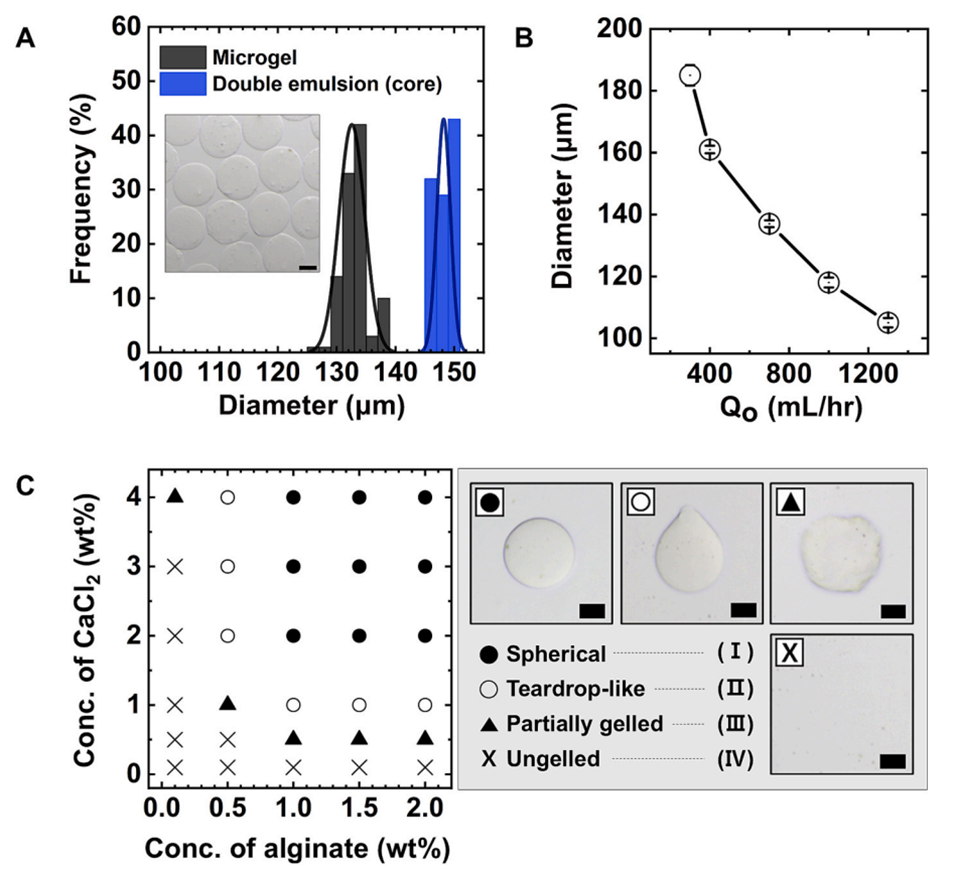
图2. 通过流动条件与组分调控海藻酸盐微凝胶的尺寸及形态。
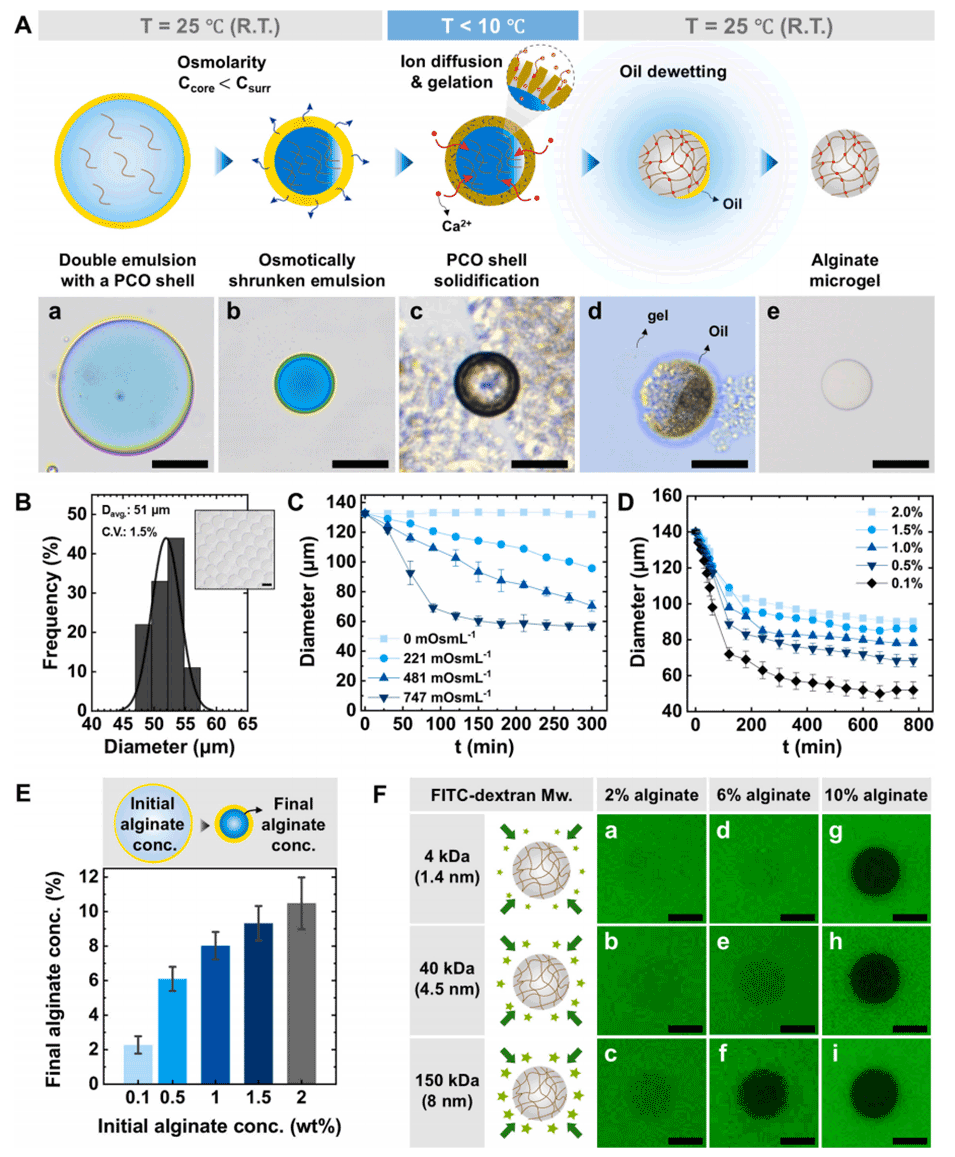
图3. 利用渗透收缩实现海藻酸盐微凝胶的组分调控。
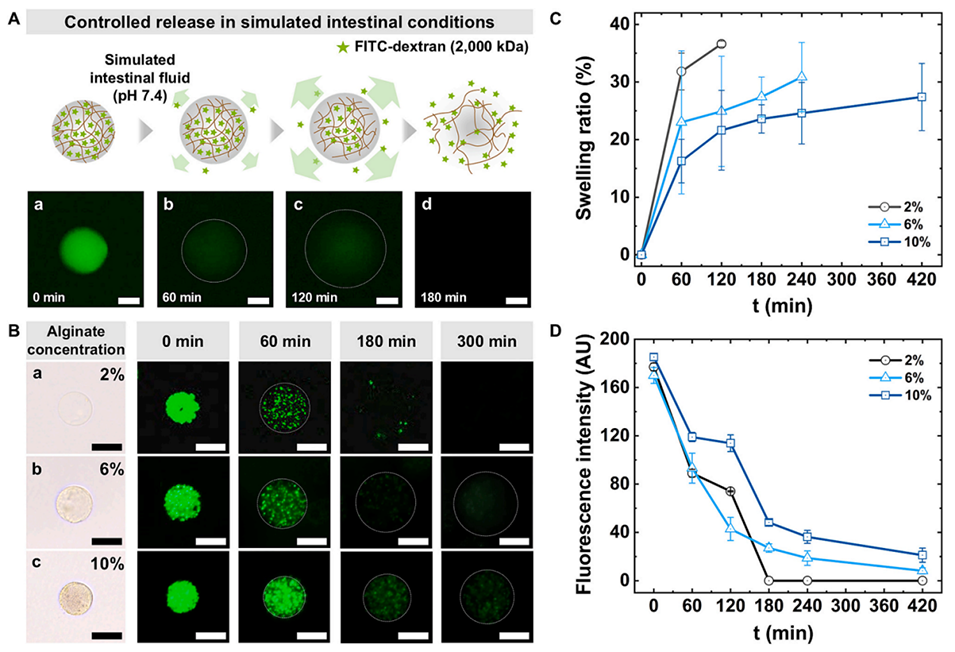
图4. 海藻酸盐微凝胶在模拟肠道环境中的控释行为。
论文链接:https://doi.org/10.1016/j.jcis.2025.138874
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














