肌腱病作为高发的肌肉骨骼疾病,以持续性低度炎症、细胞外基质紊乱为核心特征,网球肘、跟腱炎都属于这类问题。由于肌腱组织血管分布少、代谢慢,传统治疗始终存在痛点:口服非甾体抗炎药易引发胃肠、肾脏副作用,局部注射的药物又会快速扩散流失,疗效短暂且难以实现组织的有效修复。

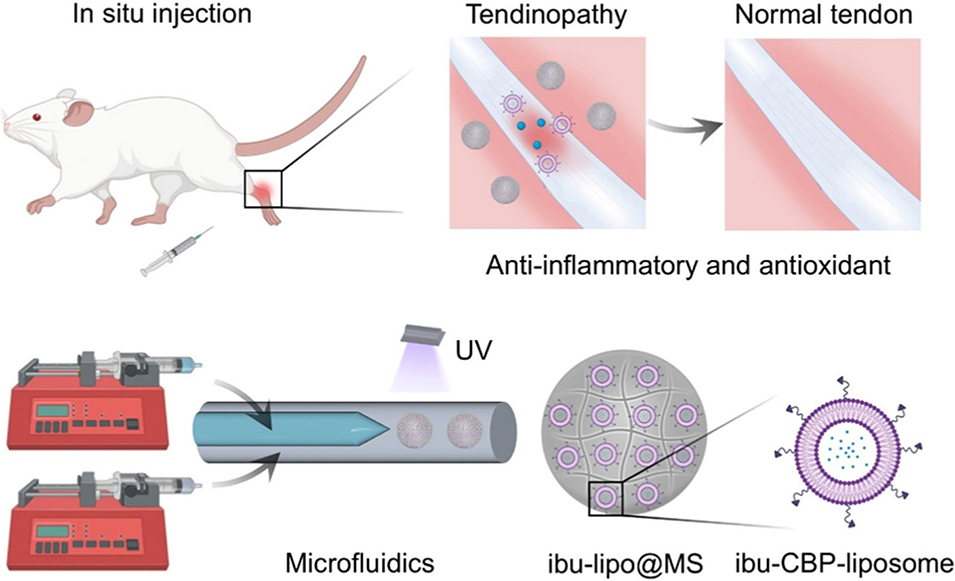
近日,发表在《Materials Today Advances》的一项研究,为肌腱病的局部精准治疗带来了新方案!清华大学联合中国人民解放军总医院研究团队开发出一种可注射的布洛芬负载脂质体-水凝胶微球纳/微复合递送系统(ibu-lipo@MS),通过层级化的结构设计,完美解决了药物局部滞留短、释放难控、靶向性差的临床难题,在大鼠肌腱病模型中实现了炎症抑制、基质重塑与肌腱功能恢复的协同效果,还为其他机械活性软组织病变的治疗提供了通用范式。
研究亮点
构建可注射、可规模化制备的层级化纳/微复合递送体系
将胶原结合肽修饰的布洛芬脂质体高效包封于微流控制备的甲基丙烯酰化透明质酸水凝胶微球中,实现“纳米载药 + 微球药库”的一体化设计。
采用特定的微流控光交联制备技术
通过微流控光交联技术制备出粒径可控的单分散甲基丙烯酰化透明质酸水凝胶微球,该微球可构建亲水微环境,显著提升药物局部滞留效果并实现可控缓释。
实现肌腱部位的精准靶向
依托胶原结合肽与胶原的亲和作用,增强递药体系在富胶原肌腱细胞外基质中的靶向性与滞留性,改善游离药物因扩散、清除导致的疗效短暂问题。
具备动物实验转化依据
在肌腱病体内模型中,布洛芬脂质体-水凝胶微球递药体系可显著减轻组织炎症与水肿,改善肌腱组织结构、降低Bonar组织学评分,促进肌腱功能恢复。
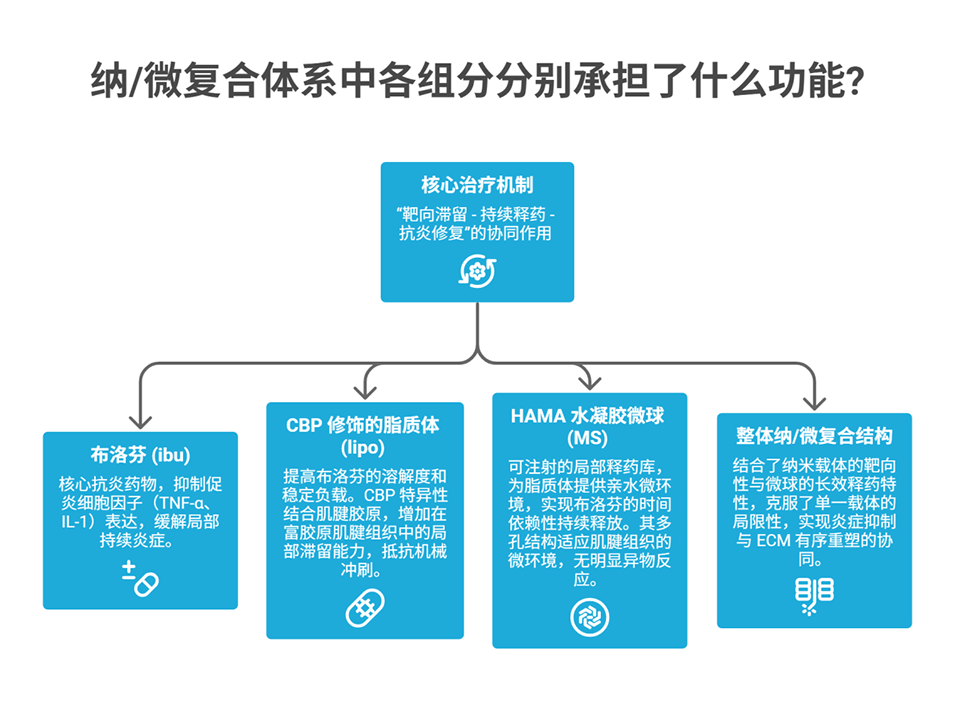
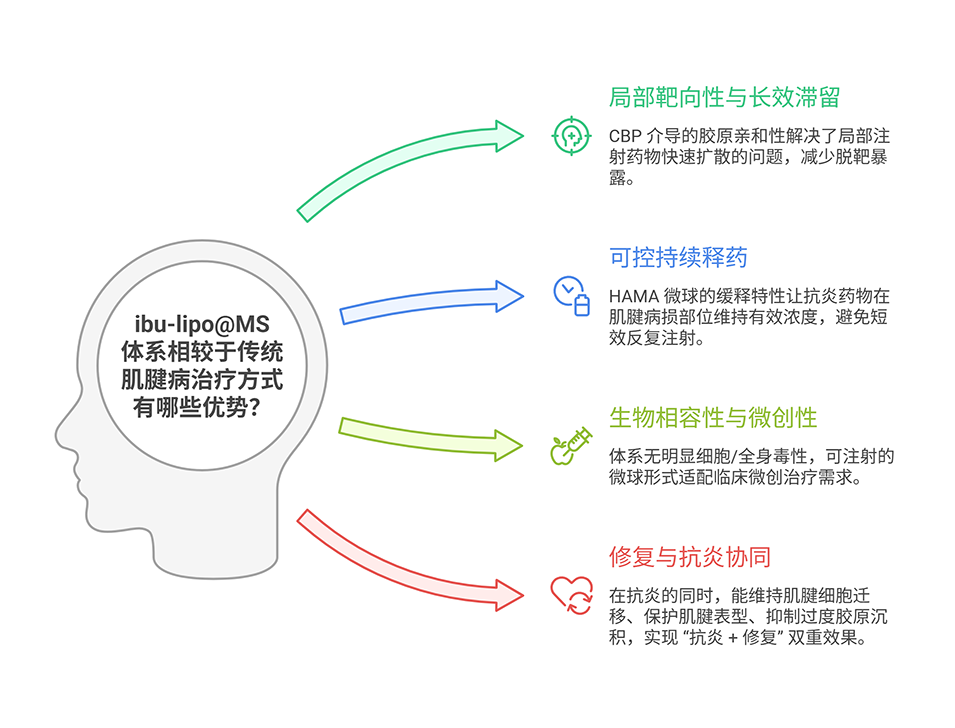
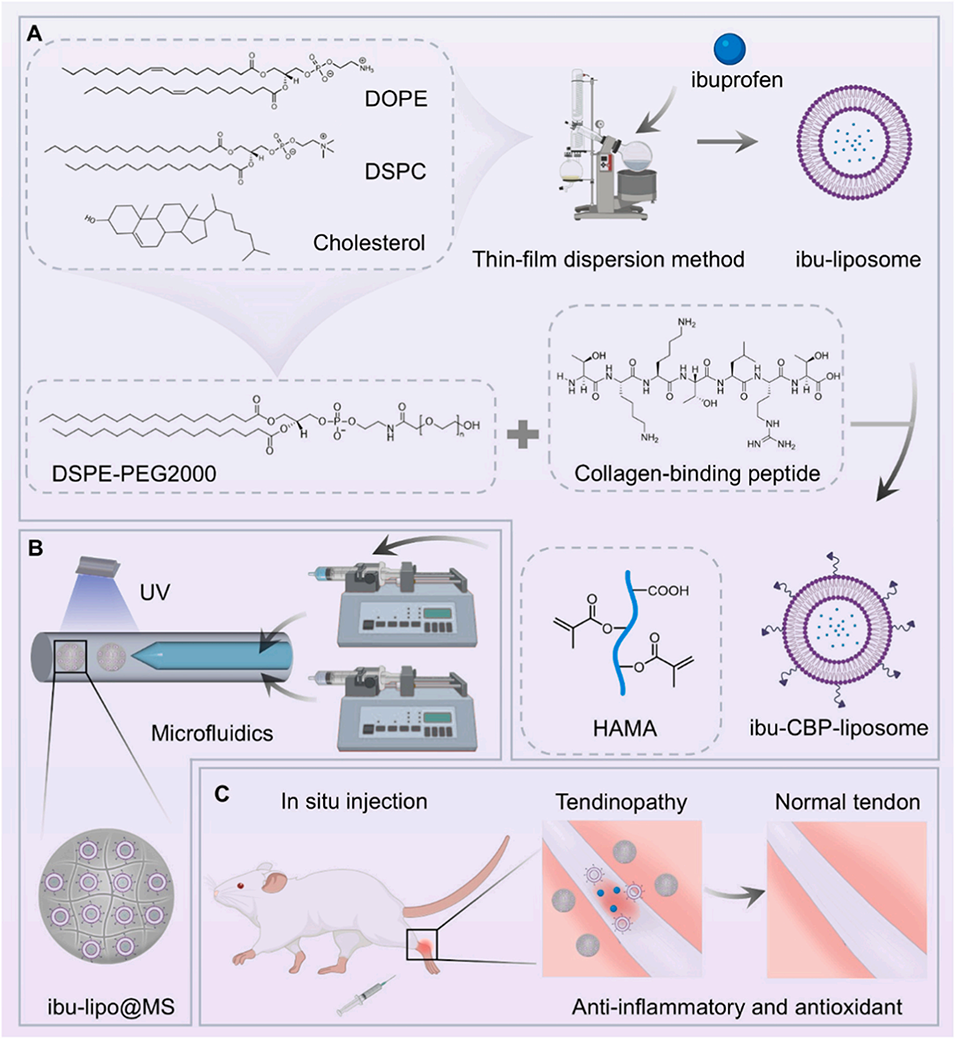
图1 ibu-lipo@MS的制备及作用机制示意图。A)胶原结合肽修饰布洛芬脂质体的制备流程示意图。B)布洛芬脂质体-水凝胶微球的制备流程示意图。C)大鼠肌腱病模型的原位注射示意图
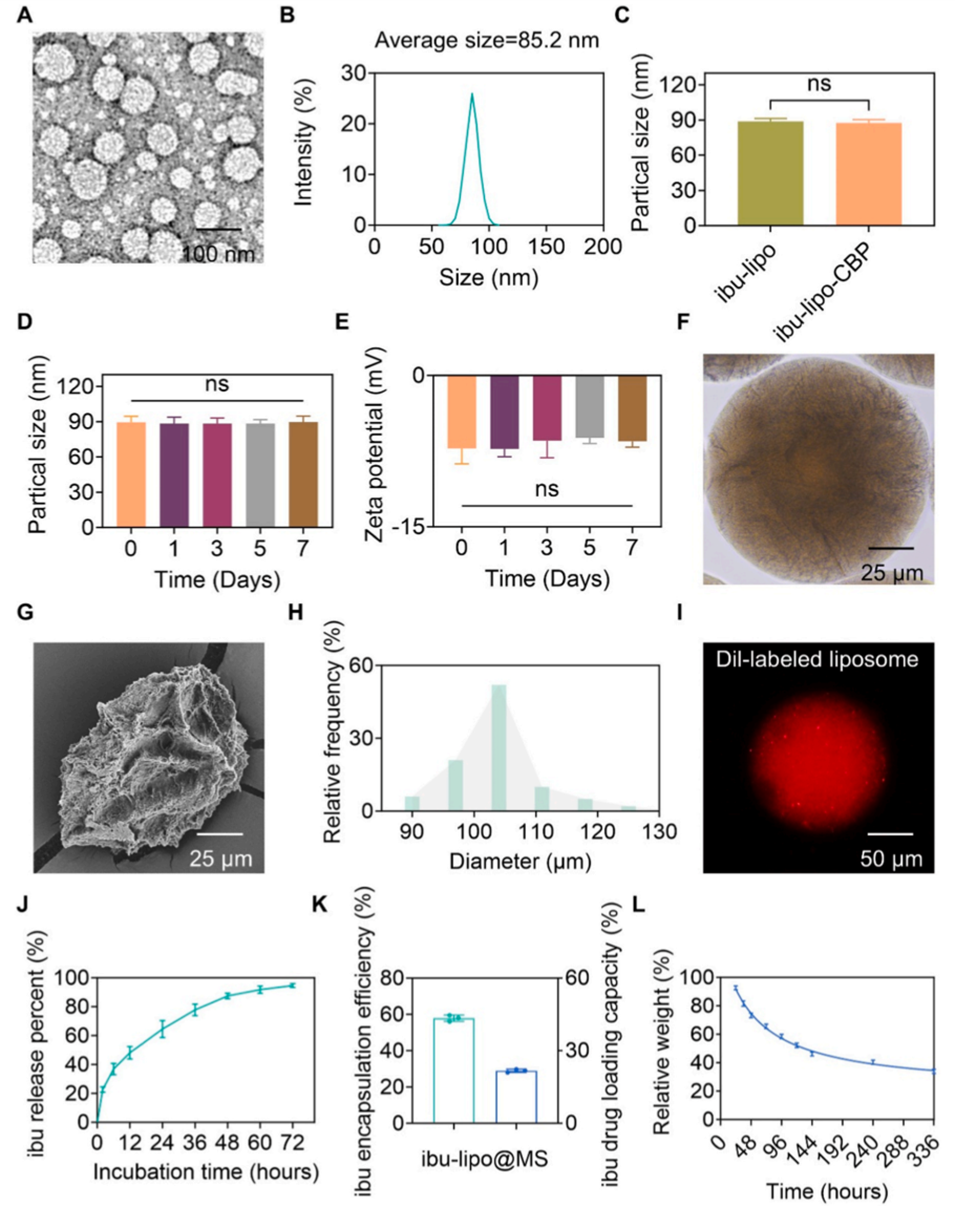
图2 脂质体及负载脂质体的甲基丙烯酰化透明质酸水凝胶微球的理化表征
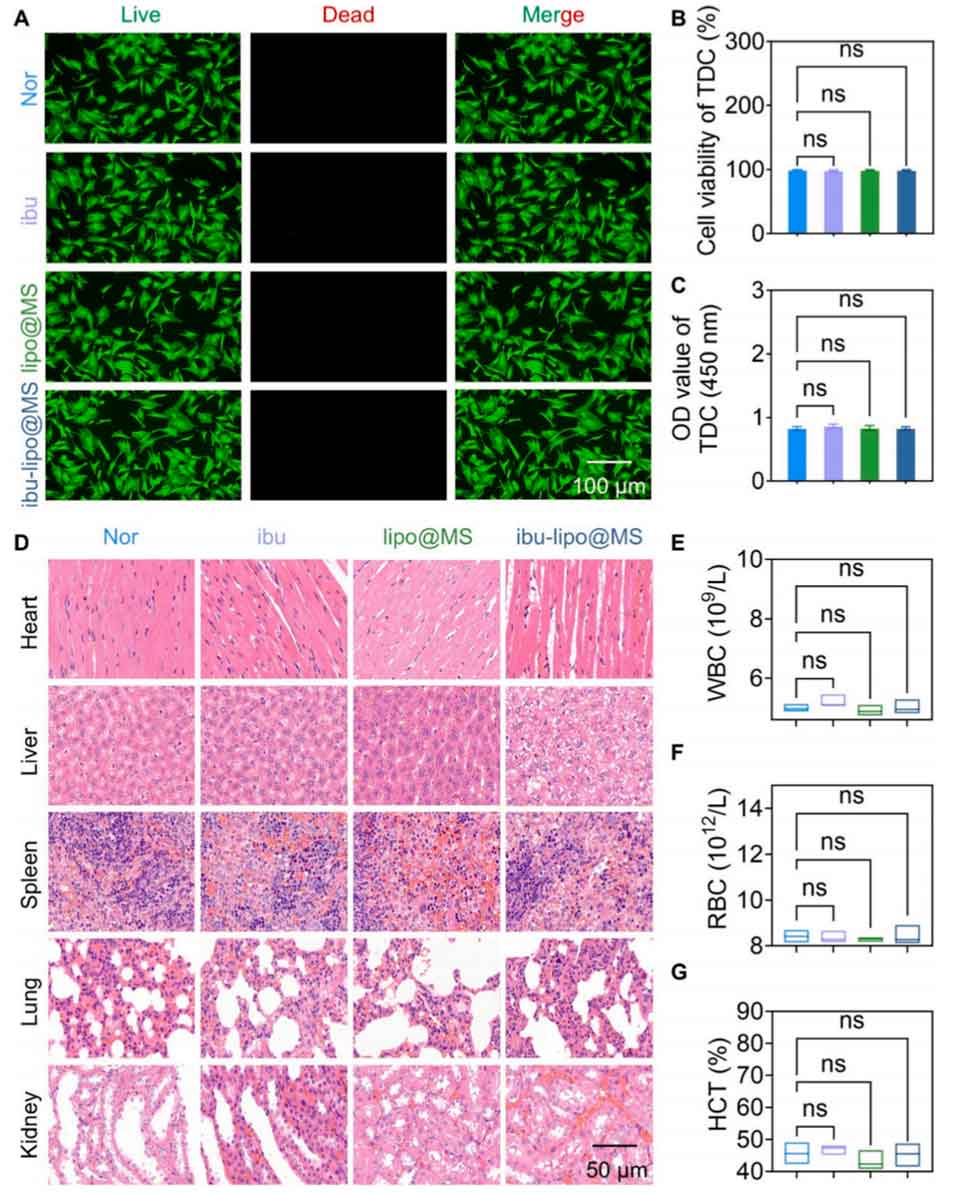
图3 体外细胞相容性与体内生物安全性评价
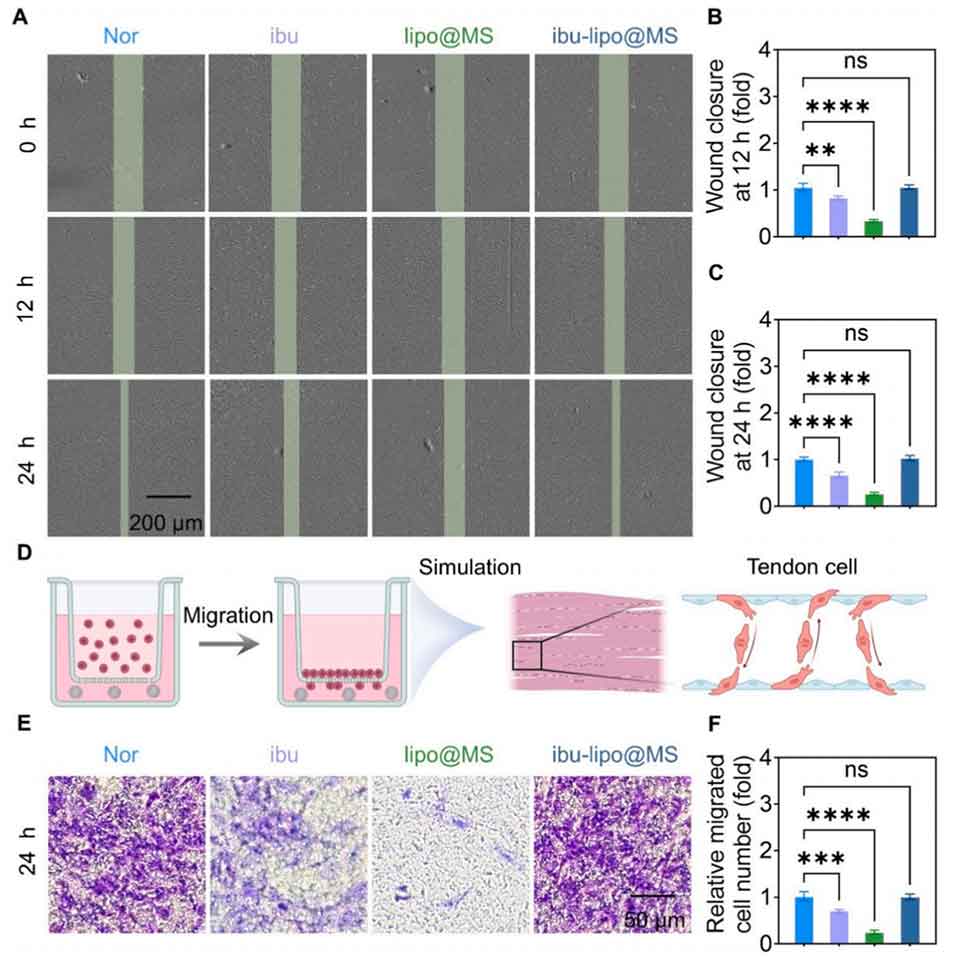
图4 不同制剂对肌腱细胞迁移能力的影响
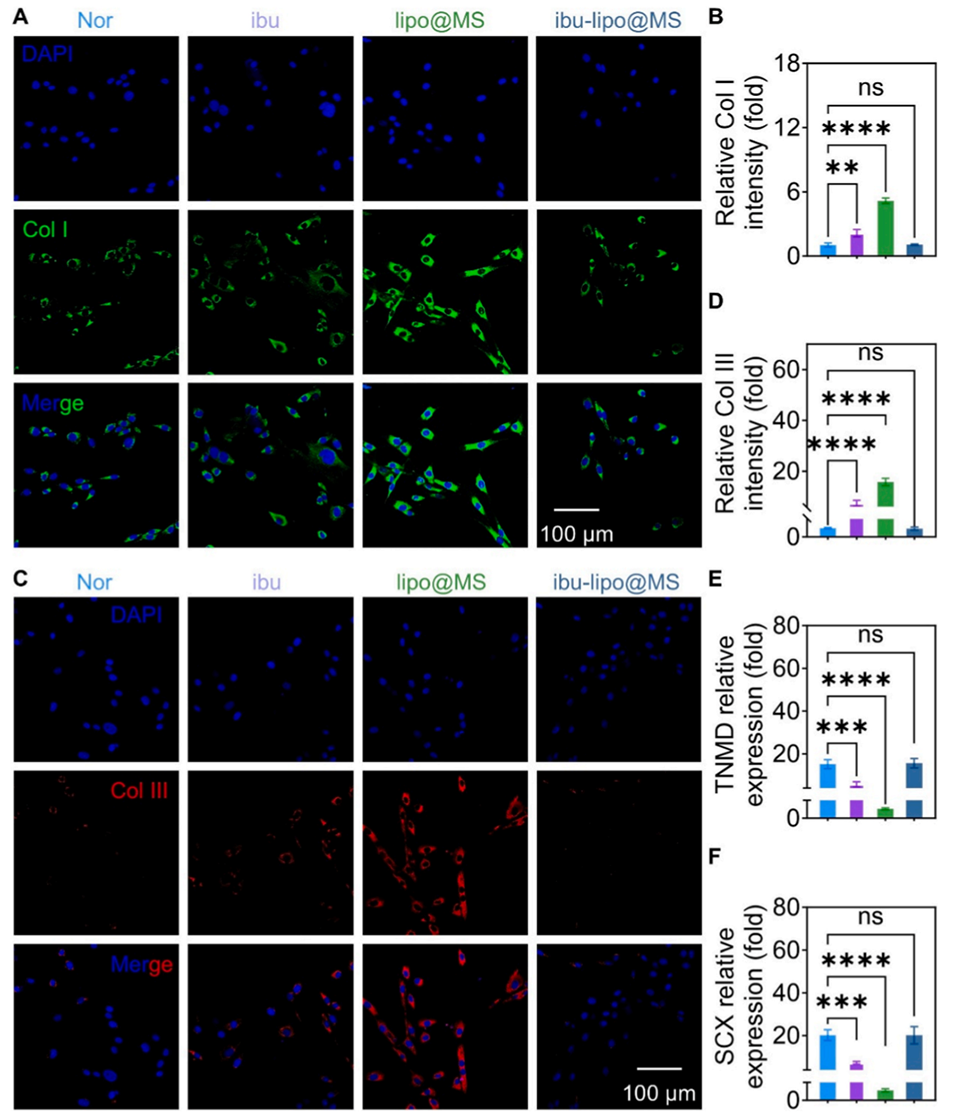
图5 不同制剂对肌腱细胞细胞外基质合成及肌腱表型标志物的影响
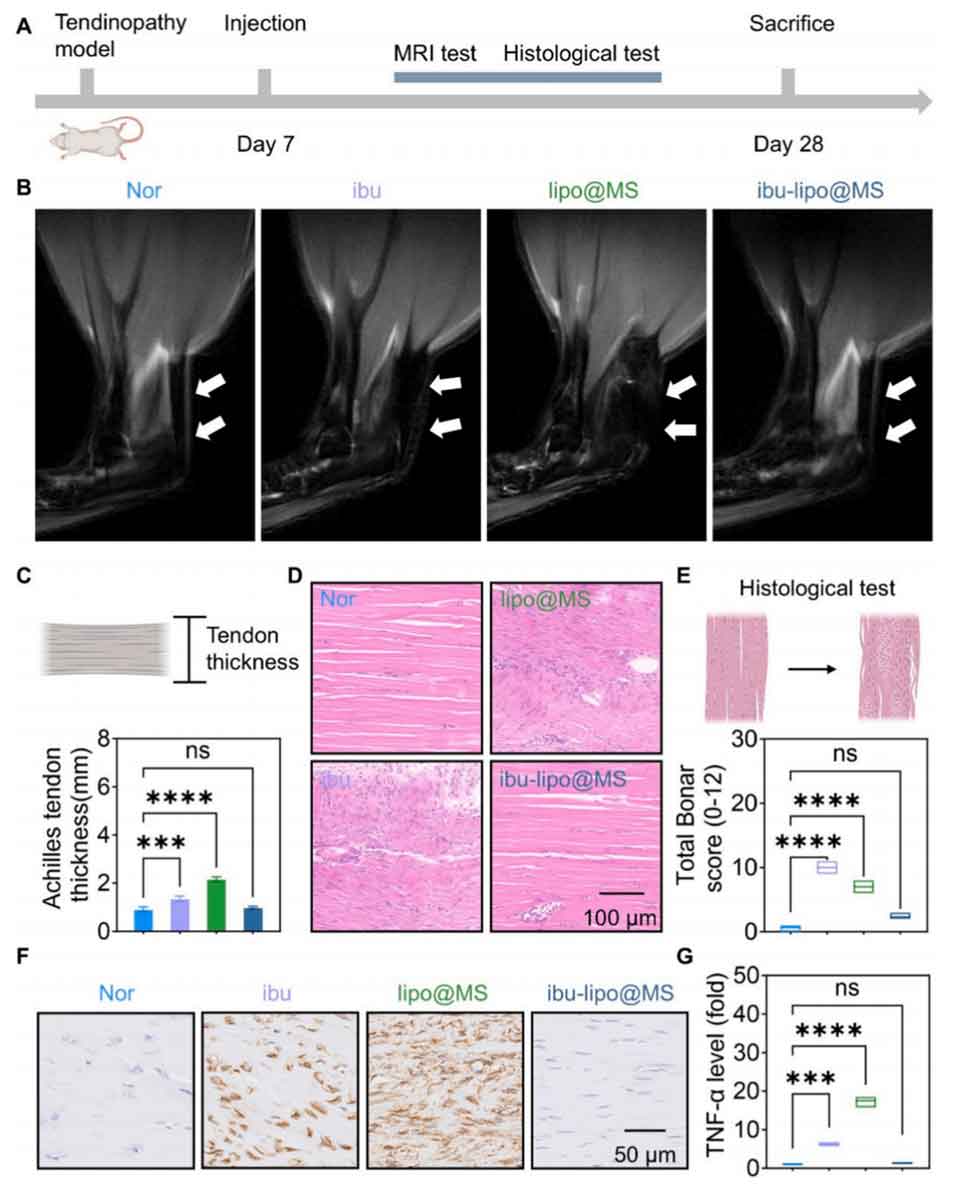
图6 布洛芬脂质体-水凝胶微球在大鼠跟腱肌腱病模型中的体内治疗效果
论文链接:https://doi.org/10.1016/j.mtadv.2026.100736
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
上一篇:生物无机杂化微球系统!调控免疫-软骨生成微环境,实现腱骨愈合
下一篇:暂无














