糖尿病患者的创面愈合过程复杂,且因伤口微环境紊乱(以慢性炎症、高血糖为典型特征)受到显著阻碍。干细胞治疗与药物治疗相结合被视为未来极具应用前景的治疗手段,但干细胞增殖能力有限、药物利用效率不足的问题,为实现理想的治疗效果带来了巨大挑战。

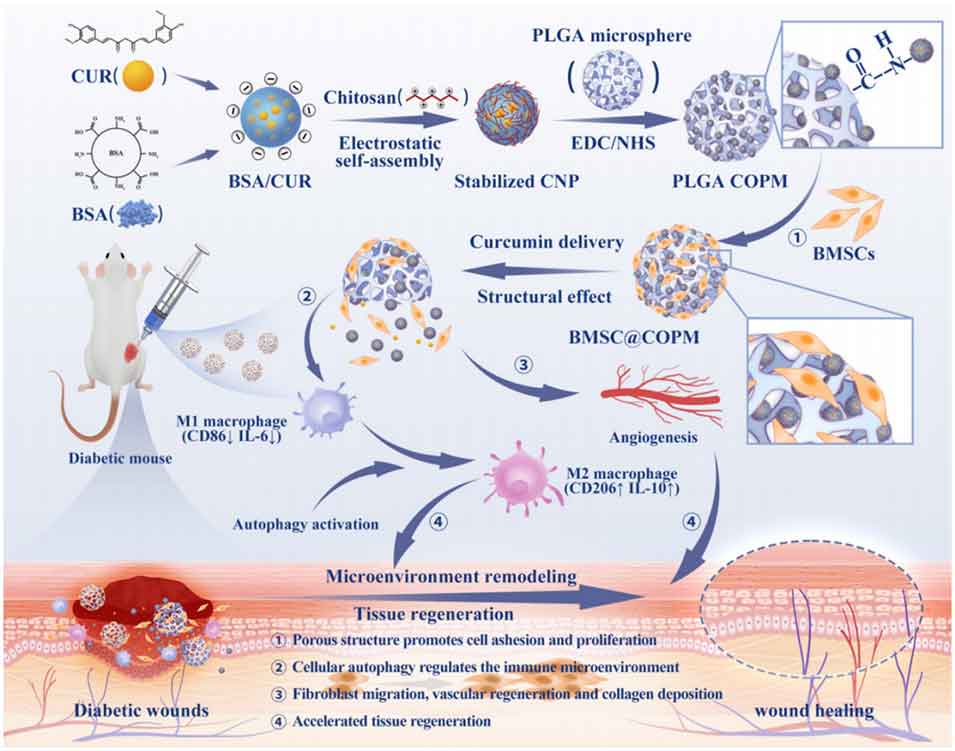
针对这一难题,南昌大学附属口腔医院廖岚教授联合牡丹江医科大学袁晓环教授、武艳副教授等人设计并研发了负载姜黄素@牛血清白蛋白纳米粒(Curcumin@BSA NPs)和骨髓间充质干细胞(BMSCs)的开放多孔微环境调控PLGA微球(BMSC@COPM),通过材料设计、体外实验和动物模型验证了其优异的糖尿病创面修复效果,并揭示了相关作用机制。该研究以“Open Porous Microenvironment-regulatory Microspheres Loaded with Curcumin@BSA NPs/BMSCs for Diabetic Wound Treatment”为题目,发表于期刊《Theranostics》。
本文要点:
1、本研究通过气体辅助挥发微乳液技术结合表面碱处理,设计合成了开放多孔聚乳酸-羟基乙酸共聚物(PLGA)微球,将姜黄素与牛血清白蛋白(BSA)制备为纳米颗粒并接枝于微球,同时负载骨髓间充质干细胞(BMSCs)构建出BMSC@COPM复合体系。
2、该体系实现了79.57%的姜黄素包封率、7.62%的载药率及35天持续释药,微球的开放多孔结构为BMSCs提供了良好的黏附增殖环境,且材料溶血率< 5%、体内外生物相容性优异。
3、通过体外高糖环境细胞实验和糖尿病小鼠8mm全层皮肤伤口体内实验证实,BMSC@COPM依赖非经典PI3K/Akt/mTOR信号通路激活细胞自噬,一方面诱导巨噬细胞从M1向M2极化、抑制促炎因子分泌,重塑伤口免疫微环境以缓解慢性炎症,另一方面上调HIF-1α/VEGF/PDGF/FGF等因子表达,促进成纤维细胞增殖迁移、内皮细胞血管生成及胶原网络再生,最终使糖尿病小鼠伤口21天愈合率达97%,显著优于对照组及其他微球实验组。
4、该研究构建的注射式、可降解的BMSC@COPM复合微载体,实现了材料、药物与干细胞的协同作用,为糖尿病伤口的临床治疗提供了新型多功能生物材料策略,同时也指出该体系未来仍需解决产品价格、稳定性及干细胞应用伦理等问题。
本研究采用多步工艺制备BMSC@COPM复合体系,具体步骤如下:
1、PLGA微球制备:以PLGA为基材,通过气体辅助挥发微乳液技术,利用NH₄HCO₃分解产生NH₃和CO₂造孔,结合0.25M NaOH醇溶液碱处理,依次制备实心微球(MS)、多孔微球(PM)、开孔微球(OPM),优化搅拌速度为800rpm,获得尺寸均一的微球;
2、姜黄素纳米粒(CNPs)制备:采用去溶剂法,将姜黄素包封于BSA中,加入戊二醛交联,再通过壳聚糖静电稳定形成带正电的CNPs,提升姜黄素的水溶性和稳定性;
3、PLGA COPM制备:通过EDC/NHS活化OPM表面羧基,将CNPs接枝于OPM表面,实现姜黄素的负载;
4、BMSC@COPM制备:将第三代/第四代BMSCs与COPM共培养2h,使细胞黏附于微球的开孔结构中,实现干细胞与微球的复合。
本研究制备的BMSC@COPM复合体系在材料设计和制备工艺上有哪些核心创新点?
①工艺上,采用气体辅助挥发微乳液技术结合表面碱处理,制备出具有互连开孔结构的PLGA开放多孔微球(OPM),解决了传统PLGA微球孔隙单一、细胞黏附性差的问题;
②载药方式上,将疏水性姜黄素包封于BSA并结合壳聚糖静电稳定制备姜黄素包覆纳米颗粒(CNPs),再通过EDC/NHS法接枝于OPM表面,实现了疏水性药物的高效负载(载药率7.62%)和35天持续释放,解决了姜黄素释放失控的问题;
③体系设计上,将开孔微球、姜黄素纳米粒、BMSCs三者结合,开孔微球为BMSCs提供黏附增殖的微环境,姜黄素持续释放提升BMSCs活性,实现了材料-药物-干细胞的协同作用,而非简单混合。
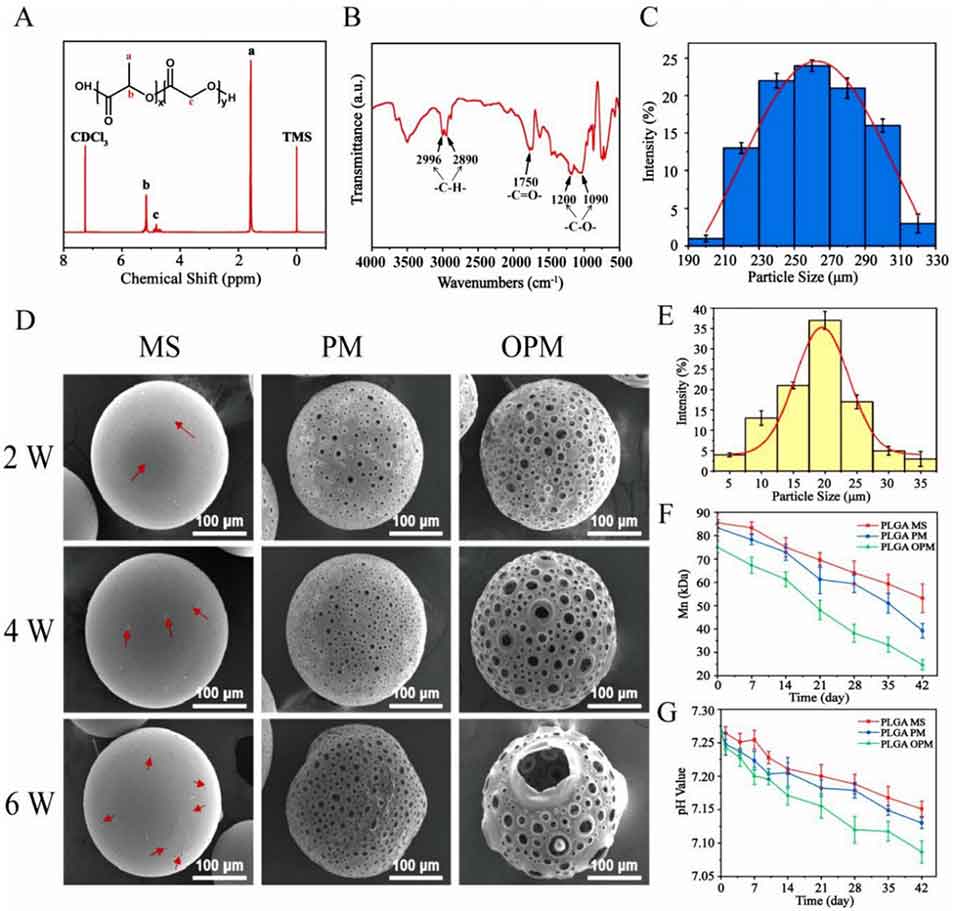
图1 微球的化学结构与表面形貌分析
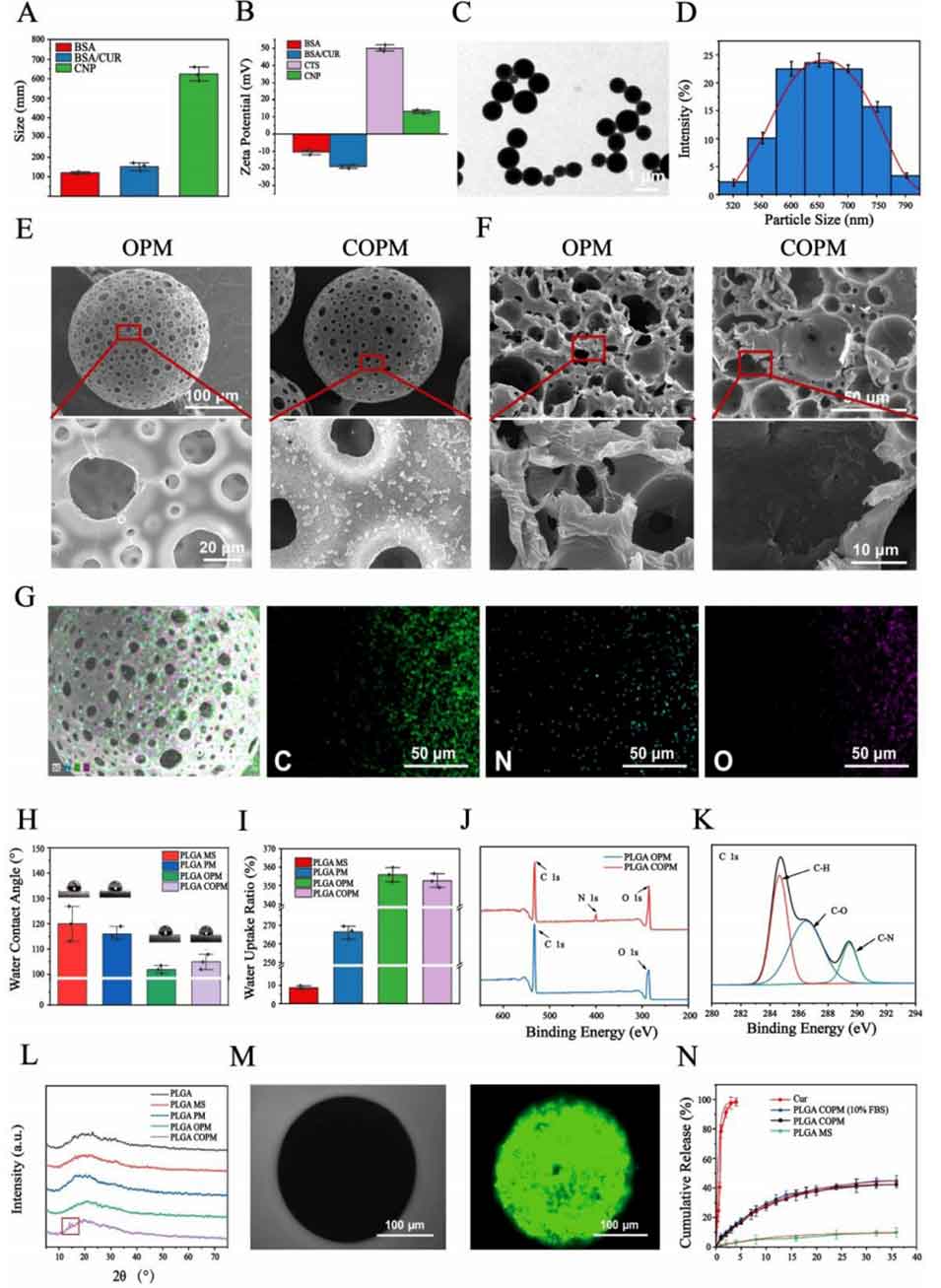
图2 姜黄素包覆纳米粒(CNPs)与PLGA COPM的特性分析
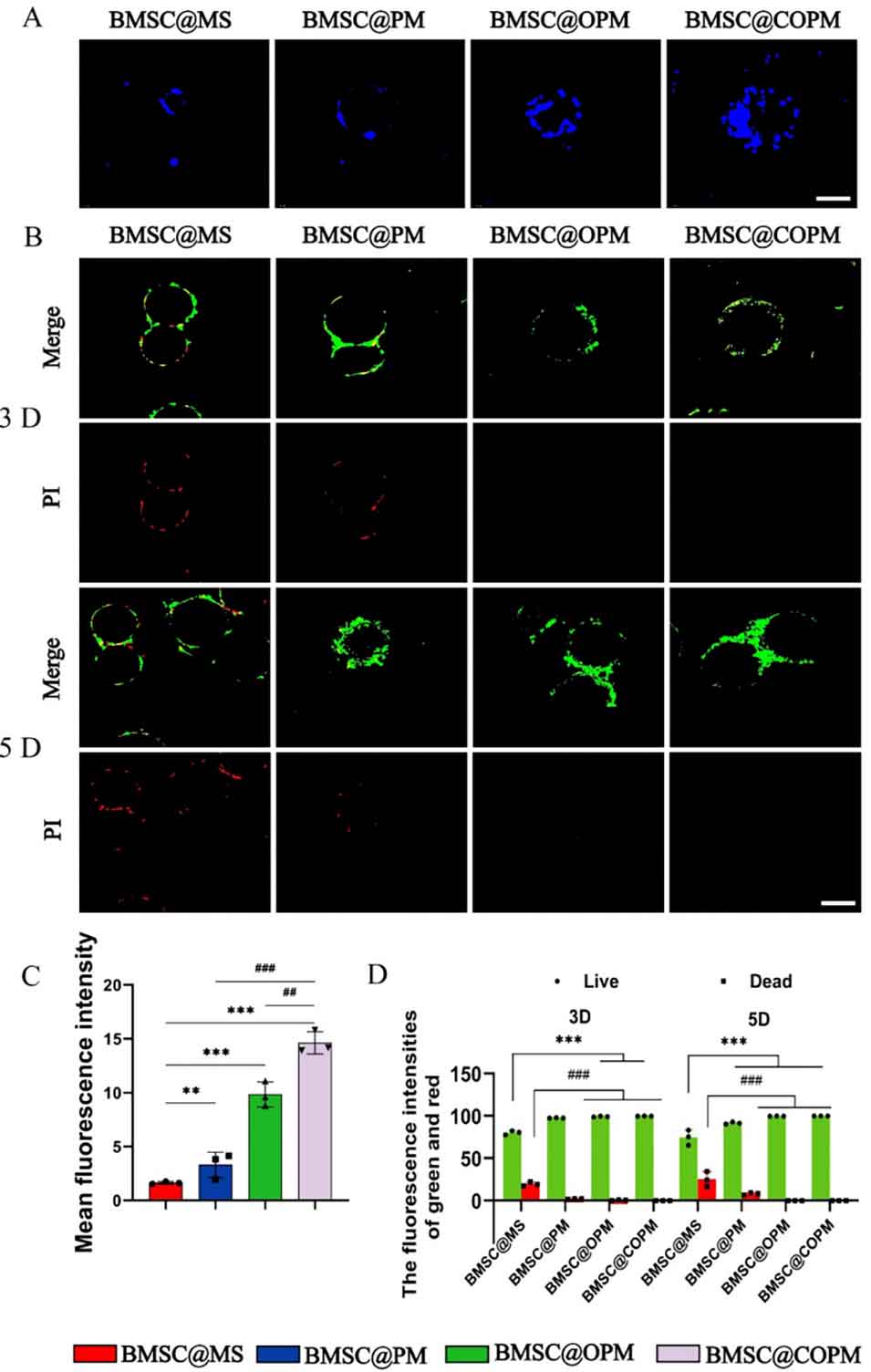
图3 骨髓间充质干细胞(BMSCs)在开放多孔微球上的黏附与存活情况
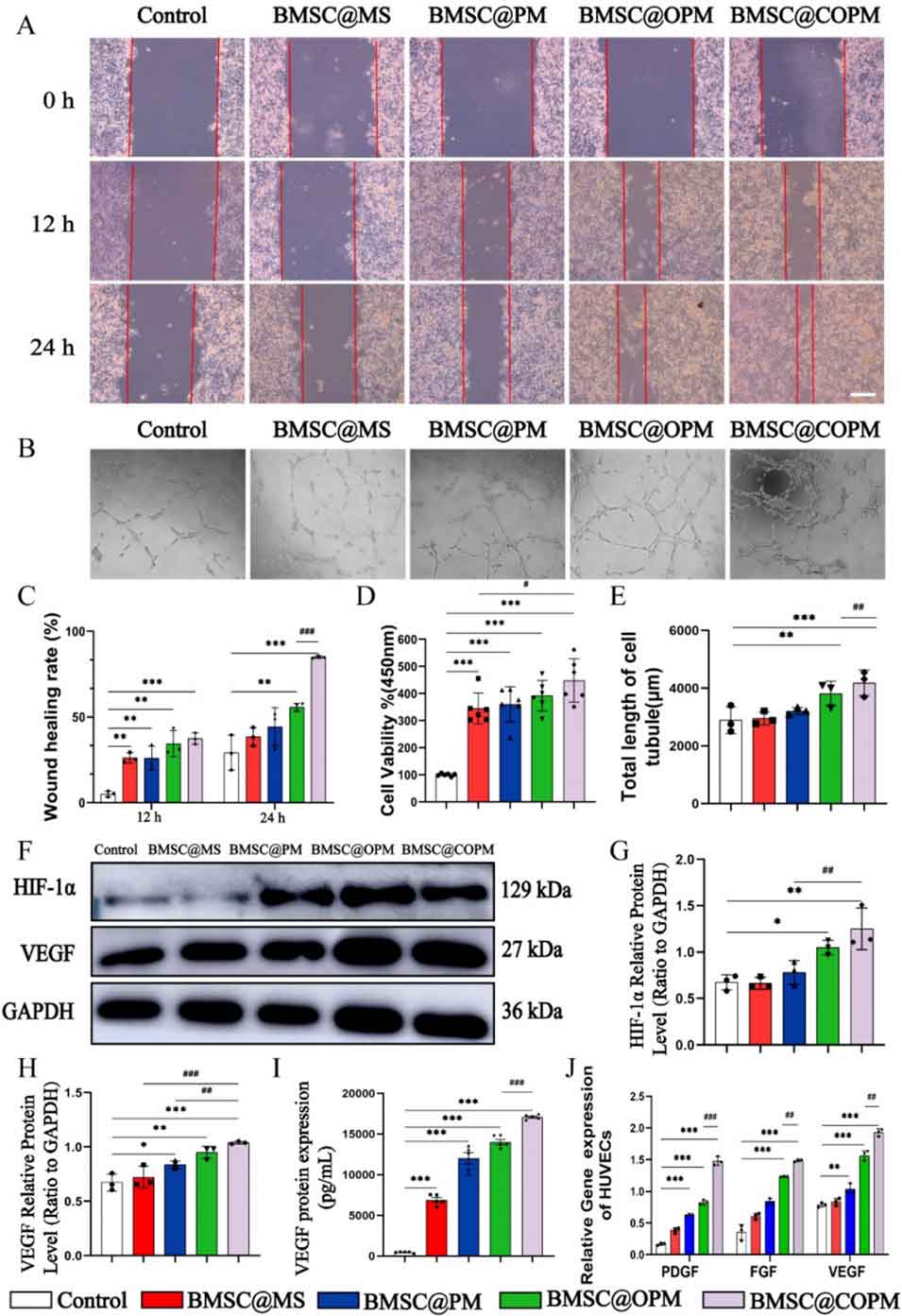
图4 体外血管生成与迁移实验
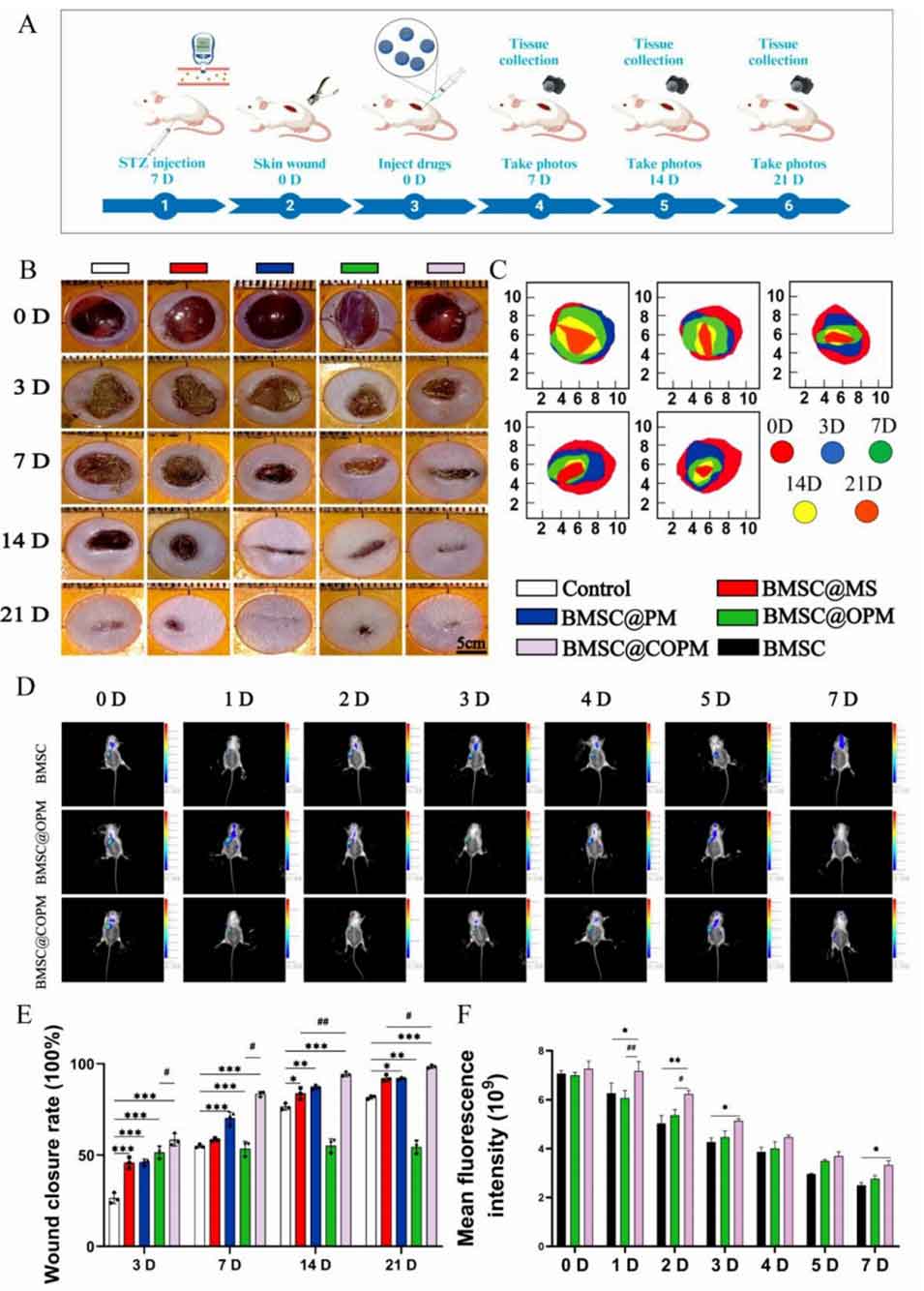
图5 负载BMSCs的微球对糖尿病创面愈合的促进作用
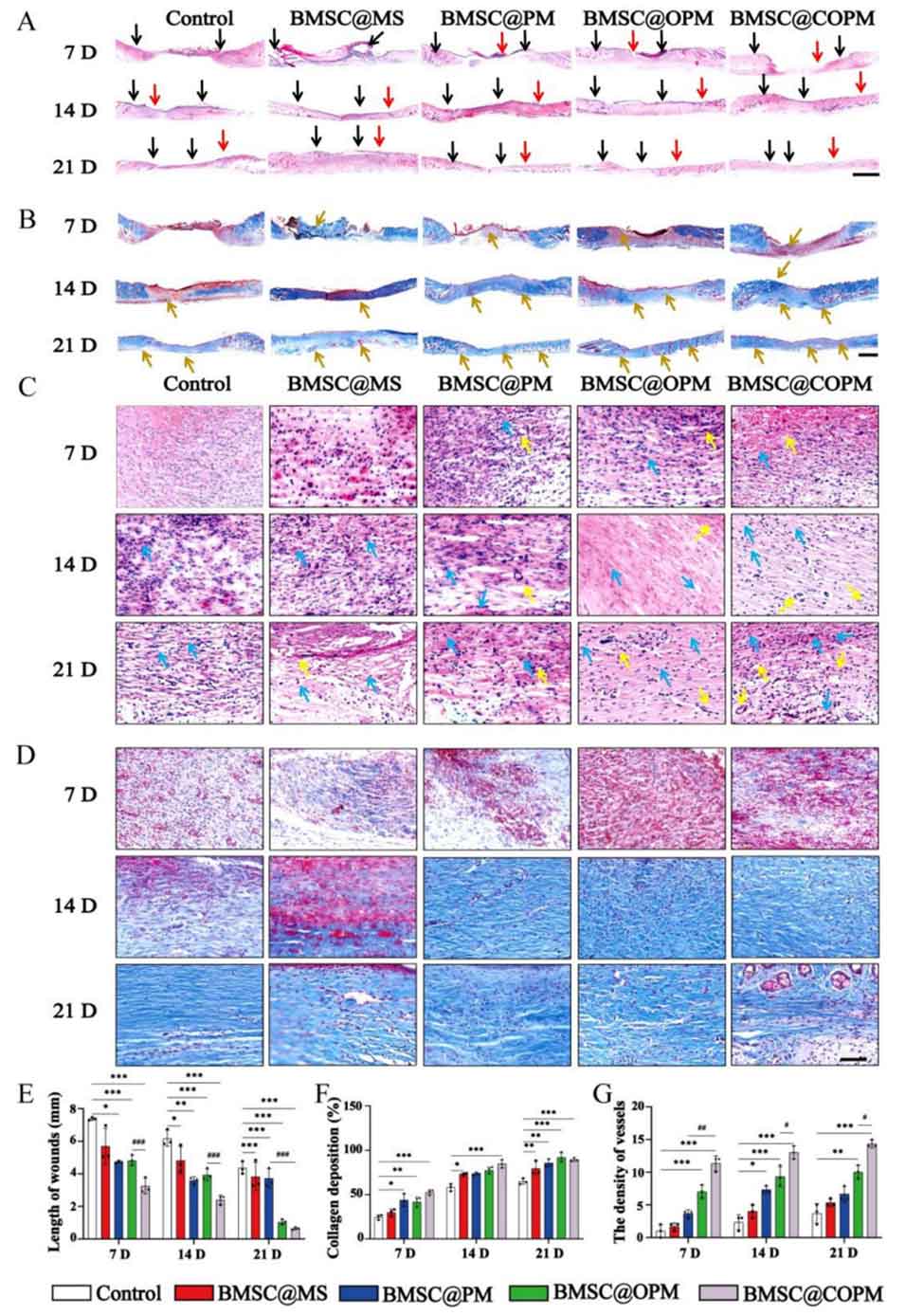
图6 BMSC@COPM处理糖尿病创面的组织学检查
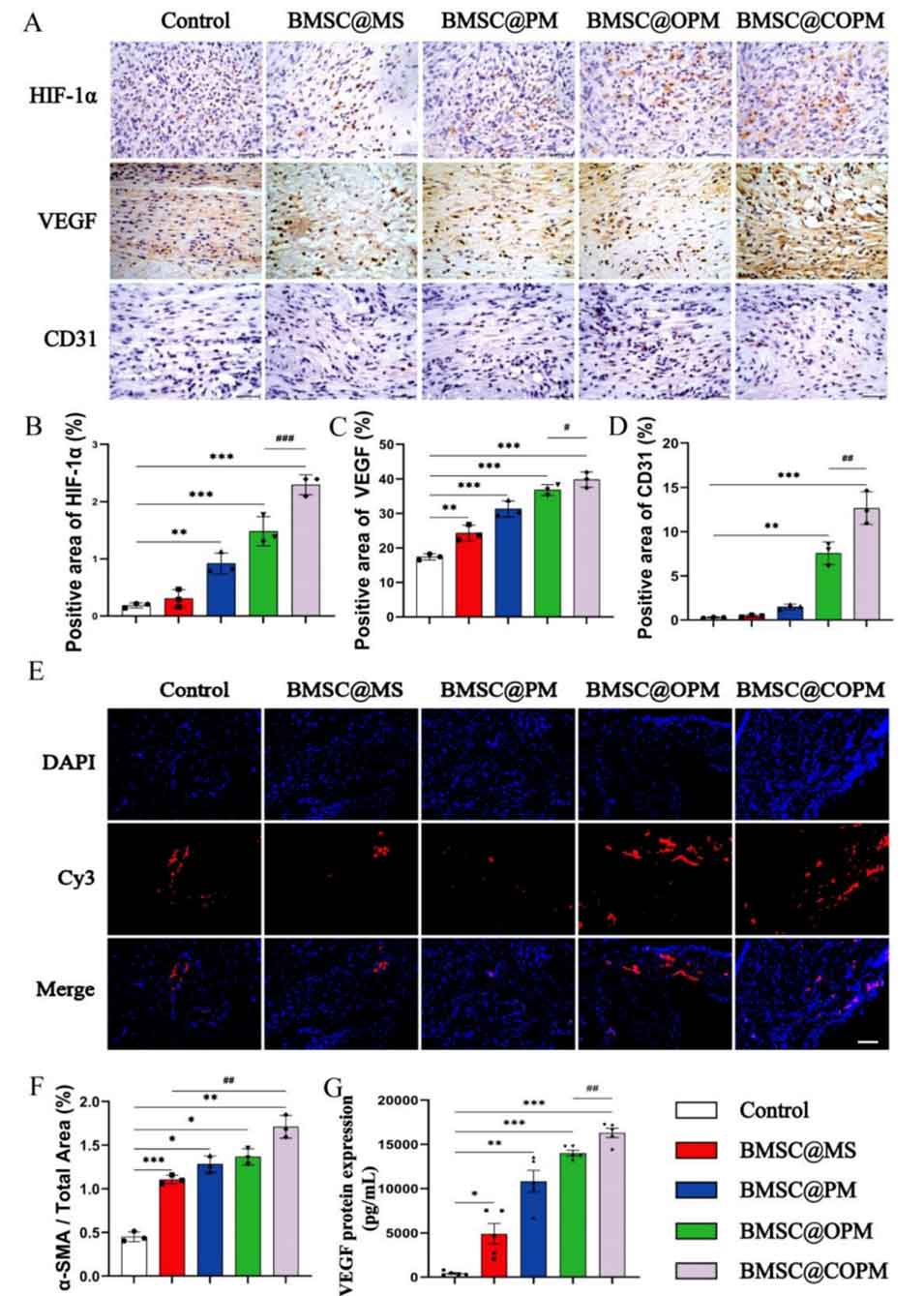
图7 BMSC@COPM对糖尿病创面血管生成的影响
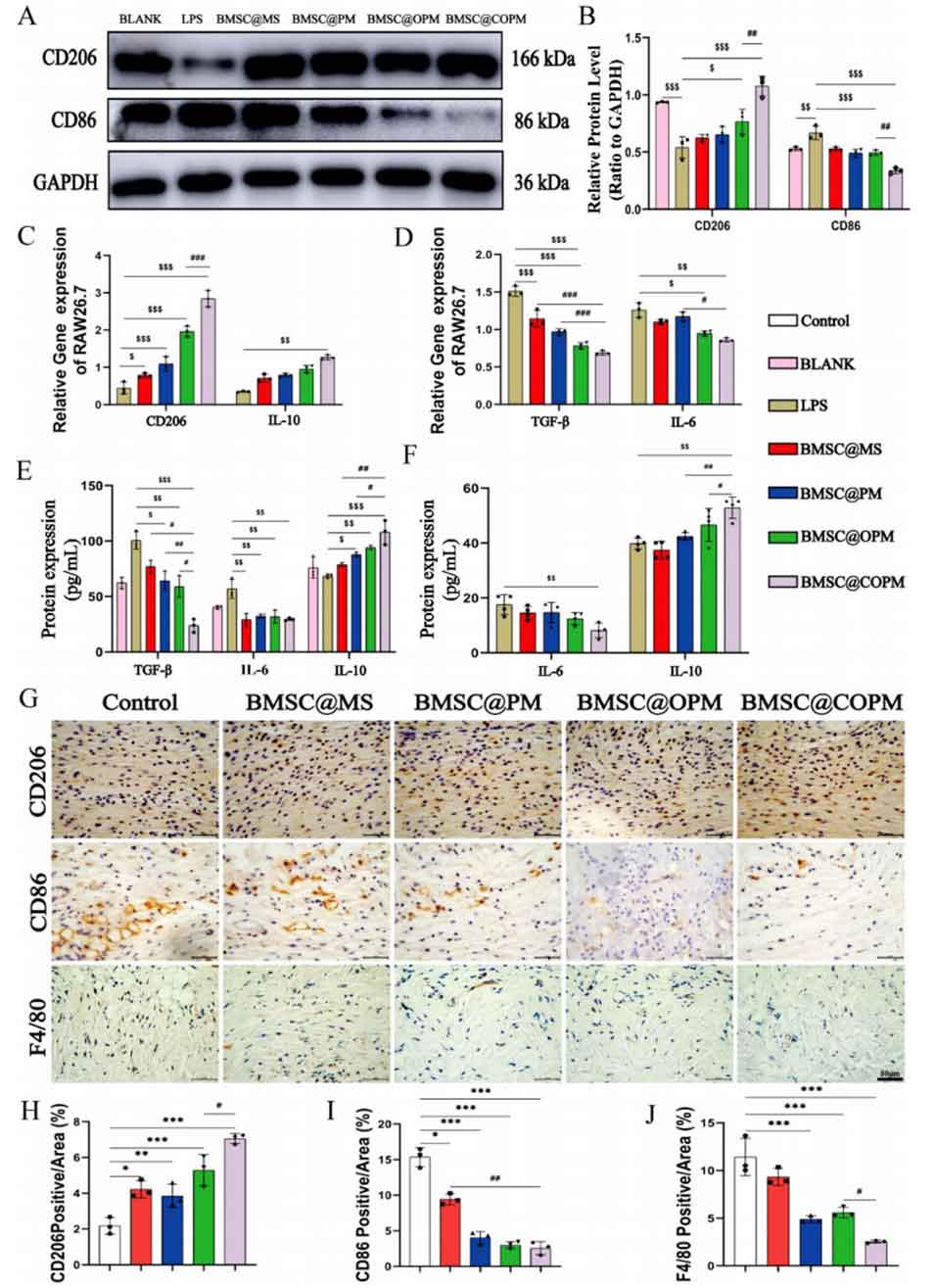
图8 BMSC@COPM对巨噬细胞极化的影响
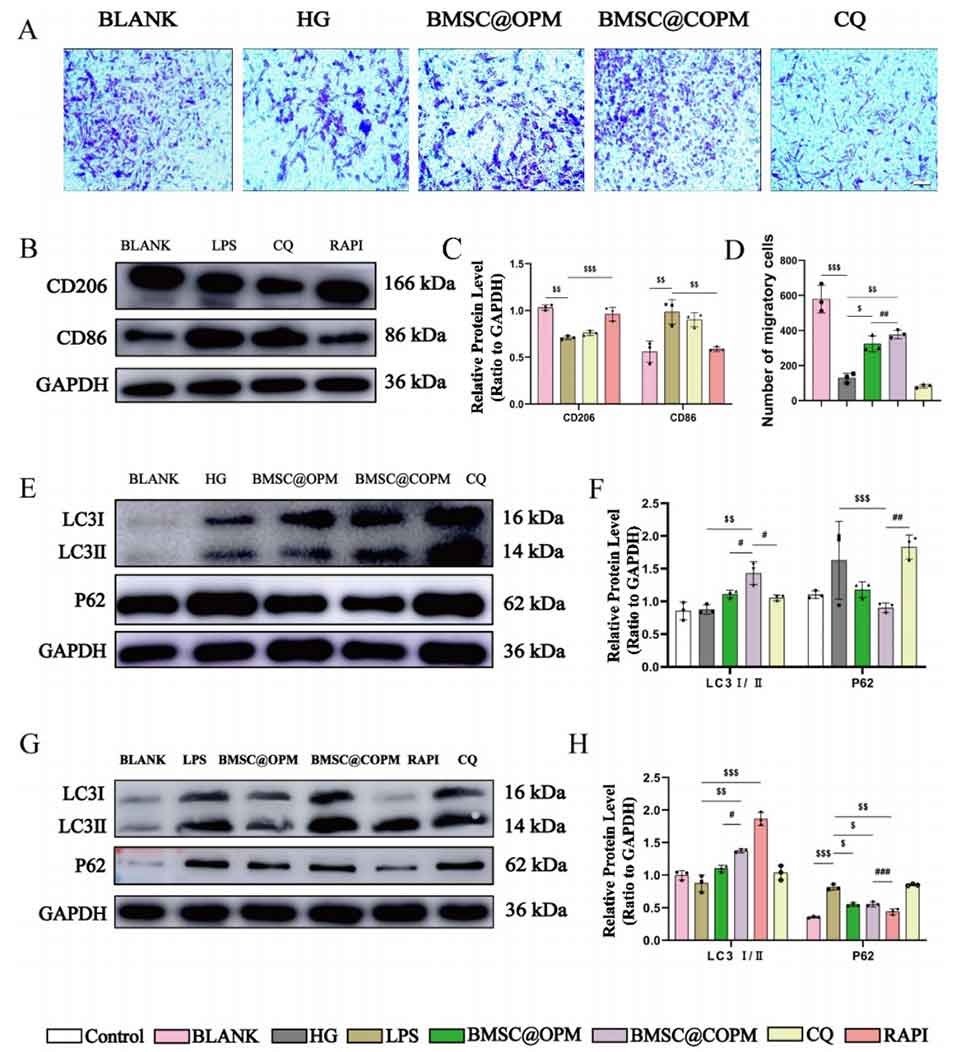
图9 BMSC@COPM诱导自噬以增强巨噬细胞极化并促进细胞迁移与增殖
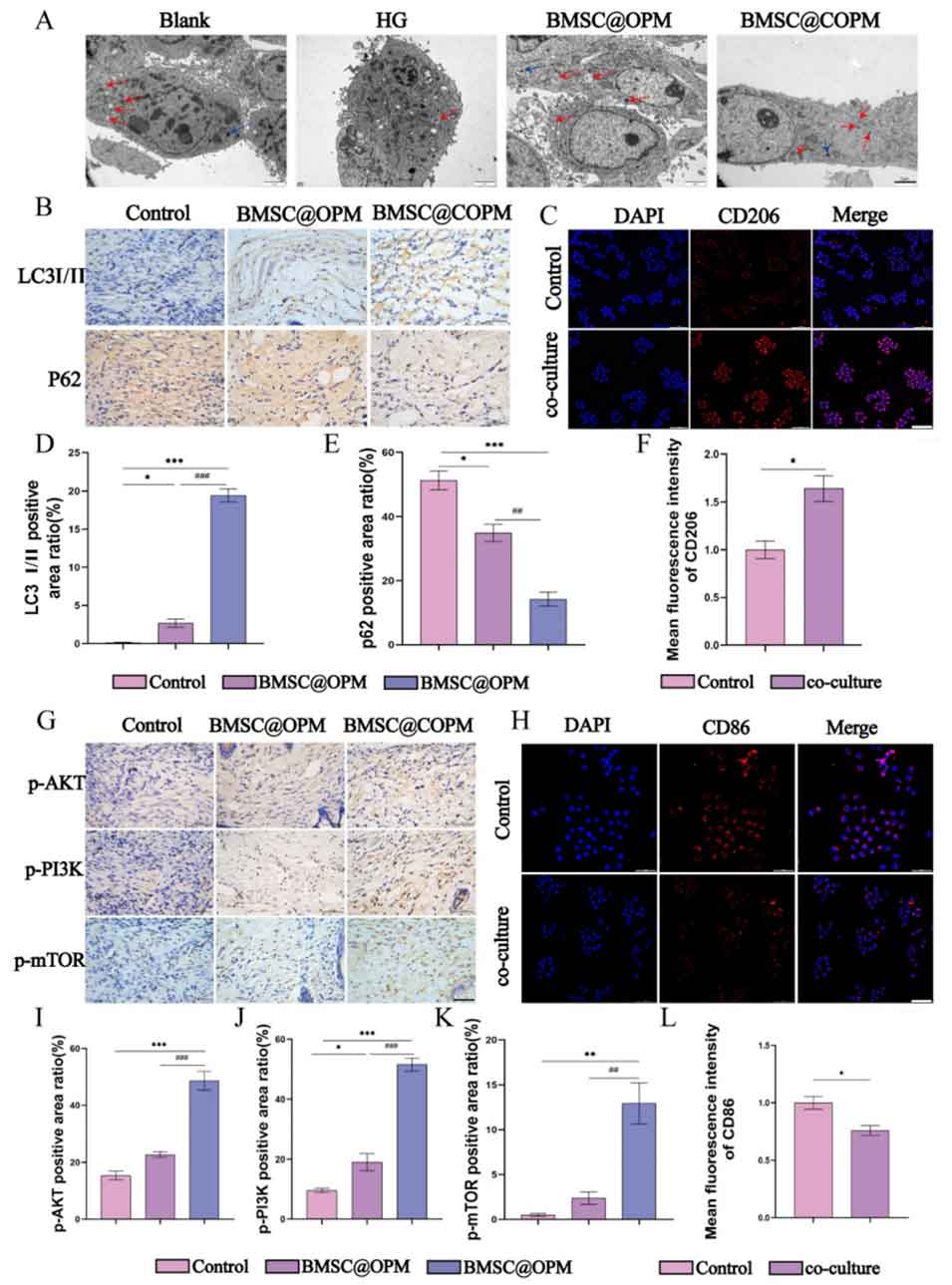
图10 自噬与PI3K/Akt/mTOR信号通路的关系
原文DOI:10.7150/thno.120285
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














