槲皮素(Que)是一种广泛存在于植物中的黄酮类化合物,具有抗氧化、抗炎、抗菌、抗癌、调节血糖等多种药理活性,但因水溶性极差(仅9 ng/mL)、口服吸收有限、生物利用度低,限制了临床应用。
现有改善策略,如环糊精包合、纳米技术等存在不足,而深共熔溶剂(DES)具有增溶与促渗透潜力,但直接应用存在生物安全性与稳定性问题,故开发基于DES的微乳体系,结合微流控技术解决上述痛点。

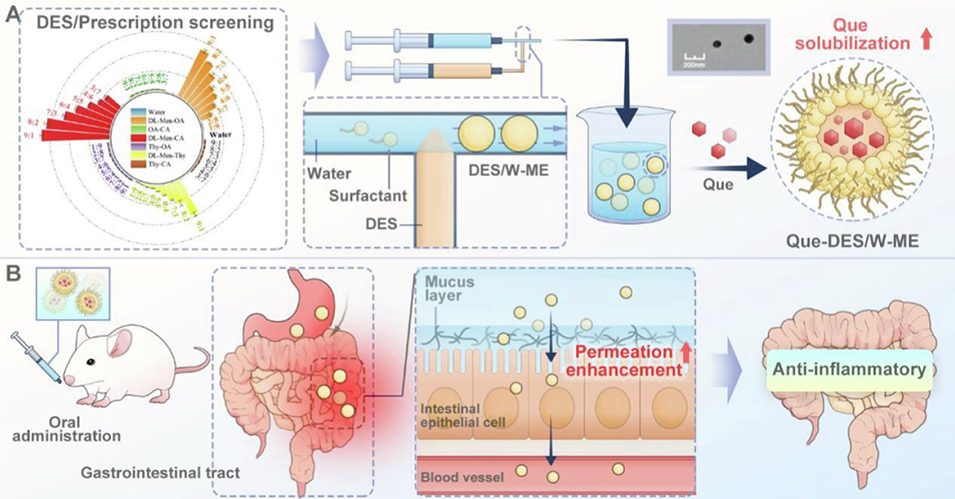
浙江工业大学杨庆良副教授团队将微流控技术与深共熔溶剂(DES)相结合,开发出新型槲皮素口服递送微乳系统。该系统通过仅1.37%的低表面活性剂用量提升生物安全性,同时强化药物肠道黏附与跨黏膜吸收,在结肠炎模型中展现出优于传统制剂的治疗效果。相关研究以“Two-birds-one-stone, microfluidic producing DES/W microemulsions to solubilize quercetin and penetrate intestinal mucosa for enhanced oral bioavailability”为题,发表在期刊《European Journal of Pharmaceutics and Biopharmaceutics》上。
本文要点:
1、该研究针对槲皮素水溶性差、口服生物利用度低的问题,开发了一种基于微流控技术制备的槲皮素负载深共熔溶剂/水微乳体系(Que-DES/W-ME)。
2、该体系以摩尔比7:3的DL-薄荷醇和癸酸组成深共熔溶剂(DES),选用吐温20为表面活性剂,在优化的工艺参数(表面活性剂浓度1.37%、水相流速30.98 mL/h、分散相流速3.15 mL/h)下制备而成。
3、实验表明,该微乳显著提升了槲皮素的溶解度(较水溶解度提高2675.47倍),增强了黏膜穿透性和肠道黏附性,延长药物肠道滞留时间;药代动力学研究显示,其血药浓度-时间曲线下面积(AUC₀₋ₜ)较游离槲皮素提高5.54倍,相对生物利用度达553.69%。
4、在DSS诱导的结肠炎小鼠模型中,该制剂展现出更优的抗炎治疗效果,且因微流控技术减少了表面活性剂用量,具有良好的生物安全性。该体系为难溶性药物的口服递送提供了有效解决方案。
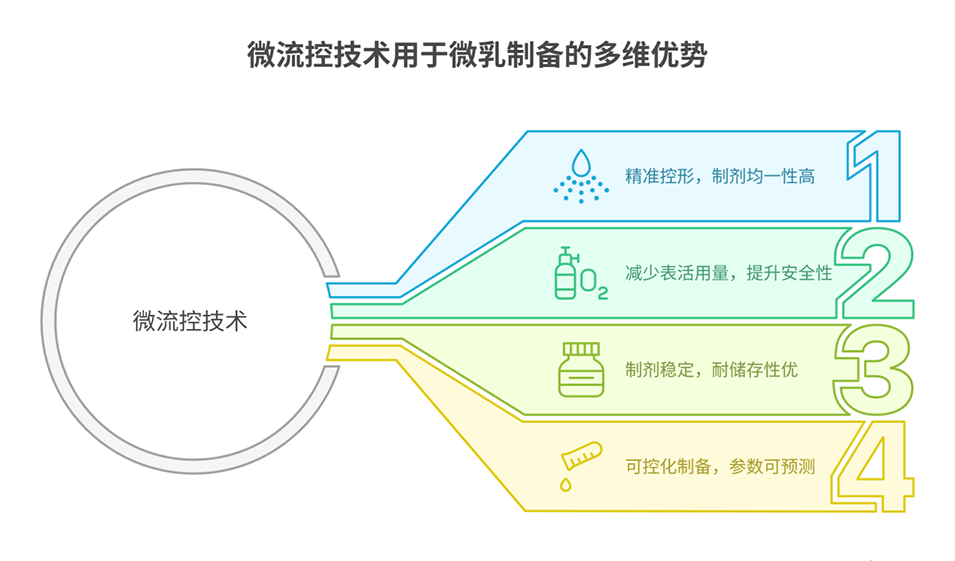
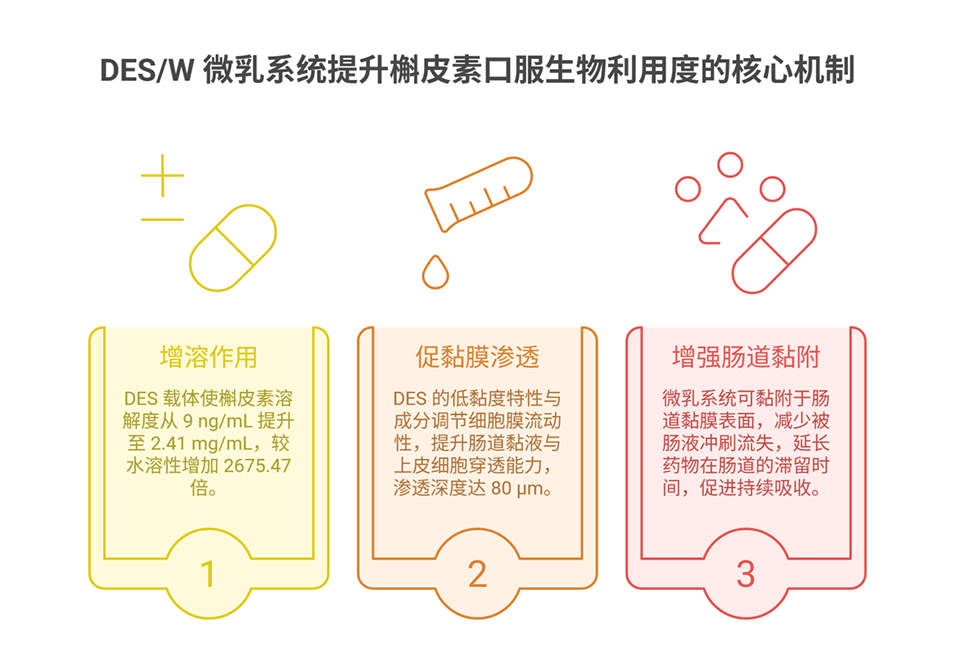
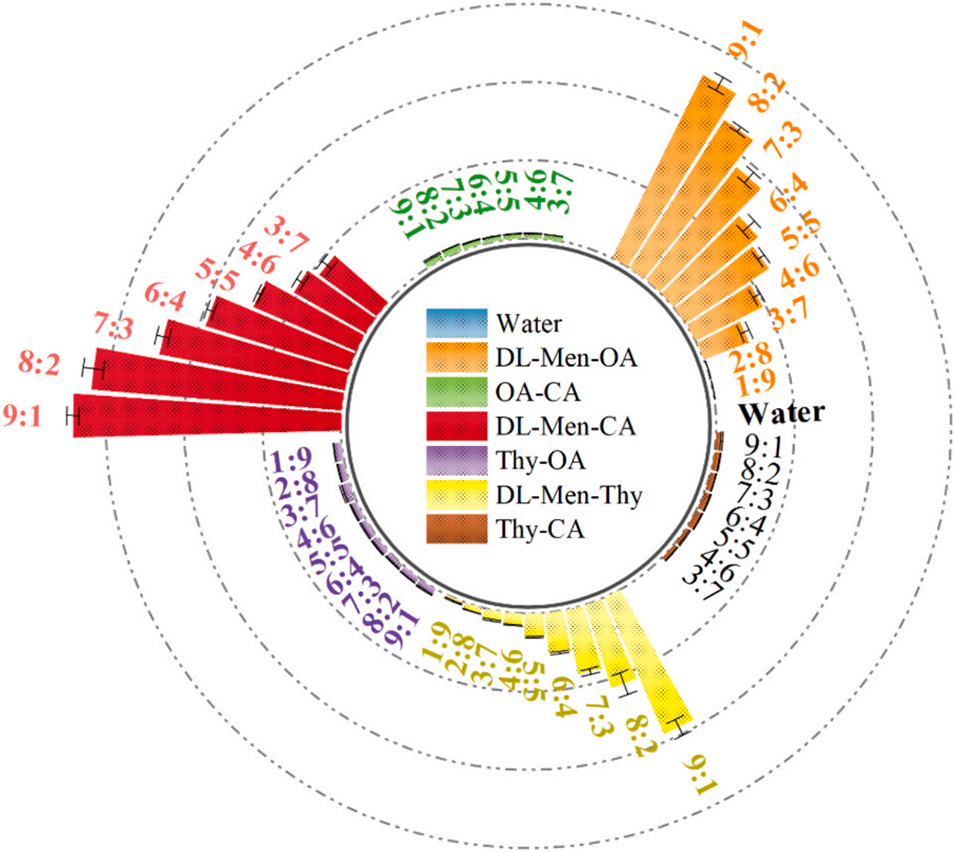
图1:槲皮素(Que)在不同深共熔溶剂(DES)中的溶解度
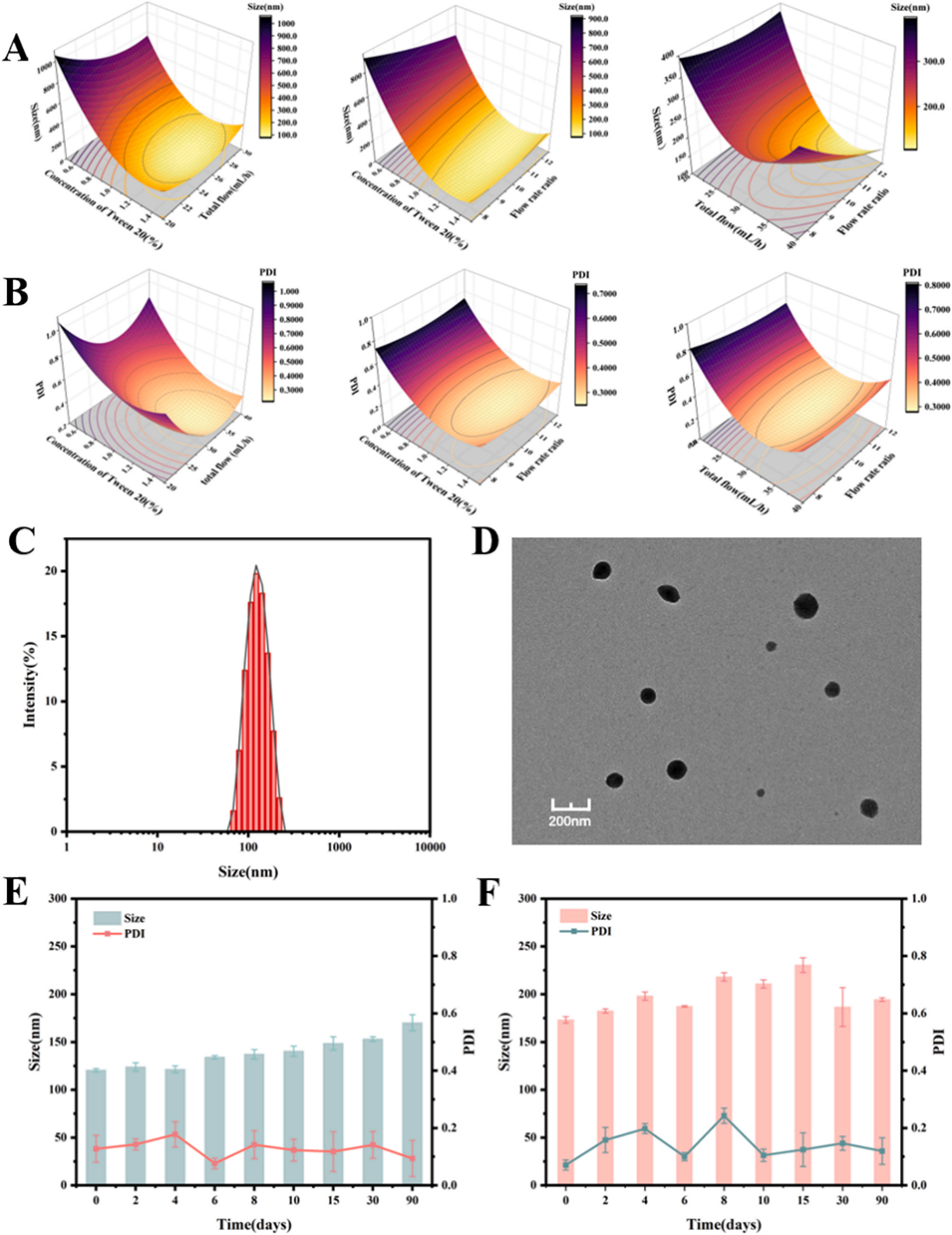
图2:DES/W微乳(DES/W-ME)的响应面优化配方及表征:A. 粒径响应曲面,B. 多分散指数(PDI)响应曲面,C. 空白DES/W微乳的粒径分布,D. DES/W微乳的透射电镜照片,E. 空白DES/W微乳90天放置稳定性(n=3),F. 载槲皮素DES/W微乳(Que-DES/W-ME)90天放置稳定性(n=3)
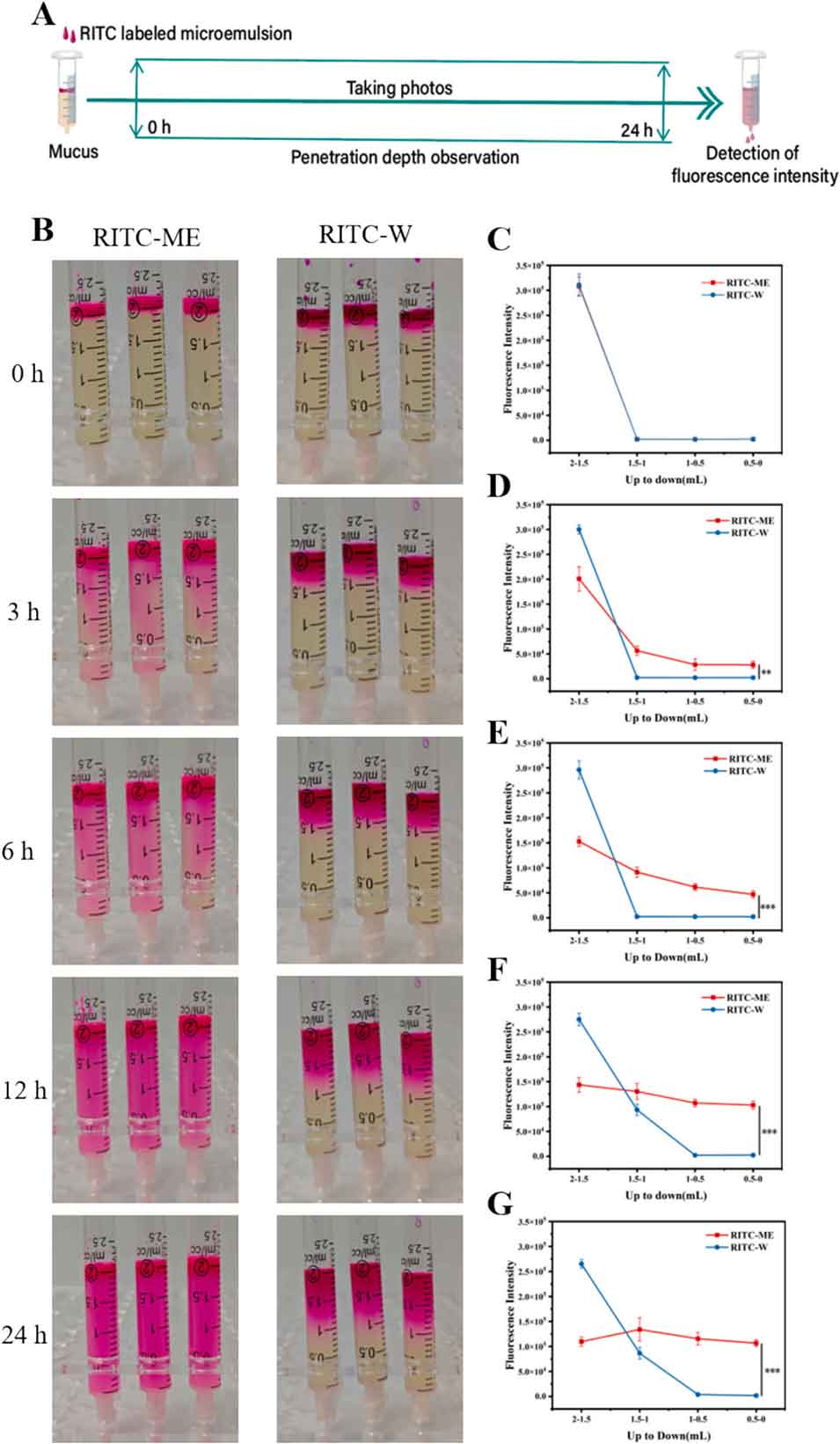
图3:人工黏液(AM)渗透实验:A. 实验示意图,B. 罗丹明B标记的DES/W微乳(RITC-ME)和罗丹明B标记的水相(RITC-W)在0~24 h穿透人工黏液的图像,C~G. 0~24 h不同时间点人工黏液层从上至下每0.5 mL渗出液的荧光强度(n=3)
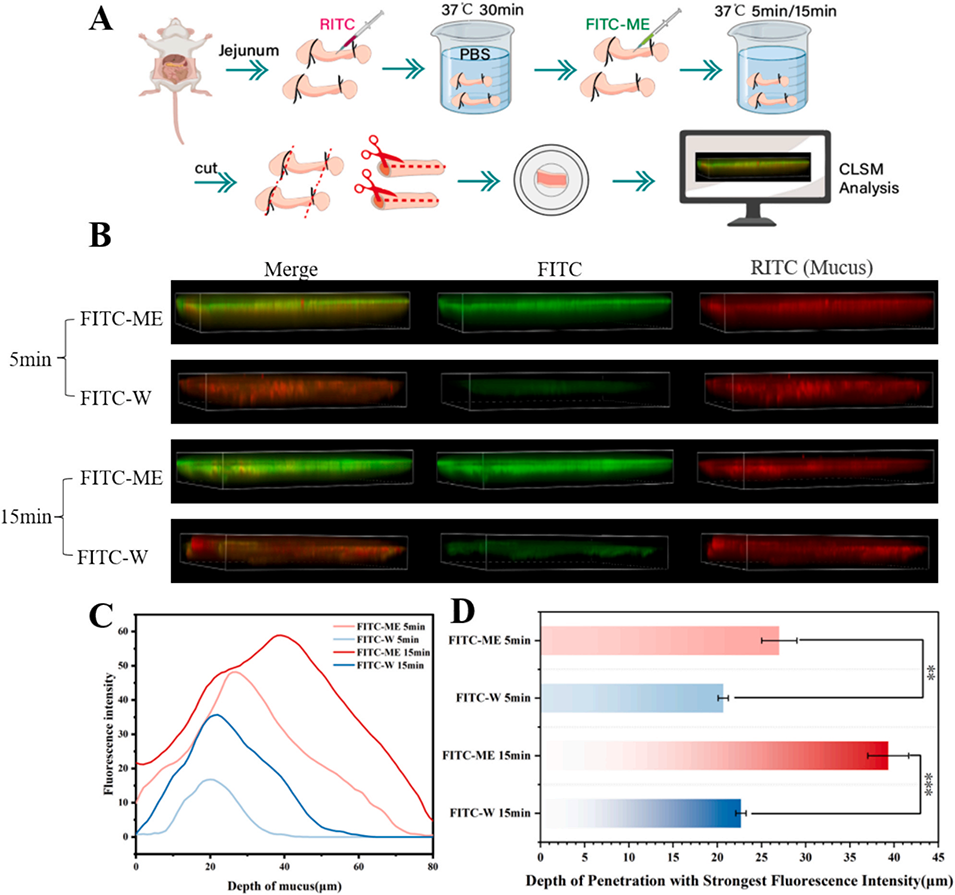
图4:体外肠袢黏液渗透实验:A. 实验示意图;B. 荧光素异硫氰酸酯标记的DES/W微乳(FITC-ME,绿色)和荧光素异硫氰酸酯标记的水相(FITC-W,绿色)在肠黏液(红色)中的渗透行为3D图像;C. 不同人工黏液深度的荧光强度,D. 最大荧光强度对应的人工黏液渗透深度(n=3)
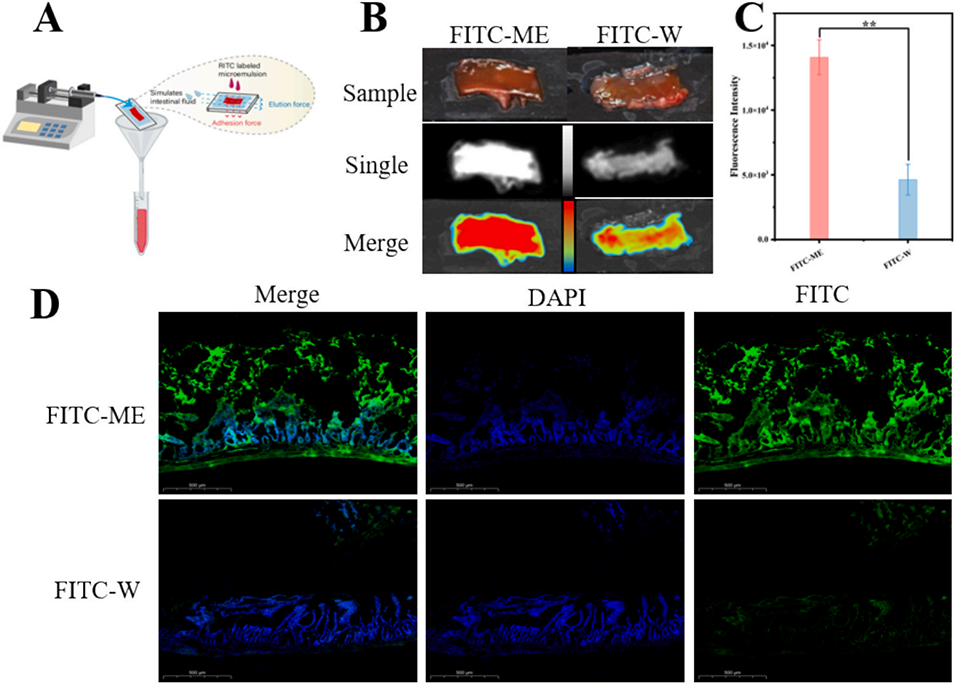
图5:肠道黏附实验:A. 实验示意图;B. 模拟肠液洗脱后离体肠黏膜的生物黏附照片及荧光图像;C. 模拟肠液洗脱后离体肠黏膜单位面积上荧光素异硫氰酸酯(FITC)的平均累积量,D. 模拟肠液洗脱后离体肠黏膜的荧光图像(蓝色:DAPI染色的绒毛细胞核;绿色:负载FITC的载体;比例尺:500 μm;n=3)
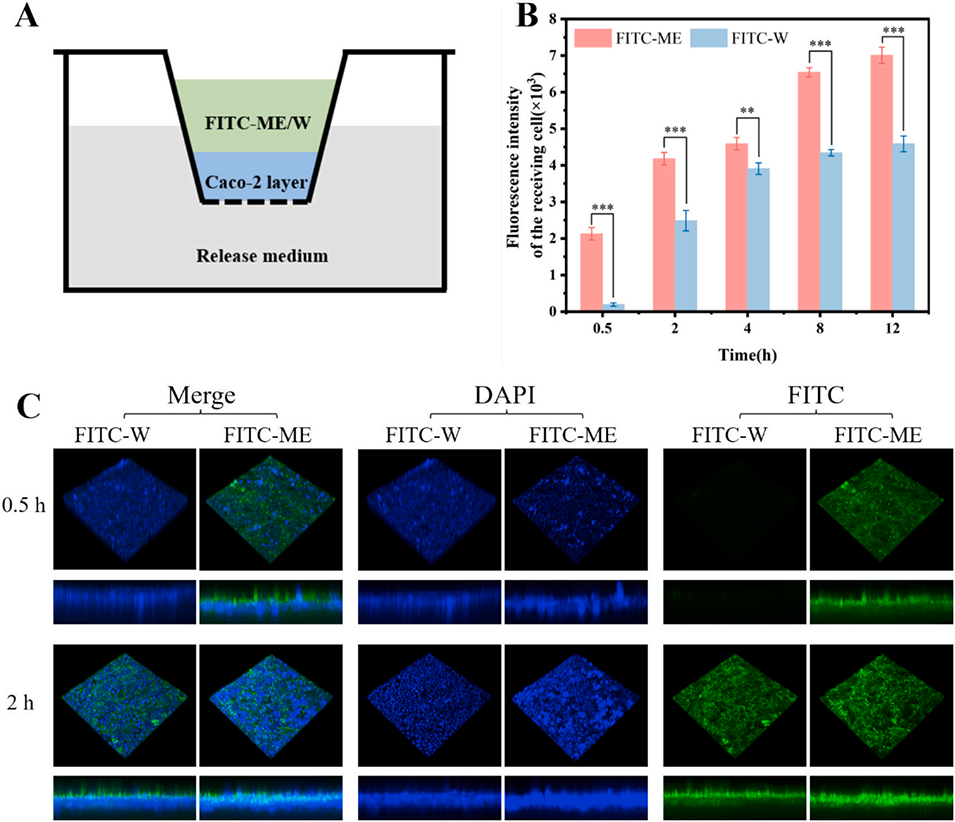
图6:DES/W微乳(DES/W-ME)跨上皮转运评价:A. 搭载Caco-2细胞单层的Transwell小室示意图;B. 与FITC-ME和FITC-W孵育后Transwell接收室中的累积荧光强度,C. 与FITC-ME和FITC-W孵育后Caco-2细胞层的3D立体扫描图像(蓝色:DAPI染色的Caco-2细胞核;绿色:FITC标记的载体;比例尺:50 μm;n=3)
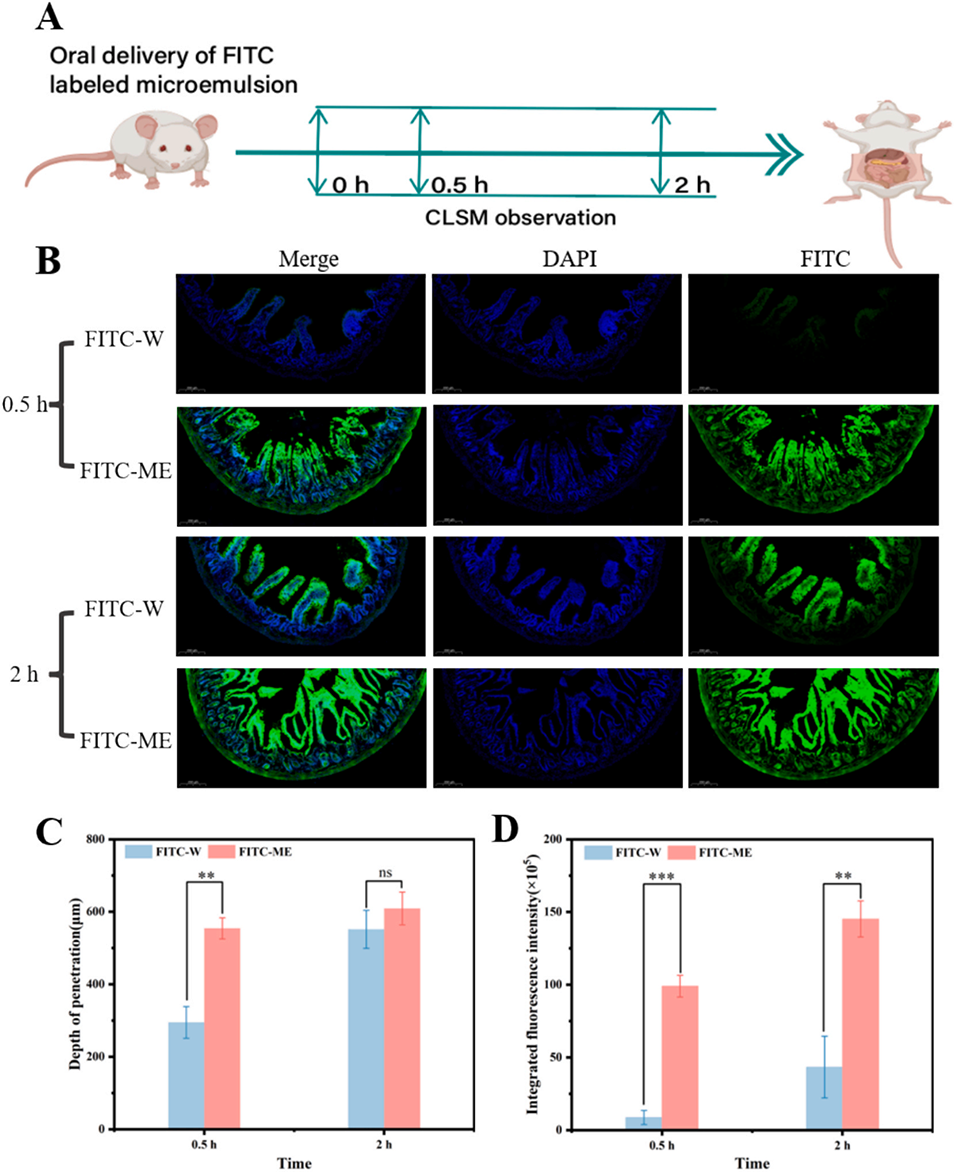
图7:体内肠道通透性实验:A. 肠道通透性实验处理流程,B. FITC-ME和FITC-W穿透小鼠小肠的激光共聚焦显微镜(CLSM)图像(蓝色:DAPI染色的肠绒毛细胞核;绿色:FITC标记的载体;比例尺:200 μm),C. 从CLSM图像中获取的FITC-ME和FITC-W的渗透深度,D. 从CLSM图像中获取的FITC-ME和FITC-W的荧光积分强度
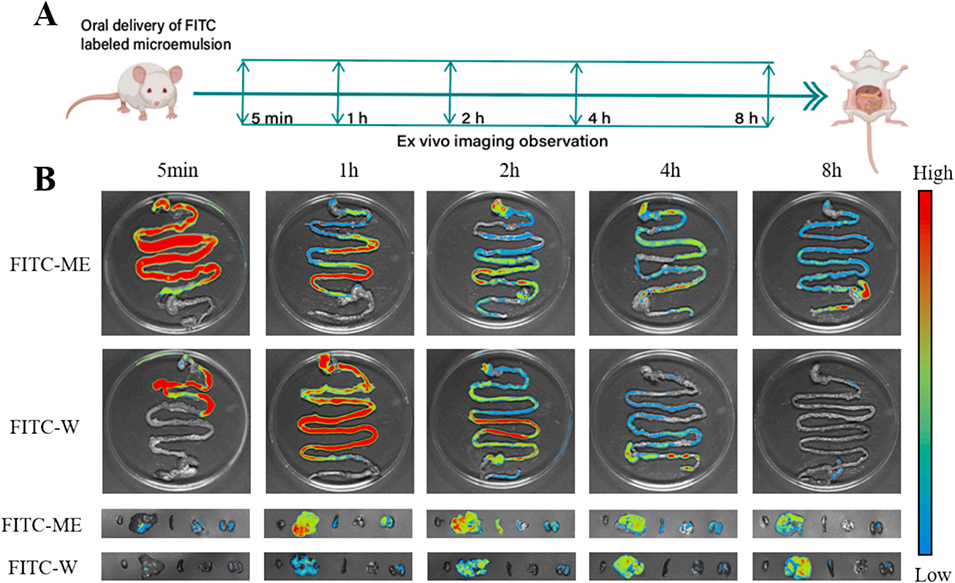
图8:DES/W微乳(DES/W-ME)在胃肠道(GIT)中的分布:A. FITC标记的DES/W微乳(FITC-ME)和FITC标记的水相(FITC-W)在胃肠道中分布的实验处理流程,B. 口服给药后不同时间点FITC-ME和FITC-W在小鼠全胃肠道中的残留荧光图像(n=3)
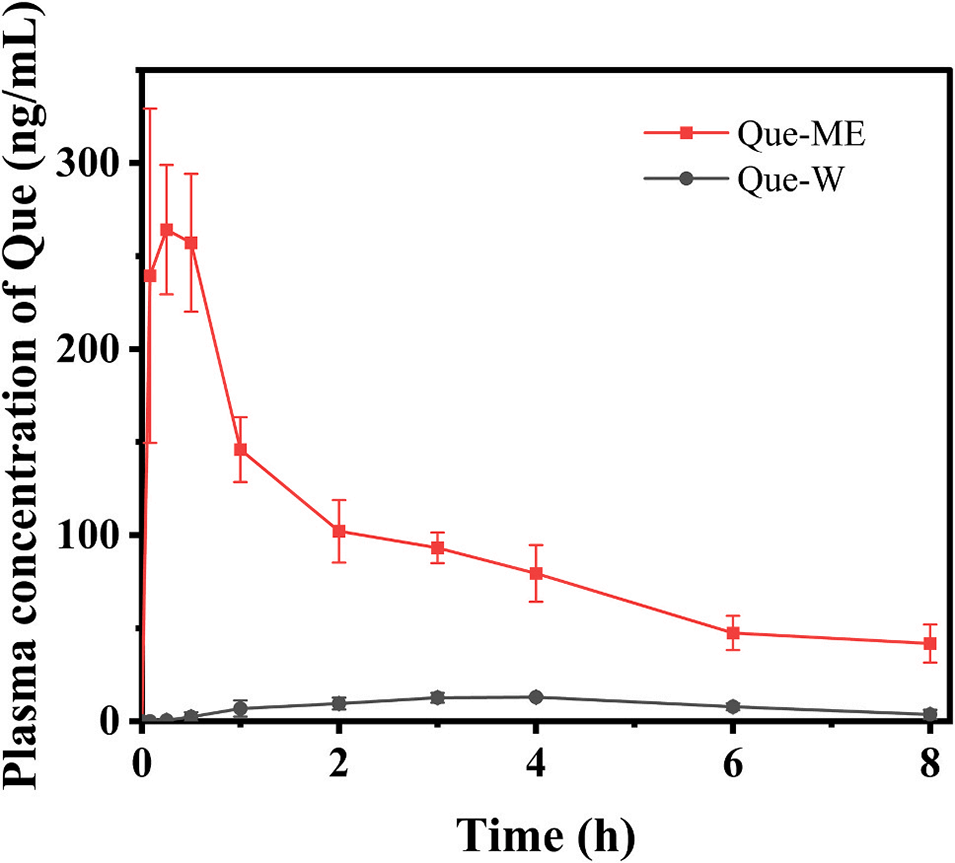
图9:大鼠体内槲皮素(Que)的血药浓度-时间曲线(n=6)
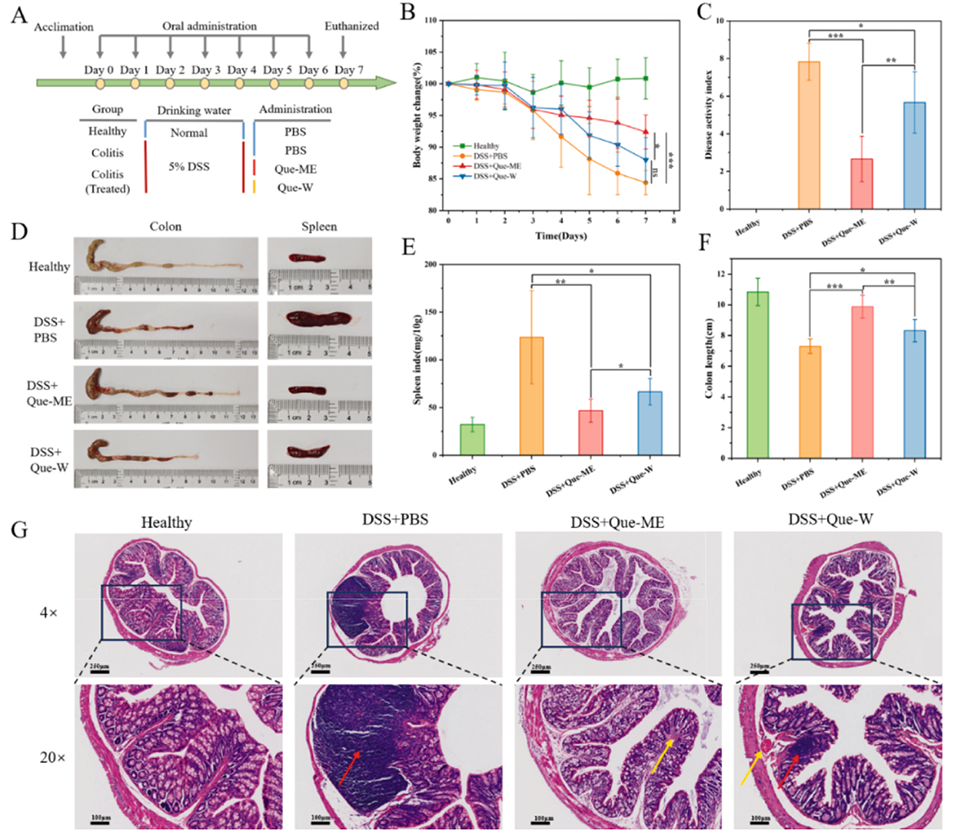
图10:载槲皮素DES/W微乳(Que-ME)对结肠炎小鼠的治疗效果评价:A. 葡聚糖硫酸钠(DSS)诱导结肠炎小鼠模型建立的示意图;B. 各组小鼠每日体重变化;C. 实验最后一天小鼠的疾病活动指数(DAI)评分(n=6);D. 小鼠结肠缩短和脾脏损伤的代表性照片;E. 小鼠脾脏指数测定结果(n=6);F. 小鼠结肠长度统计(n=6);G. 结肠炎小鼠结肠组织的代表性HE染色切片(黄色箭头:红细胞聚集及出血点;红色箭头:炎症细胞浸润),比例尺:250 μm和100 μm
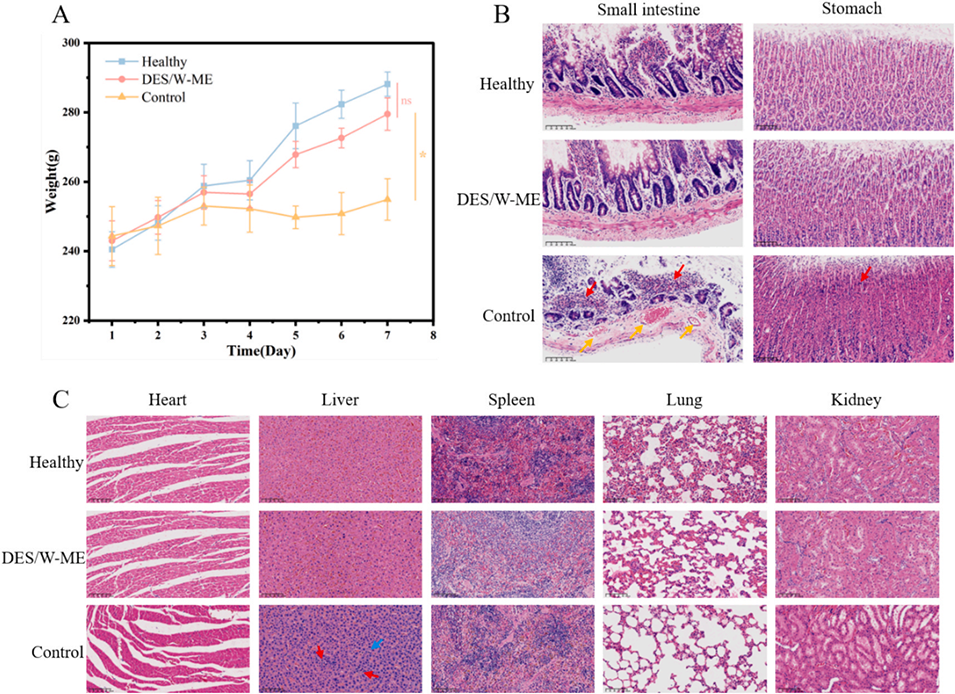
图11:体内安全性评价:A. 不同制剂对大鼠体重的影响;B. 不同制剂对大鼠胃肠道的影响(黄色箭头:红细胞聚集及出血点;红色箭头:炎症细胞浸润);C. 不同制剂经胃内给药对大鼠主要脏器(心、肝、脾、肺、肾)的影响(红色箭头:炎症细胞浸润;蓝色箭头:核溶解);DES/W-ME组为采用微流控技术制备的低表面活性剂含量深共熔微乳;对照组为未采用微流控技术、通过机械搅拌法制备的高表面活性剂含量DES/W微乳(10%DES + 40%吐温20 + 50%水)
论文链接:https://doi.org/10.1016/j.ejpb.2026.115007
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














