导读:
子宫内膜损伤易引发不孕、宫腔粘连等问题,传统治疗存在结构修复不足、干细胞滞留率低、支架静态化等缺陷,为此,南通大学附属医院朱玉娟教授、Mei Yang等人设计并研发了一种超声响应的时空可编程核壳压电微球(SPCM),用于子宫内膜损伤修复并改善妊娠结局,为子宫内膜损伤及相关妇科疾病的局部治疗提供了新型转化方案。相关研究以“Spatiotemporal piezoelectric microspheres for wireless endometrial repair with improved pregnancy outcomes”为题目,发表在期刊《Materials Today Bio》上。

本文要点:
1、该研究提出一种新型时空响应性压电微球治疗平台,可应用于超声引导下的子宫内膜再生与生育功能恢复。
2、该微球通过微流控技术制备,呈核-壳结构:内核为负载金石蚕苷(ACT)的水凝胶并嵌入金修饰钛酸钡(Au@BTO)压电纳米晶,外层包裹粘性聚多巴胺(PDA)壳层。
3、其中,ACT负载水凝胶可抑制炎症细胞因子的释放,并发挥植物雌激素的作用,协同改善生殖功能、促进组织修复;PDA壳层能清除活性氧(ROS),缓解氧化应激与慢性炎症。
4、同时,包埋于微球内的金修饰四方相钛酸钡(Au@BTO)纳米颗粒在超声激活下可产生具有杀菌作用的活性氧,保障局部微环境的无菌状态,且超声可调控ACT的快速释放,提升局部药效。
5、血管芯片模型与子宫内膜损伤大鼠模型的实验结果证实,该微球具备优异的生物相容性,能有效刺激细胞增殖、迁移及血管生成。微球经宫腔递送后,可加速子宫内膜上皮再生、促进血管新生、恢复子宫肌层完整性,并最终保留大鼠的生育能力。
6、该微球系统兼具精准的时空调控能力与多模态治疗功能,为妇科疾病的局部治疗提供了一种革新性解决方案。
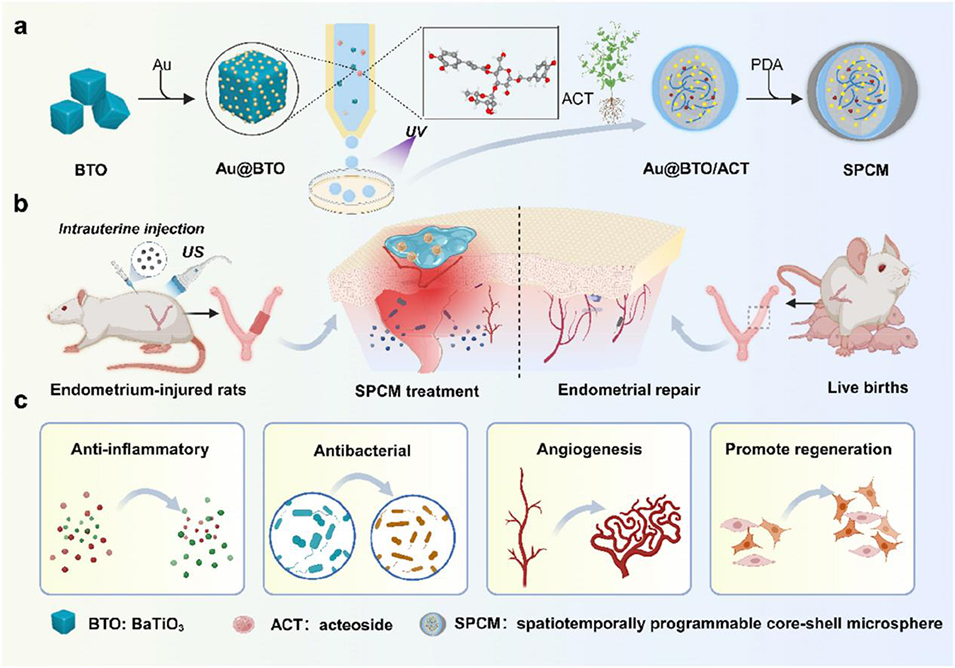
图1. 时空压电微球的制备及子宫内膜修复的作用机制。a 时空压电微球的合成工艺概述;b~c 子宫内膜损伤大鼠模型中,本研究制备的时空压电微球可促进组织修复。借助超声增强的透皮递送作用,该核壳微球发挥抗炎、抗菌、促进血管再生及细胞增殖的作用。上述作用共同促进受损子宫内膜的修复,并显著改善生殖结局。BTO:钛酸钡;US:超声;ACT:金石蚕苷;PDA:聚多巴胺;SPCM:时空可编程核壳微球
该制备方法的优势体现在哪些方面?
依托同轴毛细管微流控装置,实现微球的单分散、高均一性制备
一步式工艺整合多组分负载与结构成型,简化流程且保障核壳结构的完整性
各制备环节的参数精准可调控,实现 SPCM 的可编程化制备,适配个性化需求
温和的制备条件,保留各功能组分的生物活性与理化性能
制备流程的可放大性与工程化潜力,适配后续的生物医学转化
工艺与材料功能的高度协同,为 SPCM 的超声响应特性提供结构基础

图2. 时空可编程核壳微球(SPCM)的表征。a 时空可编程核壳微球的结构示意图;b 钛酸钡(BTO)的扫描电镜图像(比例尺:200 nm);c 金修饰钛酸钡(Au@BTO)的扫描电镜图像(比例尺:200 nm);d 金修饰钛酸钡(Au@BTO)的透射电镜图像(比例尺:150 nm,左上为放大图,比例尺:5 nm);e 时空可编程核壳微球的 STEM-EDX 元素映射;f 时空可编程核壳微球的粒径分布;g 时空可编程核壳微球的明场图像(比例尺:600 μm);h 冷冻干燥后时空可编程核壳微球的扫描电镜图像(比例尺:100 μm);i 冷冻干燥后表面包覆聚多巴胺的时空可编程核壳微球扫描电镜图像(比例尺:1 μm)
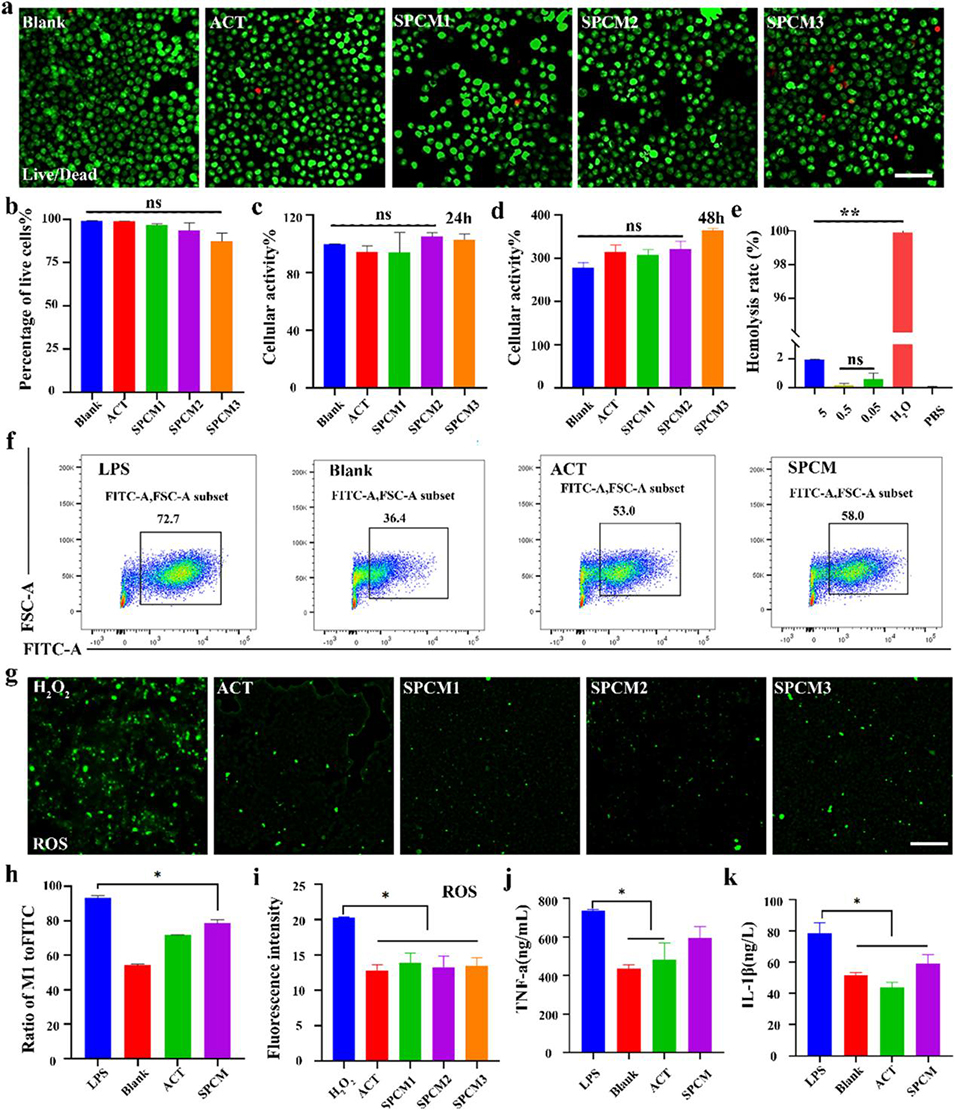
图3. SPCM的生物相容性及抗炎效果表征。a 金石蚕苷(ACT)和核壳微球处理后的活/死细胞染色实验(活细胞为绿色,死细胞为红色,比例尺:200 μm);b 处理后活细胞占比的定量分析;c~d 24 h(c)和 48 h(d)的细胞计数试剂盒 - 8(CCK-8)检测结果;e 核壳微球与血细胞共孵育后的红细胞溶血实验及溶血率定量分析;f 流式细胞术检测核壳微球作用下巨噬细胞的活性氧(ROS)生成情况;g 荧光探针 DCFH-DA 标记法观察金石蚕苷和核壳微球作用下巨噬细胞内的活性氧(绿色荧光,比例尺:100 μm);h 流式细胞术检测结果的定量分析;i 不同处理后活性氧信号的荧光强度分析;j~k 酶联免疫吸附实验(ELISA)检测金石蚕苷和核壳微球作用下细胞上清液中炎症因子的分泌水平。(注:每组随机选取至少 3 张图像进行定量分析,*P<0.05,**P<0.01,单因素方差分析)
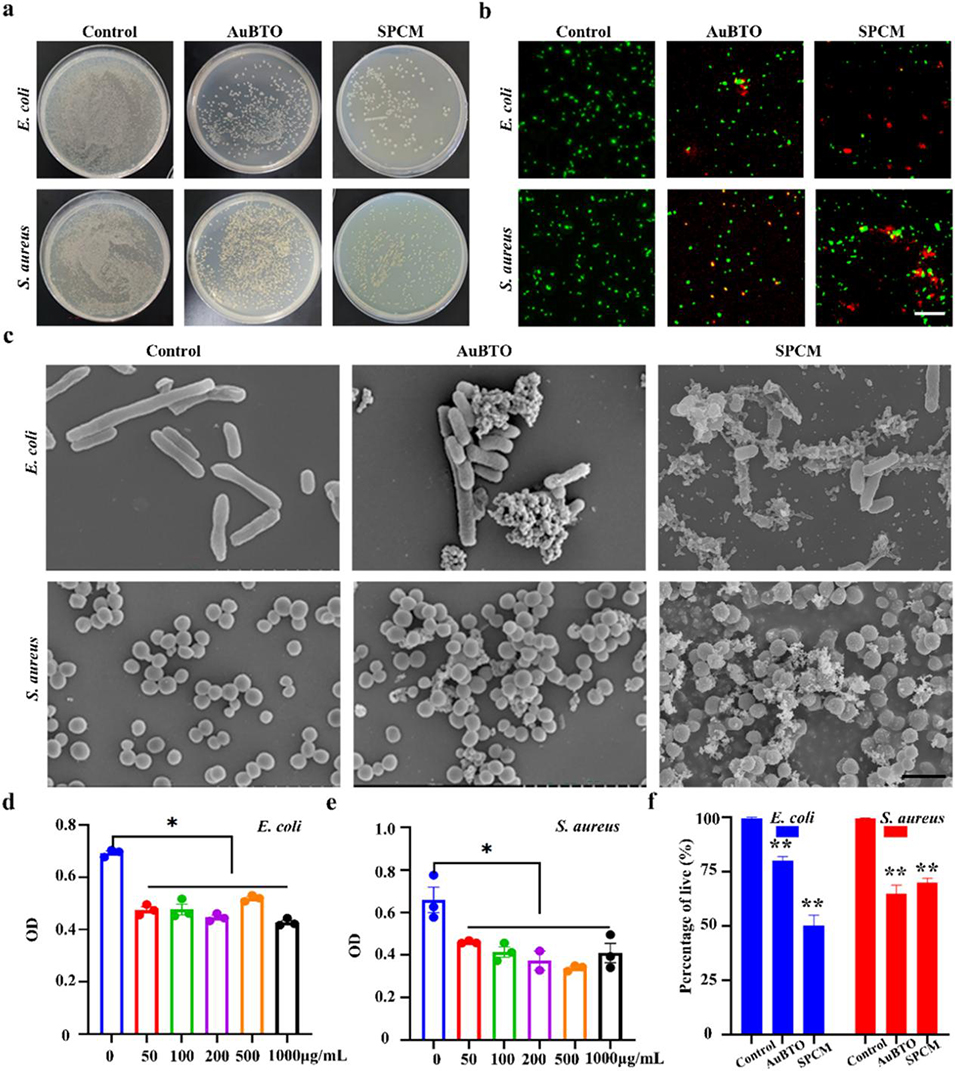
图4. SPCM的抗菌效果表征。a 不同处理后菌落的琼脂培养平板图像;b 不同组别细菌活性的荧光染色结果(活菌为绿色,死菌为红色,比例尺:100 μm);c 不同处理后细菌的扫描电镜图像;d~e 液体培养基(LB)的吸光度(OD)检测结果;f 细菌存活率的定量分析。(注:*P<0.05,**P<0.01,单因素方差分析)
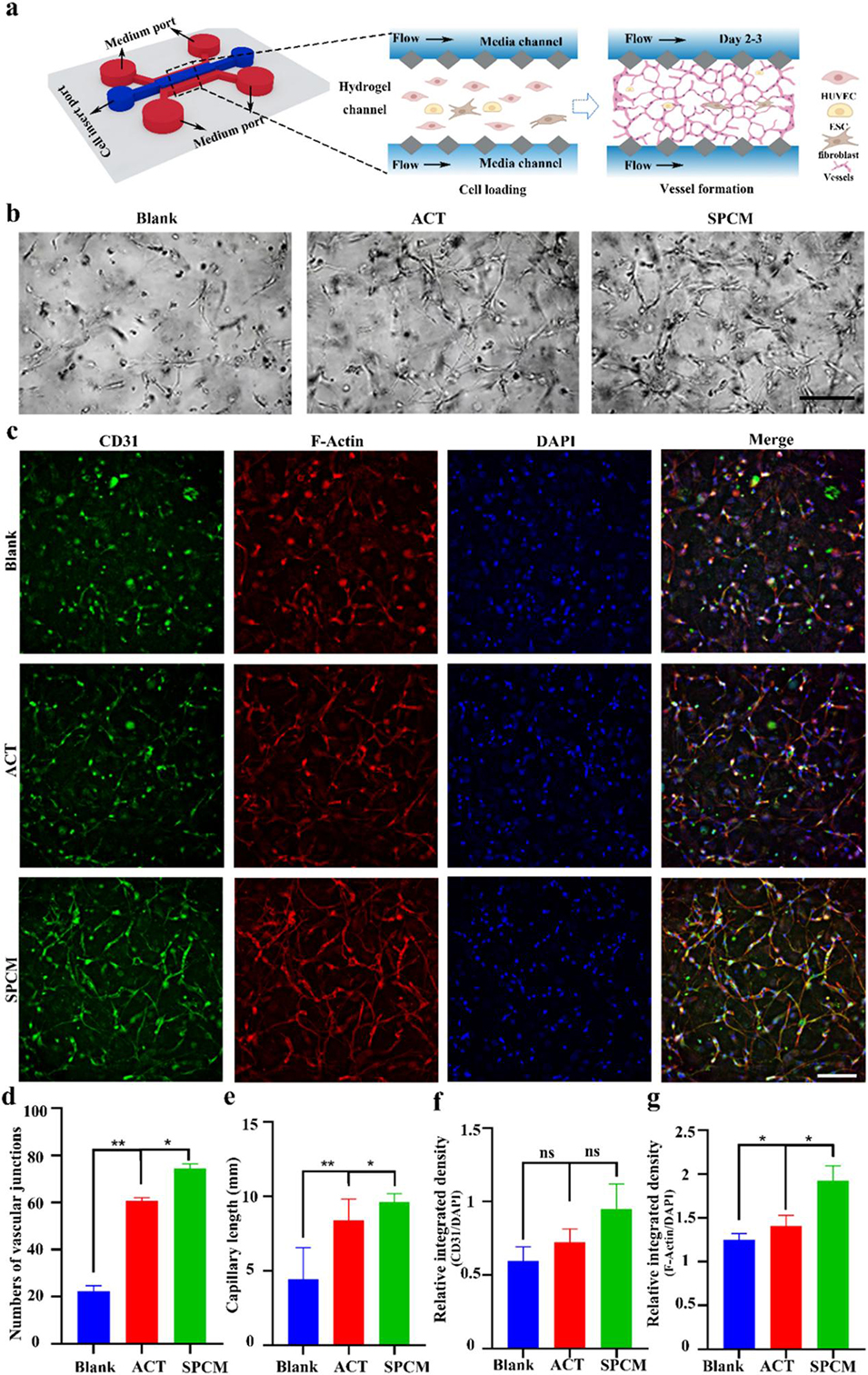
图5. 金石蚕苷(ACT)和SPCM对血管管腔形成的影响。a 三通道微流控芯片模型示意图,以及接种细胞在纤维蛋白水凝胶中重排形成相互连通的微血管网络的示意图;b 微流控芯片中不同干预处理下微血管网络形成的明场图像(比例尺:100 μm);c 表达 CD31 和 F - 肌动蛋白的微血管网络荧光图像(比例尺:100 μm);d~e 血管连接点数和毛细血管长度的定量分析;f~g CD31 和 F - 肌动蛋白相对荧光信号的统计分析。(注:*P<0.05,**P<0.01,单因素方差分析)
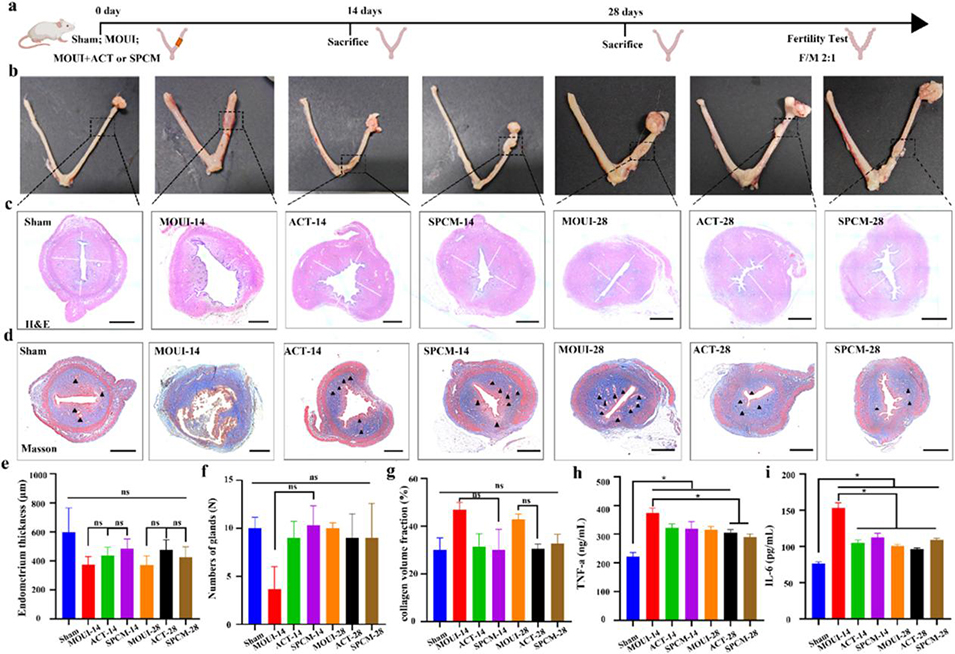
图6. SPCM在大鼠子宫内膜机械损伤模型(MOUI)中的治疗效果。a 体内实验流程;b 大鼠子宫角的大体形态;c 苏木精-伊红(H&E)染色切片(白色线条指示子宫内膜厚度,比例尺:400 μm);d 马松(Masson)染色图像(黑色三角标指示腺体,比例尺:400 μm);e~g 子宫内膜厚度(e)、腺体数量(f)和胶原体积分数(g)的定量分析;h~i 酶联免疫吸附实验(ELISA)检测血清中肿瘤坏死因子 -α(TNF-α)和白细胞介素 - 6(IL-6)的含量。(注:所有数据以均值±标准差表示,n=3,*P<0.05,单因素方差分析)
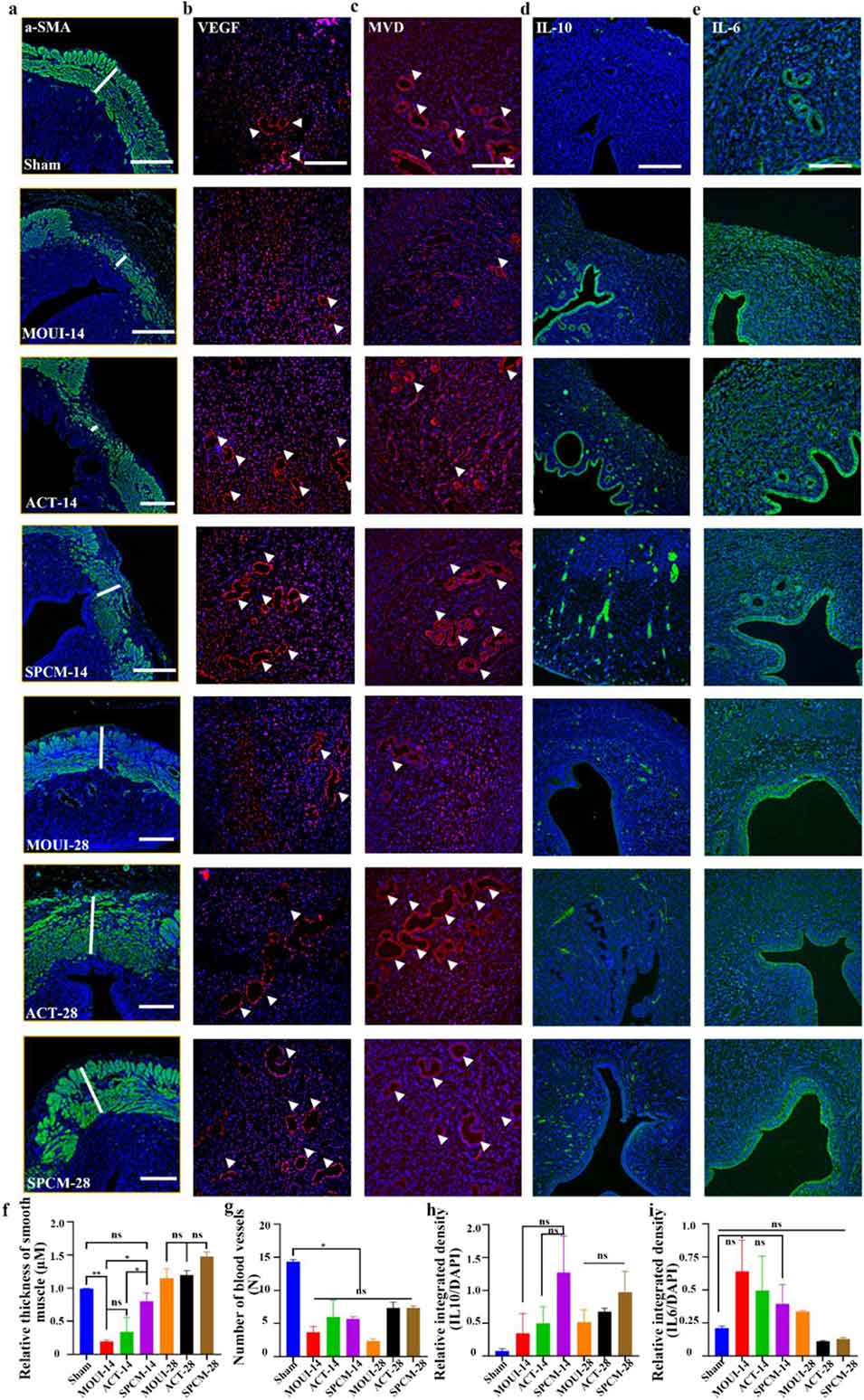
图7. SPCM处理后大鼠子宫组织的表征。a α- 平滑肌肌动蛋白(α-SMA)染色检测子宫平滑肌厚度(白色线条指示平滑肌厚度,比例尺:100 μm);b~c 血管内皮生长因子(VEGF)/微血管密度(MVD)免疫荧光染色标记血管分布(比例尺:200 μm);d~e 白细胞介素 - 10(IL-10)和白细胞介素 - 6(IL-6)染色对局部炎症水平的定量分析(比例尺:200 μm);g~i 大鼠子宫组织中上述分子表达水平的定量分析。(注:*P<0.05,单因素方差分析)
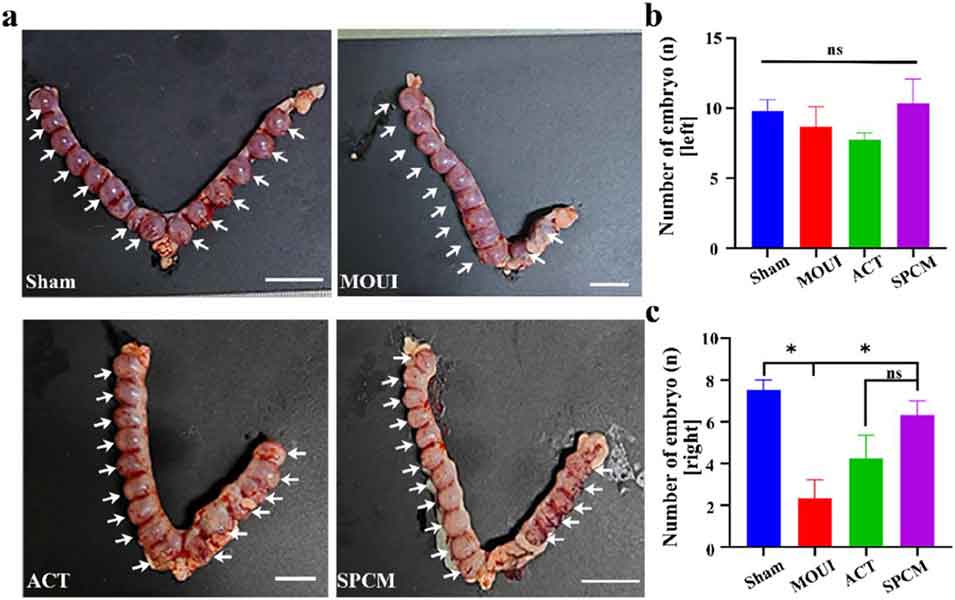
图8. SPCM介导的大鼠生育能力恢复。a 假手术组、子宫内膜损伤组及经金石蚕苷(ACT)/核壳微球(SPCM)处理的损伤组大鼠子宫角的胚胎着床情况(白色箭头指示胚胎,比例尺:2 cm);b 大鼠单侧子宫角的胚胎着床点数统计(n=4,*P<0.05)
论文链接:https://doi.org/10.1016/j.mtbio.2026.102915
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














