近年来,水凝胶成型技术取得了显著进展,并在生物医学领域得到了广泛应用。水凝胶作为一种三维聚合物网络结构,由亲水性聚合物组成,能够吸收并保留大量水分,同时保持其结构完整性和类似软组织的特性。然而,传统的块状水凝胶由于其毫米级的尺寸,在应用中常面临需要侵入性植入、营养扩散效率低以及细胞分布不均等问题。为了克服这些挑战,微米和纳米尺度的水凝胶结构,如微球(HMs),逐渐成为研究热点。HMs具有高比表面积、可调的机械性能和较大的设计灵活性,是实现特定生物功能的理想材料。

本文旨在全面综述水凝胶微球(HMs)在生物医学领域的最新研究进展,涵盖其核心生物基材料、主要制备方法、在各类生物医学应用中的作用机制,以及当前面临的挑战与未来发展方向。通过系统梳理现有研究成果,本文以期激发新的探索思路,加速HMs从实验室研究向临床应用的转化,进而推动生物医学领域的创新发展。相关研究成果以“Hydrogel Microspheres for Biomedical Applications”为题目,发表于期刊《Small Science》。
本文要点:
1、该综述聚焦水凝胶微球(HMs)在生物医学领域的应用,系统梳理了其天然材料(海藻酸盐、壳聚糖等)和合成材料(PLGA、PEGDA等)两类生物基原料、乳化法、微流控技术等多种制备方法及各自优劣。
2、重点阐述了其在药物递送、细胞培养、再生医学、伤口愈合、肿瘤免疫等核心场景的应用机制与研究进展,提及已获批的临床产品(如Embosphere、DC Bead)和在研项目。
3、同时指出当前材料体系有限、机械性能与降解调控不足等挑战,展望了智能设计、多功能整合与临床转化的未来方向。
一张图读懂全文
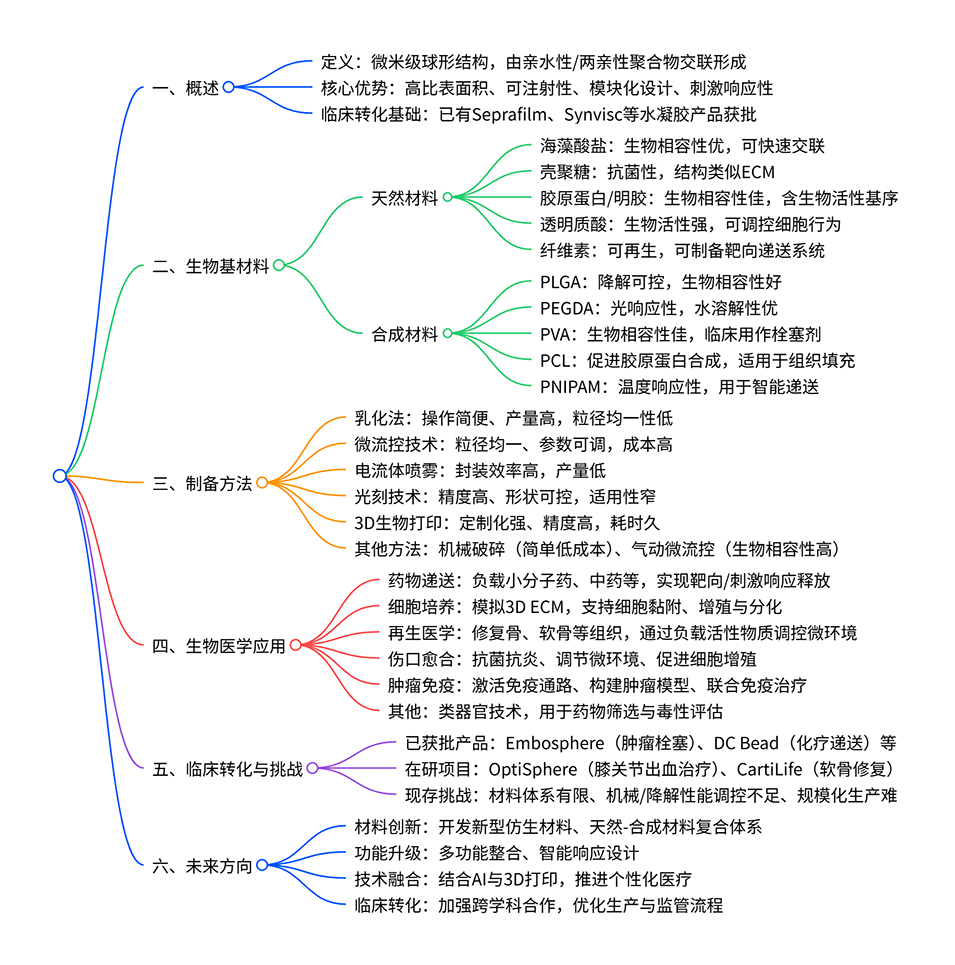
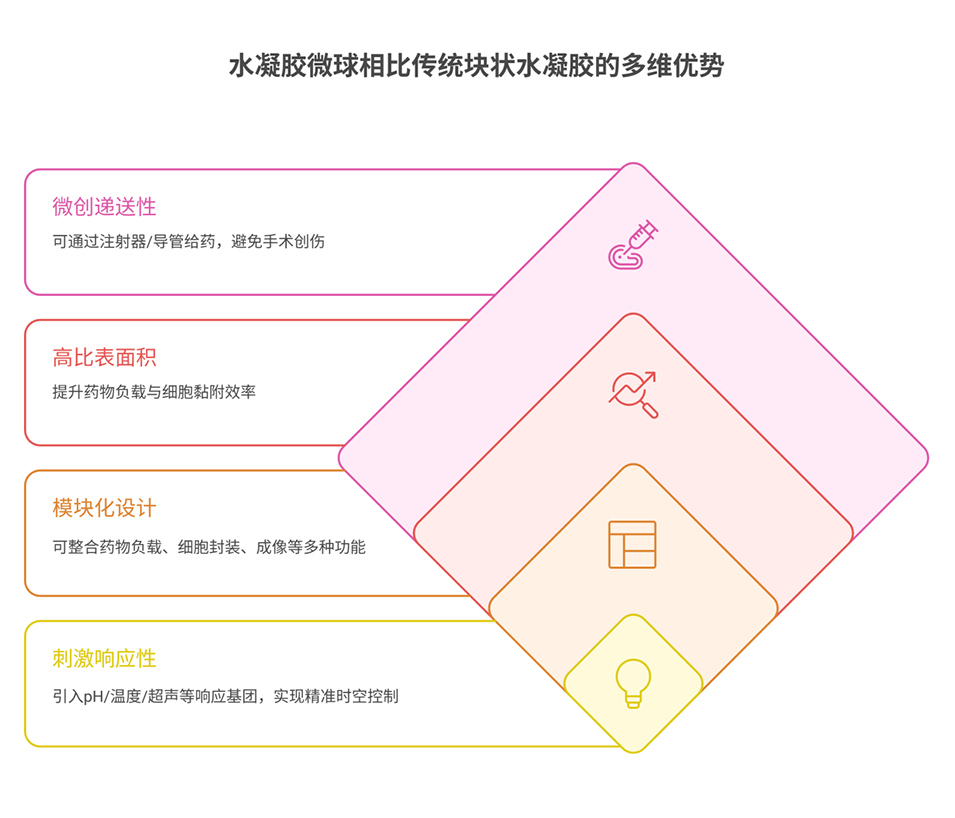
水凝胶微球制备方法对比表
制备方法 | 粒径均一性 | 产量 | 成本 | 优势 | 局限性 |
乳化法 | 低 | 高 | 低 | 操作简便、效率高、工艺参数易调控 | 存在溶剂残留、乳液分散不均、粒径分布宽 |
微流控技术 | 高 | 高 | 高 | 形貌与尺寸均一、参数可高度调控、重现性优异 | 设备维护成本高、操作复杂、加工耗时较长 |
电流体喷雾 | 高 | 低 | 高 | 尺寸均一、封装效率高、对细胞损伤小 | 产量低、操作复杂、单分散性欠佳 |
光刻技术 | 高 | 低 | 高 | 控制精度高、可制备特定形状、材料适应性广 | 适用范围窄、成本高昂、效率低下 |
3D 生物打印 | 高 | 低 | 高 | 精度高、定制化程度高、适用范围广、可控性强 | 设备参数复杂、生产耗时久、成本较高 |
机械破碎法 | 低 | 高 | 低 | 操作极其简便、成本低、产量高 | 生物相容性差、尺寸均一性低 |
气动微流控技术 | 高 | 高 | 高 | 效率高、清洁无污染、生物相容性好 | 难以制备复杂结构 |
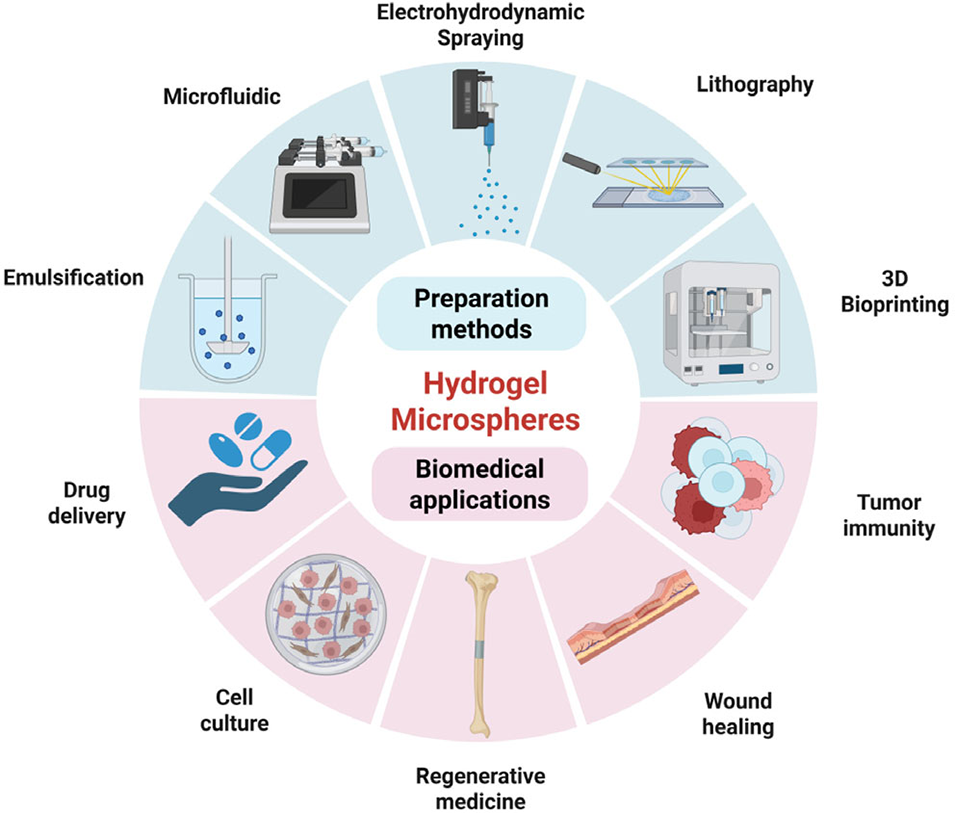
图1. HMs的制备方法及生物医学应用
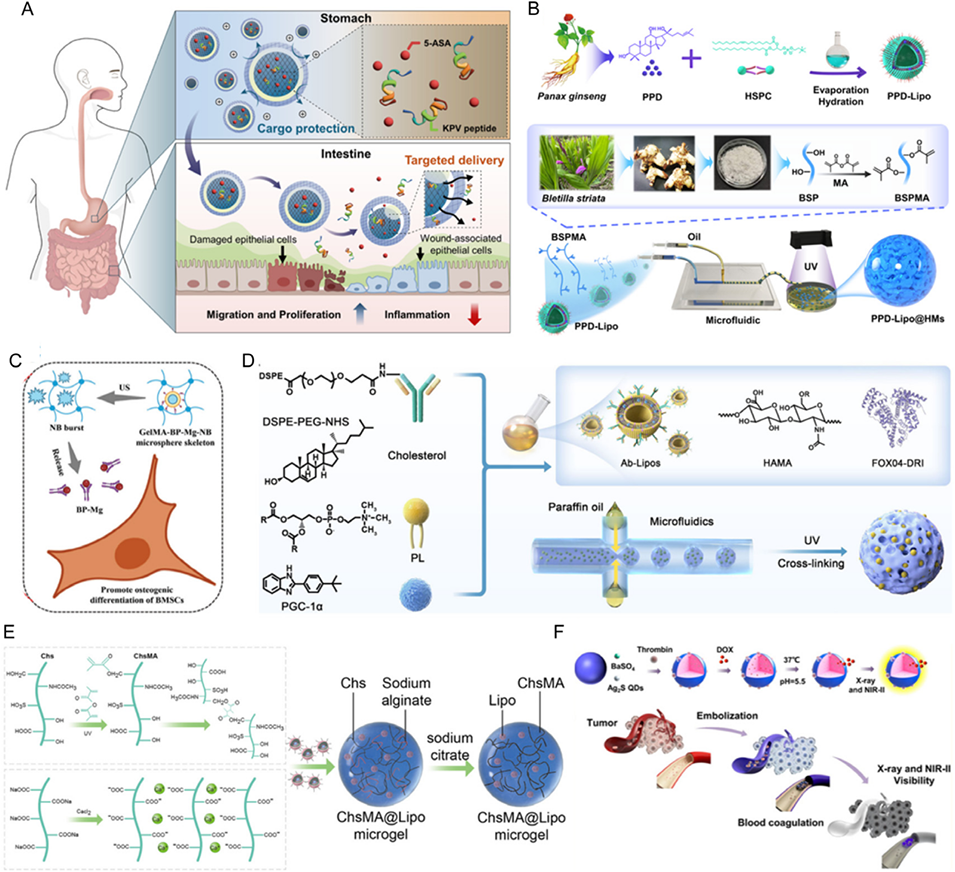
图2. HMs在药物递送中的应用
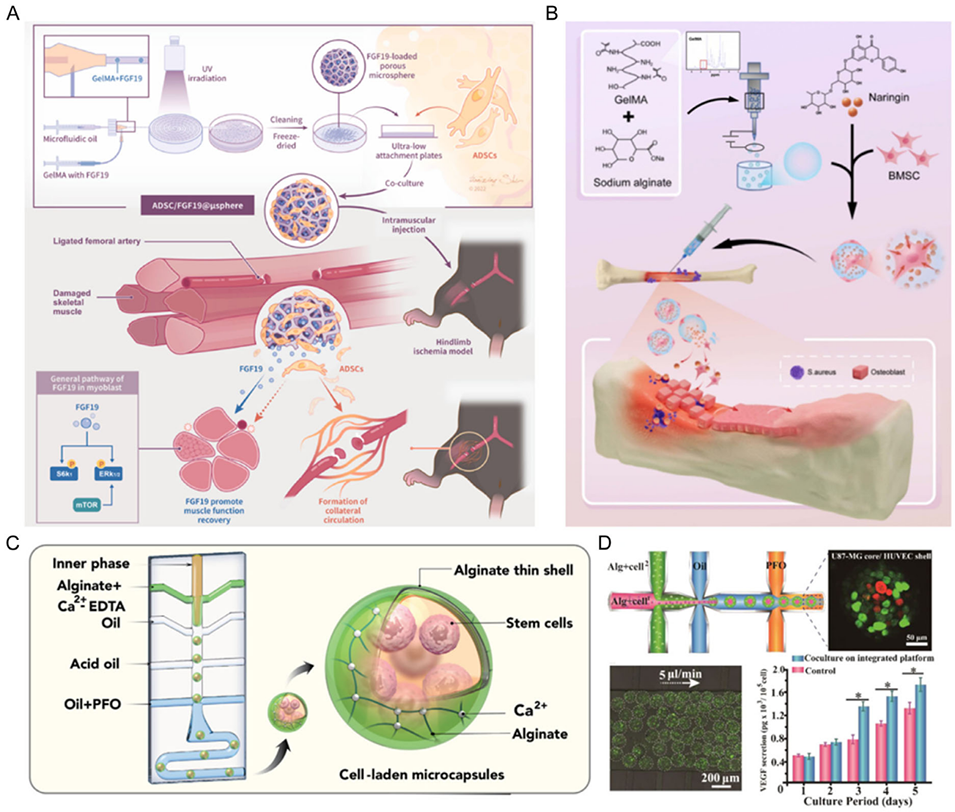
图3. HMs在细胞培养中的应用
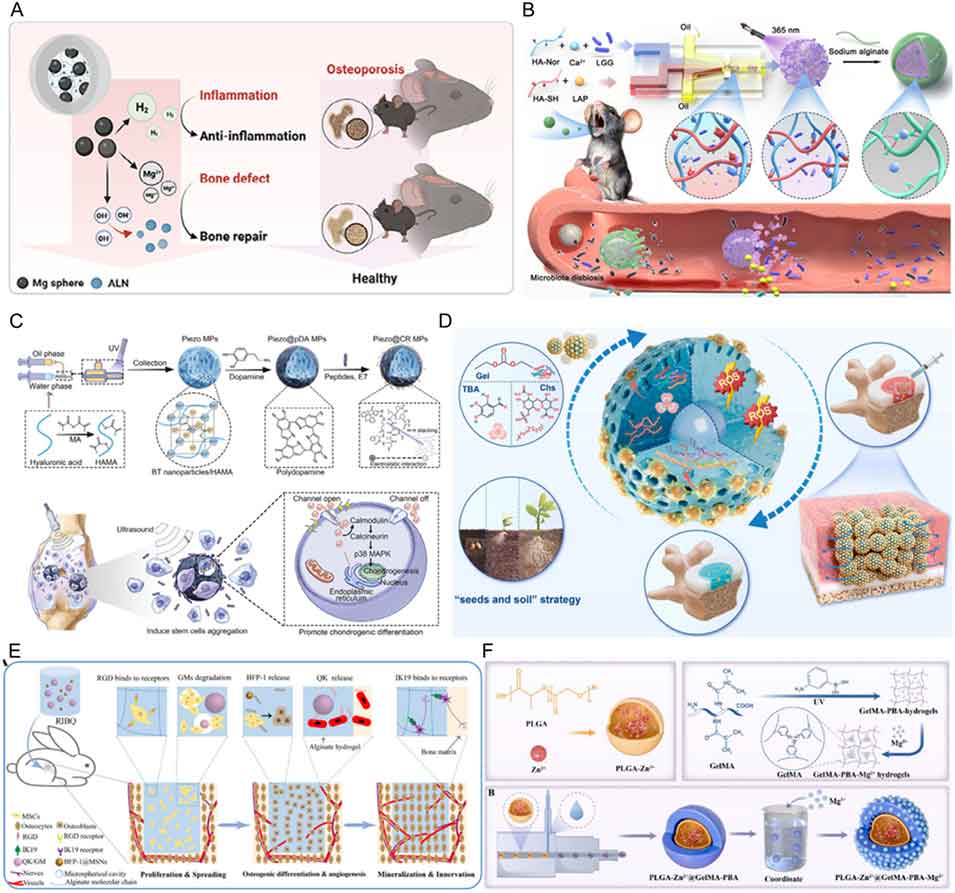
图4. HMs在再生医学中的应用
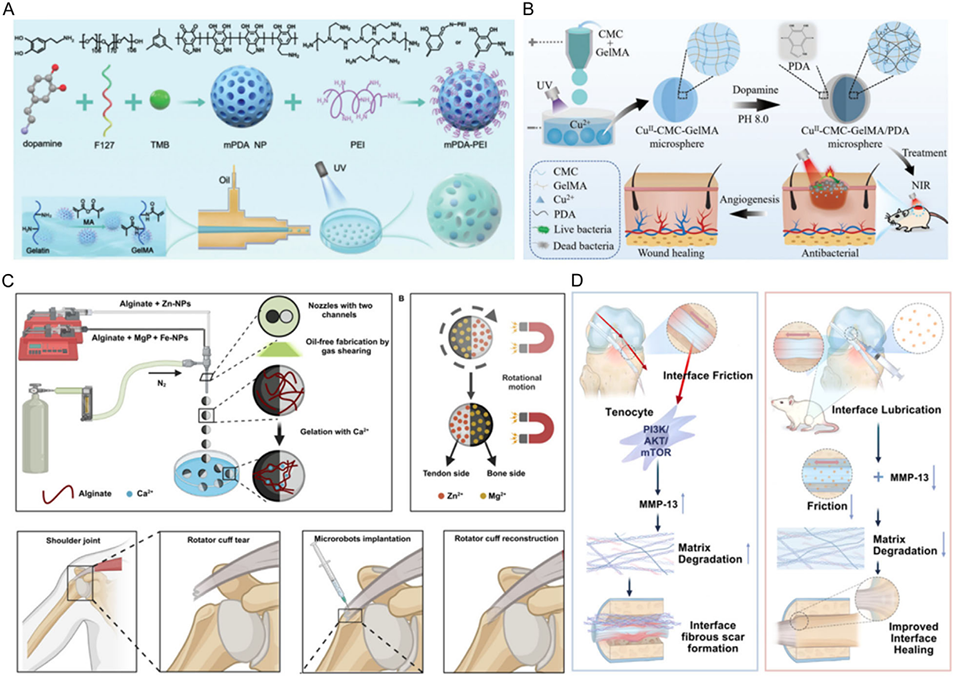
图5. HMs在伤口愈合中的应用
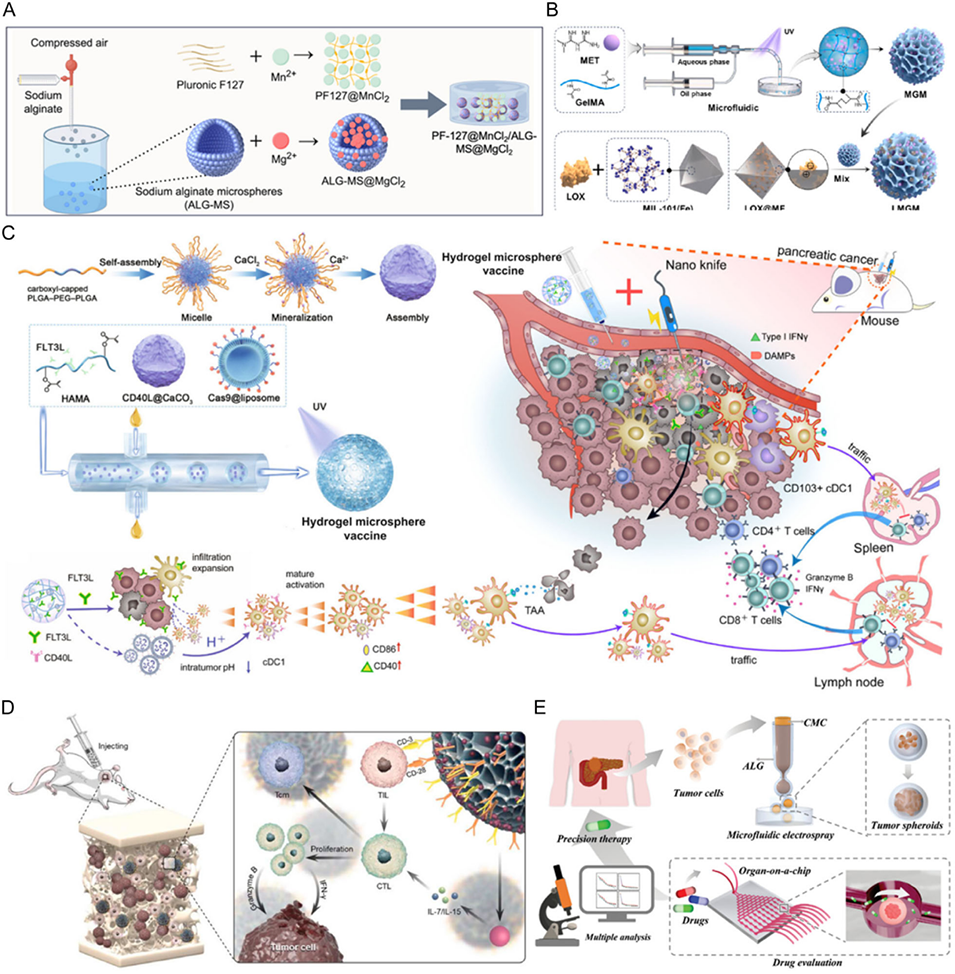
图6. HMs在肿瘤免疫中的应用
论文链接:https://doi.org/10.1002/smsc.202500453
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














