双乳液为制备可包封多种核心材料的功能微胶囊提供了多功能平台。尽管微流控技术被广泛用于制备单分散性高、尺寸控制精准的此类乳液,但传统装置制造需专业技术以实现精确的几何对准和选择性表面润湿性,这限制了通量并阻碍了可扩展性。

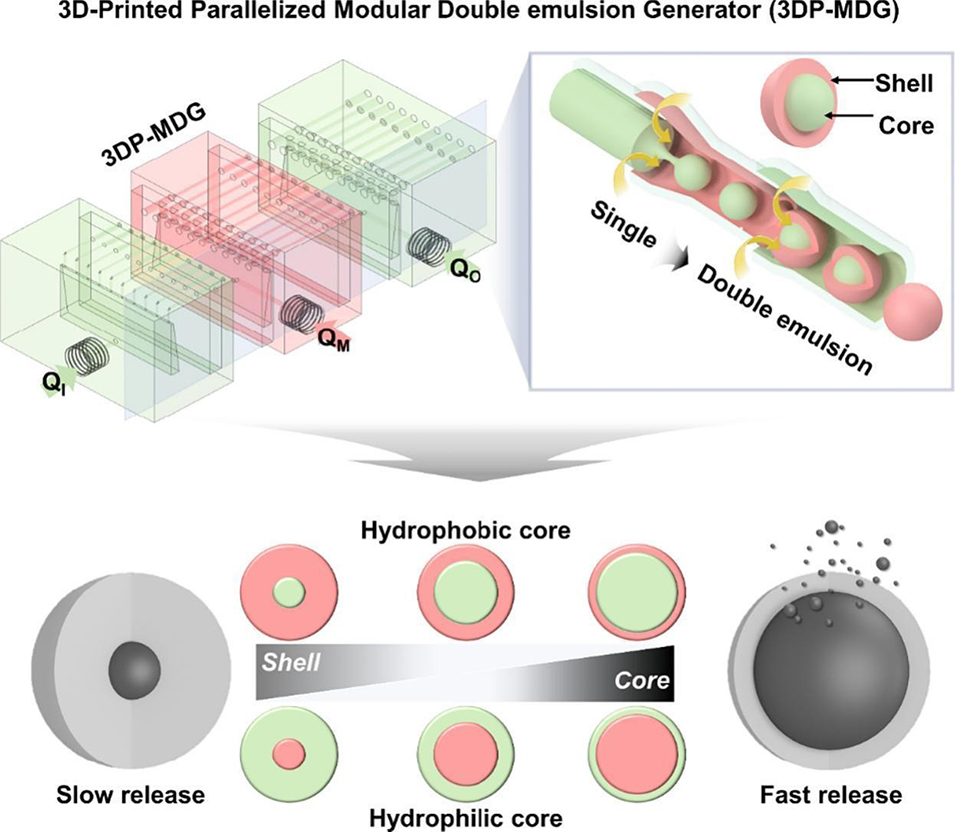
近期,韩国浦项科技大学联合国立釜庆大学研究团队提出一种3D打印并行模块化双乳液生成器(3DP-MDG),通过二氧化硅纳米颗粒(SiNPs)表面改性实现通道亲水性调控,结合管套管结构设计和CFD优化的流量分配器,解决了传统微流控技术产量低、制造复杂的痛点,可稳定生产O/W/O和W/O/W两种双乳液,最大吞吐量分别达115 mL h−1和155 mL h−1,且乳液分散系数(CV)低于3%。该装置具备低成本、易组装、可重复使用和规模化潜力,为药物递送、化妆品等领域的功能微胶囊生产提供了高效平台。相关研究以“Robust and scalable production of double emulsion templated microcapsules using a 3d-printed parallelized modular device”为题目,发表在期刊《Chemical Engineering Journal》上。
本文要点:
1、该研究提出了一种3D打印并行模块化双乳液生成器(3DP-MDG),旨在解决传统双乳液生产中存在的产量低、设备制造复杂、表面润湿性控制难等问题,实现功能微胶囊的稳健且可扩展生产。
2、通过计算机辅助设计(CAD)和计算流体动力学(CFD)模拟优化了装置结构,包括管套管型液滴生成器和锥形流量分配器,确保流体均匀分布并最大化剪切力。
3、采用二氧化硅纳米颗粒(SiNPs)涂层对装置内表面进行亲水性改性,结合模块化的一键组装设计,可选择性控制表面润湿性,成功制备出O/W/O和W/O/W两种类型的双乳液。
4、该装置展现出优异性能:O/W/O乳液的最大产量达115 mL/h,W/O/W乳液达155 mL/h,且乳液分散性好(变异系数低于3%);可通过调节内、中、外相的流量比,精准调控双乳液的内外核尺寸及内核比例(40.4%-90.5%);经24小时连续运行验证,装置稳定性强、可重复使用。
5、此外,以海藻酸盐为壳材制备的pH响应型微胶囊,其释放行为可通过内核比例调控,在不同pH环境下呈现定制化的释放曲线,表明该装置在药物递送、化妆品等领域具有广泛应用潜力。未来研究将聚焦于装置微型化及数据驱动的设计优化,进一步推动双乳液技术的工业化转化。
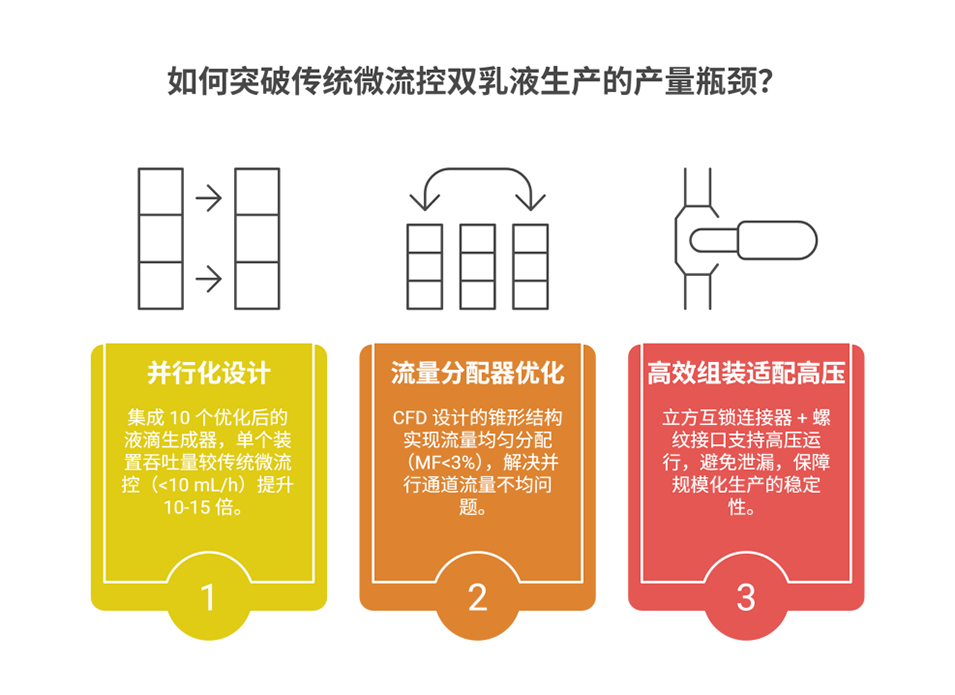
3DP-MDG如何实现双乳液核壳比的精准调控,且该调控对微胶囊功能有何影响?
核壳比调控方式:通过系统调节内相(Q₁)、中相(QM)、外相(QO)的流量比例,实现O/W/O(4%-62.7%)和W/O/W(51.3%-90.5%)的核壳比可调;
功能影响:核壳比直接决定微胶囊的释放特性——以pH响应型海藻酸盐微胶囊为例,内芯体积比越低(外壳越厚),释放起始时间越长(45%内芯组80s,75%内芯组41s),且储存稳定性更优(7天泄漏率仅8%),可根据快速释放或长效缓释等具体应用场景定制核壳比例。
与传统表面改性技术相比,SiNPs涂层在3DP-MDG中的优势及稳定性表现如何?
传统技术如O₂等离子体、水解等,难以在3D打印表面形成足量活性基团,而SiNPs涂层通过酸性条件(pH=2.0)下的共价交联,形成均匀纳米层(~7nm),既实现亲水性转变(接触角从92°降至26°),又不引入额外粗糙度异质性;
其稳定性表现:① 连续运行≥24h,涂层润湿性无衰减;② 经多次清洗、干燥及高压流体冲击后,仍能维持稳定的亲水性,保障双乳液生产的一致性,支持装置重复使用,3次12h循环无性能下降。
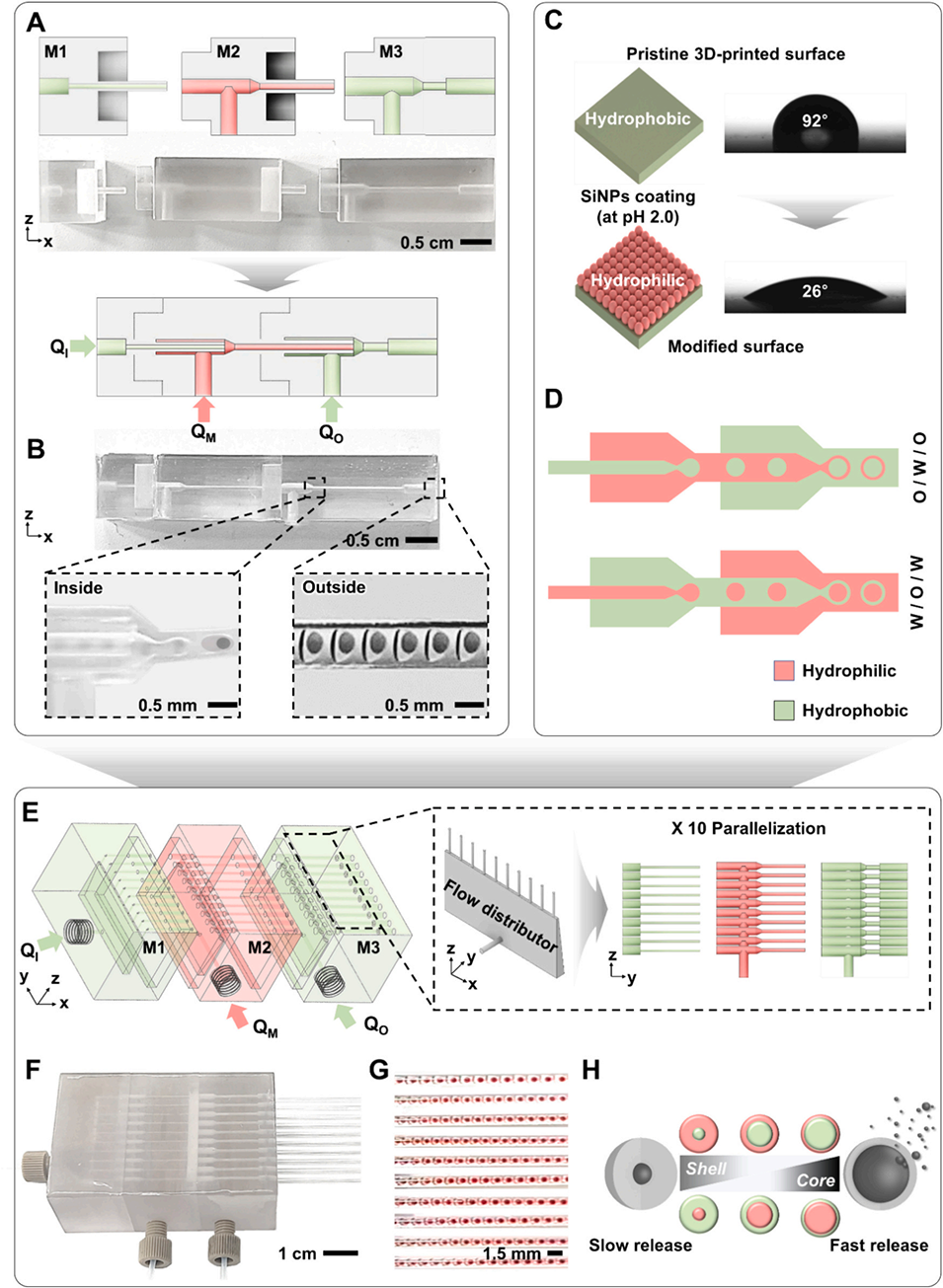
图1. 一种稳定且可规模化生产O/W/O和W/O/W型双乳液的策略
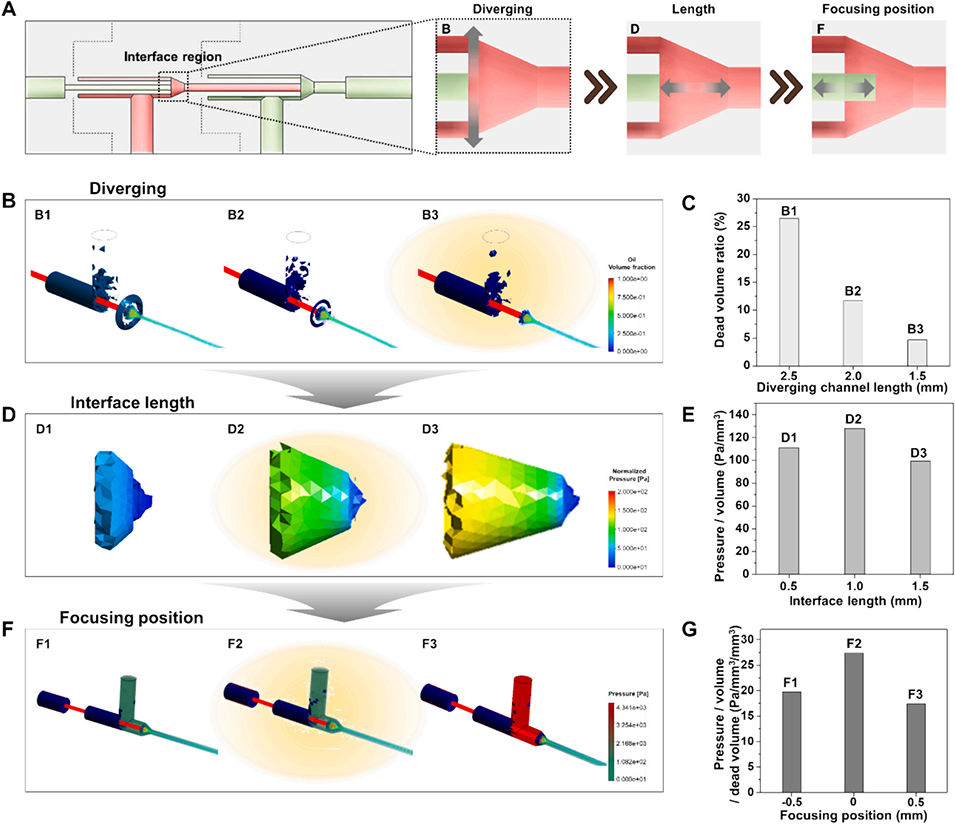
图2. 适用于长期生成宽尺寸范围双乳液的3D-MDG装置设计
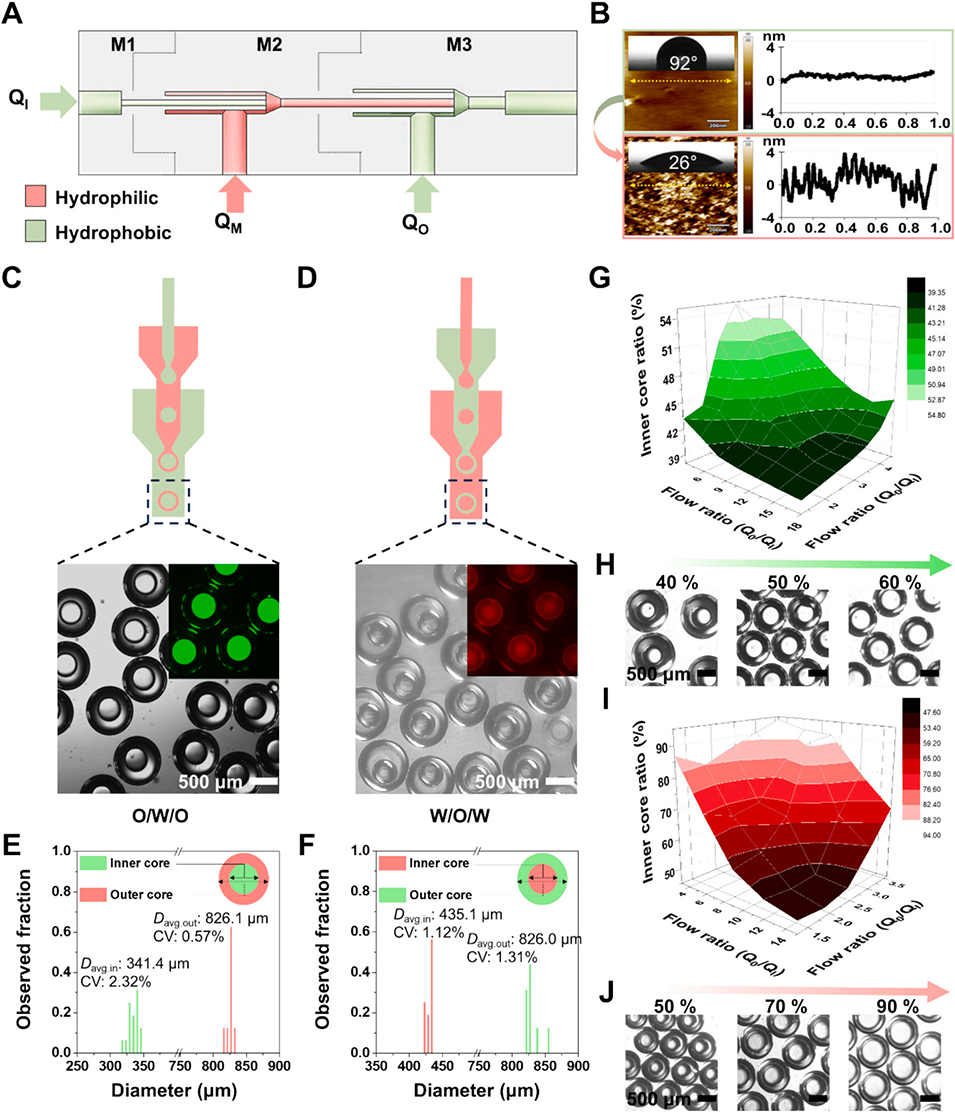
图3. 选择性表面改性3D-MDG中O/W/O和W/O/W型双乳液的稳定生成
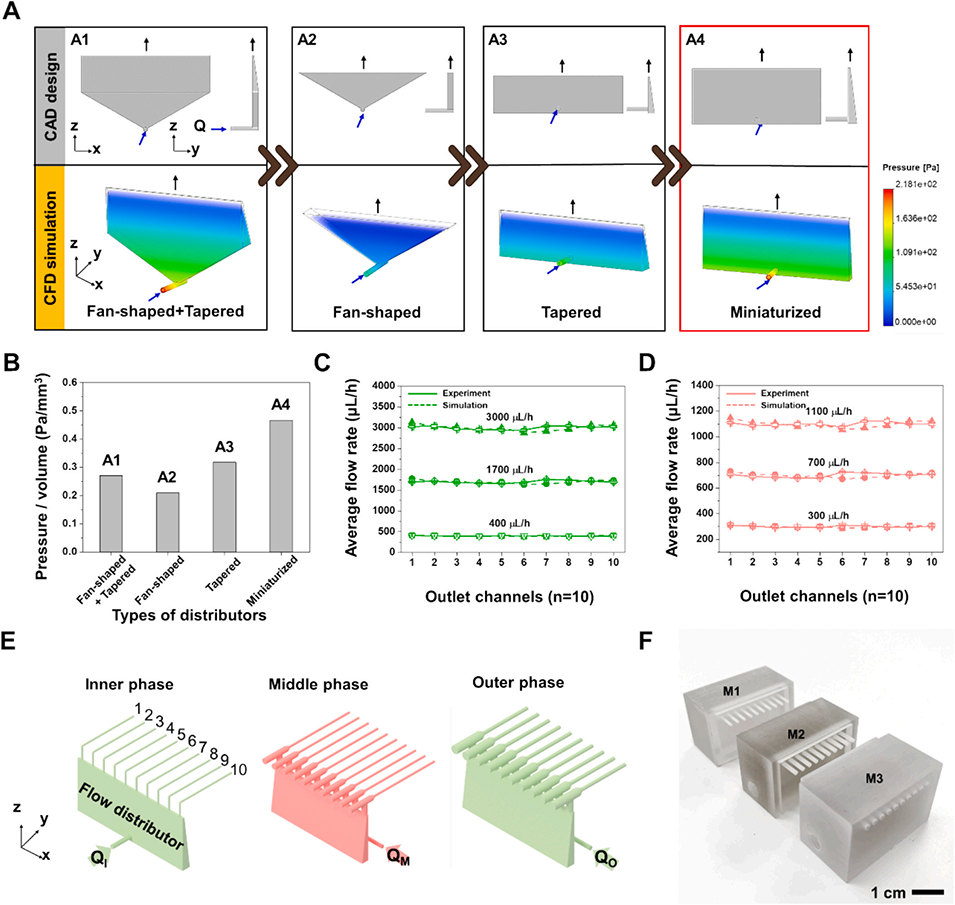
图4. 面向并行化的流量分配器设计与验证
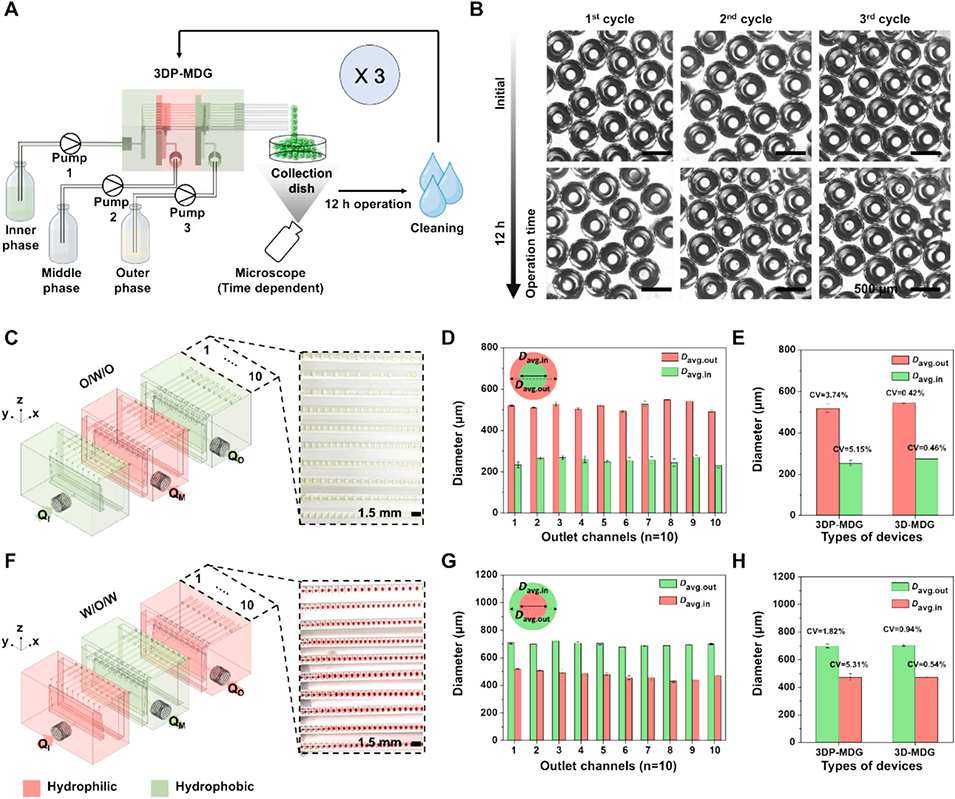
图5. 3DP-MDG双乳液长期生产性能验证
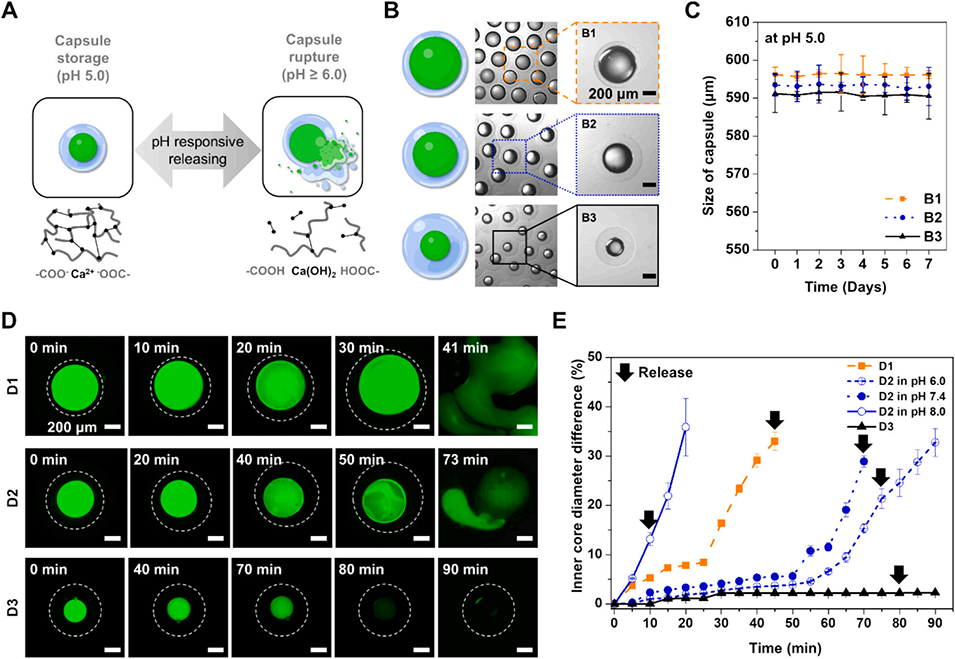
图6. 具有可控内核体积比的海藻酸盐微胶囊的pH响应释放特性
论文链接:https://doi.org/10.1016/j.cej.2025.172213
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














