
导读:
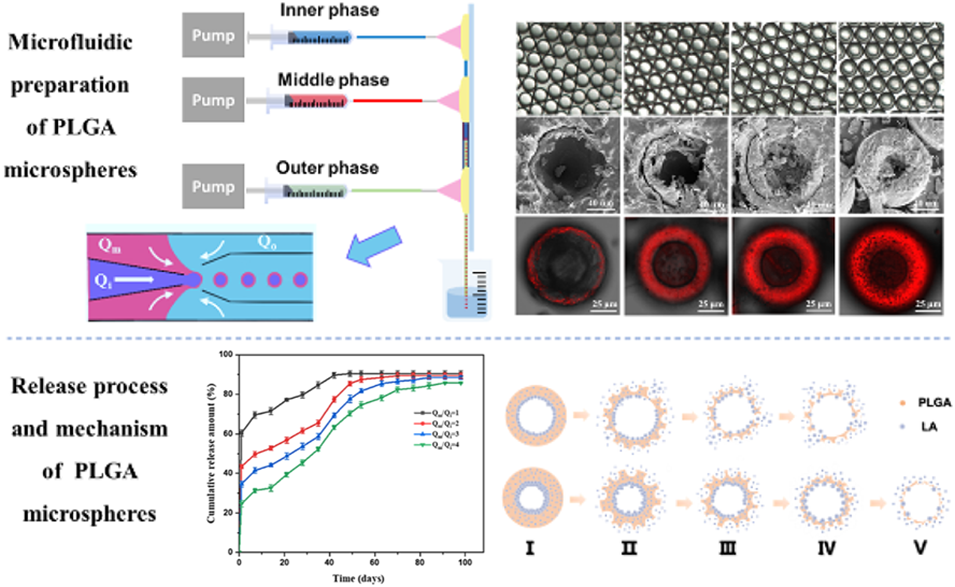
近期,华东理工大学岑莲教授团队联合上海交通大学医学院附属瑞金医院研究人员,利用微流控技术开发了一种具有核壳结构的PLGA微球,旨在实现亲水性肽类药物醋酸亮丙瑞林的长期稳定释放。研究人员通过精确调节微流控装置中各相的流速比,成功实现了对微球外壳厚度的灵活掌控。
实验结果证明,增加壳层厚度能显著提升包封率,并有效抑制药物释放初期的突释现象,使药效持续时间延长至70天。此外,研究还揭示了壳层厚度对微球降解动力学及释放机制的决定性影响,由扩散主导转变为更趋近于零级释放的骨架侵蚀模式。该成果为设计可预测且性质可调的长效给药系统提供了科学依据与技术支撑。相关研究以“Microfluidic Engineering of Core–Shell PLGA Microspheres with Adjustable Shell Thickness for Long-Acting Delivery of Leuprolide Acetate”为题目,发表在期刊《Langmuir》上。
本文要点:
1. 研究背景与目的
挑战:小分子亲水性多肽药物(如LA)具有半衰期短、易降解等局限,传统的PLGA微球制备技术(如乳化溶剂挥发法)常面临粒径分布广、包封率低以及严重的初始突释问题。
目标:利用微流控技术制备单分散性好、核壳结构可控的微球,探索壳层厚度对药物包封和释放行为的影响机制。
2. 技术方法
微流控装置:采用一种三相玻璃毛细管微流控装置(W/O/W双乳液产生器),通过调节流速比(Qm/Qi)来精确控制微球的壳层厚度。
关键参数:将中间相与内相的流速比(Qm/Qi)从1调节至4,从而获得不同壳厚(约5至28 μm)的PLGA微球,其平均粒径保持在约80 μm。
3. 核心发现
性能提升:壳层厚度的增加显著改善了微球性能。包封率(EE)从48%提升至87.66%,而初始突释从59.24%降低至23.52%。
持续释放:随着壳厚增加,药物的持续释放时间从约30天大幅延长至70天。
浓度调节:在适当的壳厚下,调节内相中LA的浓度可以进一步优化载药量和包封稳定性。厚壳微球(Qm/Qi= 4)在不同LA浓度下表现出最稳定的包封效果。
4. 释放与降解机制
释放动力学:动力学拟合显示,薄壳微球的释放主要受扩散控制;而厚壳微球则逐渐向骨架侵蚀控制转变,其释放曲线更趋于零级动力学(更加稳定、连续)。
结构完整性:降解研究表明,薄壳微球在降解早期(如第28天)易发生表面破裂和塌陷,导致药物流失;厚壳微球则能更久地维持稳定的球形结构,从而实现可预测的长效释放。
5. 研究意义
本文阐明了核壳PLGA微球的结构与性能相关性,证明了通过调节壳层厚度可以实现对亲水性多肽递送行为的精准调控,为设计可预测和可定制的长效药物递送系统提供了理论与技术支持。
微流控技术能精准调控壳厚的核心源于微尺度层流控制与流量比定量调控两大技术特性,这是传统方法无法实现的:
1、流体状态优势:传统方法为湍流搅拌,剪切力不均、液滴融合严重,壳厚随机且分布宽;微流控装置内为稳定层流,三相流体(内水相/中间油相/外水相)分层流动不混溶,液滴生成高度均一。
2、参数定量可控:通过固定外相流量与微通道尺寸,仅调整中间相/内相流量比(Qm/Qi),即可线性控制壳层厚度(5~28 μm),无液滴变形、多核等缺陷。
3、结构均一性:微流控制备的微球粒径 CV 值极低,批间重复性好,为壳厚-释药关联研究提供了标准化技术基础。
技术启示
微流控的微尺度精准流体操控,解决了传统递药载体“结构不可控、批间差异大”的技术痛点,是实现结构-性能定量关联研究的核心技术平台,为长效递药系统的精准设计提供了技术可能。
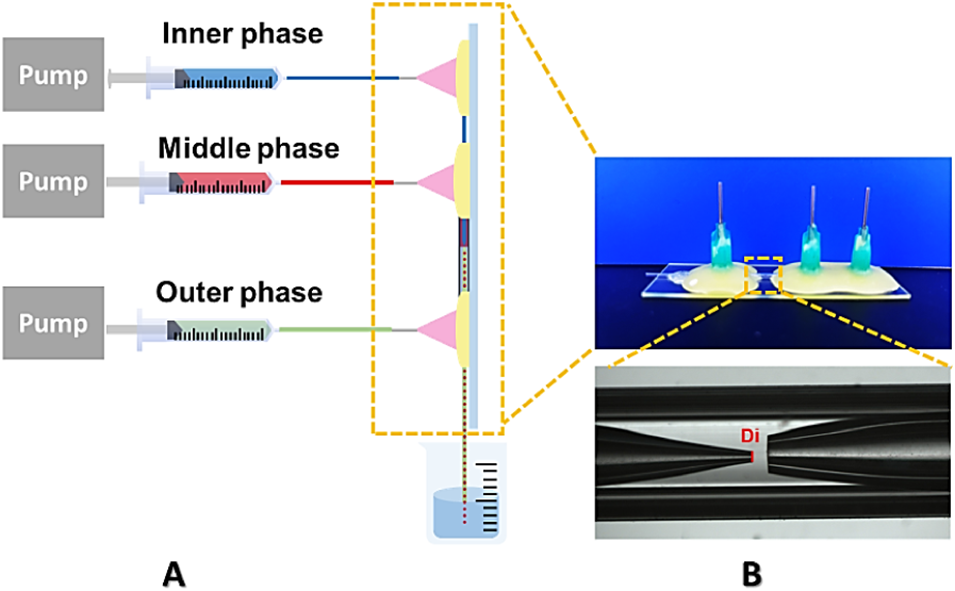
图1. 核壳结构 LA-PLGA 微球的微流控法制备。 (A) 用于生成核壳结构 LA-PLGA 微球的毛细管微流控装置示意图。(B) 毛细管微流控装置的光学照片。Di 表示短毛细管的内径。
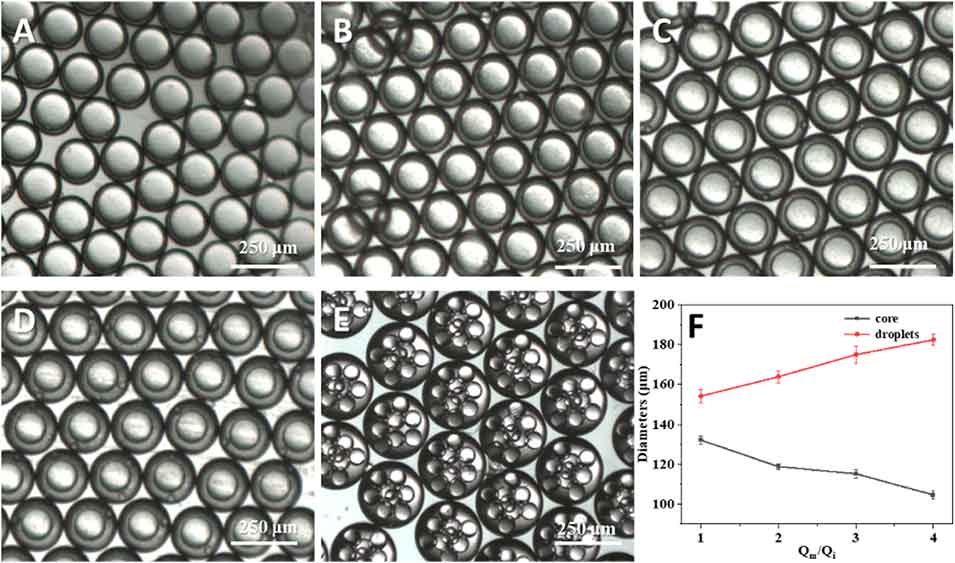
图2. 壳层厚度可调的核壳结构液滴。 (A–E) 在不同中相与内相流速比(Qm/Qi = 1, 2, 3, 4 和 6)下形成的液滴光学显微照片。(F) 核壳液滴内径和外径随 Qm/Qi 变化的曲线。

图3. 在不同中相与内相流速比(Qm/Qi = 1, 2, 3, 4 和 6)下制备的不同壳层厚度核壳结构 LA-PLGA 微球的 SEM 和荧光图像。 (A1–E1) 表面形貌;(A2–E2) 横截面结构;(A3–E3) 微球内尼罗红(Nile Red)荧光分布。
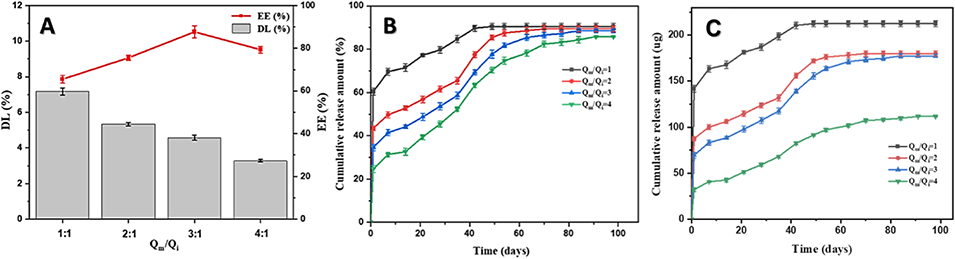
图4. 不同壳层厚度核壳结构 LA-PLGA 微球的载药量和体外释放曲线。 (A) 壳层厚度对 LA-PLGA 微球载药量(DL)和包封率(EE)的影响。(B) 不同壳层厚度 LA-PLGA 微球中 LA 的体外释放累积百分比曲线。(C) 不同壳层厚度 LA-PLGA 微球中 LA 的体外释放量(μg)曲线。

图5. 核壳结构 LA-PLGA 微球在体外降解过程中的形貌变化。 LA-PLGA 微球在 37 °C、PBS(pH 7.4)中孵育 0、1、28、49、70 和 84 天后的代表性 SEM 图像。
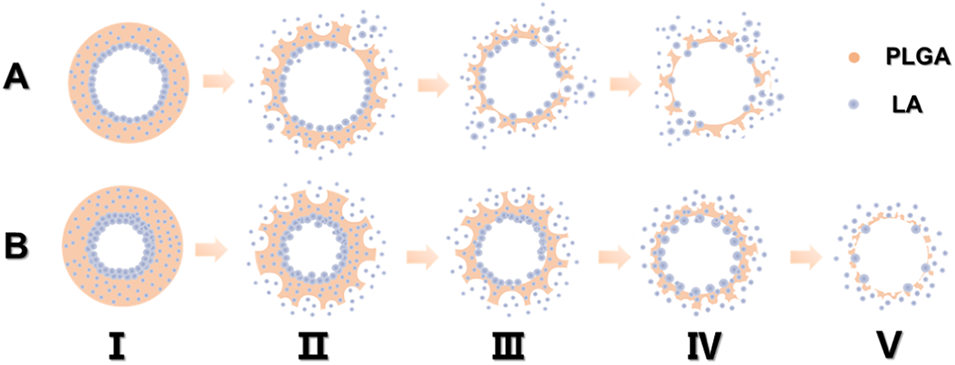
图6. 核壳结构 LA-PLGA 微球 LA 释放现象的示意图。 (A) 薄壳 LA-PLGA 微球的释放过程。(B) 厚壳 LA-PLGA 微球的释放过程。
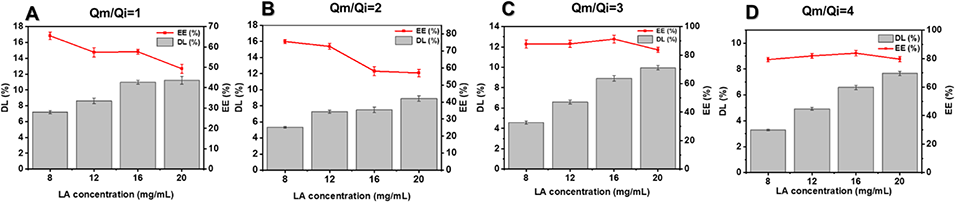
图7. LA 浓度对不同壳厚 LA-PLGA 微球包封率(EE)和载药量(DL)的影响。 LA-PLGA 微球是在不同的中相与内相流速比下获得的:Qm/Qi = 1 (A);Qm/Qi = 2 (B);Qm/Qi = 3 (C);以及 Qm/Qi = 4 (D)。
论文链接:https://doi.org/10.1021/acs.langmuir.6c00309
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
上一篇:双水相微流控技术制备肠溶包衣液芯胶囊,助力益生菌高效包封与靶向递送
下一篇:暂无














