
导读:
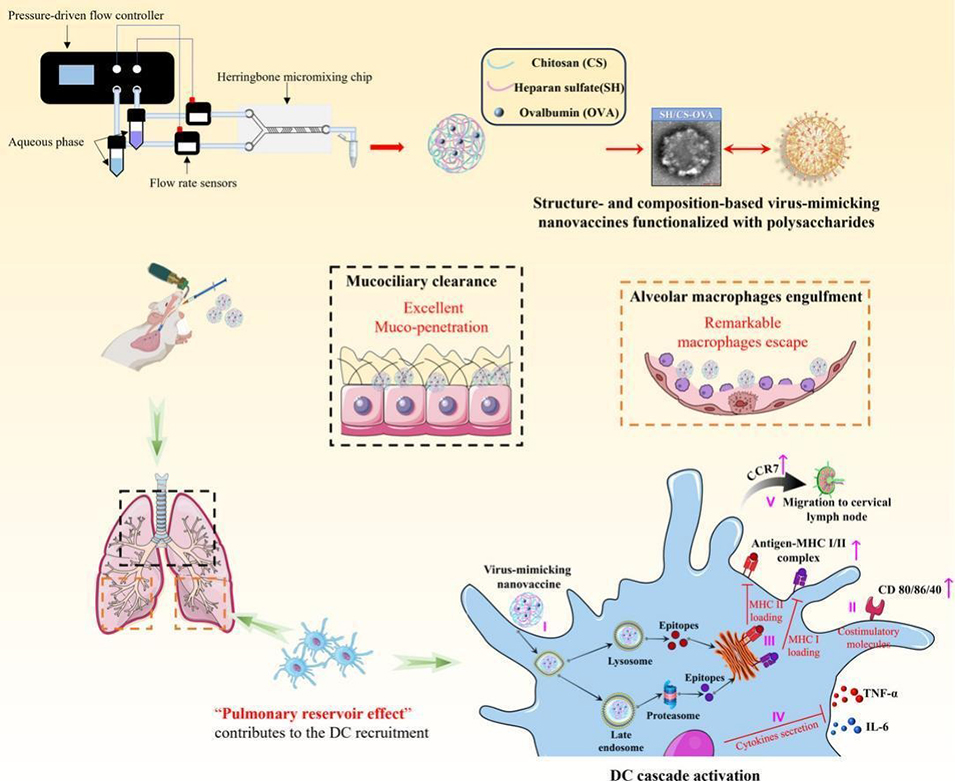
近期,COVID-19变异株与流感日益频发,使得肺部疫苗备受关注。然而,肺部固有的免疫屏障往往会显著削弱纳米疫苗的功效。此外,安全有效的吸入式佐剂之匮乏,也制约了纳米疫苗的进一步发展。近期,沈阳药科大学药学院毛世瑞教授团队采用微流控技术成功构建了一种硫酸乙酰肝素修饰的病毒模拟纳米疫苗。该制剂不仅能高效穿越肺部黏液屏障、规避巨噬细胞吞噬,还可显著增强树突状细胞募集与抗原递呈,从而激发系统性的体液免疫、细胞免疫与黏膜免疫应答。相关研究以“A facile microfluidics based polysaccharide-functionalized virus-mimicking nanovaccine for circumventing pulmonary innate physiological barriers and augmenting immunity”为题,发表在期刊《Carbohydrate Polymers》上。
本文要点:
1、本研究开发了一种基于微流控技术的多糖功能化病毒模拟纳米疫苗(SH/CS-OVA),以克服肺部先天生理屏障并增强免疫应答。
2、该疫苗以壳聚糖-卵清蛋白复合物为核心,表面修饰硫酸乙酰肝素,模拟病毒外部的组成与结构。
3、与未修饰疫苗相比,SH/CS-OVA 在穿透黏液层和逃逸巨噬细胞吞噬方面表现卓越,效率分别提升了3倍和4.8倍,并显著增强了树突状细胞的招募、摄取与成熟。
4、体内实验显示其在肺部滞留时间延长,且能快速引流至淋巴结。
5、经肺内给药后,该疫苗可诱导高水平的特异性血清IgG及其亚型、激发强烈的T细胞免疫及三重免疫应答,并形成有效的T细胞免疫记忆。该研究为吸入式免疫治疗提供了一个安全有效的纳米疫苗平台。
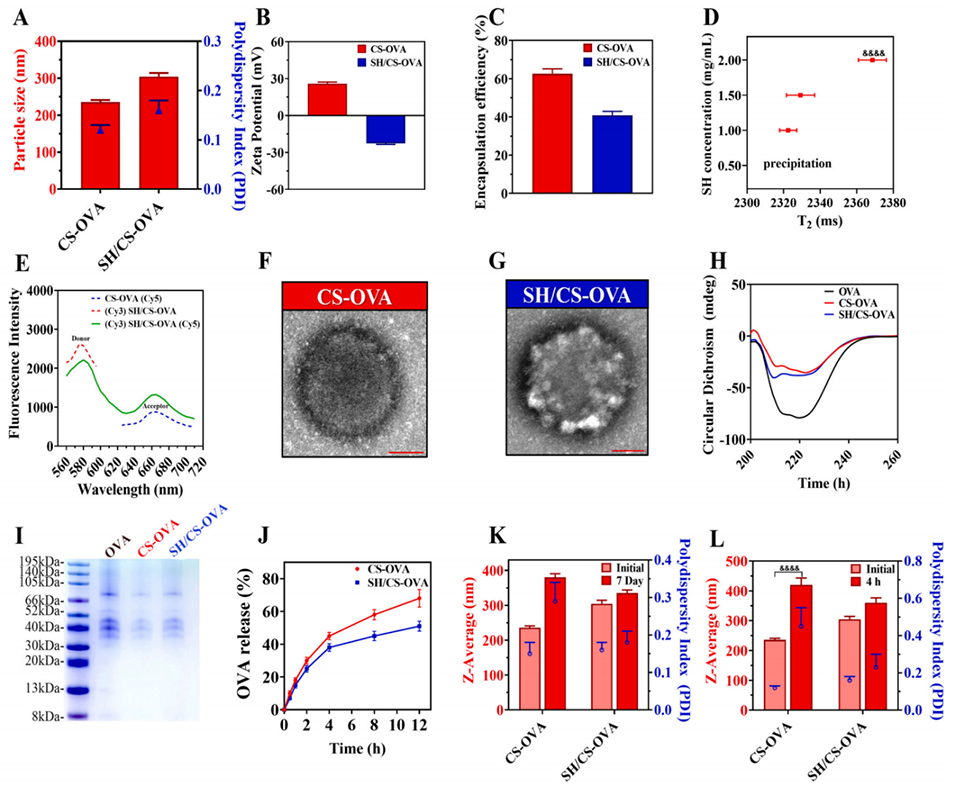
图1. 多糖功能化病毒模拟纳米疫苗的特性
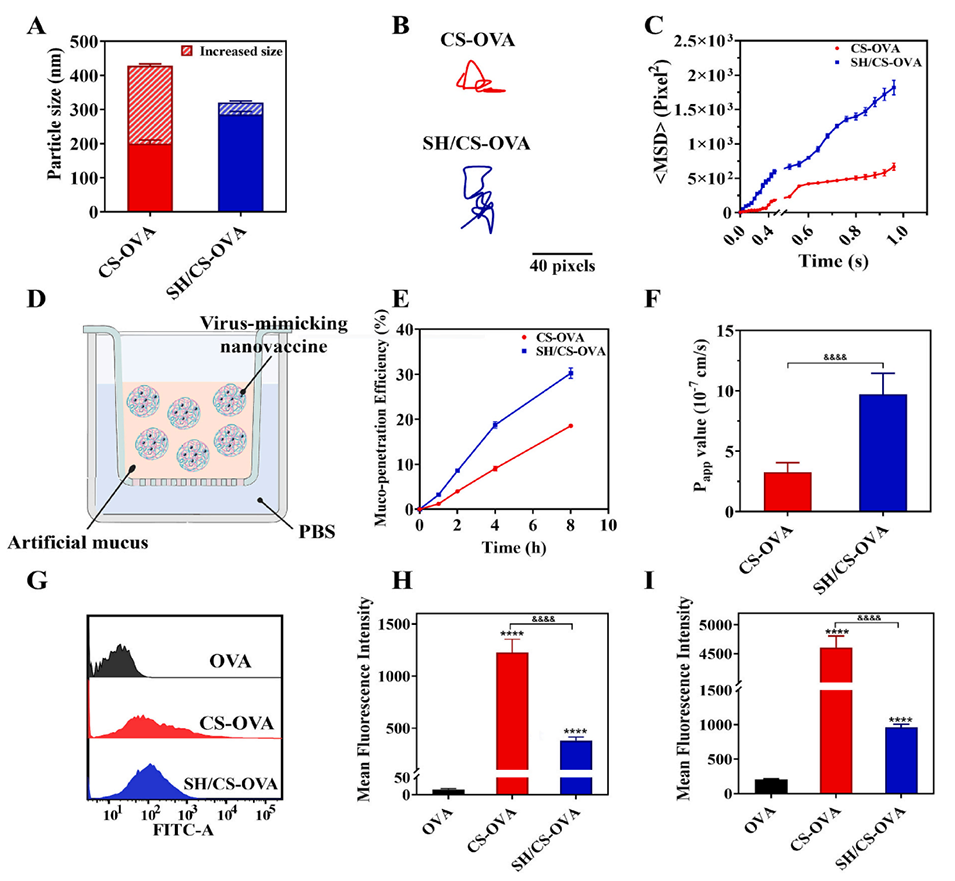
图2. 病毒模拟纳米疫苗突破固有免疫屏障递送至肺部的能力
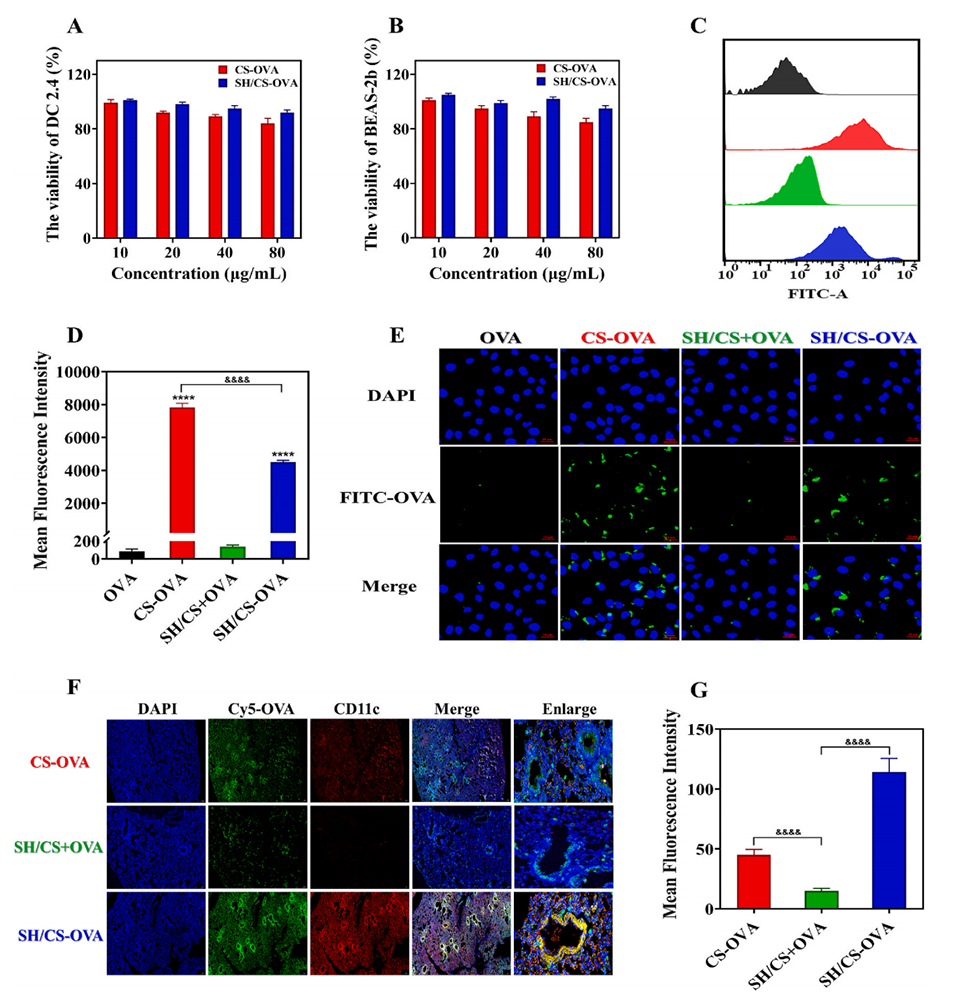
图3. 病毒模拟纳米疫苗的树突状细胞(DC)内化与招募情况
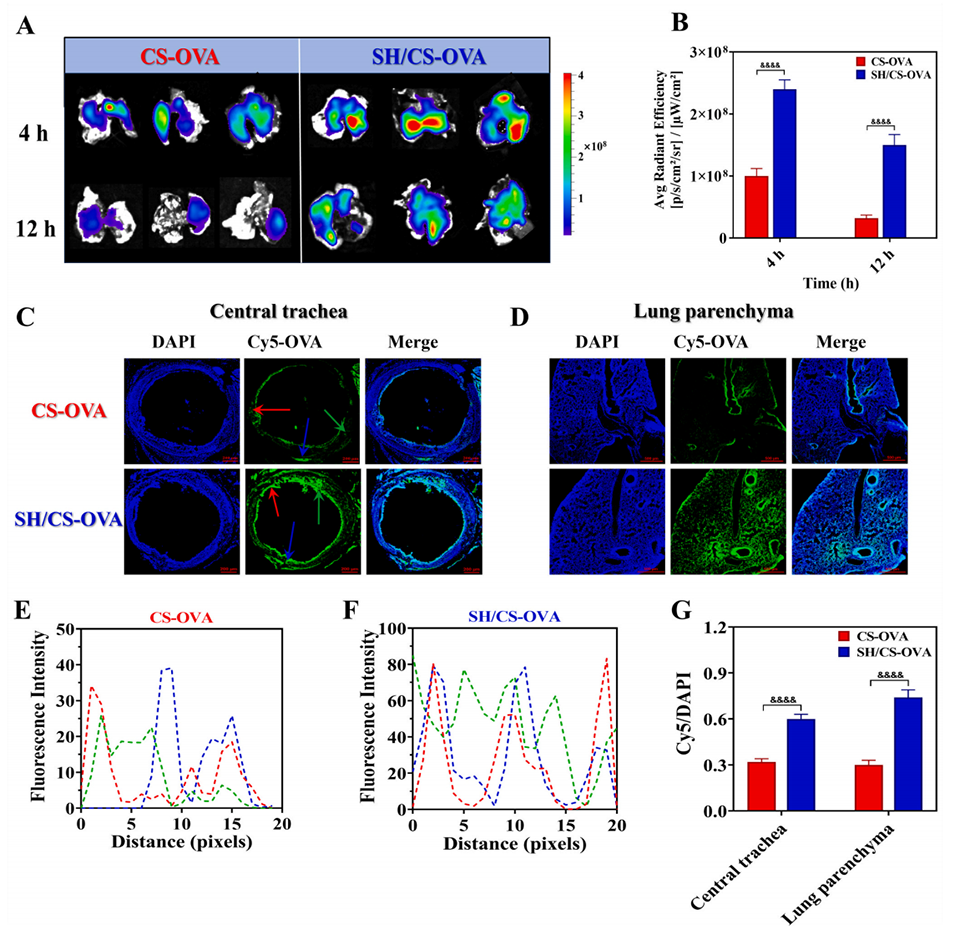
图4. 肺部储库效应的建立及疫苗滞留情况
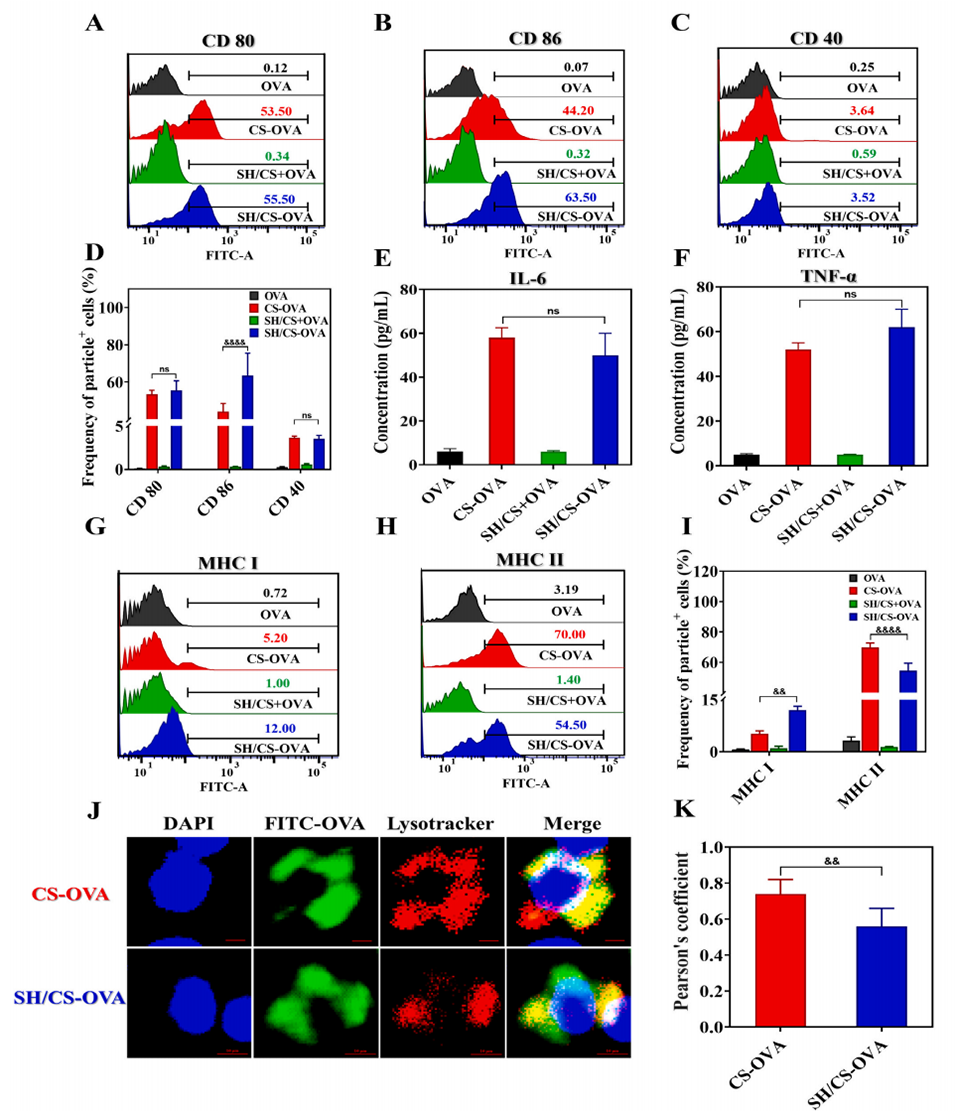
图5. 树突状细胞(DC)受刺激的活化强度
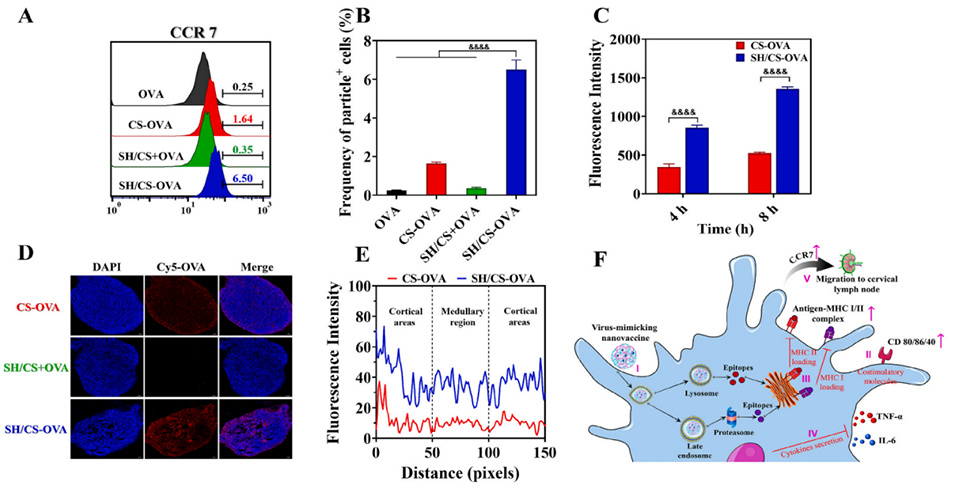
图6. 病毒模拟纳米疫苗的淋巴结转运及级联免疫触发过程
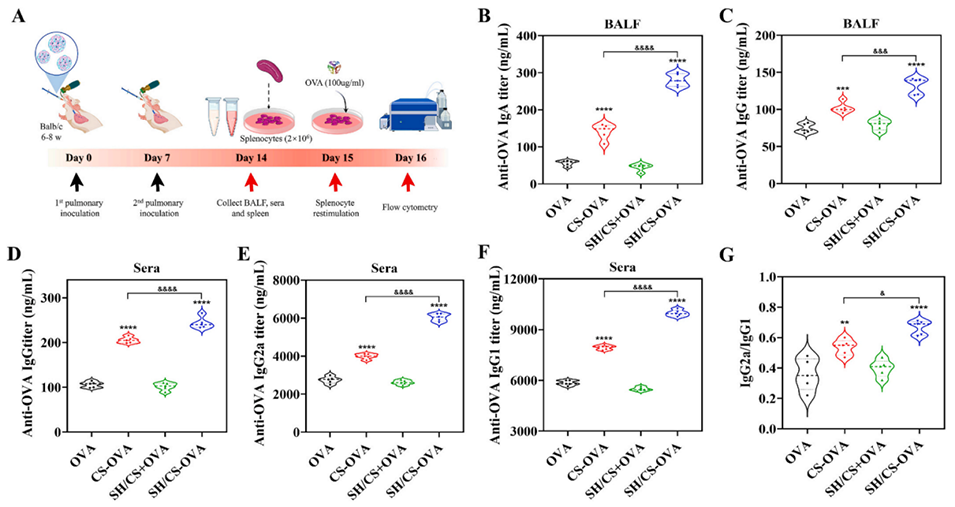
图7. 小鼠经肺部初次与加强免疫后的体内三重免疫应答
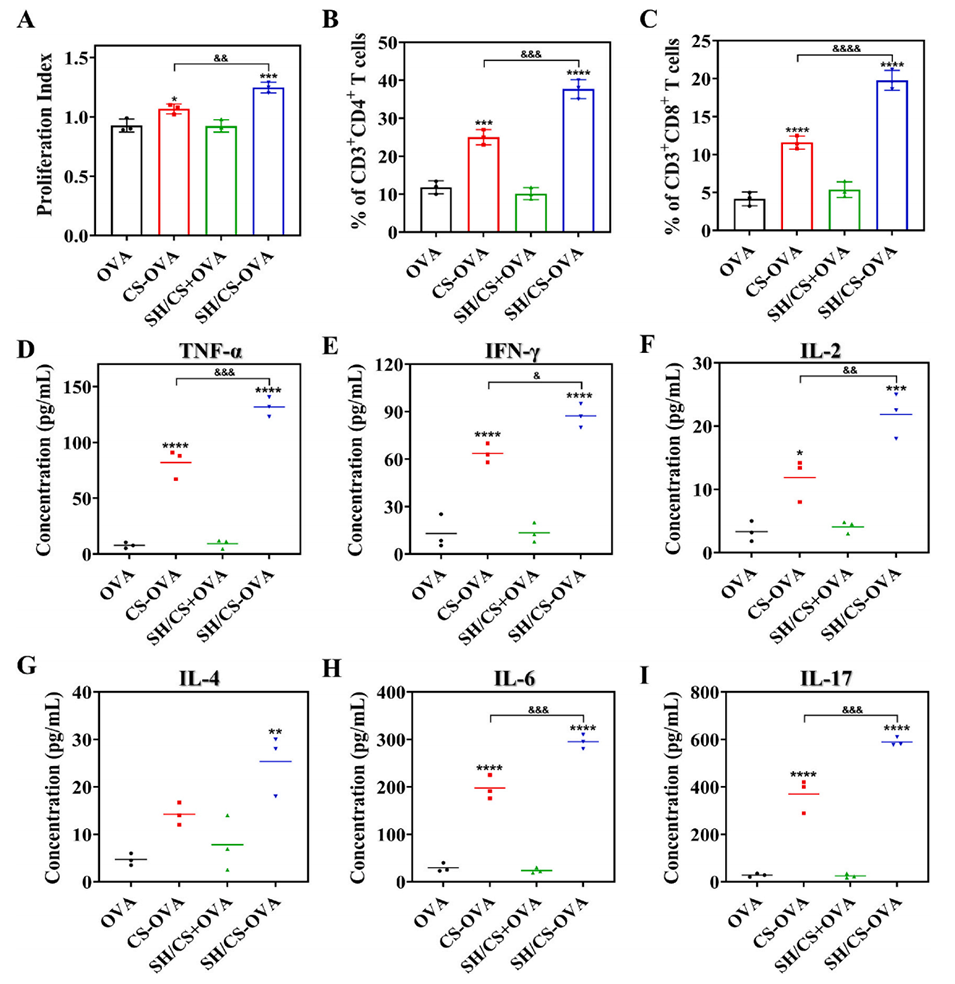
图8. 脾淋巴细胞再刺激后的 T 细胞免疫应答
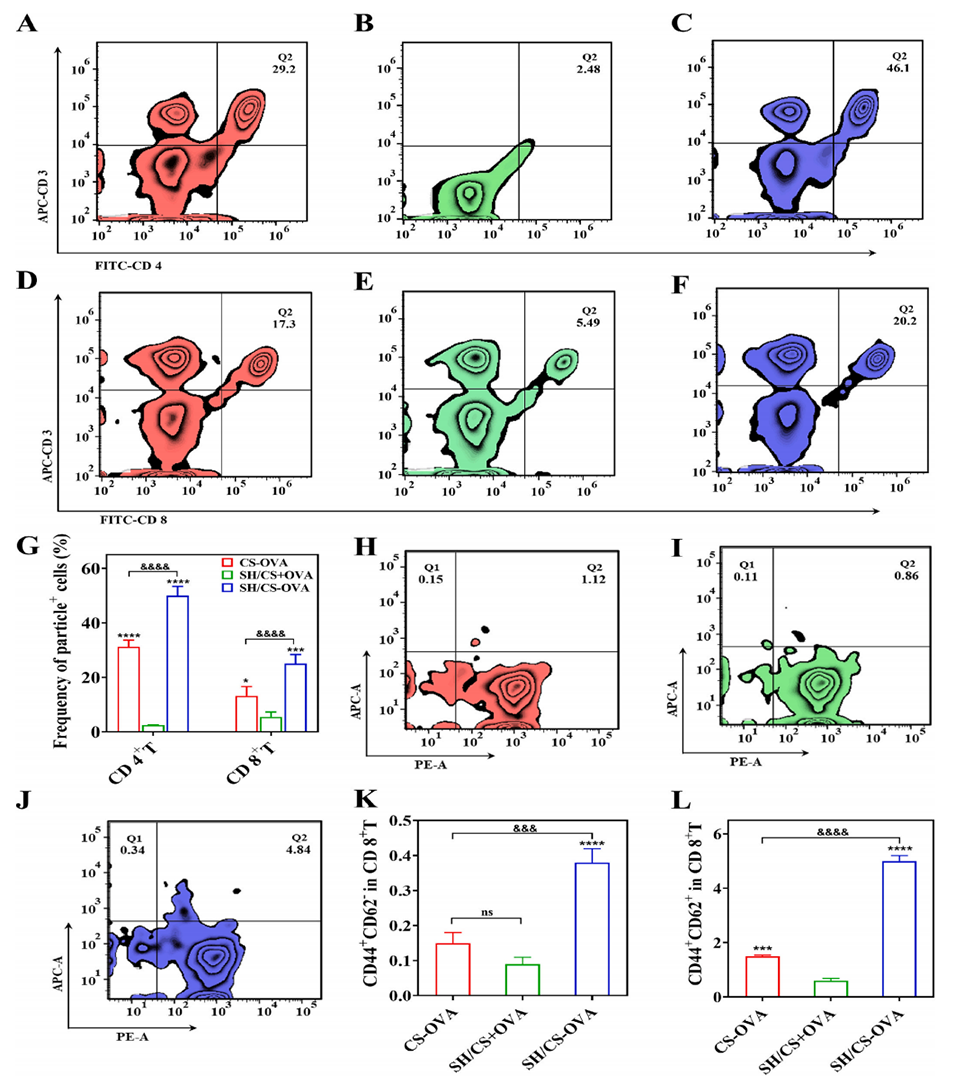
图9. 卵清蛋白(OVA)再刺激后脾淋巴细胞的免疫记忆应答
论文链接:https://doi.org/10.1016/j.carbpol.2025.124503
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














