外泌体作为细胞分泌的脂质纳米颗粒,通过包裹并递送DNA、mRNA、miRNA和蛋白质等多种生物分子,在细胞间通讯中发挥关键作用。基于其能够跨越生物屏障、利用自然通讯机制和最小化免疫原性的特点,外泌体在药物递送系统(DDS)领域展现出巨大潜力。然而,外泌体的异质性为其功能分析及基于外泌体的药物递送系统开发设置了瓶颈。

鉴于此,北海道大学工学部研究团队开发出一种一步法微流控制备技术,成功制备出表面修饰四跨膜蛋白和整合素的外泌体模拟脂质纳米颗粒,证实整合素ITG αVβ5可显著增强RNA体内外递送效率,为解析外泌体蛋白功能及开发靶向药物递送系统提供了新方法。相关研究以“Microfluidic Production of Exosome-Mimicking Lipid Nanoparticles for Enhanced RNA Delivery: Role of Exosomal Proteins”为题目,发表在期刊《ACS Applied Materials & Interfaces》上。
本文要点:
1、本研究开发了一种一步制备外泌体样脂质纳米颗粒(ELNPs)的微流控方法,可精准调控其成分和特性。
2、通过在ELNPs表面修饰特定外泌体蛋白(如四跨膜蛋白CD9、CD63、CD81和整合素ITG αVβ5、ITG α6β4),研究发现ITG αVβ5修饰的ELNPs显著增强了体内外的RNA递送效率。
3、这种微流控制备方法有助于阐明外泌体蛋白功能,推动靶向药物递送系统发展,为外泌体相关研究提供新工具。
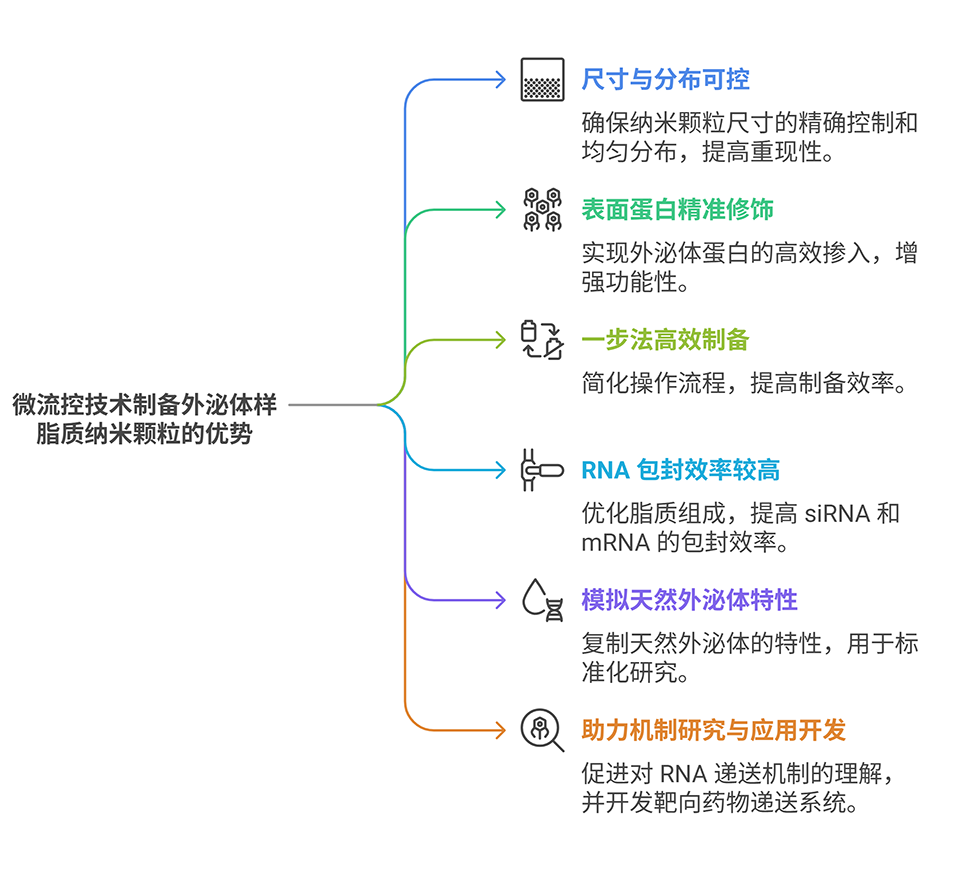
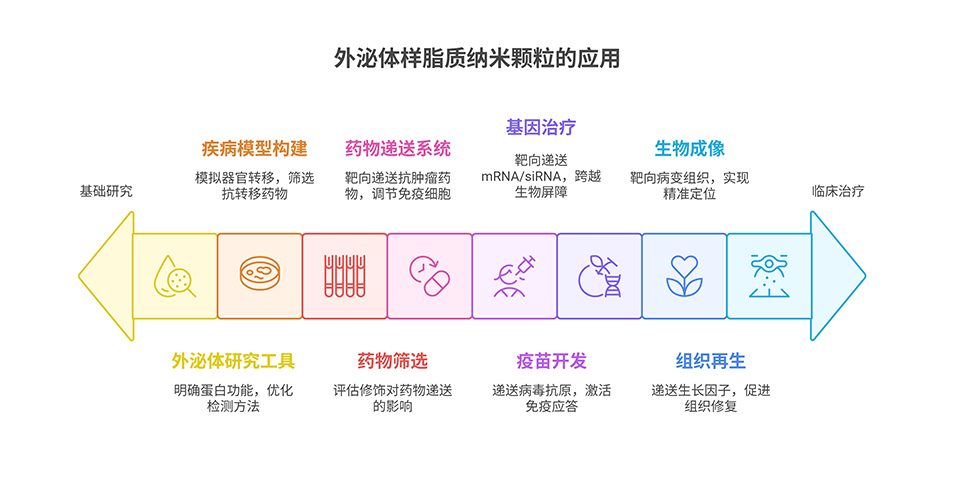
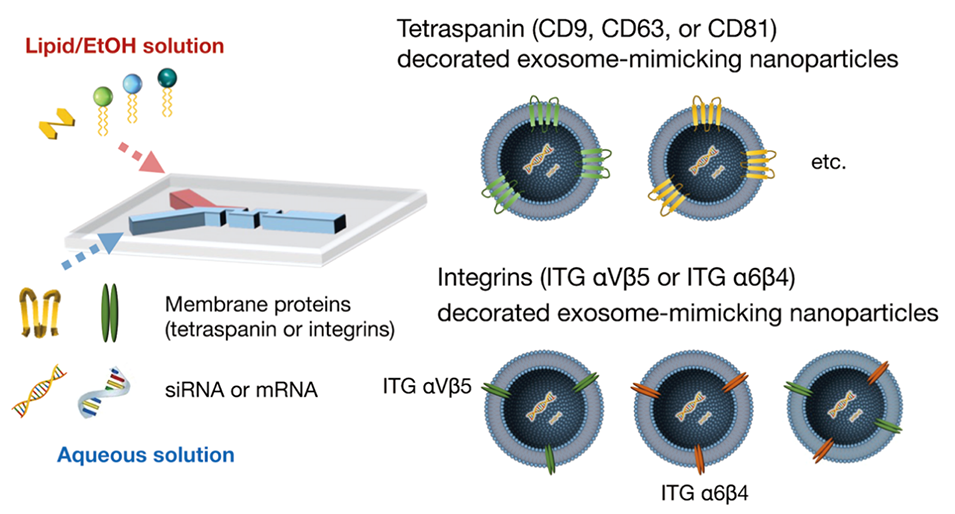
图1.利用微流控装置一步制备外泌体模拟纳米颗粒的概念示意图。在纳米颗粒自组装过程中,外泌体模拟脂质纳米颗粒表面被四跨膜蛋白(CD9、CD63或CD81)或整合素(ITG αVβ5或ITG α6β4)修饰。
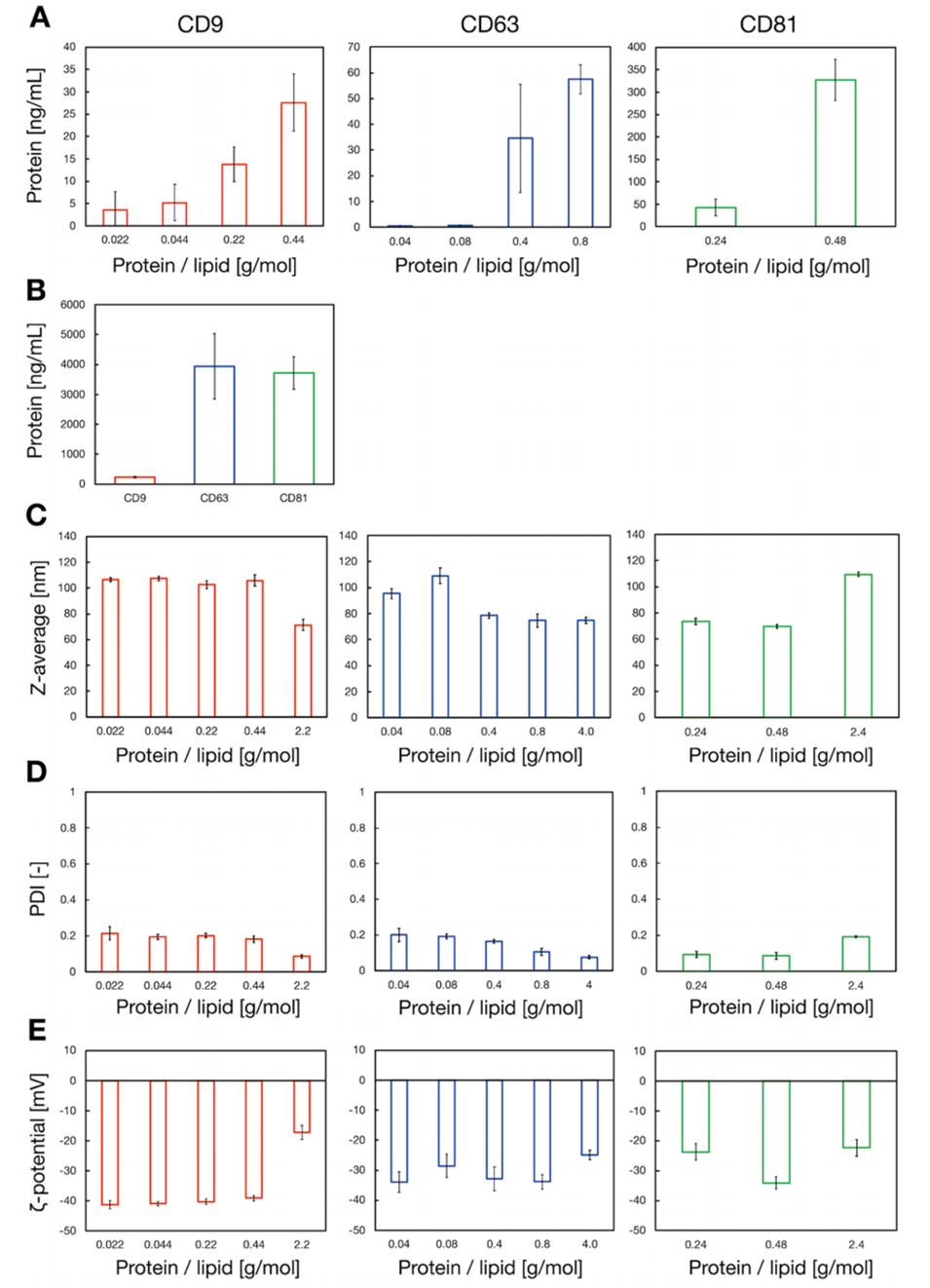
图2.不同蛋白/脂质摩尔比下CD9、CD63或CD81修饰的外泌体模拟纳米颗粒的表征。(A)蛋白/脂质摩尔比与表面蛋白呈现效率的关系;(B)各蛋白在纳米颗粒表面的呈现量(制备CD9、CD63和CD81修饰的外泌体模拟纳米颗粒时,蛋白/脂质摩尔比分别为2.2、4.0和2.4g/mol);(C-E)纳米颗粒的平均粒径(C)、多分散指数(PDI,D)和ζ电位(E)。结果为三次重复测量的平均值±标准差(mean±SD,n=3)。
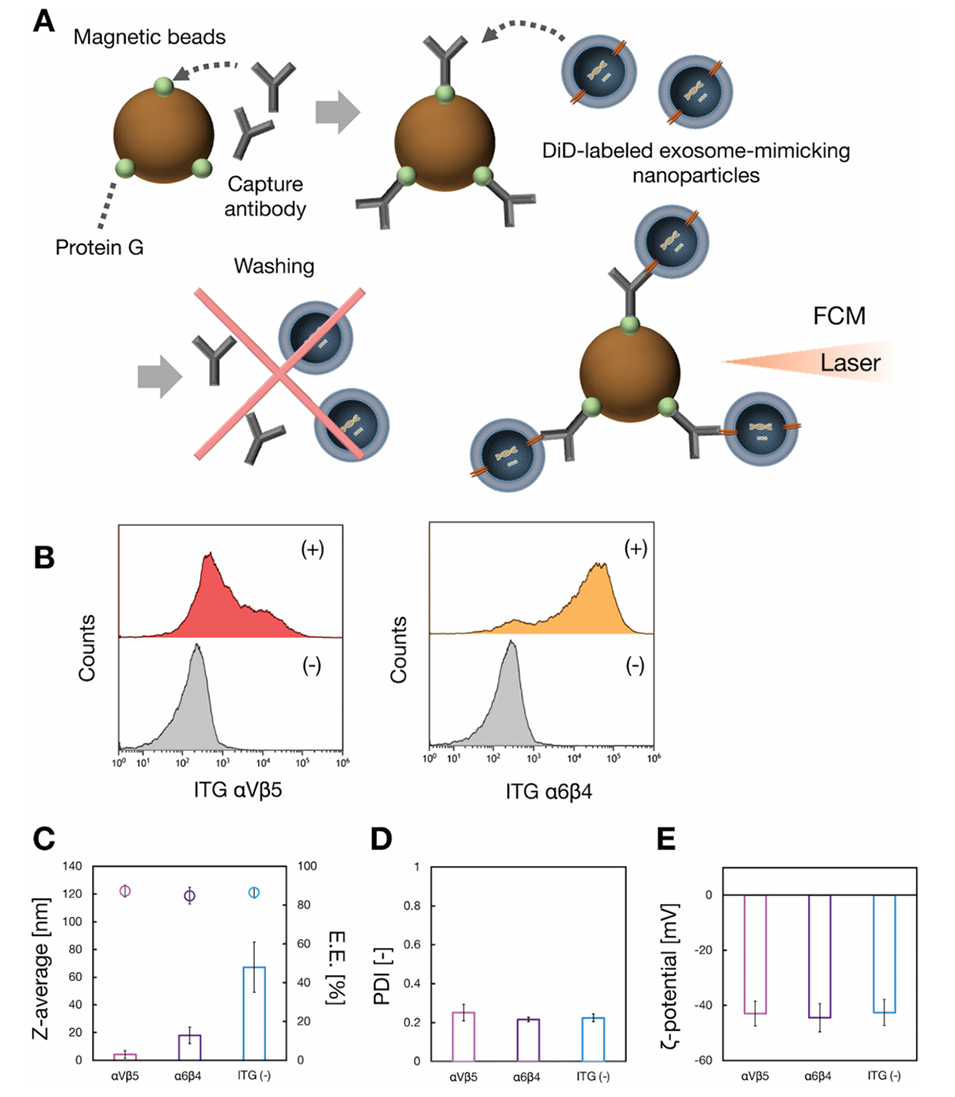
图3.整合素修饰的外泌体模拟纳米颗粒的表征。
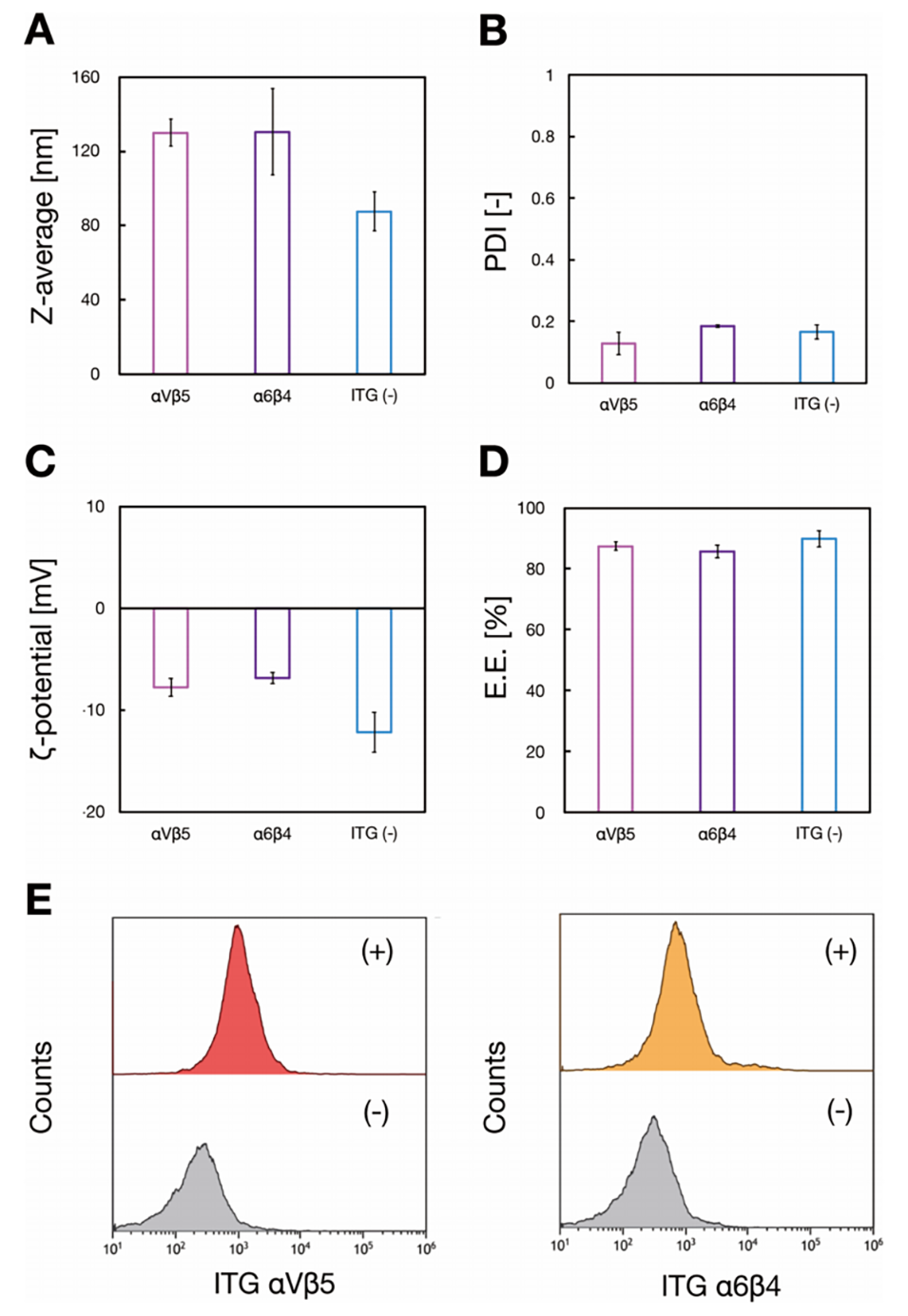
图4.含可电离脂质的siRNA负载整合素修饰外泌体模拟纳米颗粒的表征。
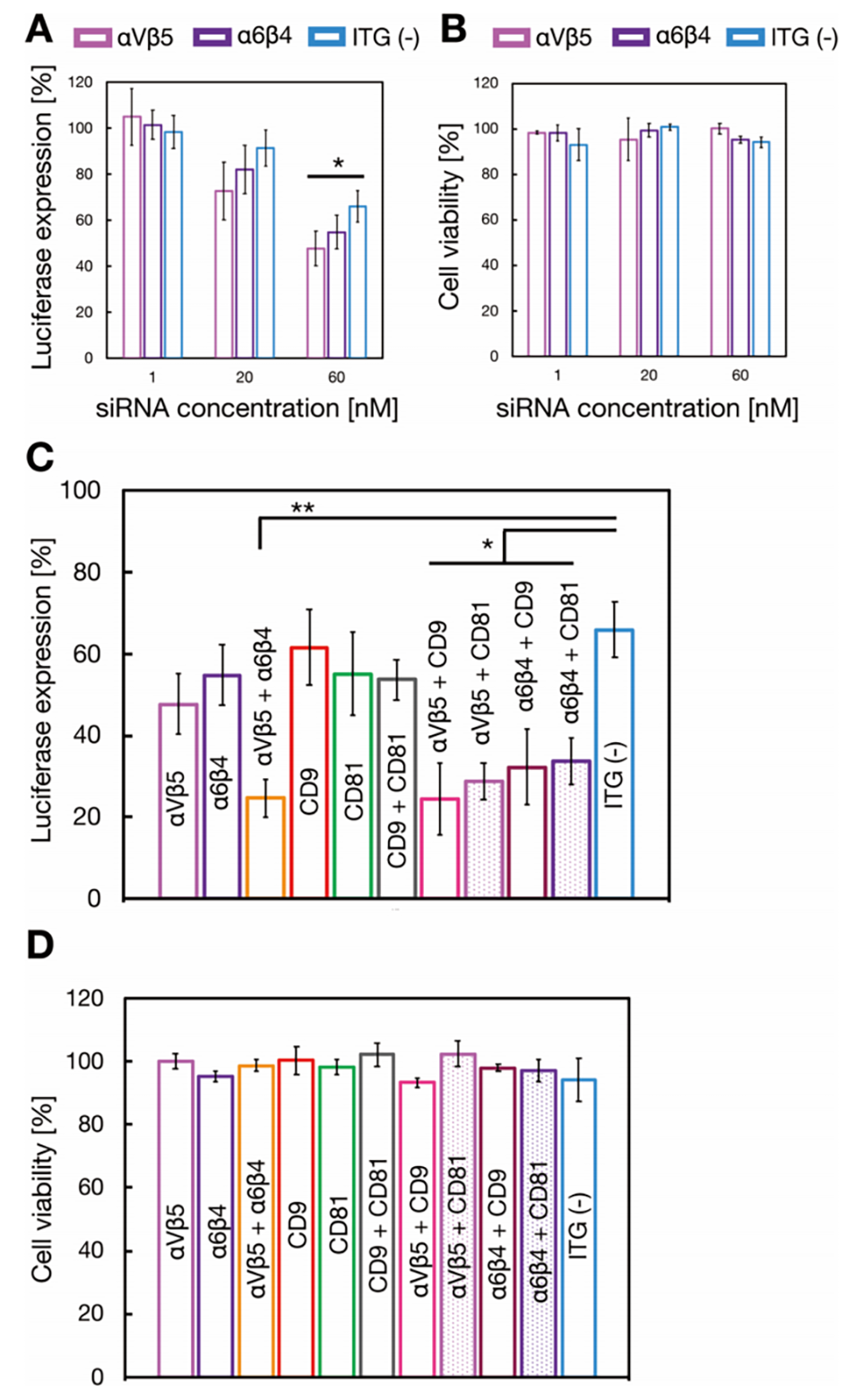
图5.外泌体模拟纳米颗粒的荧光素酶基因敲低效果及细胞活性。(A,B)ITG αVβ5或ITG α6β4修饰的外泌体模拟纳米颗粒与未修饰颗粒在1、20和60nM siRNA剂量下的荧光素酶敲低效率(A)和细胞活性(B);(C,D)双蛋白修饰的外泌体模拟纳米颗粒在60nM siRNA剂量下的荧光素酶敲低效率(C)和细胞活性(D)。CD9和CD81的蛋白/脂质重量摩尔比分别设定为0.44和0.48g/mol。结果为三次重复测量的平均值±标准差(mean±SD,n=3)。*p<0.05,**p<0.01。
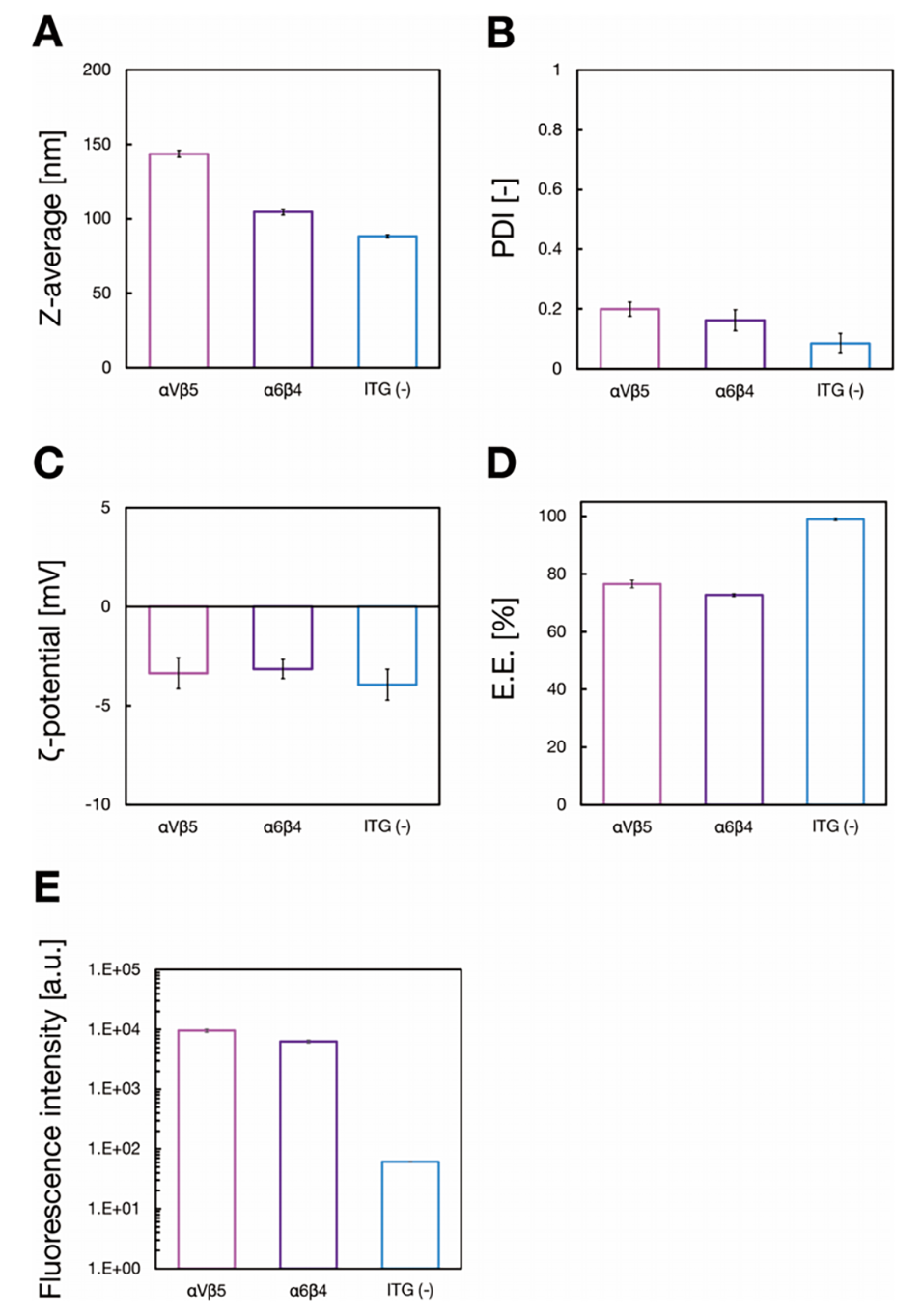
图6.含可电离脂质的mRNA负载整合素修饰外泌体模拟纳米颗粒的表征。(A-D)ITG αVβ5或ITG α6β4修饰的外泌体模拟纳米颗粒与未修饰颗粒的平均粒径(A)、PDI(B)、ζ电位(C)和mRNA包封效率(E.E.,D);(E)利用抗体偶联磁珠和流式细胞术(FCM)对纳米颗粒表面ITG呈现量的定量分析(激发和发射波长分别为638和660nm)。ITG αVβ5和ITG α6β4的蛋白/脂质重量摩尔比分别设定为4.0和3.6g/mol。结果为三次重复测量的平均值±标准差(mean±SD,n=3)。
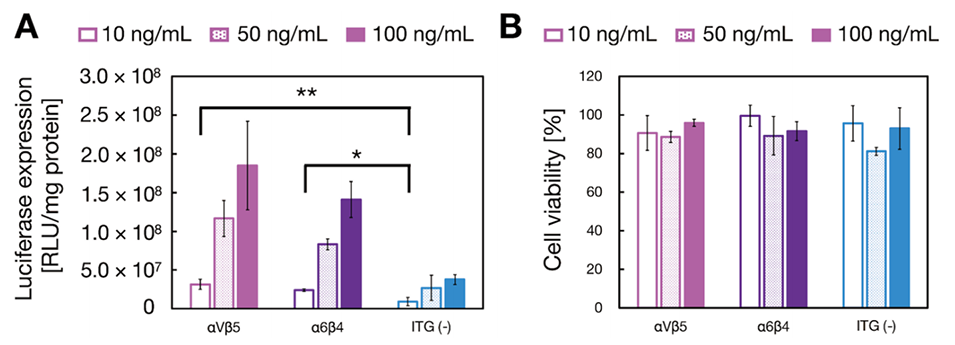
图7.mRNA负载ITG修饰外泌体模拟纳米颗粒的荧光素酶表达效果及细胞活性。(A)10、50和100ng/mL mRNA剂量下的荧光素酶表达效率;(B)细胞活性。结果为三次重复测量的平均值±标准差(mean±SD,n=3)。*p<0.05,**p<0.01,N.S.:无显著性差异。
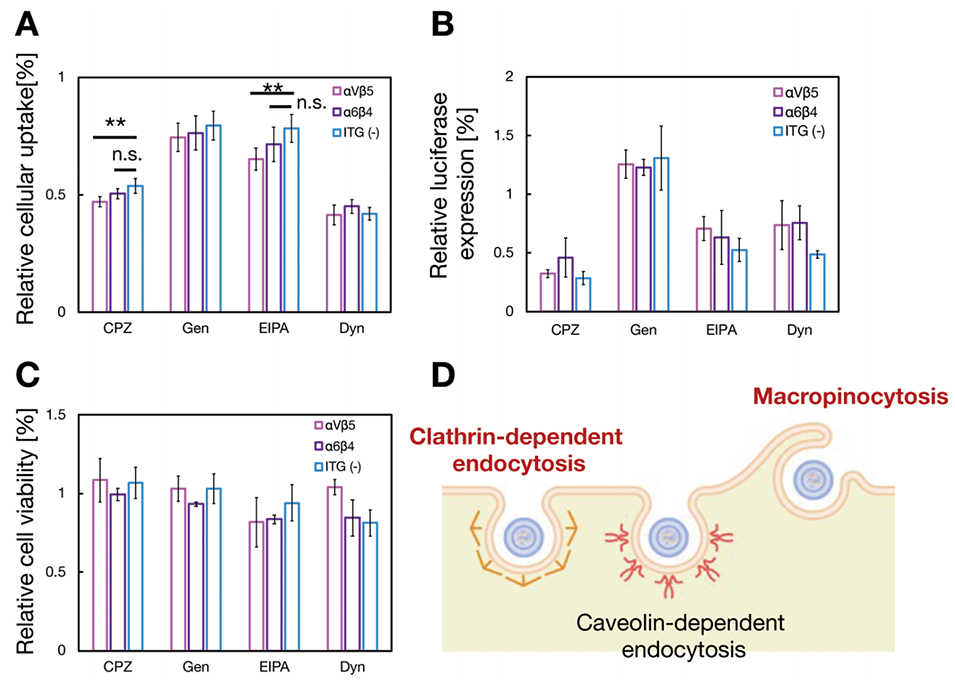
图8.mRNA负载ITG修饰外泌体样纳米颗粒的内吞抑制实验。(A-C)相对细胞摄取率(A)、荧光素酶表达效率(B)和细胞活性(C);(D)ITG修饰外泌体的内吞途径示意图。氯丙嗪(CPZ)、染料木黄酮(Gen)、5-(N-乙基-N-异丙基)阿米洛利(EIPA)和发动蛋白抑制剂(Dyn)分别作为网格蛋白介导内吞、小窝蛋白介导内吞、巨胞饮作用和动力蛋白依赖性内吞的抑制剂。mRNA剂量为100ng/mL,各相对值均以未加内吞抑制剂的结果为基准进行标准化。结果为三次重复测量的平均值±标准差(mean±SD,n=3)。**p<0.01,N.S.:无显著性差异。
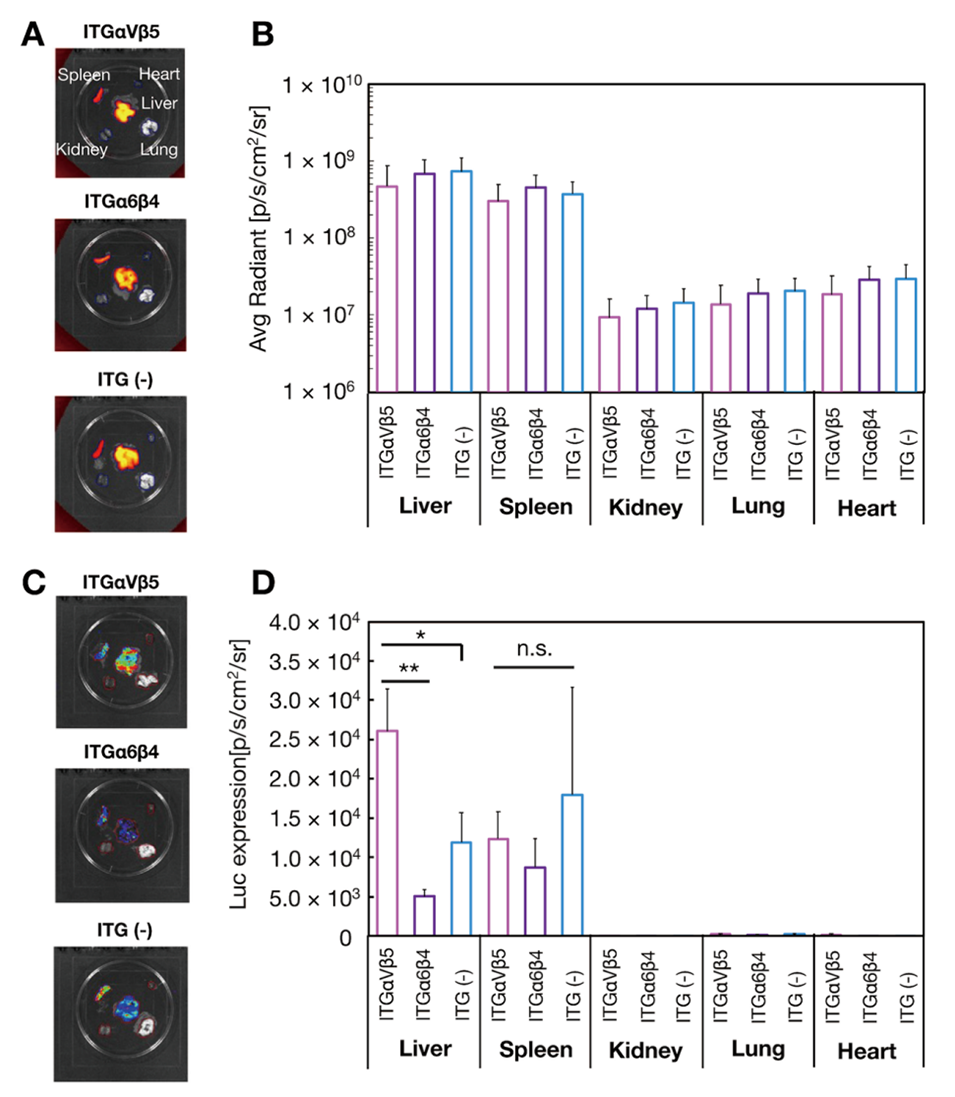
图9.体内生物分布与荧光素酶表达。(A)DiR标记的ITG αVβ5或ITG α6β4修饰外泌体及未修饰纳米颗粒的生物分布;(B)生物分布定量分析(尾静脉注射3小时后进行离体成像);(C)ITG αVβ5或ITG α6β4修饰外泌体及未修饰纳米颗粒的荧光素酶表达;(D)荧光素酶表达定量分析(小鼠尾静脉注射200μL mRNA负载外泌体样纳米颗粒或mRNA负载脂质纳米颗粒(0.05mg mRNA/kg),6小时后进行离体成像)。结果为三次重复测量的平均值±标准差(mean±SD,n=3)。*p<0.05,**p<0.01,N.S.:无显著性差异。
论文链接:https://doi.org/10.1021/acsami.5c06927














