
导读:
机械压力感知在生物过程中扮演着至关重要的角色,然而由于检测技术的匮乏以及传感器难以有效接近组织,相关感知工作面临极大挑战。近期,中南大学生命科学学院赵岳涛副教授团队开发出一种基于纳米光机械转换器的等离子体微传感器,通过将金纳米颗粒高密度封装于可压变形的海藻酸盐水凝胶微球中,实现了从溶液到生物组织的压力传感,为活体组织压力监测提供了新平台。相关研究以“Gold Nanoparticles Encapsulated in Pressure-Deformable Alginate Hydrogel Microspheres as Sensors for Pressure Sensing”为题,发表在期刊《ACS Applied Nano Materials》上。
本文要点:
1、本文提出一种基于纳米光机械转换器的等离子体微传感器,其通过将金纳米颗粒密集封装在可压变形的海藻酸盐水凝胶微球中构建而成。
2、环境压力压缩会使微凝胶尺寸收缩,减小金纳米颗粒间距并增强等离子体耦合,进而导致光吸收、散射和光声信号等光学信号发生变化。
3、实验表明,该微传感器在溶液水平下压力从0升至14kPa时吸收峰红移10nm,灵敏度达0.7nm/kPa且光声信号随压力增强。
4、在单颗粒水平下,微球在不同浓度P8K溶液中随压力变化尺寸缩小、光散射强度增加且颜色改变,响应具有可逆性和良好重现性。
5、在组织水平应用中,该传感器通过光声成像成功区分肾脏、心脏和肿瘤组织的压力差异,其光声信号与组织硬度一致。
6、此等离子体微传感器为压力传感提供了有前景的平台,有望应用于生物压力检测及疾病诊断等领域。
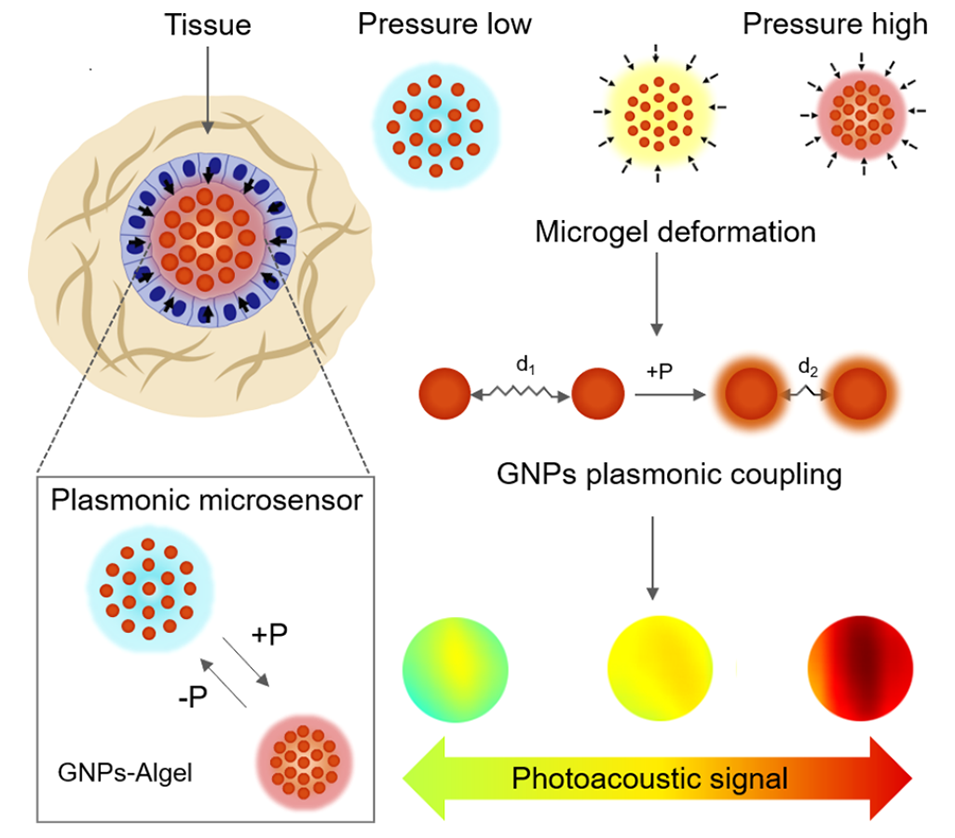
图1.等离子体微传感器用于压力传感的示意图及其相应机理。
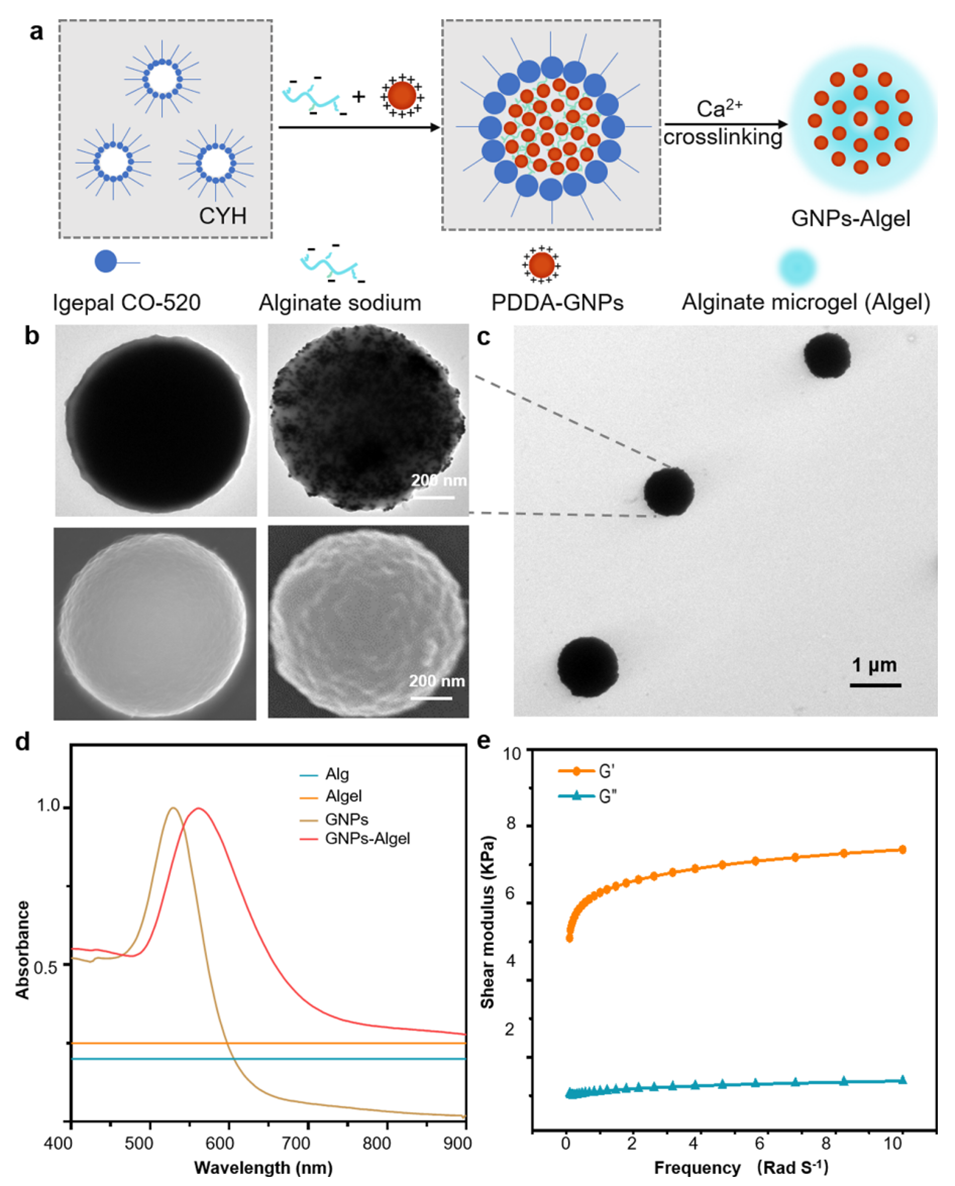
图2.等离子体微传感器的构建与表征。(a) GNPs-Algel的制备示意图。(b)海藻酸盐水凝胶(左)和GNPs-Algel(右)的透射电镜(上)和扫描电镜(下)图像。(c)多个GNPs-Algel微粒的透射电镜图像。(d) GNPs-Algel的紫外-可见-近红外光谱。(e)采用剪切流变学测得的GNPs-Algel的流变学特性。
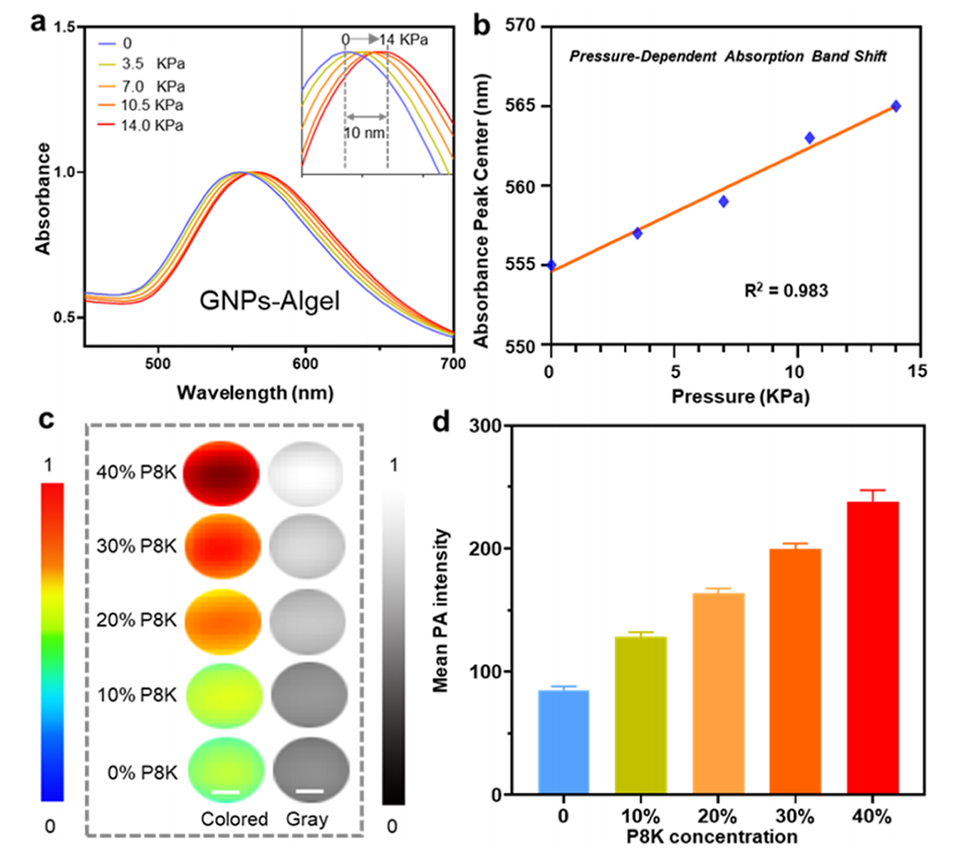
图3. GNPs-Algel在溶液水平的压力传感。(a) GNPs-Algel在不同压力下的吸收光谱。(b) GNPs-Algel的吸光度峰值质心与压力的相关性。(c)彩色和灰度光声信号。(d)计算得到的GNPs-Algel在不同浓度P8K溶液中的平均光声强度。比例尺:0.1mm。
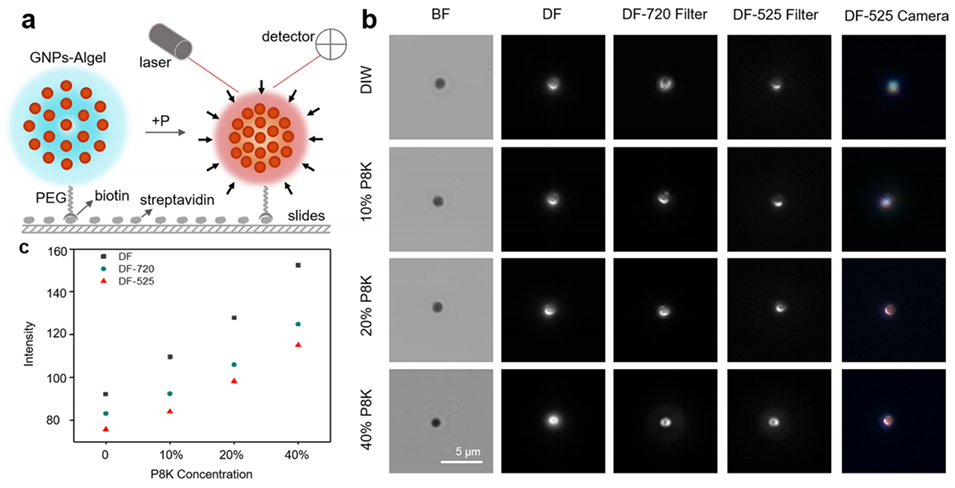
图4. GNPs-Algel在单颗粒水平的压力传感。(a)将GNPs-Algel固定在载玻片表面以观察单颗粒在压力变化下的形变和光学信号的示意图。(b)采用暗场散射显微镜观察单个颗粒在不同浓度P8K溶液中的代表性图像,分别为明场(BF)、暗场(DF)以及配备720nm和525nm滤光片的暗场(DF-720滤光片和DF-525滤光片)。最右侧图(DF-525相机)为在DF-525滤光片下通过CCD相机拍摄的微传感器图片。比例尺:5μm。(c)由图(b)计算得到的微传感器在不同P8K溶液中的散射光强度。
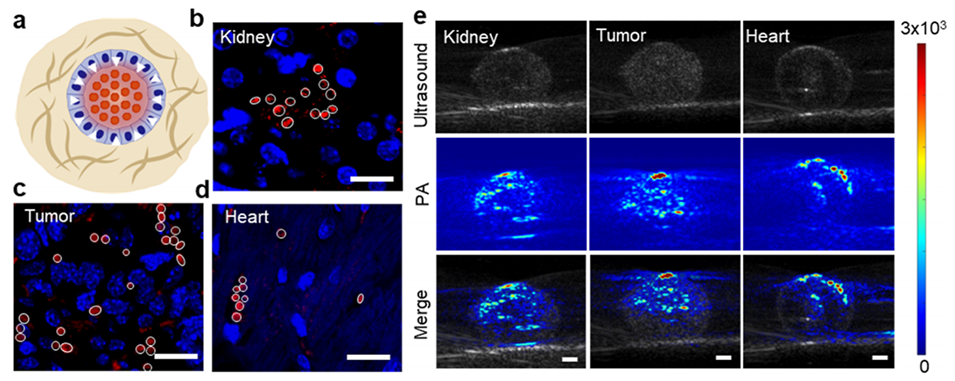
图5. GNPs-Algel在组织水平的生物压力传感。(a)微传感器用于组织中生物压力传感的示意图。(b)肾脏、(c)肿瘤和(d)心脏注射Cy5标记的海藻酸盐水凝胶后的DAPI(4',6-二脒基-2-苯基吲哚)染色图像。比例尺:5μm。(e)含有GNPs-Algel微传感器的不同离体组织的光声成像。比例尺:0.2mm。
论文链接:https://doi.org/10.1021/acsanm.5c01819














