
导读:
双乳液液滴载体的灵活操控在细胞培养、货物递送等诸多应用中意义重大。然而,现有技术受限于对专用平台和特殊功能材料的依赖,且功能单一,实用性受限。近期,东北林业大学机电工程学院解志杰教授、张凯亮副教授团队提出了一种基于可控交流电场的创新方法,实现了双乳液液滴载体的运输、旋转及内核释放等多功能操控,其载体外壳采用常见且无害的材料,可通过调节电信号参数灵活调控操控效果。相关研究以“Electrically-Controlled Multifunctional Double-Emulsion Droplet Carrier Manipulation”为题目,发表在期刊《Advanced Functional Materials》上。
本文要点:
1、本文介绍一种创新方法,可对双乳液液滴载体进行运输、旋转和内核释放等多功能操控。
2、功能样本可轻松封装于液滴内核,载体外壳由常用且无害的聚二甲基硅氧烷(PDMS)与硅油混合物构成。
3、在设计的微器件中,液滴先通过行波介电泳效应从通道入口运输至目标区域,再在旋转电场下旋转以测量其电特性,最后在足够的界面电场麦克斯韦应力作用下,外壳变薄破裂,释放纳米颗粒和抗癌药物。
4、通过改变电信号的电压、频率和相位变化方向,可灵活调节液滴操控,该方法在需样本加载、递送和释放的应用中颇具前景。
微流控器件在液滴载体操控中起到核心支撑与精准调控的作用,具体体现在以下方面:
1、提供操控平台:器件内设计有特定通道结构(如入口、目标区域、中央腔室),为液滴载体的运输、旋转和内核释放提供物理空间,确保操控过程有序进行。
2、电极集成与电场构建:底部集成四组螺旋电极,通过施加具有90度相位差的交流信号,可形成行波电场(实现运输)和旋转电场(实现旋转),为液滴操控提供电场驱动力。
3、液滴生成控制:专用玻璃毛细管微流控芯片可精准生成双乳液液滴模板,通过控制三相流体(外相、中间相、内相)的流速,调节液滴壳层和内核尺寸,为后续操控奠定基础。
4、功能实现保障:通道结构与电极排布配合,使液滴能在电场作用下完成从入口到目标区域的定向运输;中央腔室的设计利于液滴在旋转电场中稳定旋转以测量电特性;特定区域的电场分布可触发液滴壳层破裂,实现内核释放。
5、灵活调控支持:通过微流控器件的结构设计与电信号参数(电压、频率、相位)的协同调节,可灵活控制液滴的运输速度与方向、旋转状态及释放时机,满足多样化操控需求。
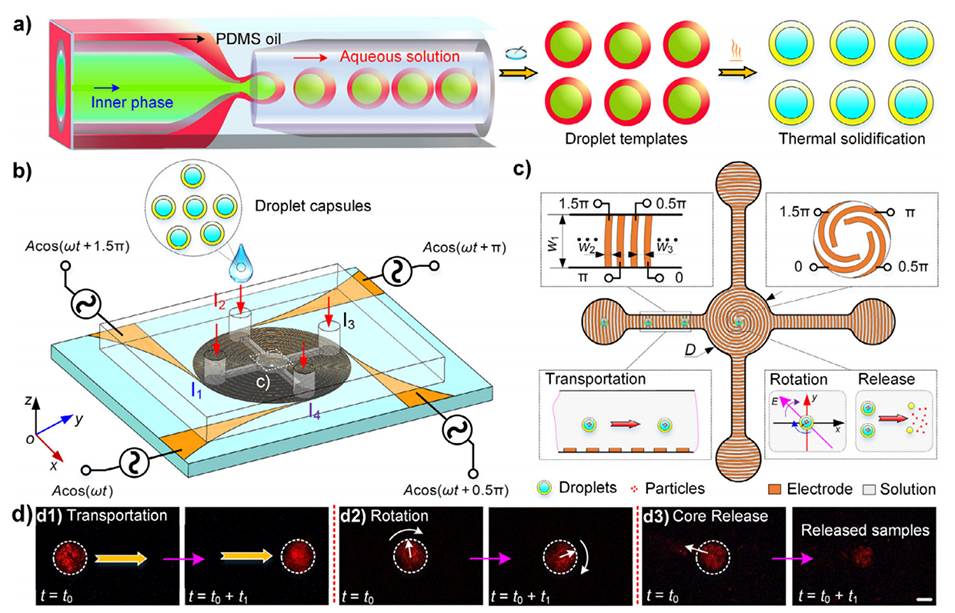
图1.电控双乳液液滴载体操控示意图。a)双乳液液滴载体的制备过程。b)用于液滴载体操控的微流控器件概览。c)微通道中电极的排布及液滴载体多功能操控示意图。d)可控电场下液滴载体按需运输(d1)、旋转(d2)和内核释放(d3)的图像。比例尺:75μm。
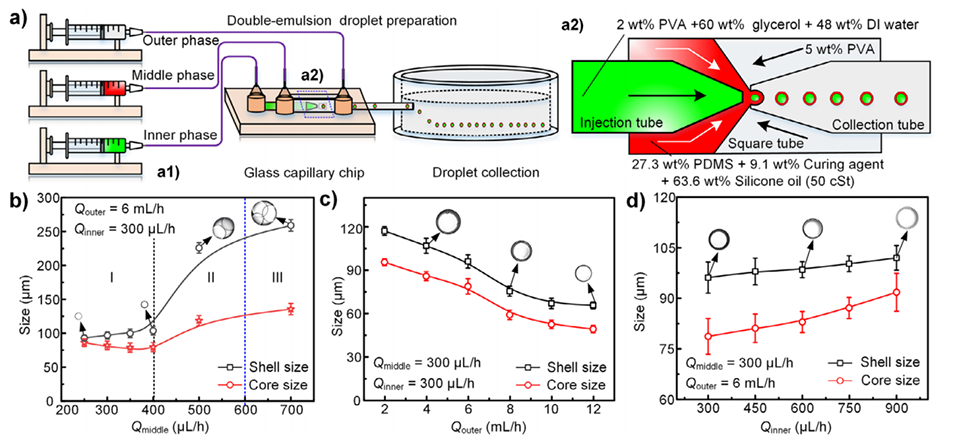
图2.双乳液液滴模板的生成。a)用于生成双乳液液滴的微流控系统示意图(a1)。a2)液滴生成器件关键结构及制备所用溶液的视图。b)中间油相流速对液滴尺寸的影响。c)外部水相流速对液滴尺寸的影响。d)液滴尺寸与内部相流速的关系图。
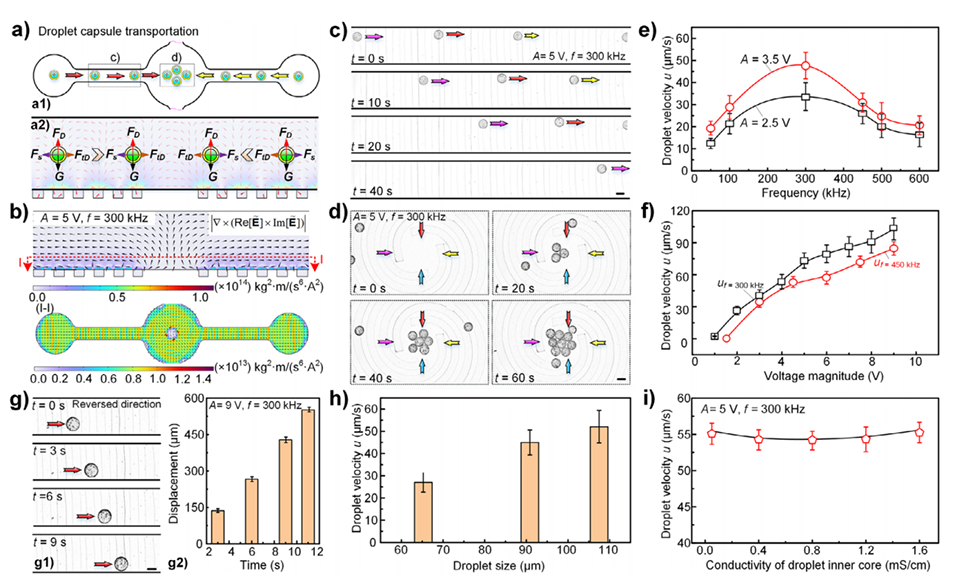
图3.可控行波介电泳作用下的液滴载体运输。
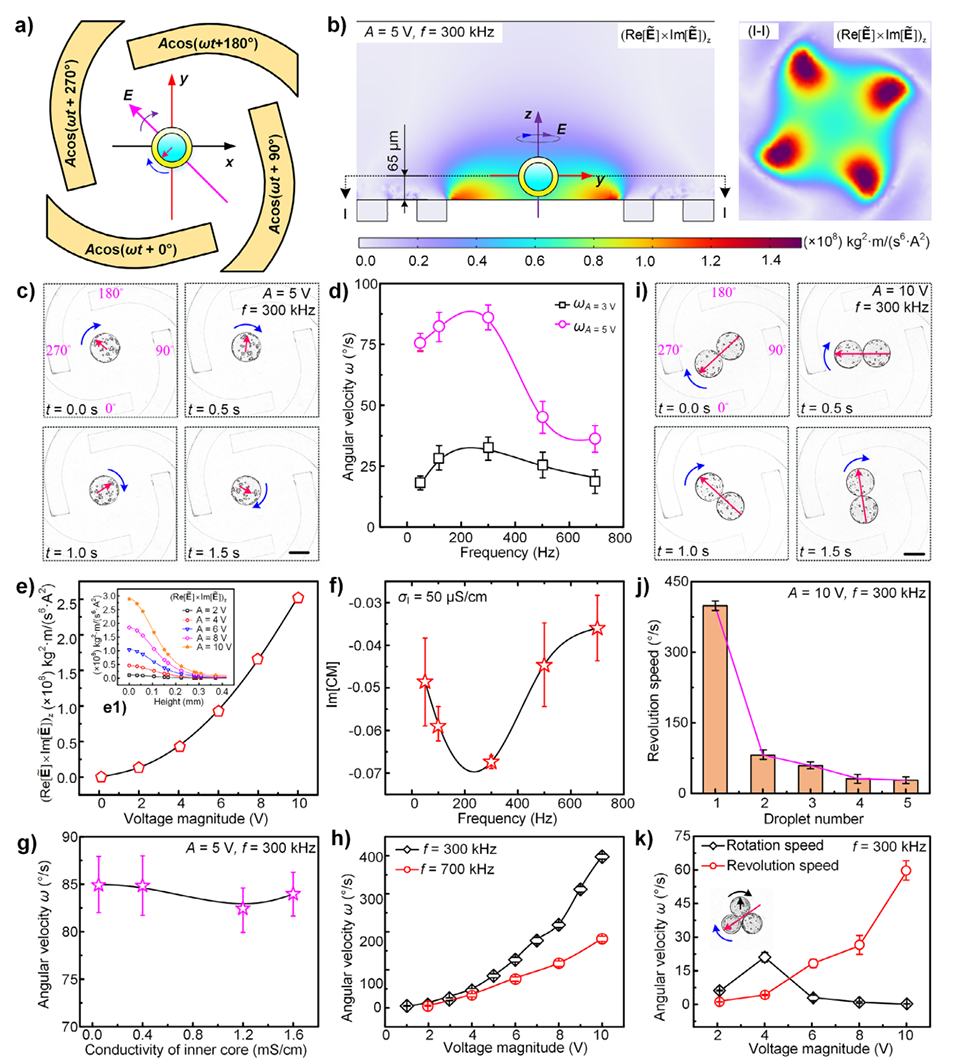
图4.旋转电场作用下的液滴载体旋转操控。
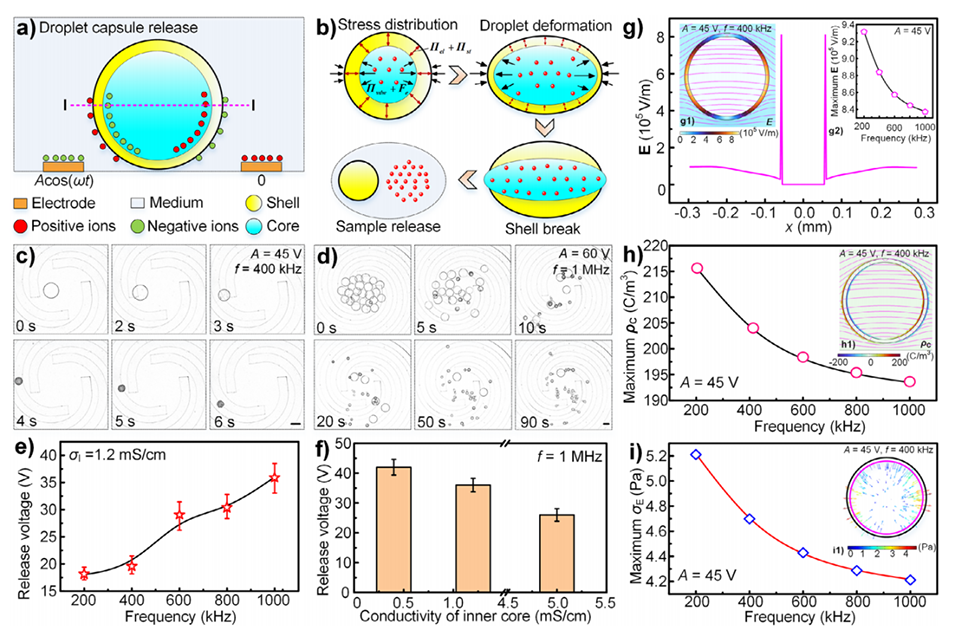
图5.电触发双乳液液滴载体的内核释放。

图6.含纳米级聚苯乙烯颗粒和抗癌药物的液滴载体的电操控。a–c)包裹荧光纳米颗粒的液滴载体的运输、旋转和释放。比例尺:75μm。d–f)含抗癌药物盐酸阿霉素的液滴载体的运输、旋转和释放。比例尺:150μm。
论文链接:https://doi.org/10.1002/adfm.202510679














