各向异性微载体(AMs)因其异质结构和多功能集成特性,在生物医学领域备受关注。与传统均质颗粒相比,AMs能够整合磁、电、光、化学等不同性能的模块,实现更为复杂的应用功能。尽管科研人员已着力开发多种形貌的AMs,但由于多数研究聚焦于材料本身或制备方法,其整体潜力尚未充分释放。

近期,广州医科大学唐国胜教授、谢茂彬教授与党元野副教授联合发表综述,系统梳理AMs近二十年的制备策略与生物医学应用进展。该研究深入分析了AMs的形貌、制造策略与应用之间的相互作用及依赖关系,针对性提出适用于不同形貌的制备方案与特定生物医学场景的选型指南。此外,就当前面临的挑战及未来发展方向进行了展望。相关研究成果以“Anisotropic Microcarriers: Fabrication Strategies and Biomedical Applications”为题目,发表于期刊《Advanced Materials》。
本文要点:
1、该综述围绕各向异性微载体(AMs) 展开,梳理了过去二十年其从制备到生物医学应用的研究进展。
2、重点阐述了微流控、光刻、3D打印、电流体动力学共喷射、离心法、气流辅助剪切法、模板法、溅射镀膜等多种制备策略的原理、优势与不足。
3、详细介绍了AMs在多药递送、细胞共培养、多功能编码材料、仿生多酶级联合成反应系统、微电机等生物医学领域的应用。
4、同时指出当前研究存在的挑战,并展望了其结合人工智能等新兴技术的未来发展方向,旨在为不同背景研究者提供针对性的制备策略和应用选择指南。
一张图读懂全文
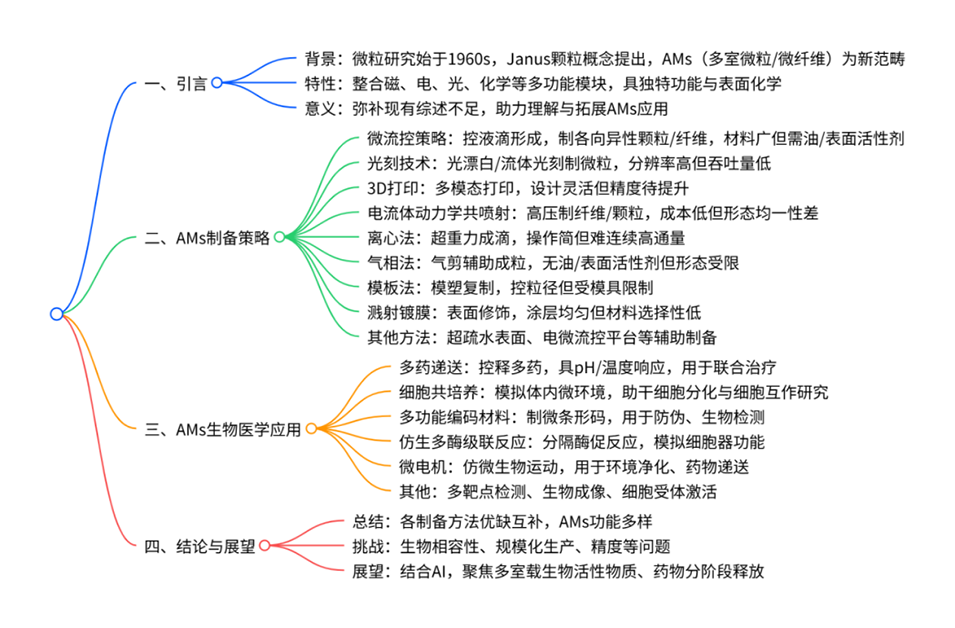

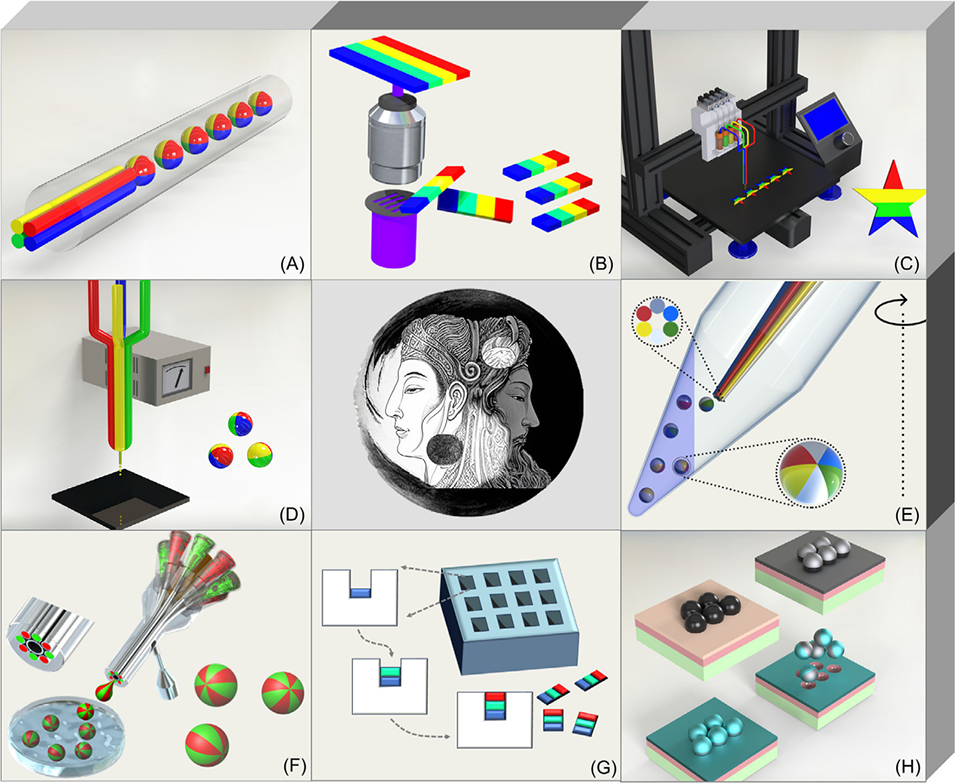
图1. 各向异性微载体的多种制备方法示意图,包括A)微流控法、B)光刻法、C)3D打印法、D)静电驱动共喷射法(EHD)、E)离心法、F)气流辅助剪切法、G)模板法、H)溅射镀膜法。
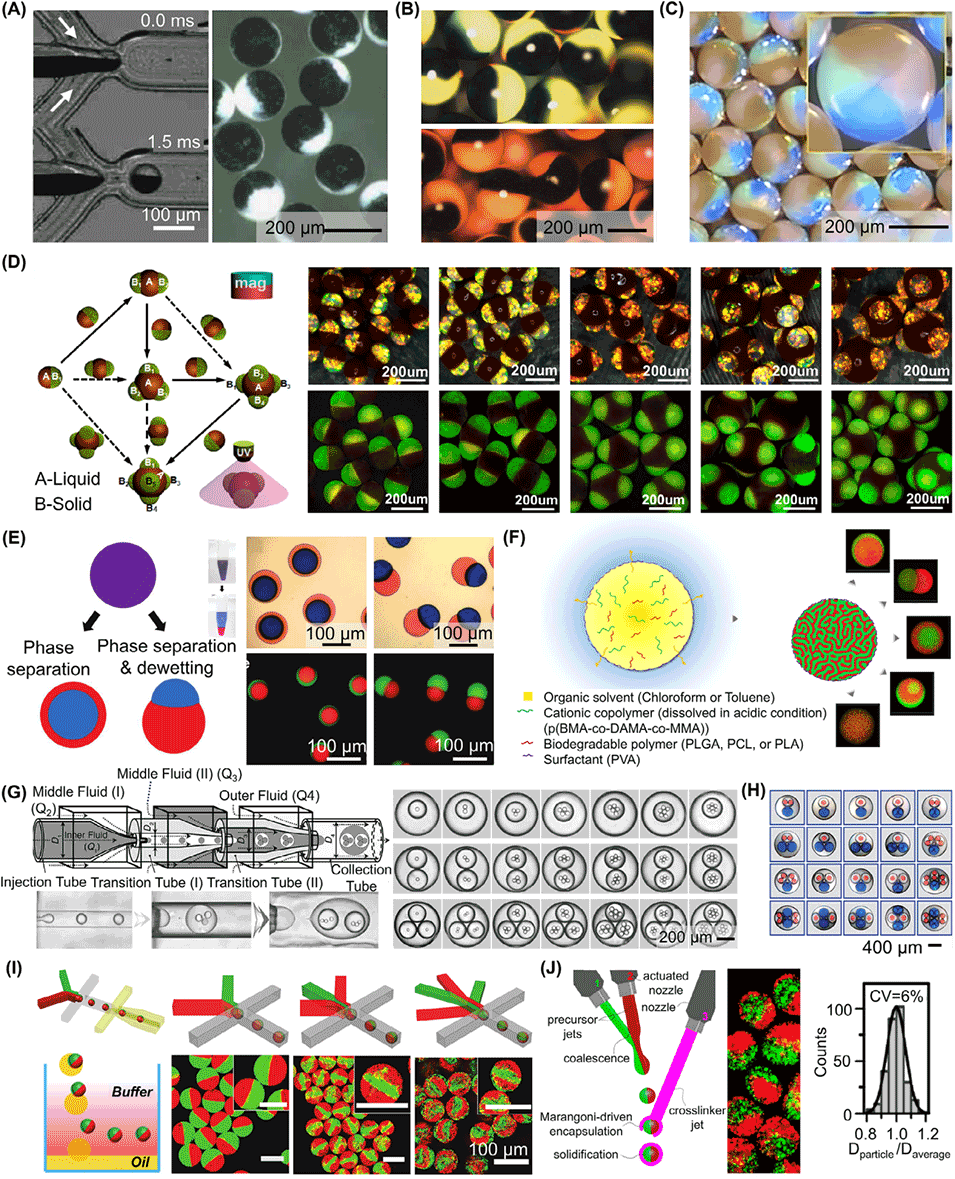
图2. 微流控法制备各向异性颗粒。
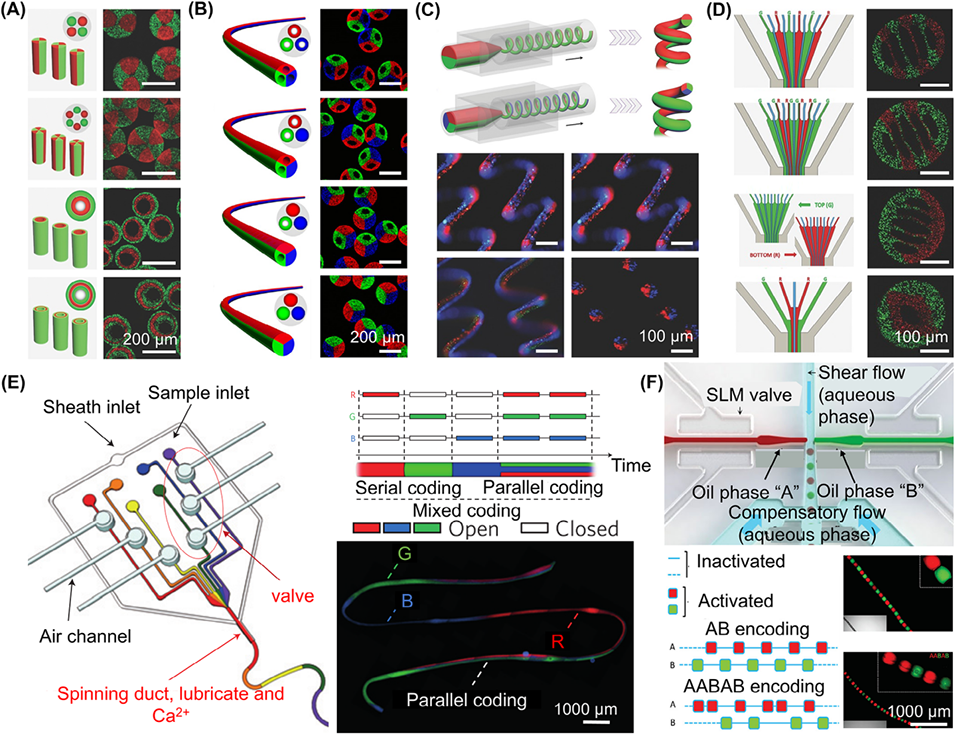
图3. 微流控法制备各向异性纤维。
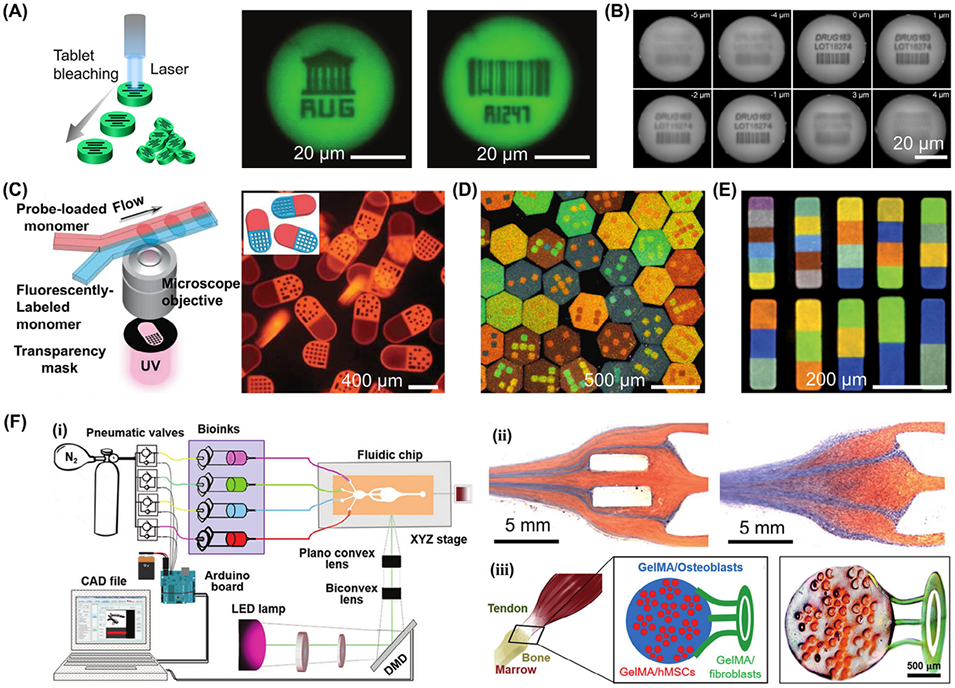
图4. 光刻法制备各向异性微载体。
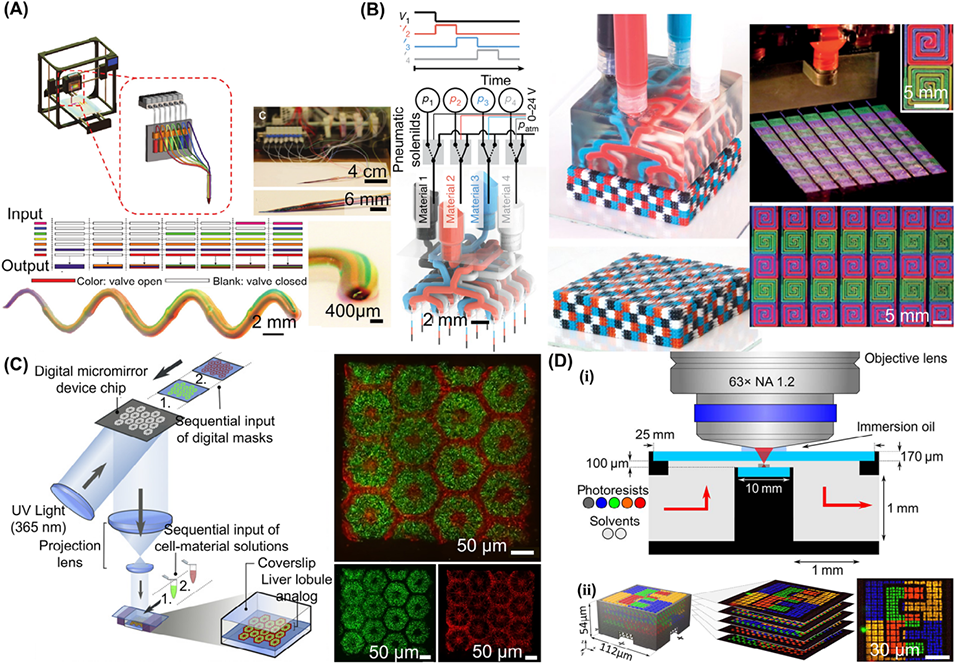
图5. 3D生物打印法制备各向异性微载体。
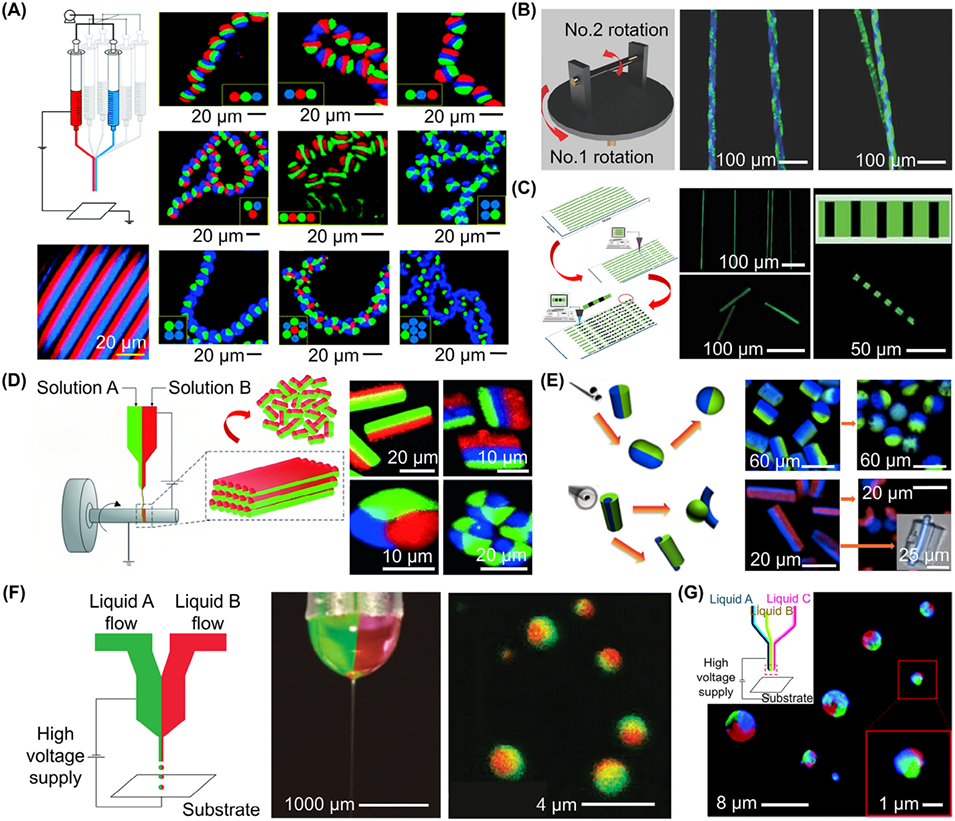
图6. 静电驱动共喷射(EHD)法制备各向异性微载体。
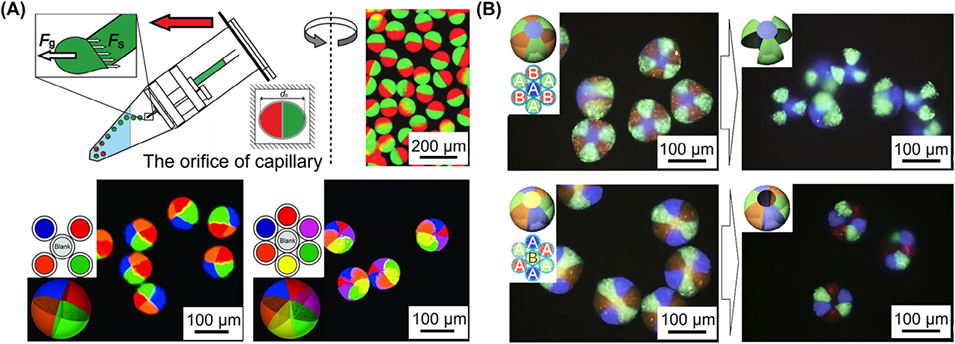
图7. 离心法制备各向异性微载体。
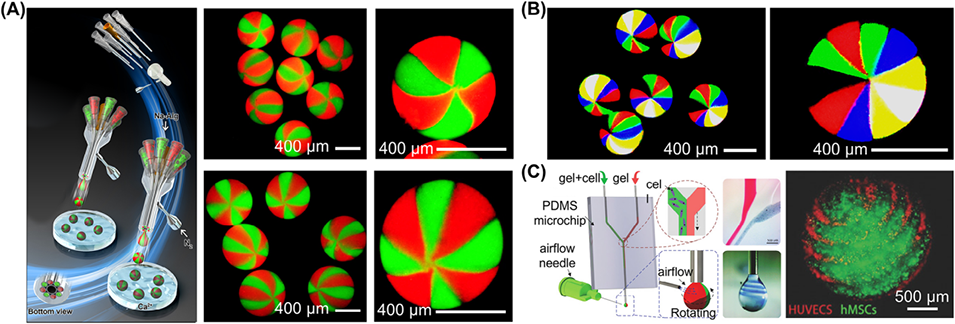
图8. 气流辅助剪切法制备各向异性微载体。
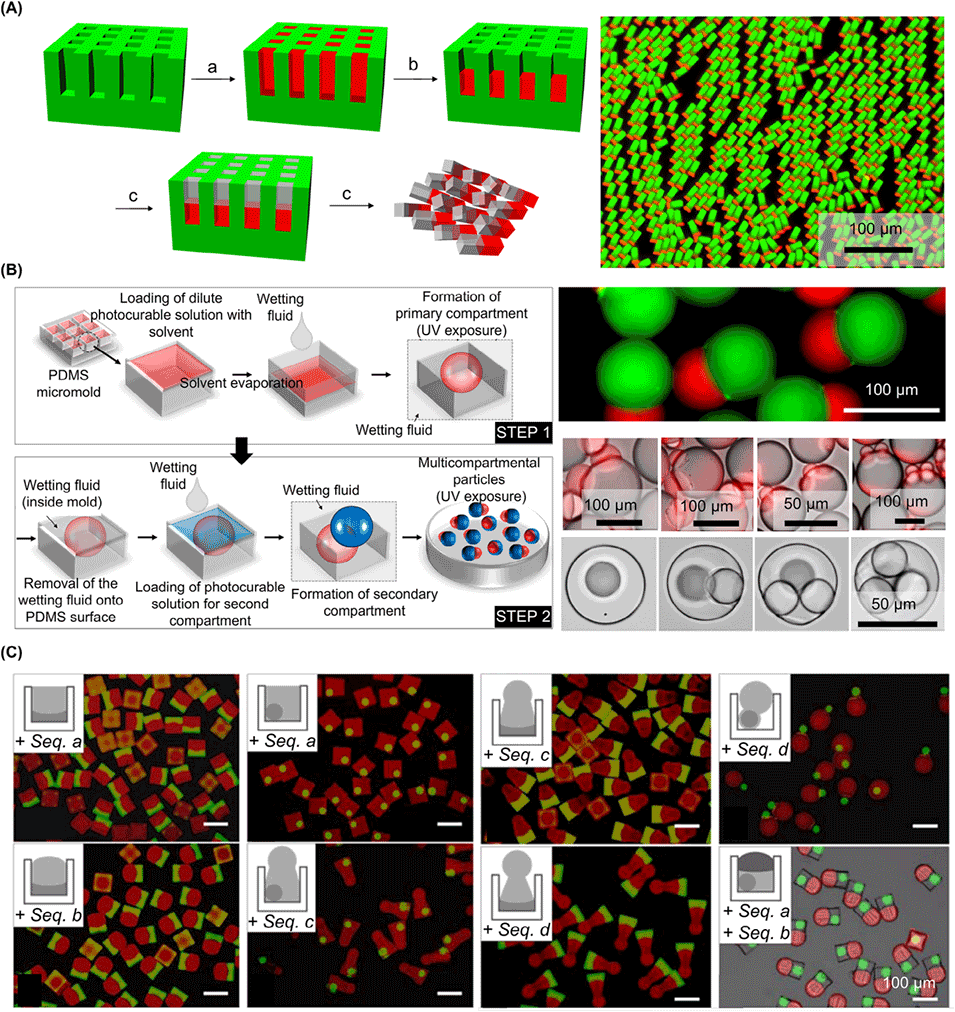
图9. 模板法制备各向异性微载体。
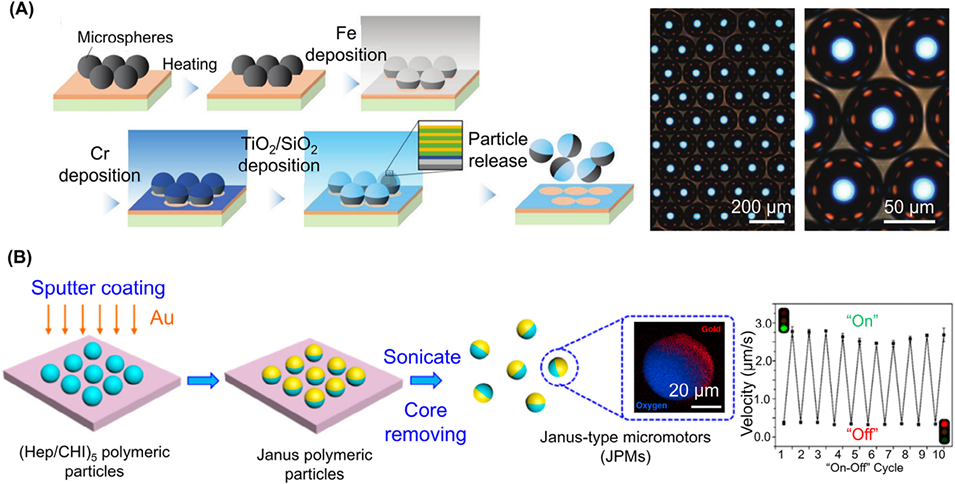
图10. 溅射镀膜法制备各向异性微载体。
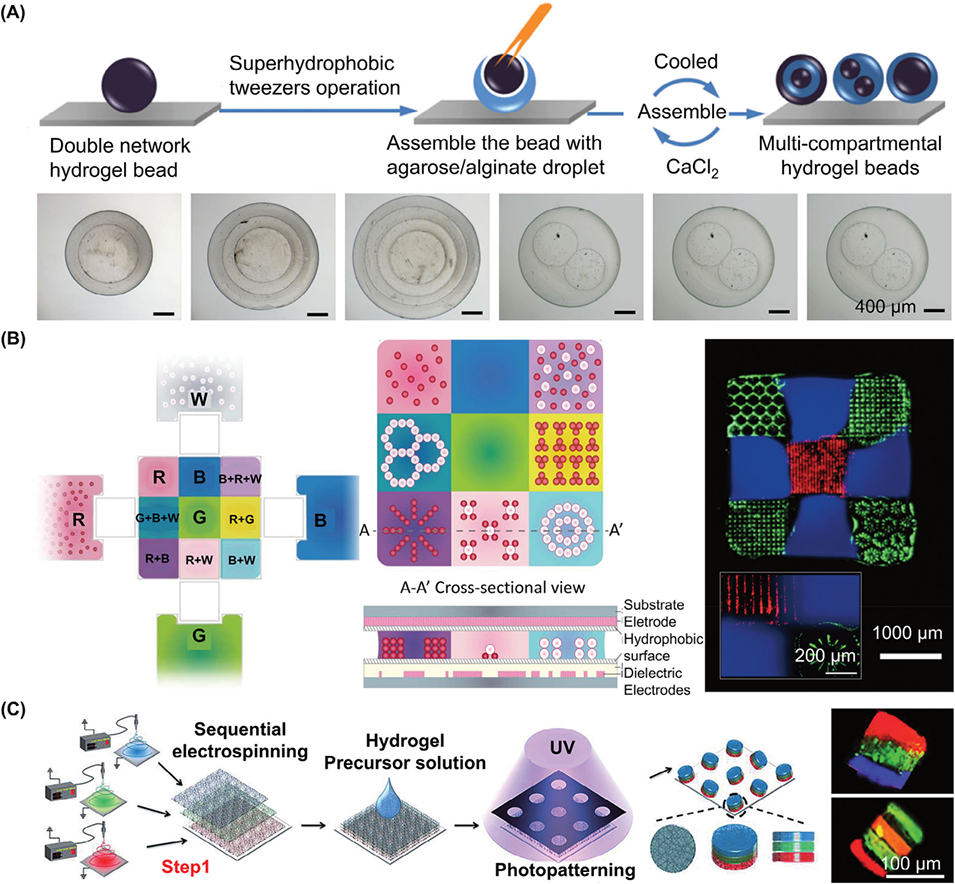
图11. 其他方法制备各向异性微载体。A)在超疏水表面上制备琼脂糖/海藻酸钠双网络多室各向异性微粒。B)通过电微流控平台两平行板间的两种主要电操纵技术(电润湿和介电泳)制备复杂三维结构。C)结合静电纺丝与光图案化技术制备非球形水凝胶微粒。
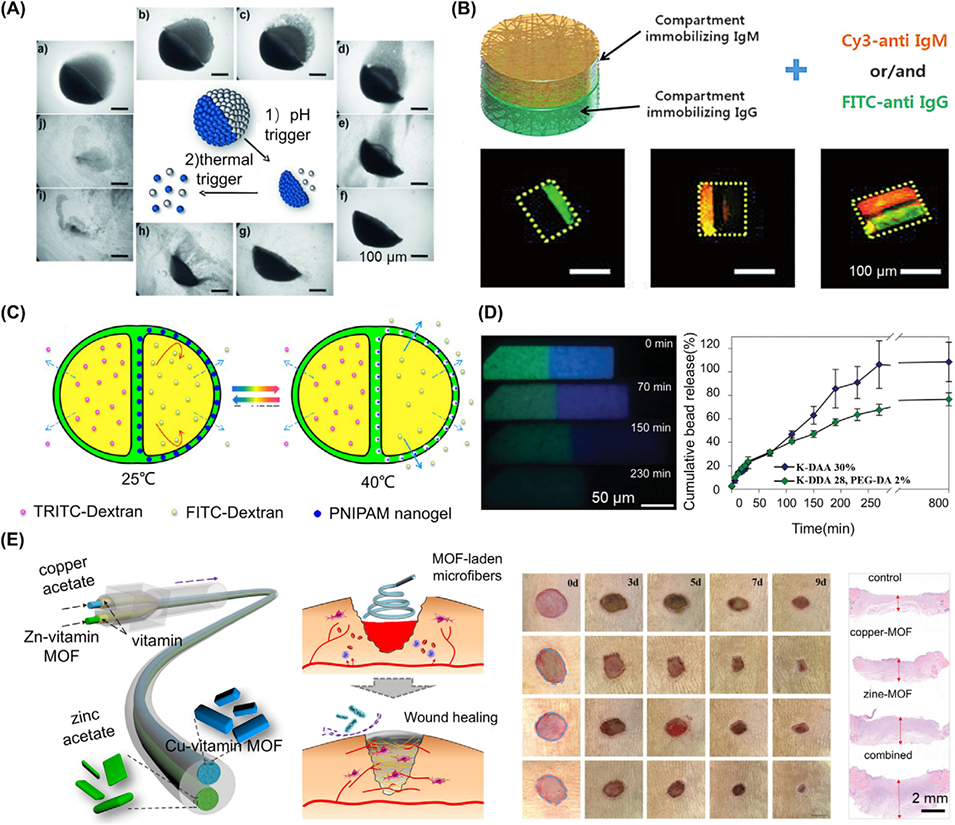
图12. 各向异性微载体在多药递送中的应用。
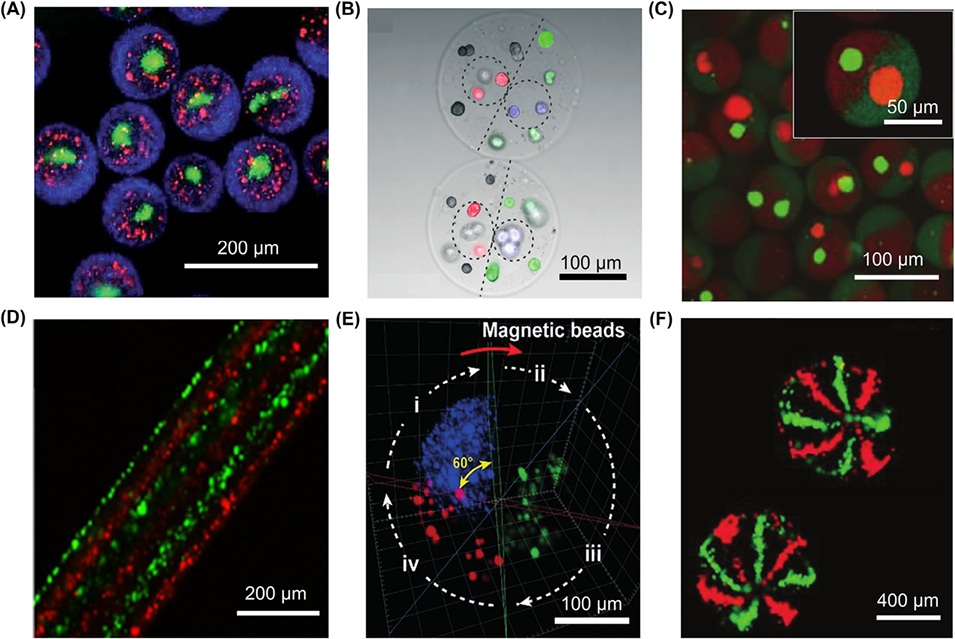
图13. 各向异性微载体中的细胞共培养。
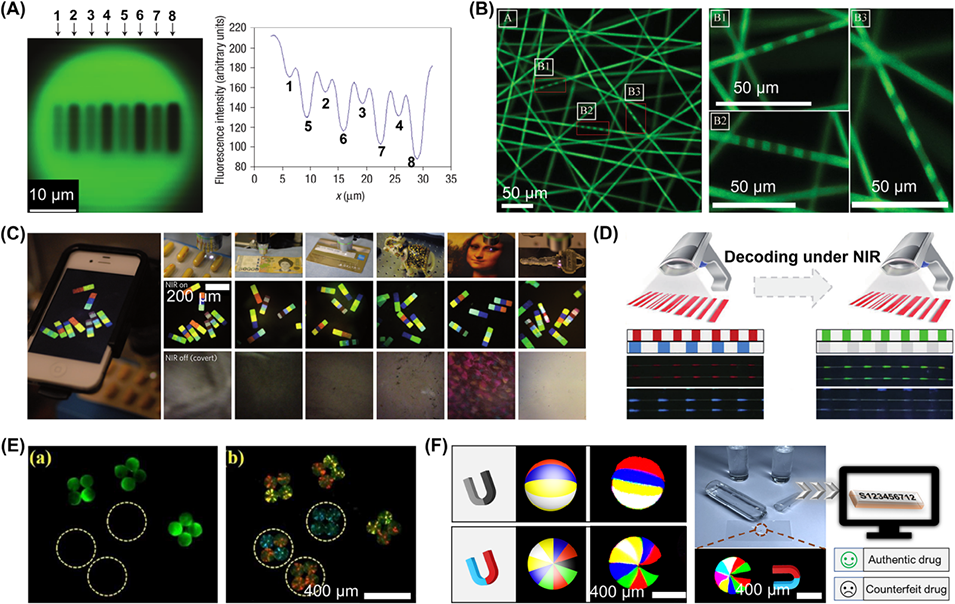
图14. 各向异性微载体在多功能编码中的应用。
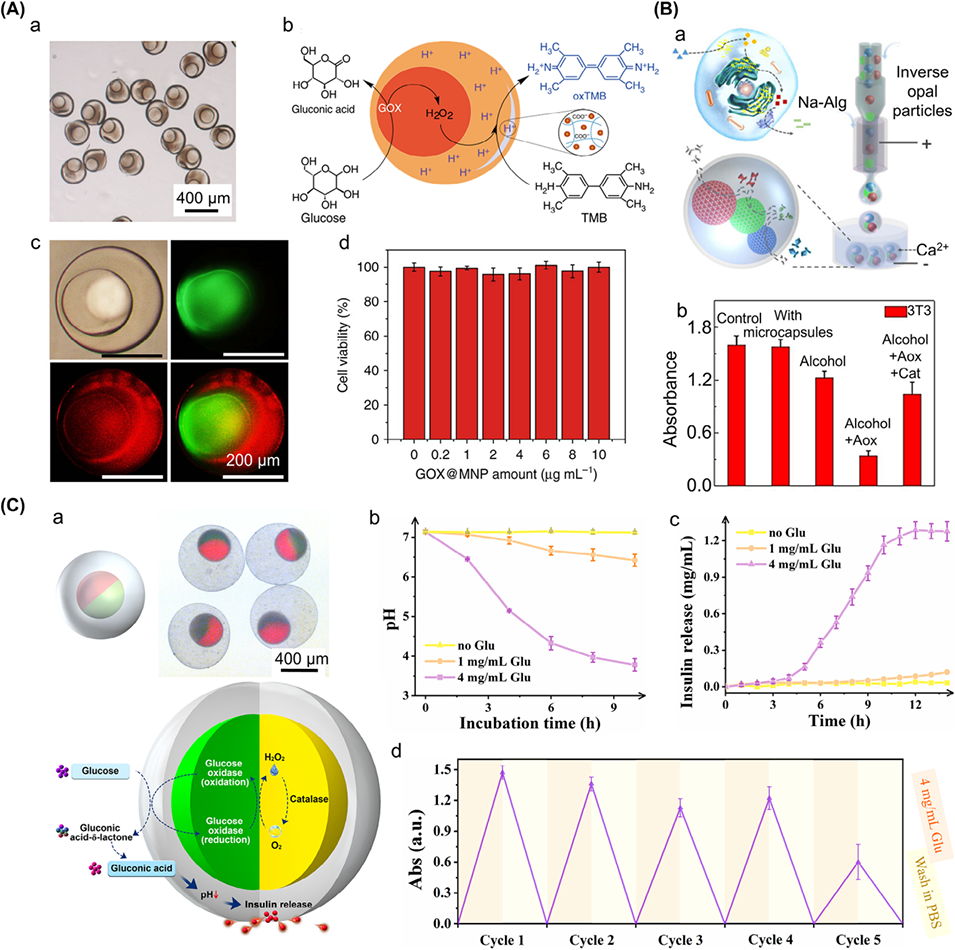
图15. 各向异性微载体中的仿生多酶级联反应系统。
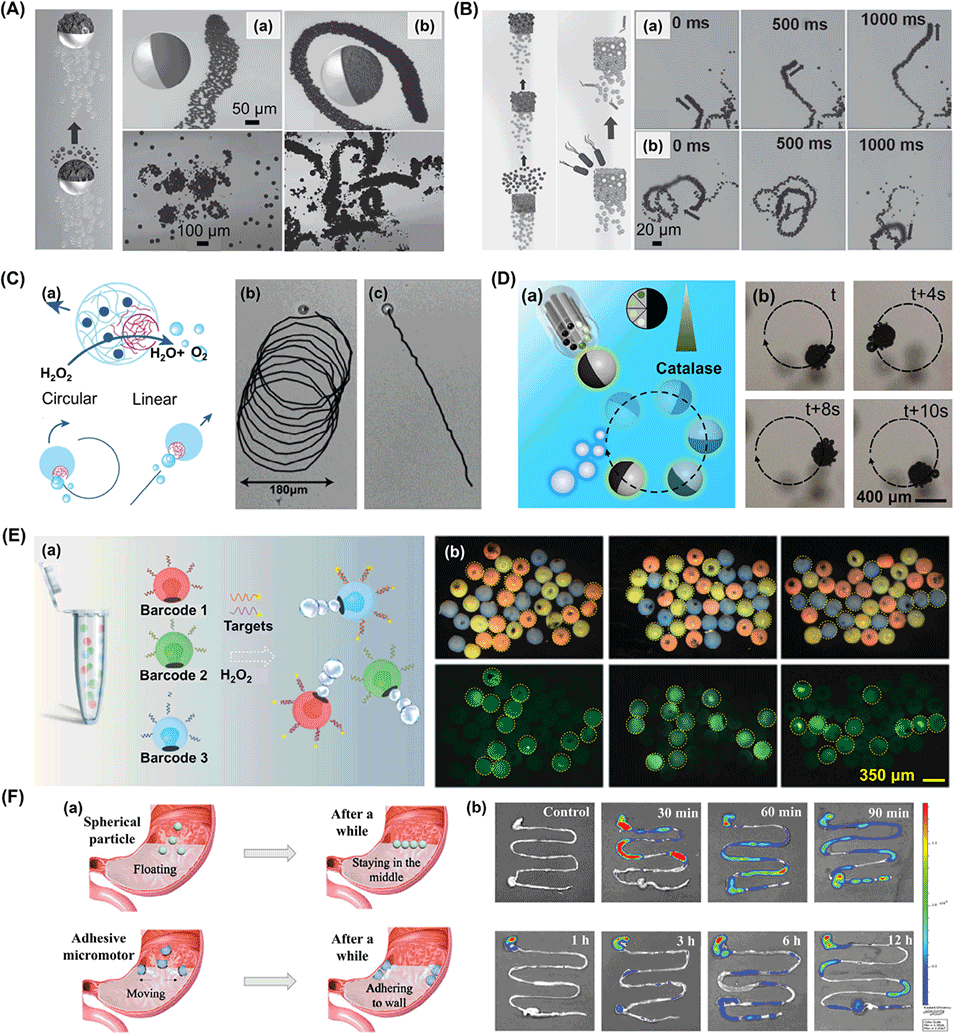
图16. 各向异性微载体作为微电机的应用。
论文链接:https://doi.org/10.1002/adma.202416862
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














