研究背景
1、3D细胞球体的核心价值:相比2D细胞培养,球体能更精准复刻体内组织的3D结构和细胞间相互作用,是药物筛选、病理研究的理想模型;其中脂肪细胞球脂代谢标志物表达更高、脂质积累更显著,是肥胖研究的关键表型模型。
2、传统制备方法的局限性
96/384孔板法:低细胞密度难以聚集,高密度形成大球体,无法大规模制备;
悬滴培养法:可制备均一球体,但操作繁琐、耗力,不适用大规模生产;
微孔板法:产量仅数千个/板,微孔内细胞密度不均导致球体尺寸变异大,无法满足高通量筛选(HTS)需求。
3、现有微流控方法的不足:依赖定制毛细管、多层PDMS装置或精准射流校准,需要专业技术和设备,普通生物实验室难以普及。

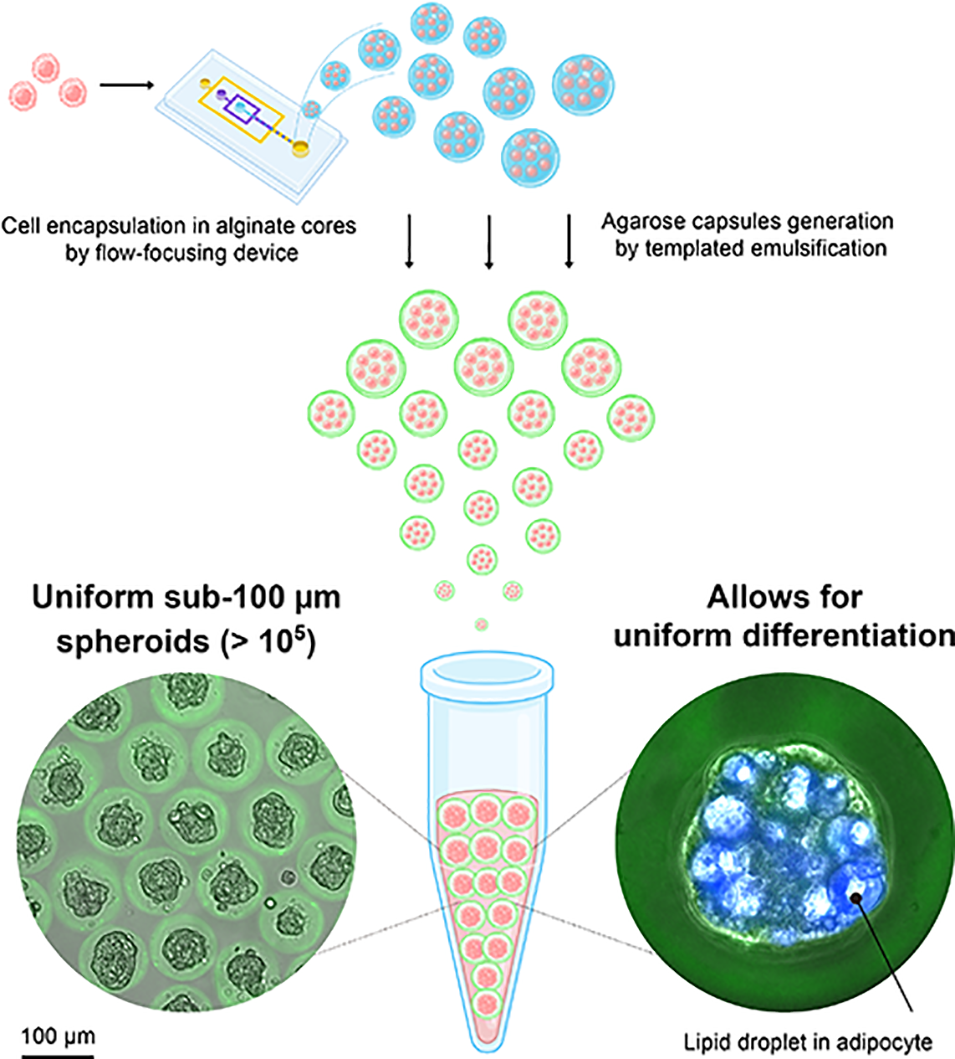
近期,东京大学先端科学技术研究中心团队开发了一种结合简易微流控技术与模板乳化法的新方法,可在空心琼脂糖微胶囊中规模化制备尺寸均一的小型前脂肪细胞球,并支持其长期分化为脂肪细胞球体。这一便捷的实验平台无需制造复杂的器件与流体控制系统,大幅降低了规模化制备脂肪细胞球的技术门槛。相关研究以“Large-Scale Production of Uniform, Small Adipocyte Spheroids in Hydrogel Microcapsules Using a Microfluidic Flow-Focusing Device”为题目,发表在期刊《ACS Biomaterials Science & Engineering》上。
本文要点:
1、该研究开发了一种结合简易微流控技术与模板乳化法的新方法,实现了空心琼脂糖微胶囊中均匀、小型脂肪细胞球的规模化制备,解决了传统方法难以大量生产均一脂肪细胞球的痛点,为肥胖研究的高通量分析提供了高效平台。
2、研究先通过微流控流动聚焦装置将前脂肪细胞包封在藻酸盐凝胶核中,再经模板乳化法包裹琼脂糖形成双层凝胶结构,溶解藻酸盐核后得到空心琼脂糖微胶囊,前脂肪细胞在其中2天即可自发形成均一球体(平均直径约60μm,变异系数约10%),单次实验可稳定生成超10万个球状体,且细胞存活率超90%。
3、经8天诱导分化后,这些球状体可转化为脂肪细胞球,相比传统微孔板培养,微胶囊培养的脂肪细胞球尺寸均一性更高、脂滴积累更显著,还能避免培养过程中的球状体融合与过度扩增。
4、该平台生成的琼脂糖微胶囊具有营养通透性高、尺寸可调节的特点,除脂肪细胞球外,还可适配多种球体和类器官模型的制备。研究也指出了该方法的改进方向,如增加细胞搅拌系统提升细胞数均一性、并行化液滴生成提高产量等。
5、该技术不仅为肥胖研究的高通量药物筛选提供了更贴合生理的3D模型,还在器官打印、组织工程等生物医学研究领域具有广泛应用潜力,是推进下一代细胞基技术的重要工具。
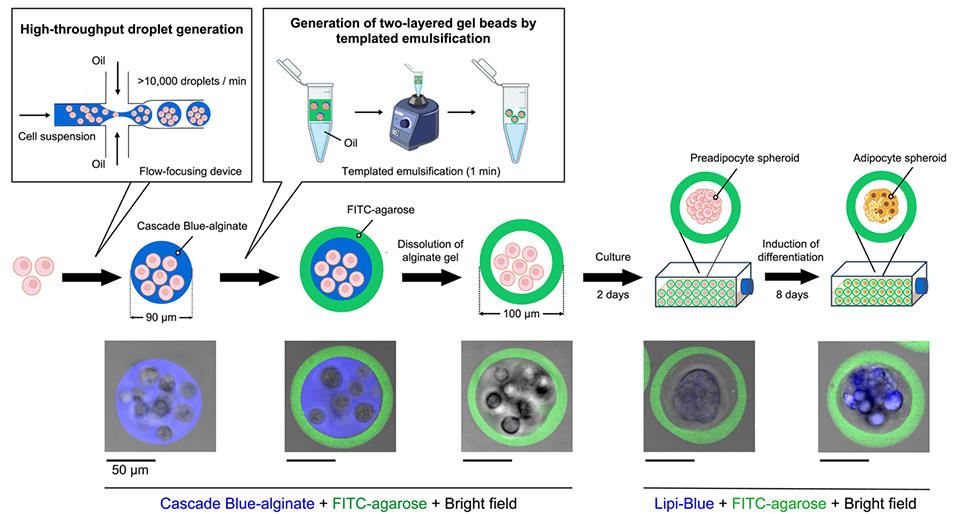
图1 基于液滴技术在琼脂糖微胶囊中大规模制备均一的小型脂肪细胞球体。该图为基于微胶囊的均一球体形成过程示意图:首先利用流动聚焦微流控装置,将前脂肪细胞包封于级联蓝标记的藻酸盐凝胶中;随后通过模板乳化技术,将上述藻酸盐芯包封于异硫氰酸荧光素(FITC)标记的琼脂糖液滴内,形成藻酸盐-琼脂糖双层凝胶结构;采用无钙缓冲液溶解藻酸盐芯,得到包封有前脂肪细胞的空心琼脂糖微胶囊。前脂肪细胞经2天培养后,在微胶囊内自发形成球体;经8天分化诱导培养基处理后,进一步分化为脂肪细胞球体。左侧三张图像为异硫氰酸荧光素标记的琼脂糖、级联蓝标记的藻酸盐与明场通道的融合图像,右侧两张图像为异硫氰酸荧光素标记的琼脂糖、脂滴蓝与明场通道的融合图像;所有图像均通过共聚焦显微镜采集,比例尺=50μm。
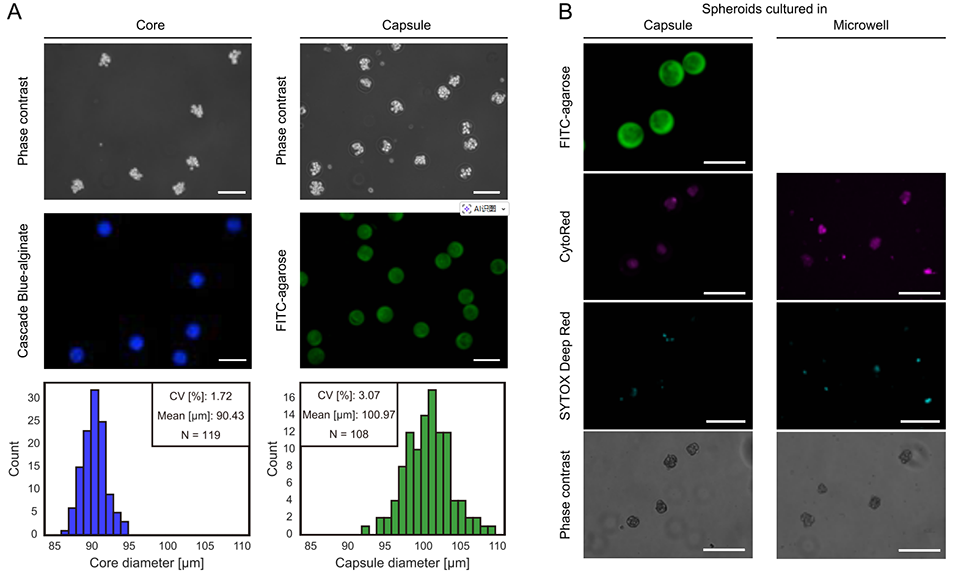
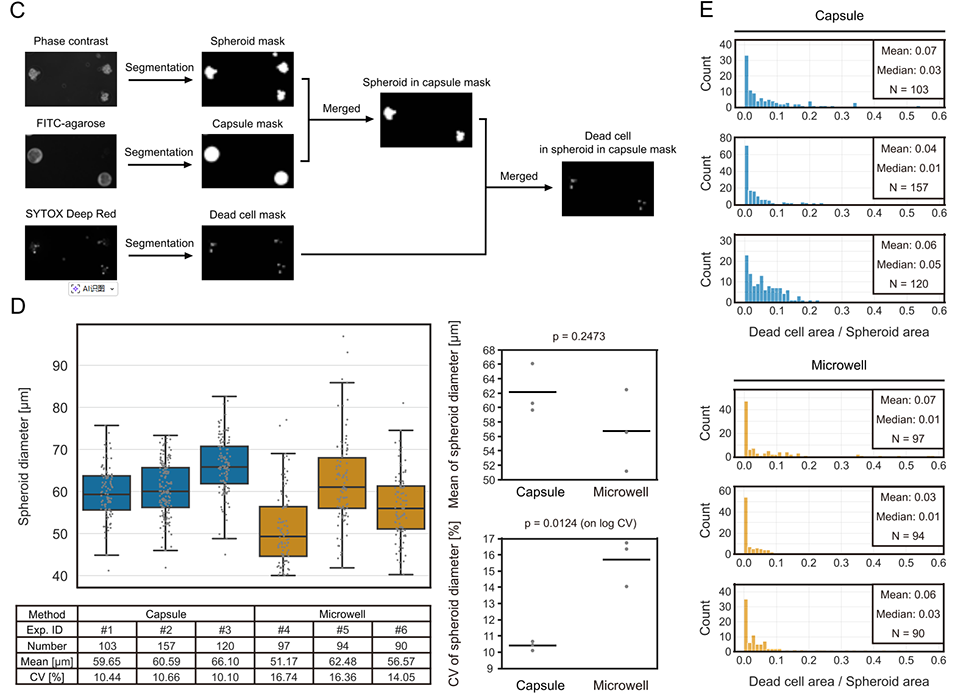
图2 在琼脂糖微胶囊内大规模制备高活力、尺寸均一的小型前脂肪细胞球体。
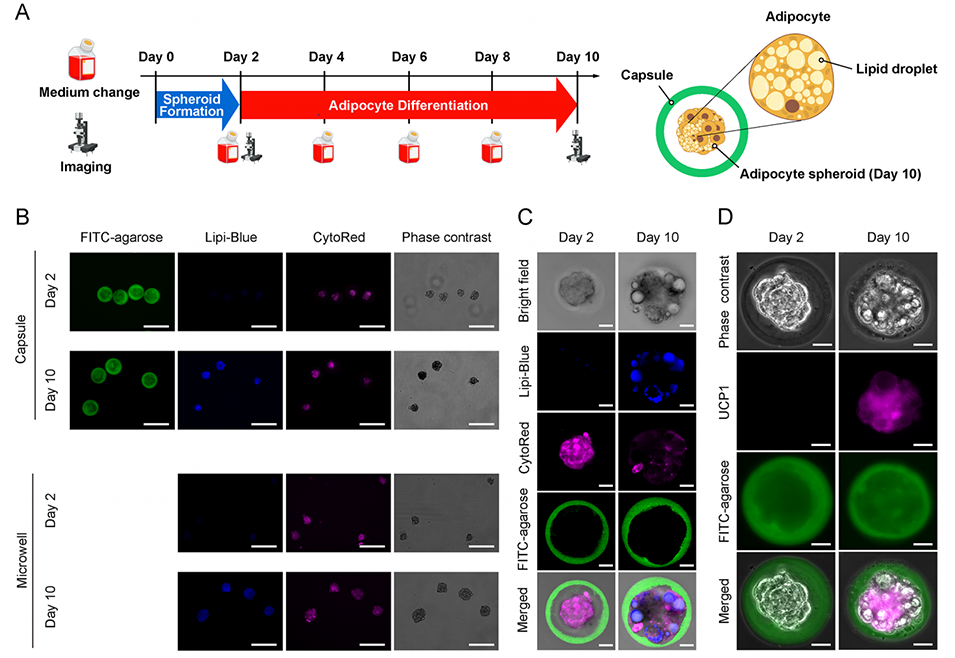
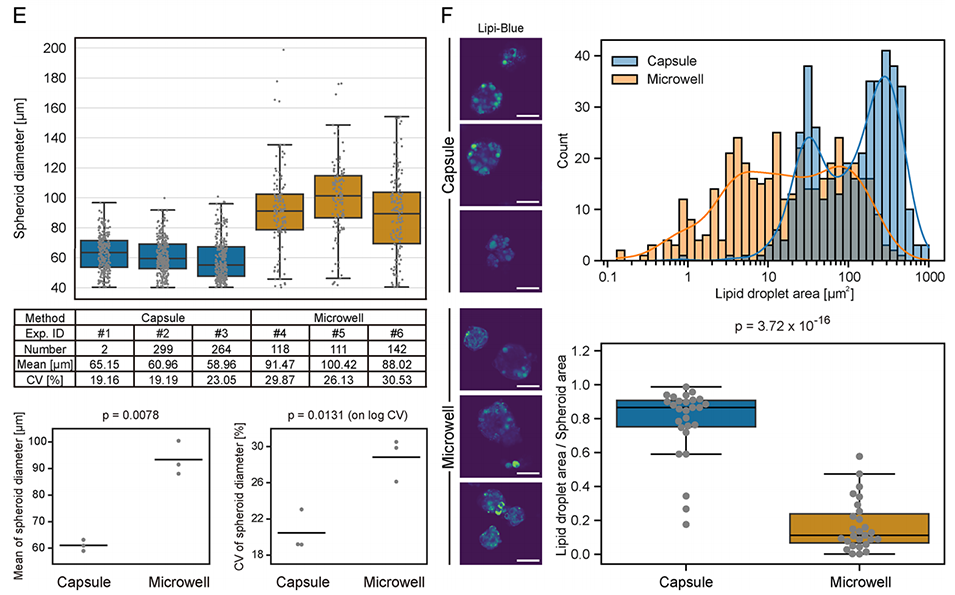
图3 空心琼脂糖微胶囊中均一脂肪细胞球体的分化及脂质积累的增强。
论文链接:https://doi.org/10.1021/acsbiomaterials.6c00142
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














