液滴微流控技术作为微纳米尺度的“精准实验室”,早已成为单细胞测序、高通量药物筛选、合成生物学等领域的核心工具。但长久以来,传统技术始终存在难以突破的痛点:油包水体系虽能形成稳定液滴,却像给液滴套上了“密封罩”,阻碍了物质交换;而更贴合生物环境的水包水体系,又因界面张力极低,液滴易破裂、难调控。

近日,浙江大学与埃因霍温理工大学等团队合作,在《Lab on a Chip》发表最新研究,提出了一种无油相、无表面活性剂的微流控新方法,成功实现了无膜水包水液滴的可控生成、稳定捕获与动态调控,还首次观察到凝聚层液滴内可逆亚区室的形成,为液-液相分离(LLPS)体系的动态研究打开了全新窗口,相关成果也为合成生物学、软物质研究等领域提供了强大的新工具。该研究以“A microfluidic method for controlled generation and trapping of membraneless water-in-water droplets”为题目,发表于期刊《Lab on a Chip》。
核心痛点:传统微流控的“两难困境”
双水相体系(ATPS)形成的水包水(W/W)液滴,因无油相、无表面活性剂的特性,更贴近生物体内的微环境,能实现水溶性分子的自由扩散,是模拟细胞、研究生物体内无膜细胞器的理想模型。
但这一体系的研究却困难重重:一方面,水包水液滴的界面张力仅为 0.001–0.1 mN/m,远低于油包水体系,液滴极不稳定,往往需要精细的流量控制或外部场力才能维持;另一方面,传统微流控多采用 PDMS 材质芯片,易出现溶剂蒸发、大分子扩散进基底的问题,无法长期稳定观测液滴的动态行为。
而此次研究的核心,就是打造了一个能破解这两大难题的全新微流控平台。
创新设计:死端腔室 + 石英芯片,让液滴“听话又稳定”
研究团队摒弃了传统依赖界面剪切力形成液滴的思路,设计了以死端腔室为核心的微流控芯片,整体由主通道、死端腔室和连接颈三部分构成,液滴的形成不再依靠流速,而是由连接颈的几何结构(长度、宽度)和主通道溶液的暴露时间精准调控。
为了实现长期稳定的实验条件,团队没有采用传统的 PDMS 芯片,而是通过飞秒激光微加工技术在熔融石英上制备芯片。石英材质完全不透气体和液体,既避免了溶剂蒸发导致的浓度变化,也防止了大分子扩散进芯片基底,让液滴的实验条件能稳定维持数天,这是 PDMS 芯片无法实现的。
更关键的是,该平台通过扩散介导的液-液相分离实现水包水液滴的原位生成,全程无需油相、无需表面活性剂,也不需要精细的流量控制,仅通过调控主通道的溶液组成,就能实现腔室内化学环境的动态变化,让液滴的物质交换不再受限制,真正实现了 “开放体系” 的研究。
双重验证:从精准调控到可逆亚区室,平台实力拉满
为了验证平台的有效性和多功能性,研究团队先后以两种经典的液 - 液相分离体系为模型展开实验,层层递进验证了平台的核心优势。
1、PEG - 葡聚糖分离型体系:精准调控,液滴均一性拉满
以研究最成熟的聚乙二醇(PEG)- 葡聚糖水相双相体系为模型,团队实现了液滴尺寸和浓度的独立精准调控:通过改变连接颈的几何结构、葡聚糖溶液的暴露时间调控液滴尺寸,通过改变主通道 PEG 溶液浓度调控液滴内葡聚糖浓度。
实验结果显示,该平台生成的液滴尺寸变异系数低至 2%,远优于传统水包水微流控方法的 10% 以上,还成功制备出直径小于 10μm 的微型液滴,为人工细胞研究提供了理想模型。
2、PAA/PDMAEMA 缔合型体系:可逆亚区室,模拟生物无膜细胞器
这是此次研究的一大亮点。团队将平台应用于聚丙烯酸/聚甲基丙烯酸N,N-二甲基氨基乙酯(PAA/PDMAEMA)缔合型凝聚层体系,仅通过调控主通道的 KCl 盐溶液浓度,就实现了凝聚层液滴内可逆亚区室的形成与消失。
当主通道通0 M KCl 溶液时,液滴内的亚区室会逐渐消失;停止溶液流动后,液滴吸水膨胀,亚区室重新形成;恢复溶液流动,亚区室又会快速出现。这一过程可反复实现,且无需大幅改变实验环境,突破了以往亚区室研究需多组分体系或剧烈环境变化的限制,为模拟生物体内无膜细胞器的动态结构变化提供了绝佳的研究模型。
此外,团队还在芯片中集成了气动阀,通过控制阀门的开闭,实现了不同腔室间液滴的可控通讯,让研究无膜液滴间的信号传递、物质交换成为可能,为探索细胞间相互作用奠定了基础。
平台优势:鲁棒性强,适配多领域研究
相较于传统微流控方法,这款新平台的优势十分显著:
✅ 无油相、无表面活性剂,贴合生物微环境,避免了油相和表面活性剂对生化反应、细胞培养的干扰;
✅ 无需精细流量控制,鲁棒性强,能稳定生成均一液滴,降低实验操作难度;
✅ 石英芯片材质,可长期稳定观测,解决了 PDMS 芯片的蒸发和扩散问题;
✅ 动态调控化学环境,实现液滴的开放体系研究,可解析液-液相分离的动态行为;
✅ 多功能拓展,既可精准调控液滴参数,又能实现可逆亚区室、腔室间通讯,适配多类研究需求。
当然,研究也指出了平台目前的局限性,比如液滴间的物质交换主要依赖扩散,多组分内相的组成调控仍有挑战。但团队表示,这些问题可通过优化芯片几何结构、修饰表面润湿性等方式逐步解决,未来的优化空间巨大。
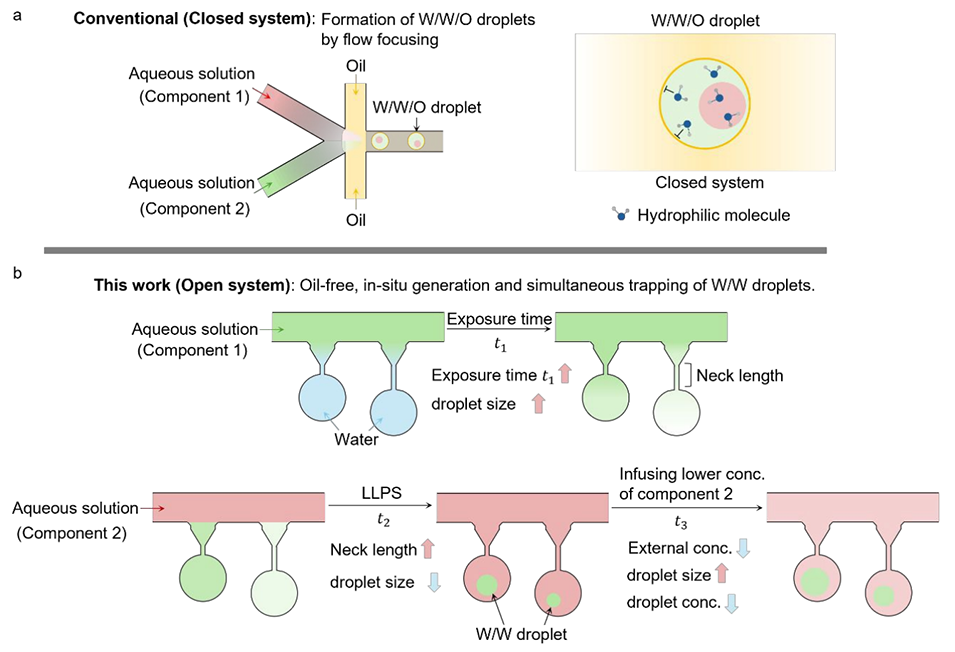
图1. 传统封闭式油包水包水(W/W/O)微流控液滴体系与本研究开放式水包水(W/W)液滴体系的对比。a 传统 W/W/O 液滴的形成依赖于流动聚焦过程中的剪切力,该体系具有高界面张力(γw/o);W/W/O 液滴为封闭体系,液滴与周围油相间的分子交换受到限制。b 本研究无油平台的原理示意图:聚合物浓度梯度驱动溶质向死端腔室迁移,无需外力或表面活性剂,通过双水相体系(ATPS)相分离在原位生成 W/W 液滴。该体系能以高稳定性实现液滴尺寸和浓度的可调调控,且不受主通道流速的影响。与组分 1 的接触时间(t1)越长,生成的液滴越大;连接颈的长度越长,液滴则越小;此外,液滴浓度由其与主通道中组分 2 的平衡状态决定。例如,在平衡状态(t3)后通入更低浓度的组分 2,会生成浓度更低、体积更大的液滴。
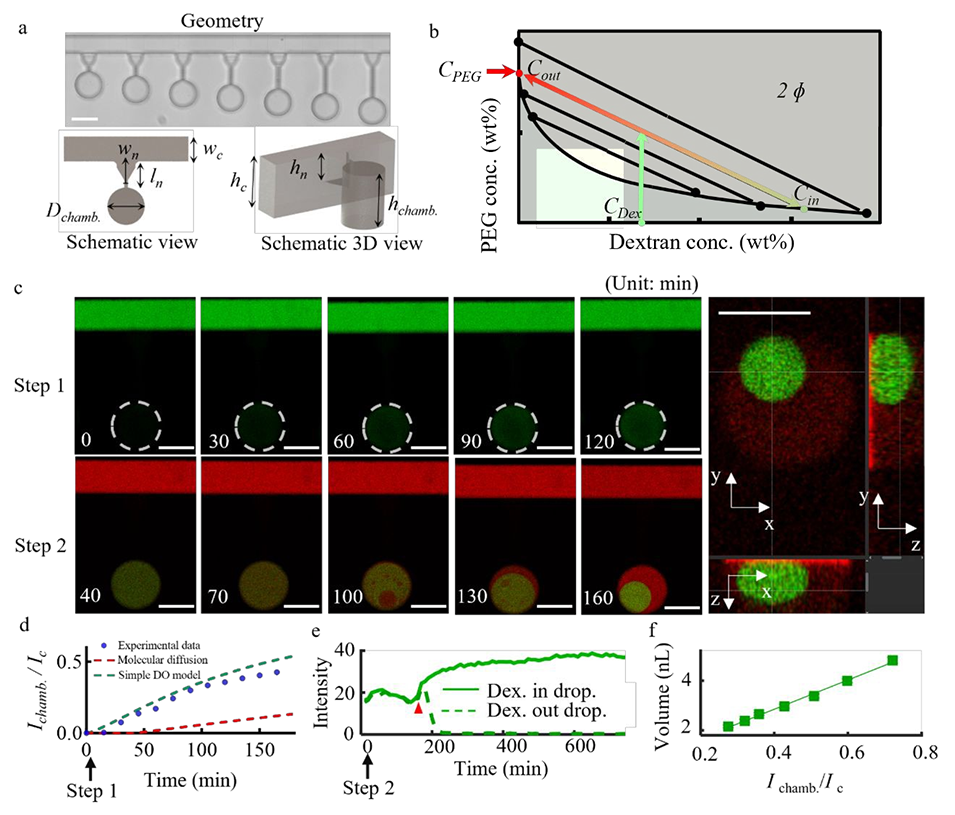
图2. 死端腔室微流控器件中,通过液-液相分离(LLPS)生成并捕获葡聚糖液滴。a 带死端腔室的微流控芯片设计参数:通道宽度wc=200 μm、通道高度hc=400 μm、腔室直径Dchamber=300 μm、腔室高度hchamber=400 μm;连接颈的尺寸(宽度wn、长度ln)可调节,宽度范围为 30~90μm,长度范围为 60~360μm。比例尺:300μm。b 聚乙二醇-葡聚糖双水相体系的典型相图。c 死端腔室中液-液相分离的分步过程:步骤 1,葡聚糖溶液(绿色,经异硫氰酸荧光素标记的葡聚糖标记)向死端腔室的扩散过程可视化,主通道持续通液以维持通道内葡聚糖浓度恒定;步骤 2,注入聚乙二醇溶液(红色,经罗丹明标记的聚乙二醇标记),其向死端腔室扩散后触发相分离。右侧图:通过共聚焦显微镜在 xy、xz、yz 三个平面的切片成像,呈现生成的葡聚糖液滴的三维形态,该腔室的连接颈宽度为wn=30 μm。比例尺:200μm。d 向微流控芯片中通入 10 wt% 的葡聚糖溶液时,腔室内(ln=210 μm、wn=30 μm)葡聚糖相对浓度随接触时间变化的实验数据(蓝点)和数值模型拟合结果(红色虚线:扩散模型;绿色虚线:扩散渗透模型)。Ic 为主通道荧光强度,Ichamber 为腔室荧光强度。e 生成过程中,液滴内外葡聚糖浓度随时间的变化,箭头指示液-液相分离的起始时刻。f 液滴体积与捕获腔室内葡聚糖相对荧光强度的相关性。
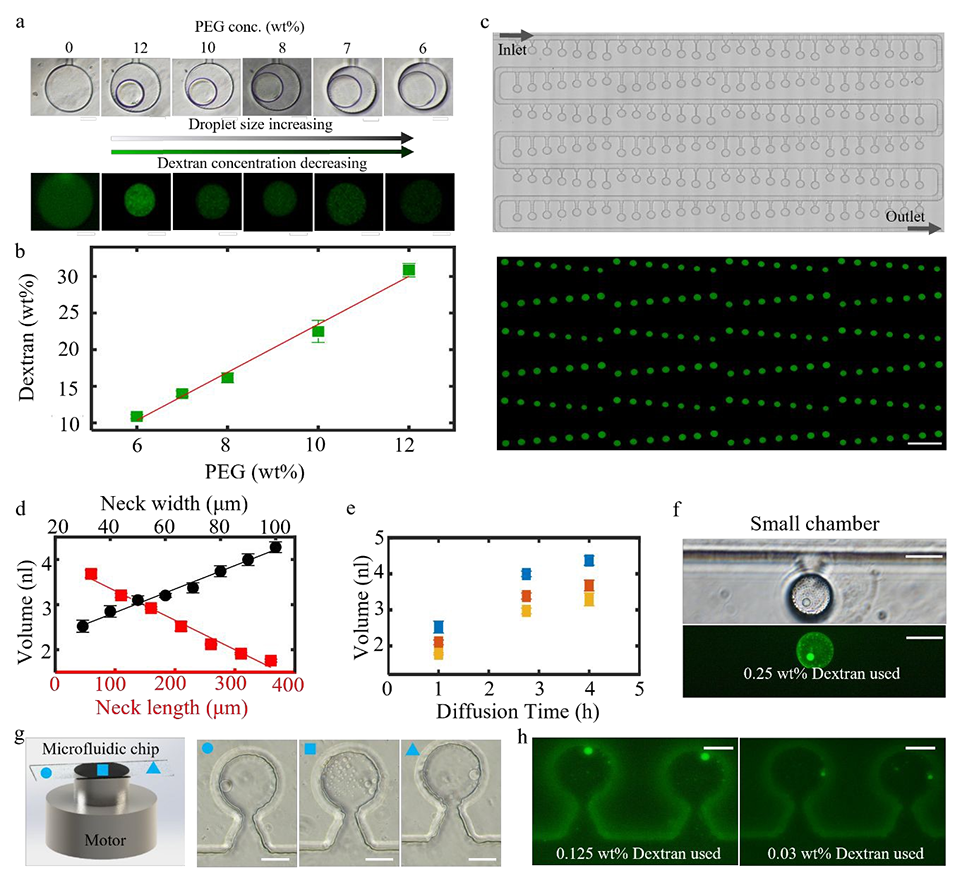
图3. 石英基微流控芯片中葡聚糖液滴的浓度与尺寸精准调控。a 向主通道中通入浓度逐级降低的聚乙二醇溶液,实现葡聚糖液滴的浓度和尺寸调控。比例尺:100μm。b 芯片外部聚乙二醇浓度与液滴内部葡聚糖浓度的关系。c 上图:葡聚糖液滴生成前,石英基微流控芯片整体结构的明场图像;下图:腔室内生成葡聚糖液滴后,同一器件的共聚焦荧光拼接扫描图像,液滴尺寸的差异体现了连接颈几何结构和扩散时间的影响。比例尺:1 mm。d 改变通道与腔室间连接颈的几何结构,实现葡聚糖液滴体积的调控:液滴体积随连接颈长度增加而减小(连接颈宽度固定为wn=50 μm,红色方形,下坐标轴),随连接颈宽度增加而增大(连接颈长度固定为ln=210 μm,黑色圆形,上坐标轴);数据的线性拟合结果(实线)表明,两种情况下液滴体积均呈近似线性变化。本实验步骤 1 和步骤 2 分别使用 10 wt% 的葡聚糖溶液和 10 wt% 的聚乙二醇溶液。e 葡聚糖液滴体积随扩散时间的变化规律,步骤 1 通入 10 wt% 的葡聚糖溶液,步骤 2 通入 10 wt% 的聚乙二醇溶液;不同颜色代表不同的连接颈几何结构(所有连接颈的高度hn=200 μm、宽度wn=50 μm,蓝色、红色、黄色标记分别对应连接颈长度 160μm、260μm、310μm)。f 采用微型死端腔室(直径 50μm)生成微型葡聚糖液滴。g 低葡聚糖浓度下,结合离心力辅助生成微型葡聚糖液滴,左侧为离心力施加方式的原理示意图;蓝色圆形、方形、三角形分别对应微流控芯片的左、中、右三个区域。h 荧光显微镜下观察离心力辅助生成的微型葡聚糖液滴。f、g、h 的比例尺均为 50μm。
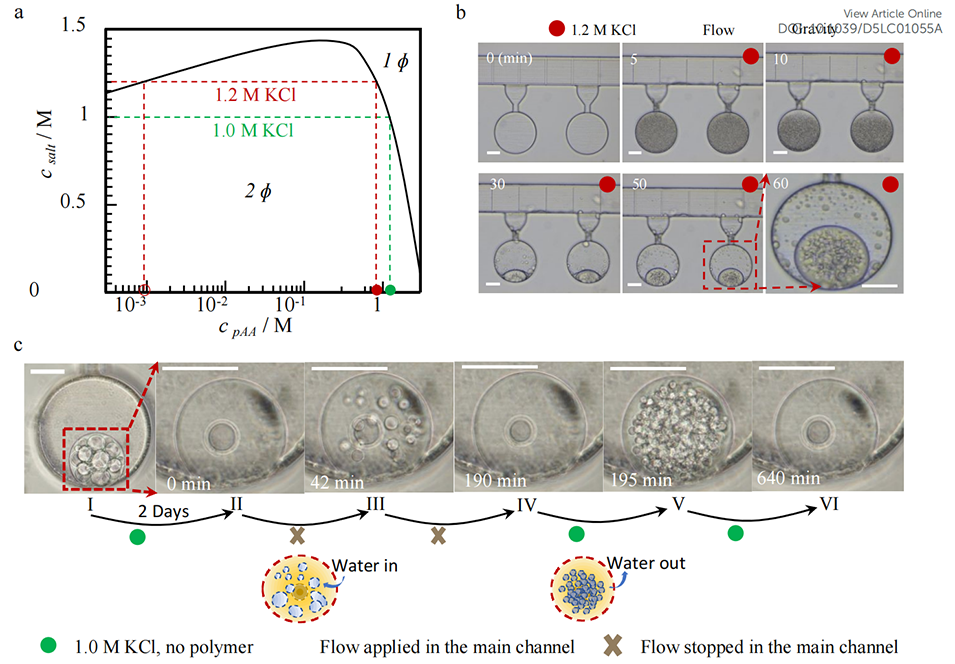
图4. 通过凝聚层相分离实现水包水(W/W)液滴的缔合型生成及可逆区室化。a 聚丙烯酸-聚甲基丙烯酸N,N-二甲基氨基乙酯体系的相图,该体系中缔合型复合凝聚层的生成条件为 pH=6.5(±0.2),此时体系正负电荷密度比为 1:1(聚丙烯酸分子量 100 kDa,聚甲基丙烯酸N,N-二甲基氨基乙酯分子量 104 kDa)。b 死端腔室中凝聚层的生成过程:步骤 1,器件内填充以 1.5 M 氯化钾稀释的 0.33 M 聚丙烯酸和 0.33 M 聚甲基丙烯酸N,N-二甲基氨基乙酯均相溶液;步骤 2,5 分钟时注入 1.2 M 氯化钾溶液以诱导相分离,并将器件竖直放置,促进分离后的凝聚层在死端腔室底部聚并。60 分钟时,单个凝聚层液滴内可观察到多个区室。c 凝聚层可逆区室化过程的时序图像:图 I,主通道通入 1.0 M 氯化钾溶液时,初始生成的含多个区室的凝聚层;图 II,经 2 天平衡后,凝聚层内除一个区室外,其余区室均消失;图 III,停止主通道 1.0 M 氯化钾溶液的通液后,区室重新形成;图 IV,经 148 分钟再次平衡,凝聚层液滴恢复至图 II 的状态;图 V,恢复主通道 1.0 M 氯化钾溶液通液后,5 分钟内凝聚层内快速重新形成多个区室;图 VI,最终凝聚层液滴达到新的准平衡状态,多个区室逐渐消失。图 II 至图 VI 左下角的时间刻度为停止 1.0 M 氯化钾溶液通液后的时长。示意图对应图 II 至图 III、图 IV 至图 V 的转变过程,分别展示了水向凝聚层内的流入和向层外的流出过程。所有图像的比例尺均为 100μm。
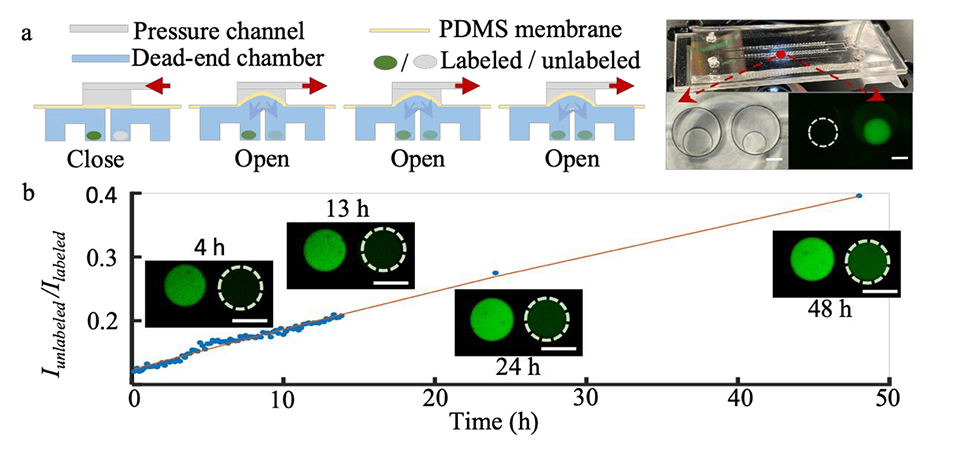
图5. 微流控芯片中的液滴间通讯。a 左侧:实现可控液滴间通讯的阀门机制原理示意图,该微流控器件包含三个核心部件:气压控制通道、聚二甲基硅氧烷膜和两个独立的死端腔室(与图 1a 所示腔室结构相似);右侧:器件实物图,以及经气动阀连通的通道中两个葡聚糖液滴的显微图像(明场 + 荧光),其中一个液滴经异硫氰酸荧光素荧光标记,另一个未标记。b 荧光强度比随时间的变化曲线及数据的线性拟合结果。比例尺:100μm。
论文链接:https://doi.org/10.1039/D5LC01055A
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














