
导读:
针对口干症现有治疗手段效果有限、副作用明显等问题,南通大学附属医院顾志峰教授、朱玉娟教授团队研发出一种基于微流控技术的口腔粘膜粘附性纳米酶微球系统(adCe-MS),为干燥综合征相关口干症的治疗提供了新型靶向策略。相关研究以“Microfluidic-based oral mucoadhesive nanozyme microspheres for immune modulation of xerostomia”为题目,发表于期刊《Materials Today Bio》。
本文要点:
1、材料设计与制备:adCe-MS 以负载氧化铈纳米颗粒(CeNP)的海藻酸钠微球为核心,外层包覆由明胶和交联聚丙烯酸构成的粘膜粘附水凝胶(adGel),通过微流控电喷雾技术制备,微球粒径 200-350μm,CeNP 包封率达 84.89%±2.93%;该水凝胶具备优异的湿组织粘附性、机械弹性(断裂伸长率超 400%),可在口腔动态湿润环境中稳定粘附。
2、核心成分特性:CeNP 具有可逆的 Ce³⁺/Ce⁴⁺氧化还原循环,模拟超氧化物歧化酶和过氧化氢酶活性,能高效清除活性氧(ROS),且生物相容性良好,可显著抑制巨噬细胞中促炎因子 TNF-α、IL-6 的分泌;adCe-MS 可在口干症病理环境中高表达的胶原酶作用下,7 天内完全降解并持续释放 CeNP。
3、体外实验验证:adCe-MS 无明显细胞毒性,能有效缓解 H₂O₂诱导的巨噬细胞氧化应激和炎症反应,水凝胶基质自身也可释放含 RGD 基序的活性肽,辅助发挥抗炎抗氧化作用,且可紧密粘附于小鼠舌组织,实现口腔局部滞留。
4、体内动物实验效果:在干燥综合征小鼠模型(NOD/LtJ 品系)中,经舌下黏膜局部施用 adCe-MS(每周两次,持续 4 周),可显著提升唾液分泌量,减少涎腺炎症细胞浸润,保护涎腺导管和腺泡结构完整性;同时上调涎腺功能关键分子 AQP5、下调异常表达的 MUC1,恢复唾液分泌功能,还能增加脾脏调节性 T 细胞比例、降低 M1 型巨噬细胞占比,减少抗 SSA/Ro、抗 SSB/La 自身抗体及促炎因子释放,缓解全身免疫激活。
5、分子机制解析:转录组分析显示,adCe-MS 通过显著下调 IL-17、TNF 等关键炎症通路及趋化因子(CCL2、CXCL1 等)的表达,同时上调淀粉酶家族、富含脯氨酸蛋白家族等唾液分泌相关基因,实现 “抑制炎症 - 促进分泌” 的双重治疗作用,且 CeNP 是该疗效的核心作用成分,与水凝胶载体协同增效。
6、研究优势与展望:相较于现有治疗,adCe-MS 为无创局部给药,规避了全身副作用和注射相关问题,释放特性适配病理微环境,且 CeNP 兼具抗菌、抗生物膜特性,可改善口干症口腔微生态失衡;该系统也为其他口腔炎症疾病的局部治疗提供了可转化的平台,未来将聚焦长期生物安全性评估、规模化生产和临床应用探索。
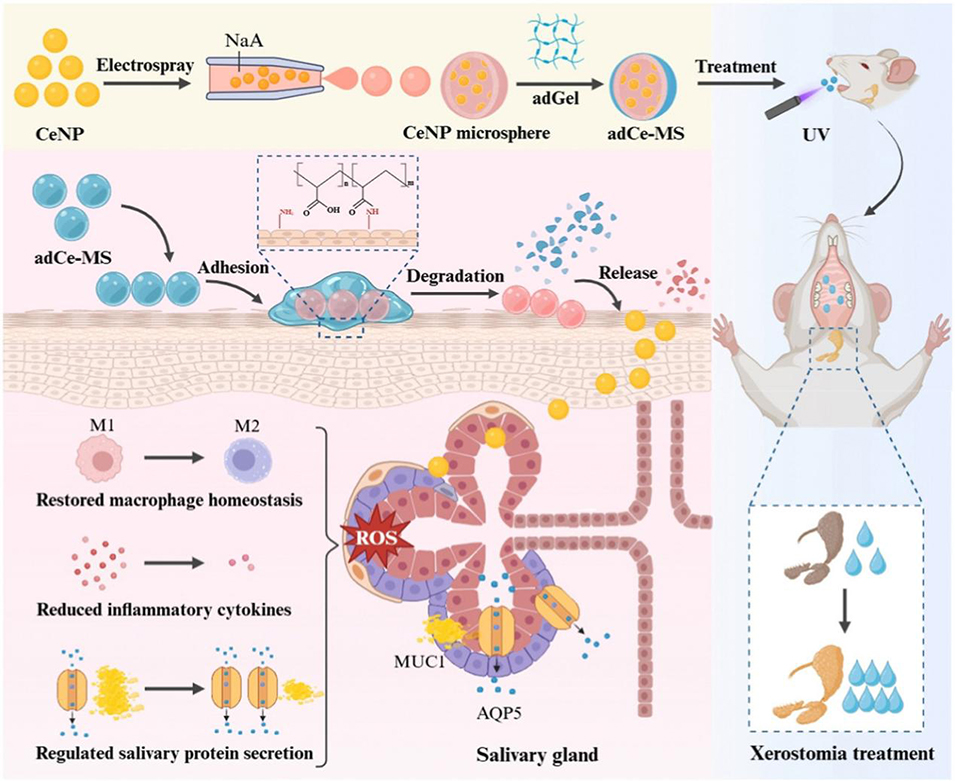
图1. 靶向治疗口干症的微纳递送系统(adCe-MS)示意图。先合成氧化铈纳米颗粒(CeNP),再通过微流控电喷雾技术将其包封于海藻酸钠(NaA)微球中,最后在微球外层包覆口腔粘性水凝胶。该分级微球系统在小鼠模型中展现出显著的治疗效果,为口干症的靶向治疗提供了全新策略。
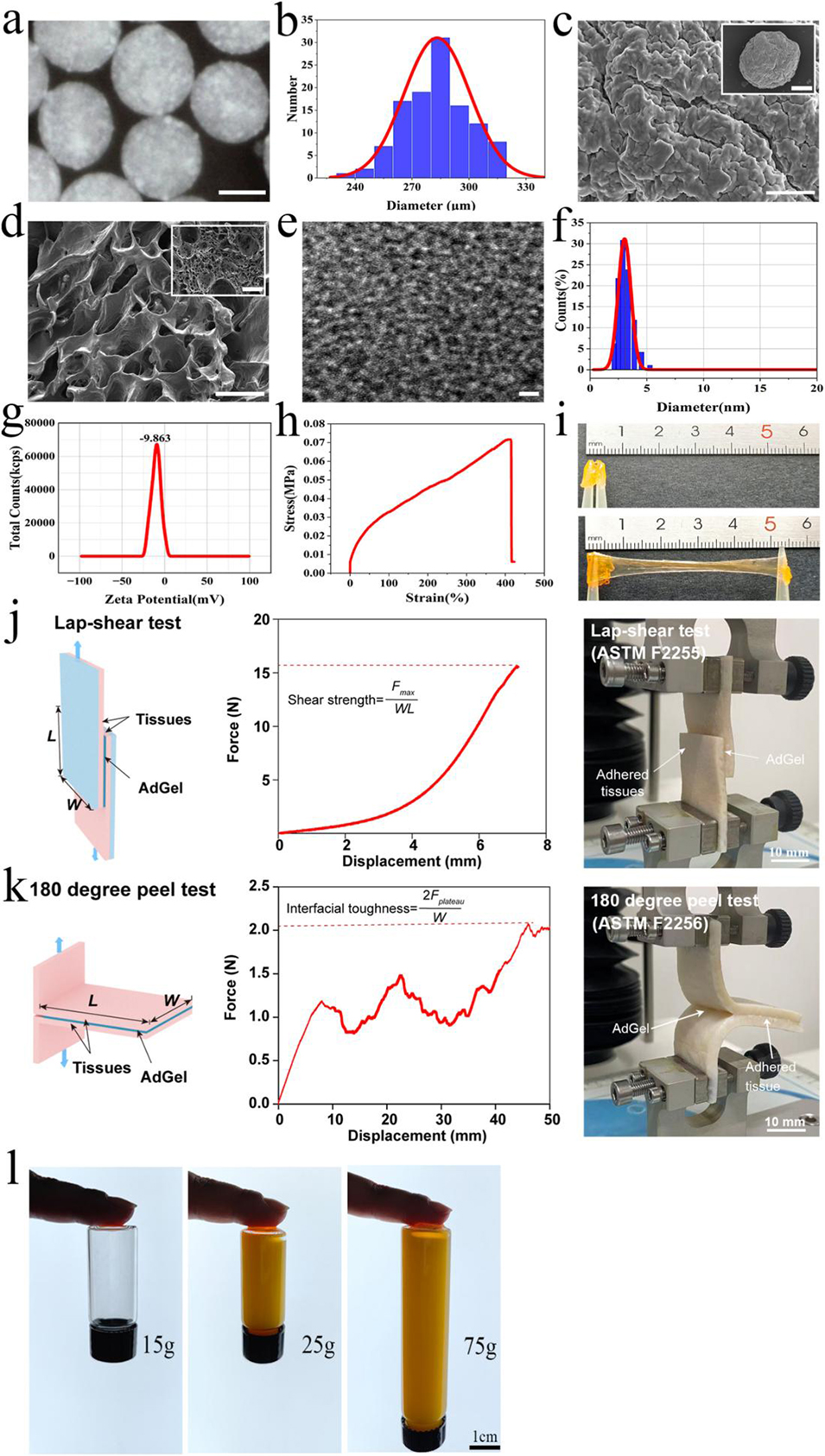
图2. 粘膜粘附性纳米酶功能化微球 adCe-MS 的制备与表征。a:adCe-MS 的明场图像,比例尺 150μm;b:微球的粒径分布;c:冻干后 CeNP - 海藻酸钠微球的扫描电镜(SEM)图像,上比例尺 50μm、下比例尺 5μm;d:adCe-MS 的扫描电镜图像,上比例尺 250μm、下比例尺 50μm;e:CeNP 的透射电镜(TEM)图像,比例尺 10nm;f:悬浮液中 CeNP 的水合粒径分布;g:CeNP 的 Zeta 电位;h-i:粘性水凝胶 adGel 的粘附性能;j:依据搭接剪切试验标准(ASTM F2255)测定的 adGel 剪切强度,比例尺 10mm;k:依据 180 度剥离试验标准(ASTM F2256)测定的 adGel 界面韧性,比例尺 10mm;l:adGel 的拉伸强度测定,比例尺 1cm。注:F 为作用力,Fmax 为搭接剪切试验中的最大作用力,Fplateau 为剥离试验中的平台作用力,L 为长度,W 为宽度。
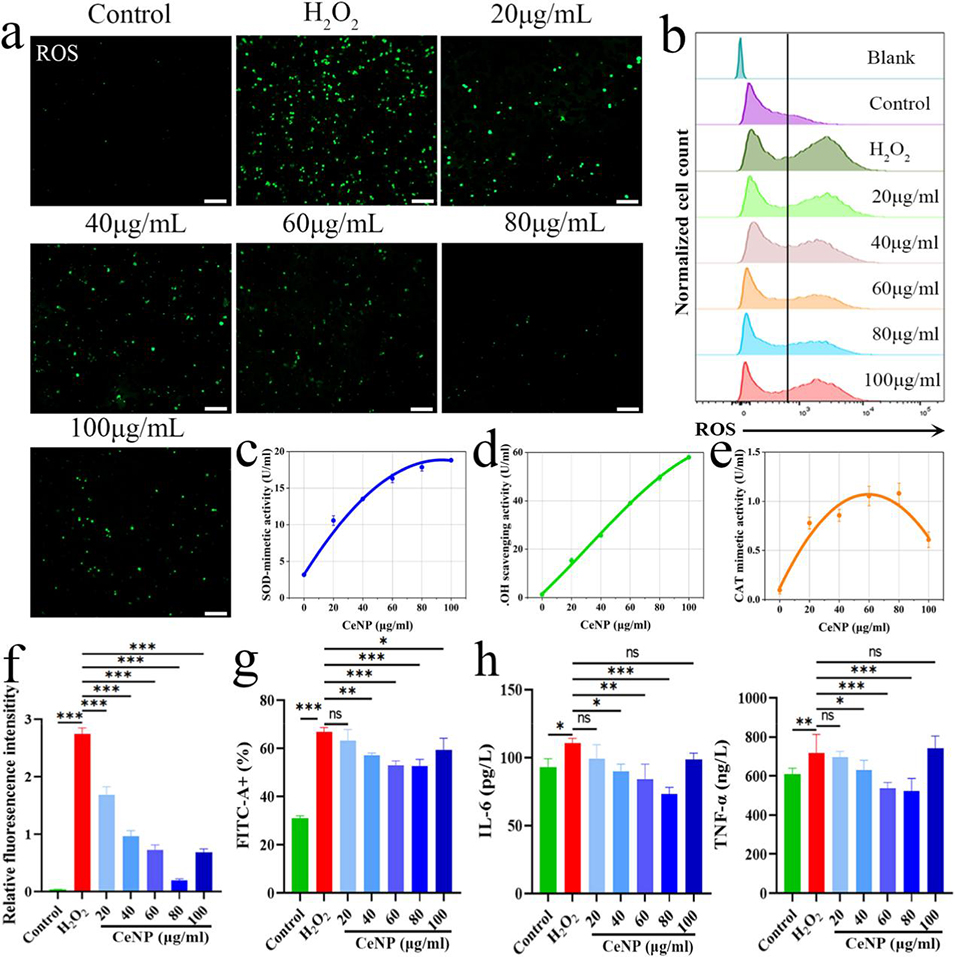
图3. CeNP 生物活性的功能表征。a:CeNP 在过氧化氢刺激的巨噬细胞中清除细胞内活性氧(ROS)的荧光图像,比例尺 100μm;b:流式细胞术检测的细胞内 ROS 水平;c:CeNP 的超氧化物歧化酶模拟活性;d:CeNP 的羟自由基清除能力;e:CeNP 的过氧化氢酶模拟活性;f:ROS 平均荧光强度的定量分析;g:流式细胞术检测的细胞内 ROS 水平定量分析;h:酶联免疫吸附试验(ELISA)检测巨噬细胞培养上清液中的细胞因子(肿瘤坏死因子 α、白细胞介素 6)水平。所有定量数据以均值±标准差表示(n=3),*P<0.05,**P<0.01,***P<0.001。
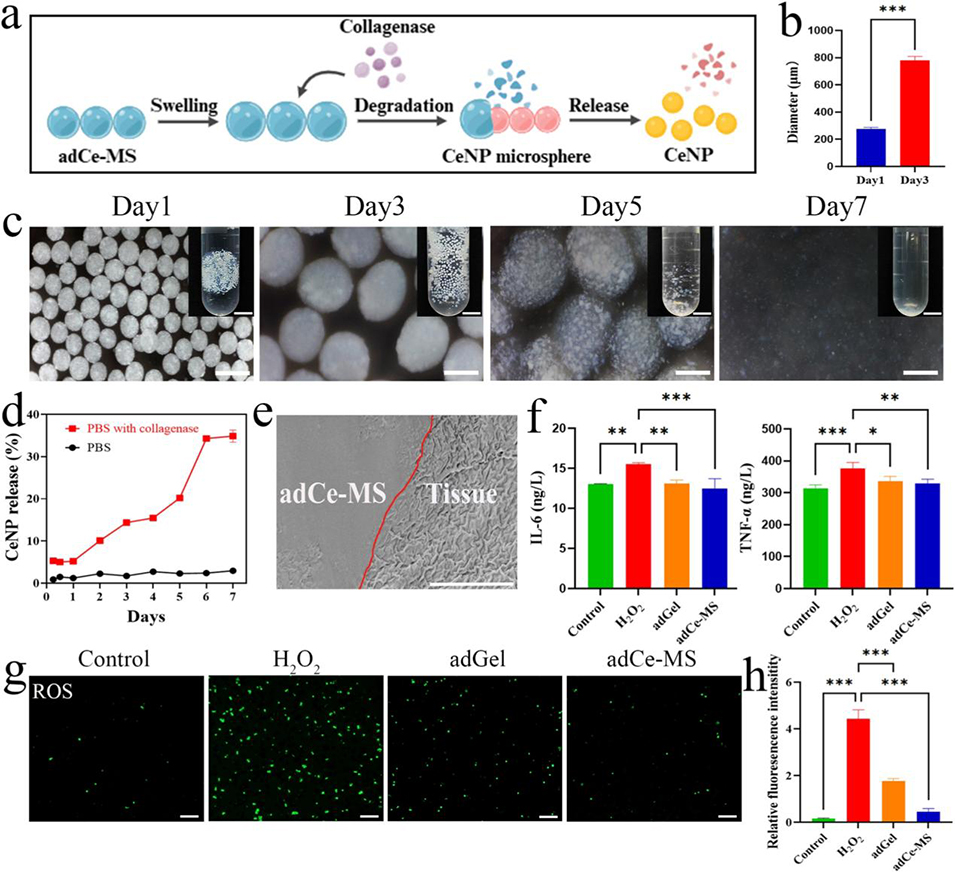
图4. adCe-MS 的体外功能评价与生物相容性。a:adCe-MS 的酶解过程示意图;b:降解过程中微球的粒径变化;c:adCe-MS 在含胶原酶的磷酸盐缓冲液中连续孵育后的形态变化,右比例尺 5mm、左比例尺 500μm;d:adCe-MS 在含/不含胶原酶的磷酸盐缓冲液中 CeNP 的累积释放曲线;e:adCe-MS 与小鼠舌组织粘附界面的扫描电镜图像(红线为融合边界),比例尺 10μm;f:酶联免疫吸附试验对细胞培养上清液中肿瘤坏死因子 α 和白细胞介素 6 释放量的定量检测;g:adGel 和 adCe-MS 的 ROS 清除活性,比例尺 100μm;h:ROS 平均荧光强度的定量分析。所有定量数据以均值±标准差表示(n=3),*P<0.05,**P<0.01,***P<0.001。
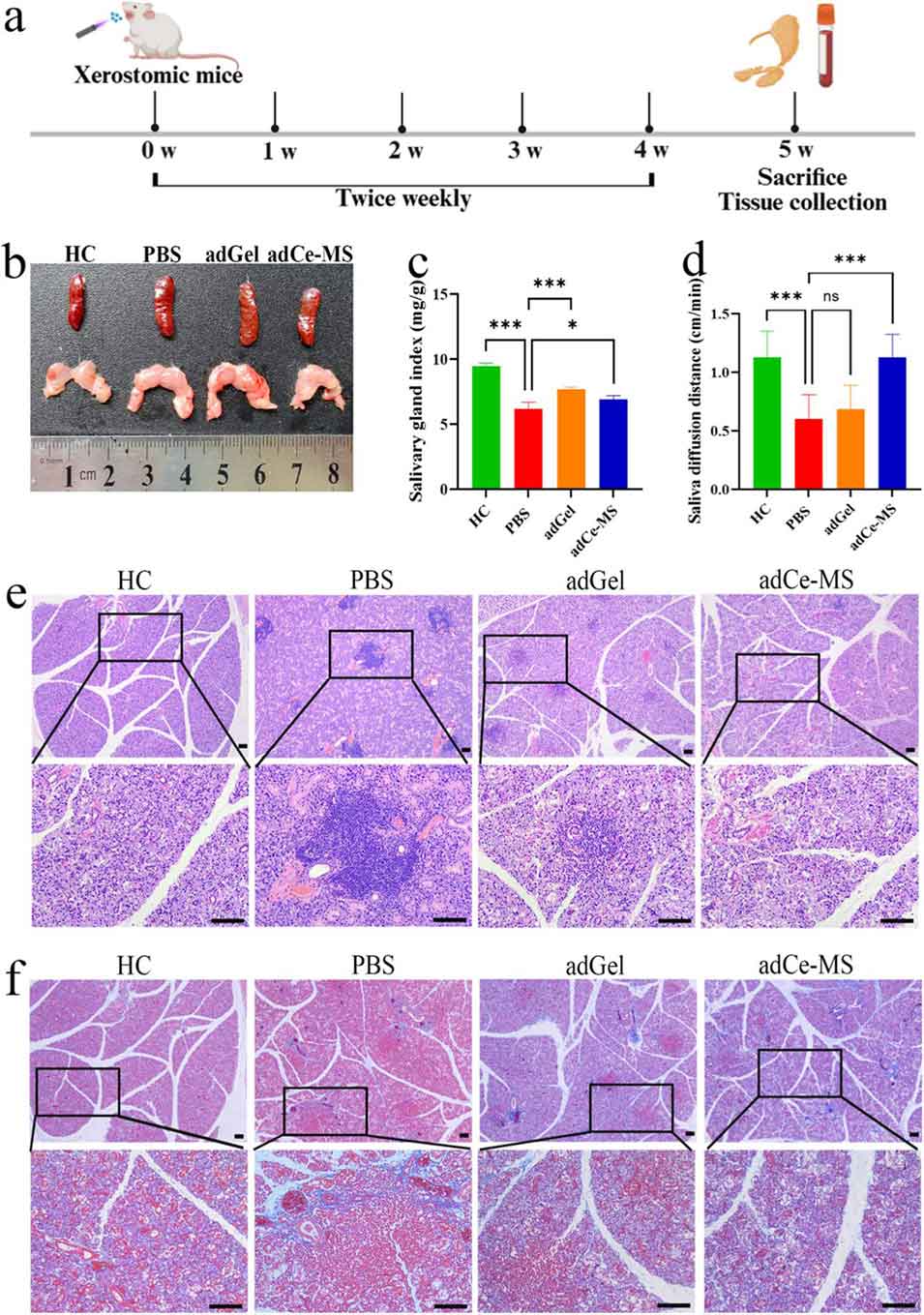
图5. adCe-MS 在口干症小鼠模型中的体内治疗效果。a:体内实验设计的时间表;b:不同处理组小鼠脾脏和涎腺的代表性大体图像;c:各实验组的涎腺指数(n=4);d:各实验组的刺激后唾液分泌量检测(n=6);e:不同组小鼠颌下腺的苏木精-伊红(H&E)染色代表性切片,比例尺 100μm;f:不同组小鼠颌下腺的马松(Masson)染色代表性切片,比例尺 100μm。所有定量数据以均值±标准差表示(n=3),*P<0.05,**P<0.01,***P<0.001。
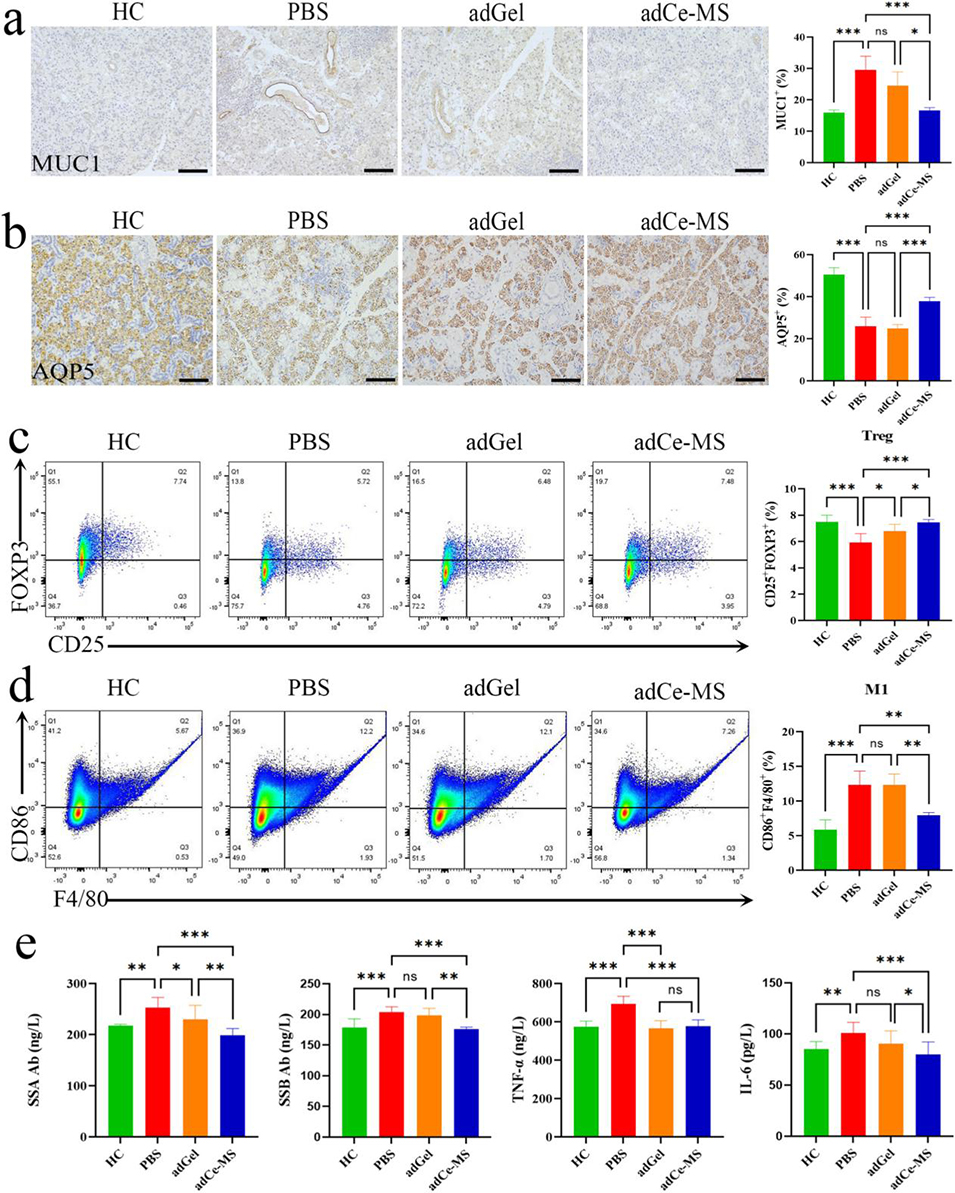
图6. adCe-MS 治疗后口干症小鼠的全身免疫调控作用及颌下腺功能恢复情况。a-b:颌下腺组织中粘蛋白 1(MUC1)(a)和水通道蛋白 5(AQP5)(b)表达的免疫组织化学分析(n=4),比例尺 100μm;c:流式细胞术检测的小鼠脾脏中调节性 T 细胞(CD25⁺FOXP3⁺)比例(n=8);d:流式细胞术检测的小鼠脾脏中 M1 型极化巨噬细胞(F4/80⁺CD86⁺)比例(n=8);e:酶联免疫吸附试验检测的小鼠血浆中自身抗体(抗干燥综合征 A 抗体、抗干燥综合征 B 抗体)和促炎细胞因子(肿瘤坏死因子 α、白细胞介素 6)水平(n=8)。数据以均值±标准差表示,*P<0.05,**P<0.01,***P<0.001。
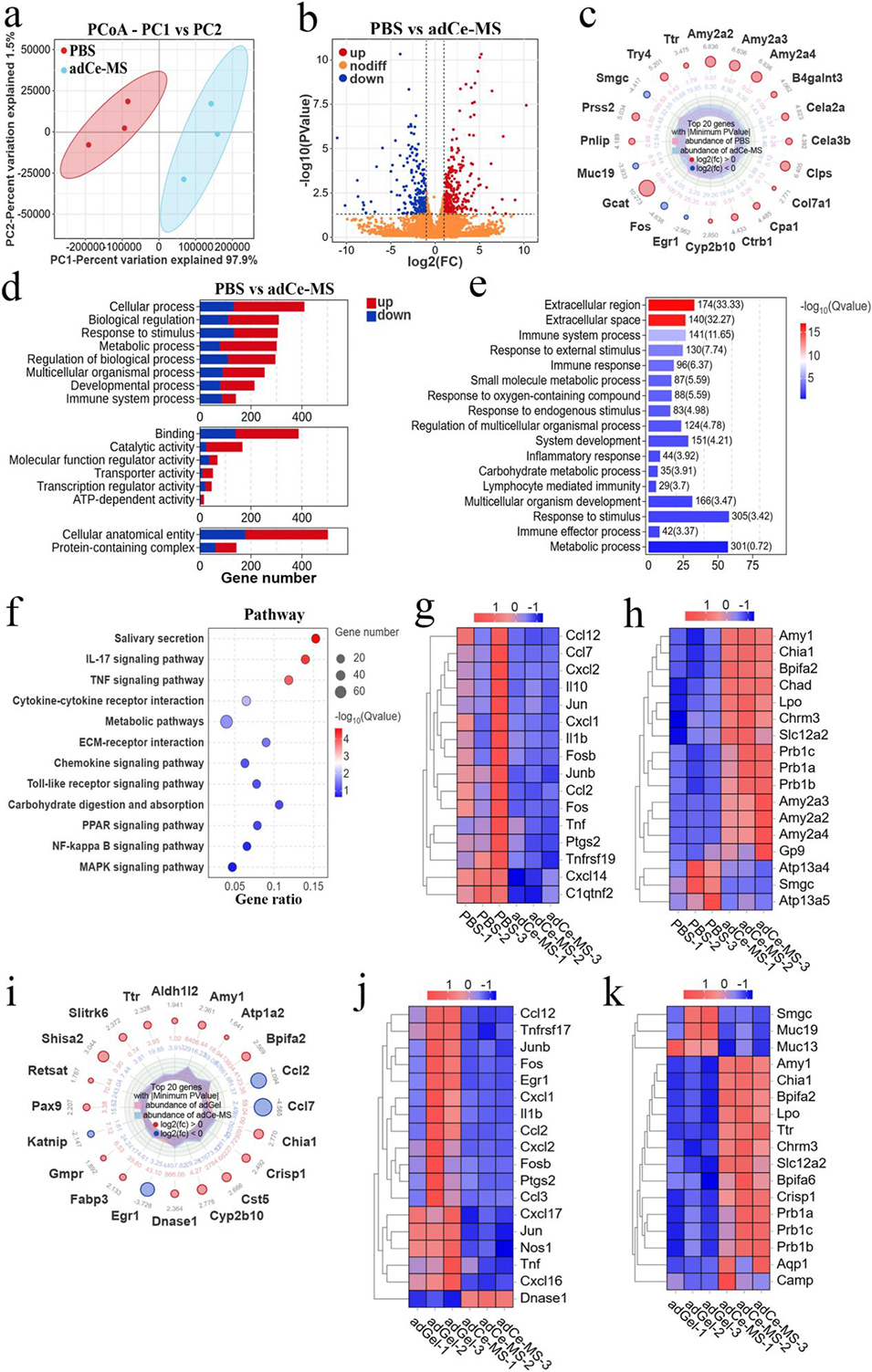
图7. 转录组分析揭示 adCe-MS 介导口干症小鼠恢复的分子机制。a:adCe-MS 处理组与磷酸盐缓冲液处理组小鼠颌下腺转录组的主坐标分析;b:磷酸盐缓冲液处理组与 adCe-MS 处理组之间差异表达基因的火山图;c:磷酸盐缓冲液处理组与 adCe-MS 处理组间表达差异最显著的 20 个基因雷达图;d:差异表达基因的基因本体(GO)功能分类;e:差异表达基因的基因本体富集分析;f:差异表达基因的京都基因与基因组百科全书(KEGG)通路富集分析;g:磷酸盐缓冲液组与 adCe-MS 组炎症相关基因表达的热图;h:磷酸盐缓冲液组与 adCe-MS 组唾液分泌相关基因表达的热图;i:adGel 处理组与 adCe-MS 处理组间表达差异最显著的 20 个基因雷达图;j:adGel 组与 adCe-MS 组炎症相关基因表达的热图;k:adGel 组与 adCe-MS 组唾液分泌相关基因表达的热图。
论文链接:https://doi.org/10.1016/j.mtbio.2026.102914
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














