膝关节骨关节炎(OA)是全球最常见的关节疾病之一,疼痛为其主要症状,严重影响患者生活质量。膝动脉栓塞术(GAE)为约20%处于“治疗缺口”的患者提供了新的治疗选择——这类患者对保守治疗反应不佳,却又不适宜接受全膝关节置换术。透明质酸(HA)因其良好的生物相容性、可降解性和低免疫原性,成为开发GAE栓塞剂的理想材料。加之HA已获FDA批准用于关节内注射,进一步降低了其临床转化门槛。然而,仅通过调节交联剂浓度难以同时优化微球的粒径、力学性能与降解时间,这是目前HA微球走向应用的关键瓶颈。

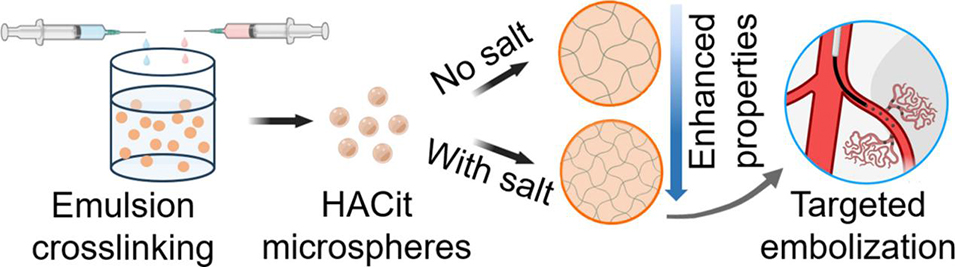
近期,加拿大多伦多大学研究团队通过引入柠檬酸钠处理技术,在交联前调控HA链的排列与相互作用,成功制备出粒径适宜、力学强度增强且降解时间可调的HA微球。该微球在体外实验中表现出良好的栓塞稳定性和细胞相容性,为GAE提供了一种极具潜力的可降解栓塞剂选项。相关研究以“Biodegradable sodium citrate-treated hyaluronic acid microspheres for genicular artery embolization”为题目,发表在期刊《Acta Biomaterialia》上。
本文要点:
1、该研究聚焦膝骨关节炎(OA)治疗,针对现有膝动脉栓塞术(GAE)用栓塞剂存在的非降解性、形状不佳等问题,研发了一种基于透明质酸(HA)的生物可降解微球栓塞剂。
2、通过乳液交联技术,结合柠檬酸钠(Cit)处理,制备出不同柠檬酸钠浓度(0-20% w/v)的BDDE交联HA微球(HACit-0至HACit-20)。
3、优化后的HACit-10微球(10%Cit处理)具有理想特性:粒径在75-300 μm(平均151±53 μm),符合GAE需求;机械强度增强,能稳定阻塞微通道;体外降解时间约56±4 h,契合临时栓塞的治疗窗口;经NMR验证柠檬酸钠完全去除,仅含FDA批准的BDDE交联HA;对人脐静脉内皮细胞(HUVECs)和人真皮成纤维细胞(HDFs)具有良好细胞相容性,且注射性佳、无导管堵塞风险。
4、该微球克服了现有栓塞剂的诸多局限,为GAE提供了安全有效的新型临时栓塞剂,有望改善OA患者的治疗效果与生活质量。
在HA微球制备中,柠檬酸钠(Cit)作为盐处理剂,核心作用是调控HA微球的物理与功能特性,而非直接参与交联。
Cit加入HA预凝胶溶液后,通过影响HA链的构象与链间相互作用,增加交联密度并使HA链排列更致密,进而实现三方面调控:① 粒径轻微减小(从 195±55 μm 降至 151±53 μm);② 溶胀比显著降低(从 24.3±3.5 降至 7.4±0.1),结构更致密;③ 降解时间延长(从 33±3 h 至 56±4 h)、机械强度提升,且这些特性经BDDE化学交联后稳定锁定,Cit最终通过洗涤完全去除,不残留于成品微球中。
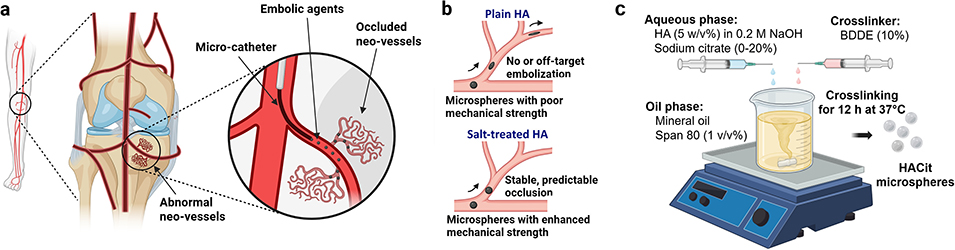
图1.(a)膝动脉栓塞术(GAE)通过微导管递送栓塞剂,选择性阻塞异常新生血管。(b)栓塞剂需具备特定机械强度以确保稳定阻塞。机械强度不足的微球(如普通透明质酸微球)质地过软,无法抵抗血压和剪切力,易发生显著变形,导致无法稳定阻塞或出现脱靶栓塞;而经盐处理的透明质酸微球等质地更坚硬的微球可避免该问题。(c)通过乳液交联法制备 HACit 微球。
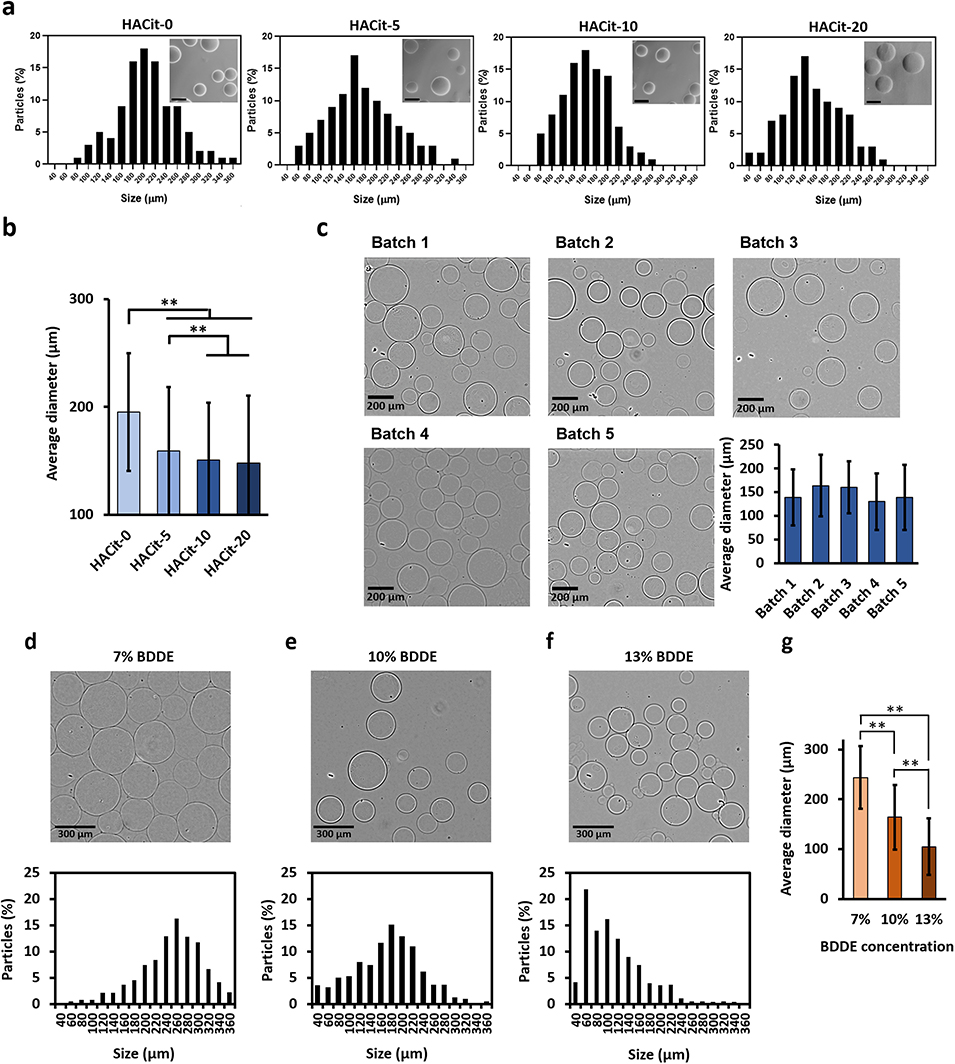
图2.(a)HACit 微球的粒径分布。插图为代表性光学显微镜图像(比例尺:200 µm)。(b)HACit 微球的平均直径,每组至少测量 600 个微球。(c)5 个独立批次 HACit-10 微球的形态和平均粒径,体现批次一致性(比例尺:200 µm),每批至少测量 800 个微球。(d-f)BDDE 浓度对 HACit-10 微球形态和粒径分布的影响(比例尺:300 µm)。(g)不同 BDDE 浓度制备的 HACit-10 微球平均粒径,每组至少测量 800 个颗粒。柱状图数据以 “平均值 ± 标准差” 表示,**p<0.01。
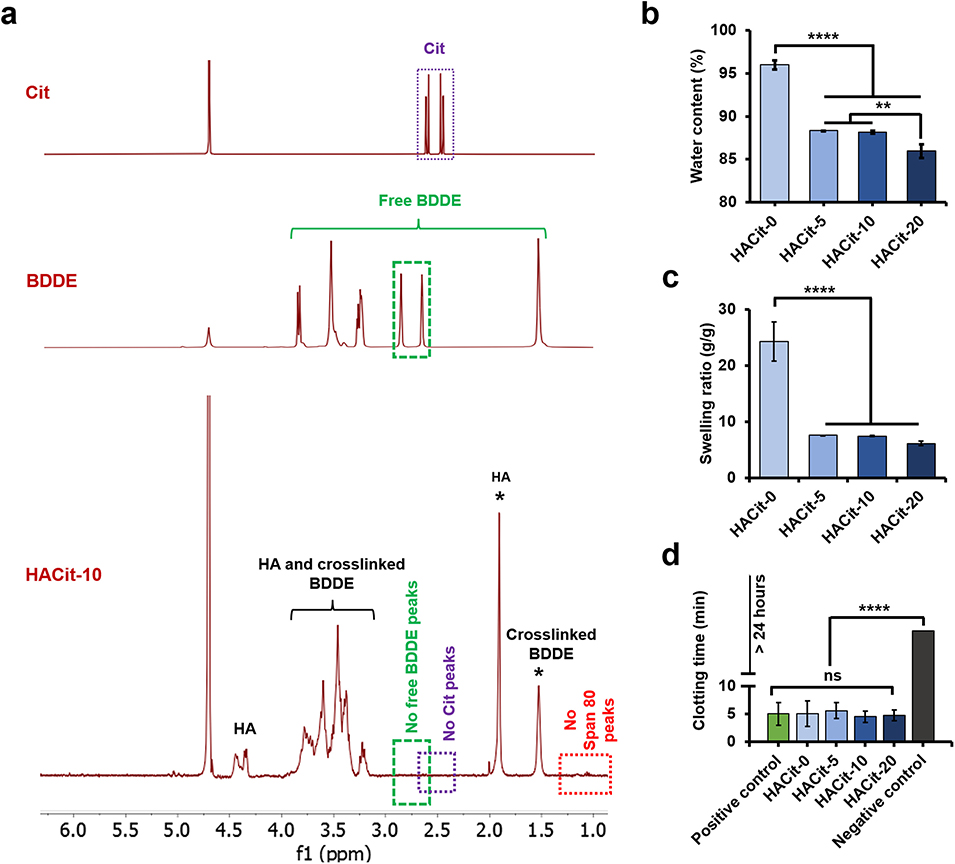
图3.(a)游离柠檬酸钠(Cit)、游离 1,4 - 丁二醇二缩水甘油醚(BDDE)及 HACit-10 微球在氘代水(D₂O)中的核磁共振(¹H-NMR)光谱。(b)HACit 微球在 37℃ PBS 中达到平衡溶胀后的含水量。(c)HACit 微球在 37℃ PBS 中达到平衡溶胀后的溶胀比。(d)HACit 微球与牛血浆在 37℃孵育后的凝血时间。柱状图数据以 “平均值 ± 标准差” 表示,N=3,**p<0.01,****p<0.0001。
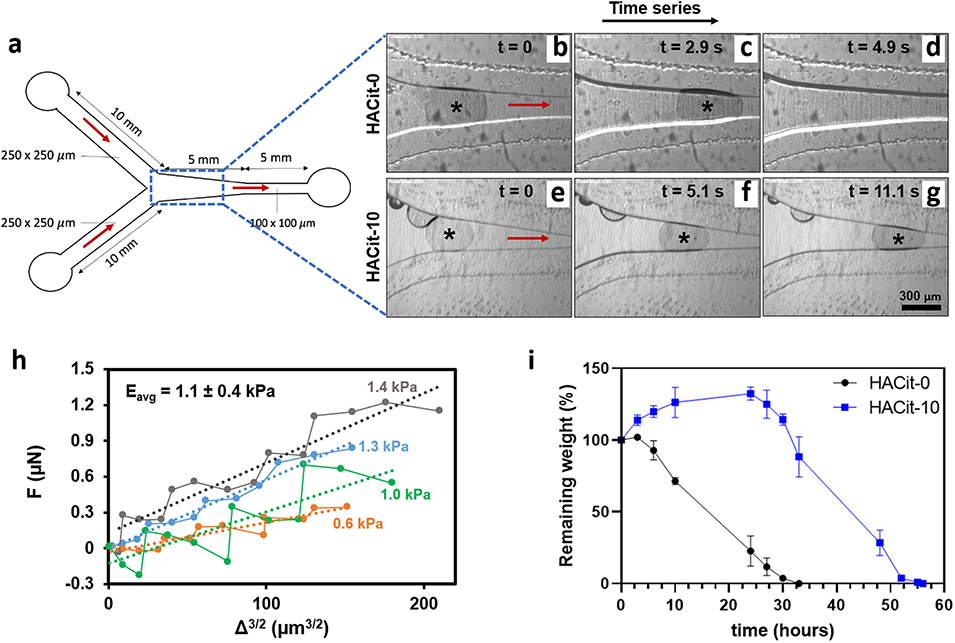
图4.(a)Y 形微通道设计示意图。(b-g)多次注射 0.2 mL HACit-0(b-d)或 HACit-10(e-g)后,微球在 Y 形 PDMS 微通道瓶颈处的动态变化时序图。红色箭头指示流动方向,星号标记微球位置。(h)HACit-10 微球的力-位移数据,每条实线代表一次实验,虚线旁数值为根据公式(3)计算的弹性模量 E。(i)HACit-0 和 HACit-10 微球在 7 U/mL 透明质酸酶作用下的体外降解行为。数据以 “平均值 ± 标准差” 表示,N=3。
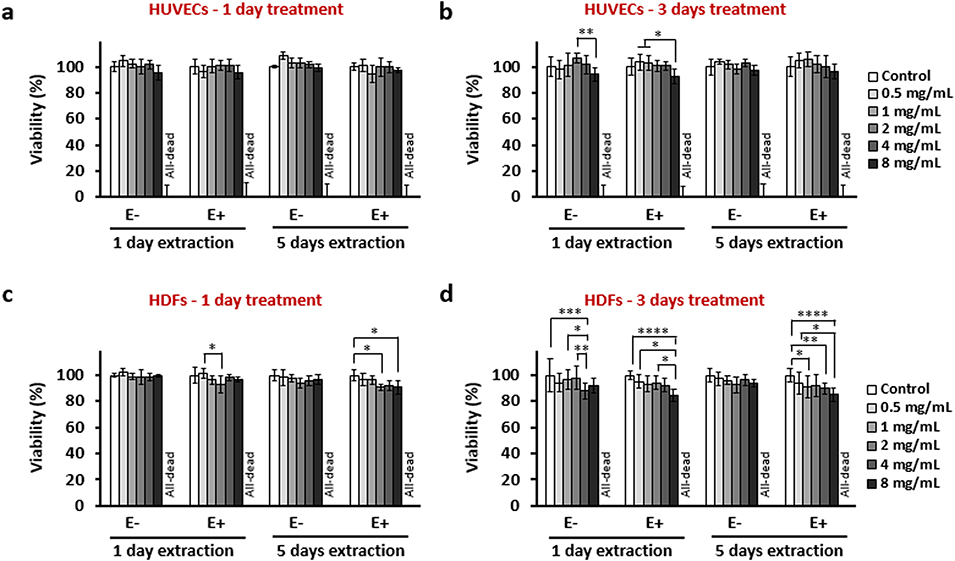
图5. 通过间接 MTT 法评估细胞存活率:人脐静脉内皮细胞(HUVECs)(a、b)和人真皮成纤维细胞(HDFs)(c、d)分别经浸提液处理 1 天(a、c)或 3 天(b、d)。浸提液制备方式为:将 HACit-10 微球按不同浓度(0.5、1、2、4、8 mg/mL,干重)在含或不含透明质酸酶(E + 表示含酶,E - 表示不含酶)的完全培养基中孵育 1 天或 5 天。阴性对照为未处理细胞(存活率 100%),阳性对照为经 20% 二甲基亚砜(DMSO)处理的细胞(全部死亡,存活率 0%)。数据以 “平均值 ± 标准差” 表示,N=6,*p<0.05,**p<0.01,***p<0.001,****p<0.0001。
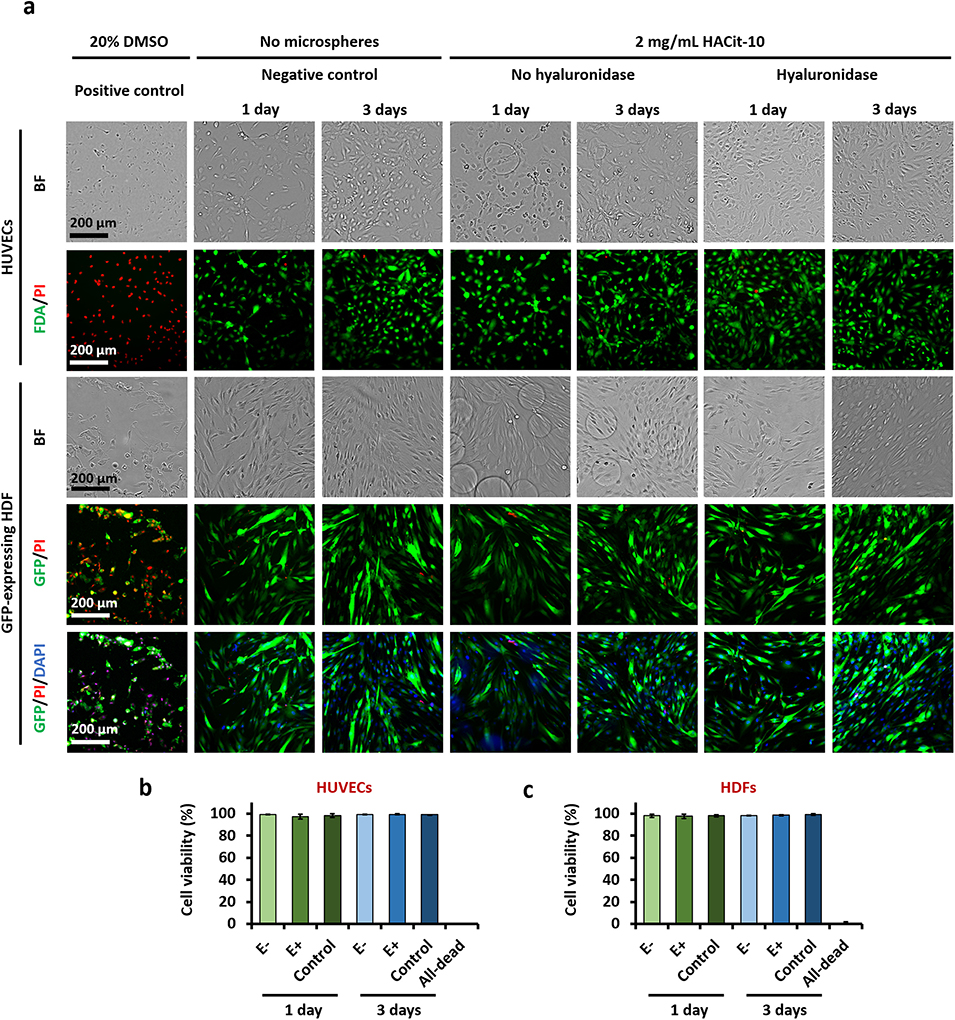
图6.(a)人脐静脉内皮细胞(HUVECs)和人真皮成纤维细胞(HDFs)与 HACit-10 微球共培养 1 天或 3 天的明场(BF)和荧光图像。不含透明质酸酶时,微球保持完整;含透明质酸酶时,微球完全降解。HUVECs 用荧光素二乙酸酯(FDA,绿色,标记活细胞)和碘化丙啶(PI,红色,标记死细胞)染色;表达绿色荧光蛋白(GFP,绿色)的 HDFs 额外用 PI(红色)和 4',6 - 二脒基 - 2 - 苯基吲哚(DAPI,蓝色)染色以精准计数单个细胞。(b、c)基于活/死染色的 HUVECs(b)和 HDFs(c)存活率定量分析。柱状图数据以 “平均值 ± 标准差” 表示,N=3。
论文链接:https://doi.org/10.1016/j.actbio.2026.01.003
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














