皮肤作为人体最大组织,是抵御外界刺激的天然屏障,但大面积深度创面(如全层烧伤)因炎症反应失调、血管生成受损,存在渗出液过多、感染风险高、愈合延迟等临床挑战。传统水凝胶微球虽在组织再生中展现潜力,但受限于高生产成本、复杂制备工艺、依赖外源生物活性添加剂,且批量乳化法制备的微球尺寸不均一,微流控法产量低、设备复杂,难以临床转化。因此,开发兼具简化制备、内在生物活性的微凝胶成为创面治疗的关键需求。

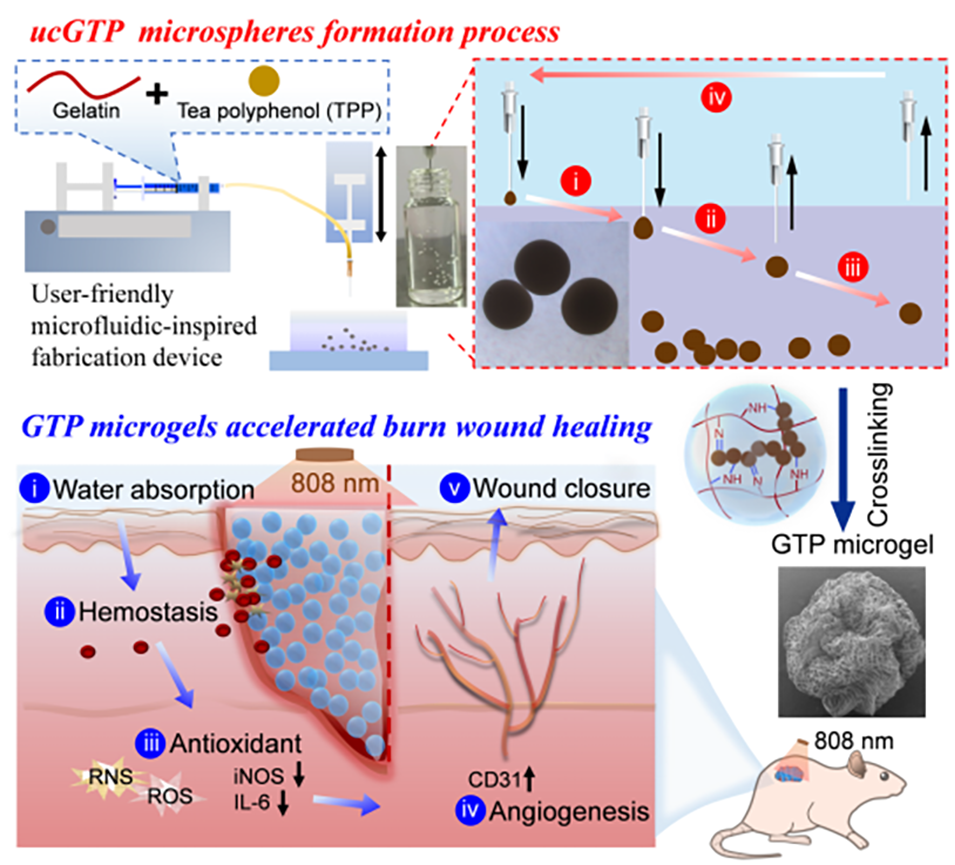
近期,扬州大学医学部陈建美博士团队提出一种受微流控启发的简易制备策略,成功开发出具有内在生物活性的明胶-茶多酚微凝胶(GTP microgels)。该材料集成了优异的止血性能、强大的抗氧化活性以及稳定的近红外光热效应,无需依赖任何外源药物添加,为烧伤创面治疗提供新方案。相关研究以“Microfluidics‐Inspired Microgels with Intrinsic Bioactivity for Advanced Burn Wound Therapy”为题目,发表于期刊《Advanced Healthcare Materials》。
本文要点:
1、本研究报道了一种多功能明胶-茶多酚微凝胶,通过简化、低成本的微流控启发平台制备。该平台可精确控制微球直径(125–570 μm),并经原位交联形成稳定(>28天)、快速吸水(1分钟内>300%)的GTP微凝胶。
2、这些微凝胶具备优异的止血性能、强大抗氧化活性和良好光热效应。在小鼠烧伤模型中,结合光热刺激的GTP微凝胶能通过减轻炎症和促进血管生成来加速伤口愈合。
3、该研究将止血、抗炎和促血管生成等内在治疗功能与简化制备工艺相结合,为高级伤口管理提供了一种具有临床可行性的新策略。
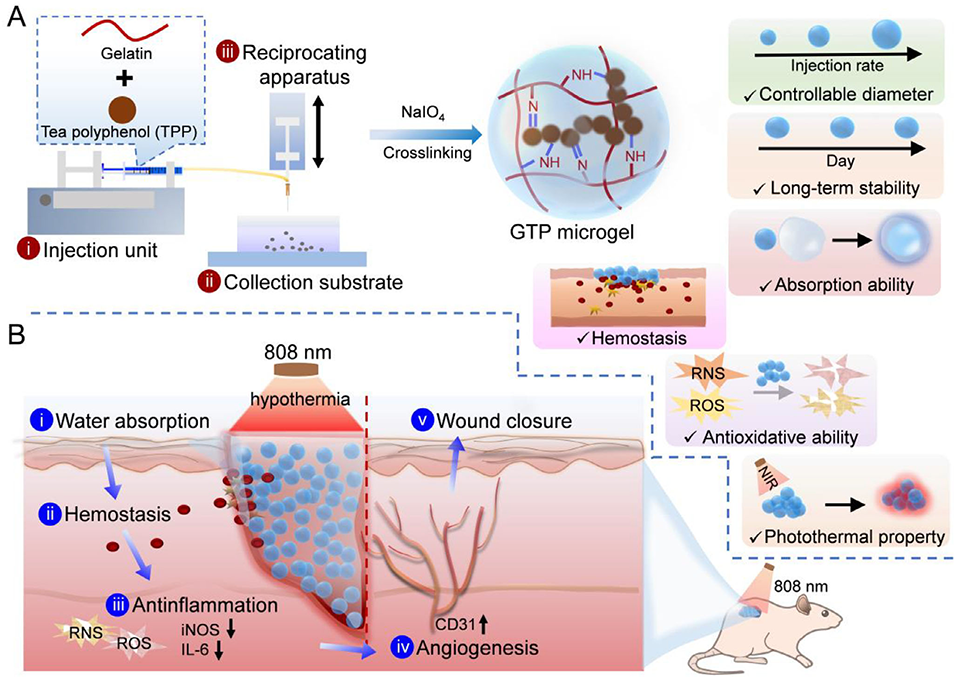
Scheme 1:明胶-茶多酚微凝胶的制备及其在创面愈合中的治疗功能示意图
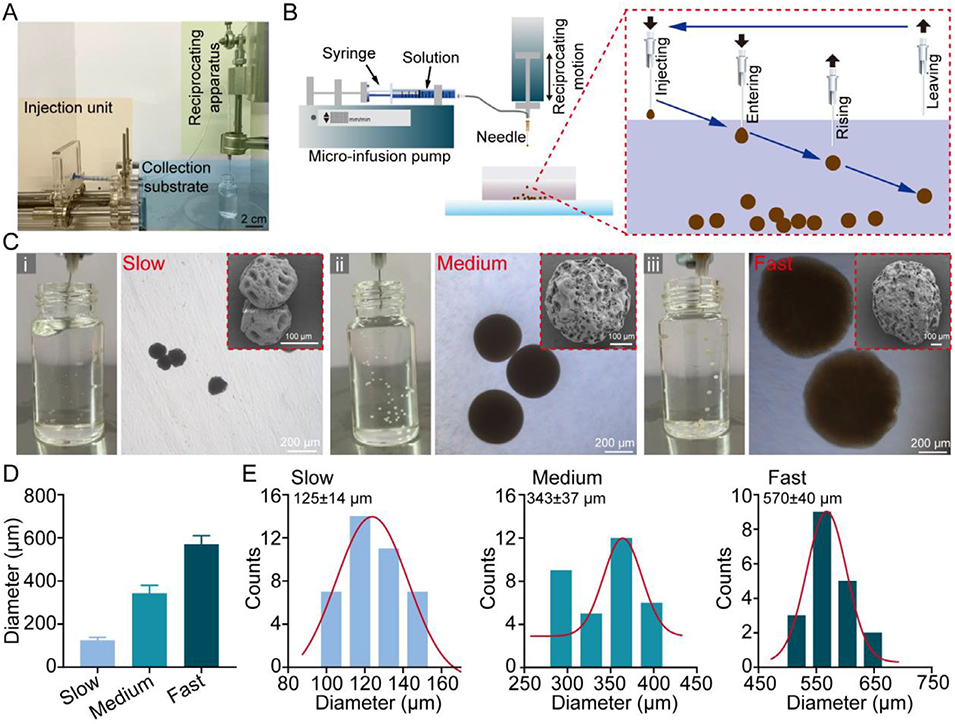
图1:未交联明胶-茶多酚微球的制备与表征
该多功能明胶-茶多酚(GTP)微凝胶的制备过程可分为以下几个关键步骤:
前体溶液配制
首先,将明胶(10% w/v)和茶多酚(TPP)(2% w/v)混合,制备成水相的前体溶液。
液滴生成
使用自制的微流控模拟装置,该装置主要包括:① 注射单元:装载有前体溶液的注射器,连接一个精密推注泵,用于精确控制溶液的推出速率。② 往复装置:带动注射器进行垂直的上下往复运动(频率为2 Hz)。③ 收集基底:一个装有石蜡油的容器,作为接收液滴的油相。
在推注泵的推动下,前体溶液通过金属针头被注入到石蜡油中。当溶液在针头末端与油相接触时,在界面张力和剪切力的作用下,会形成球状液滴。随着往复装置将针头向上移动,液滴在油相表面张力作用下与针头分离,并沉降到收集基底中,形成未交联的GTP(ucGTP)微球。通过调节推注泵的注射速率,可精确控制微球的直径。
预固化与清洗
生成的ucGTP微球在-20°C下冷冻2小时进行初步固化。随后,通过离心、并用乙醇洗涤的方法,去除包裹在微球周围的石蜡油。
原位交联
将清洗后的ucGTP微球分散在高碘酸钠(NaIO₄)溶液中。NaIO₄作为氧化剂,将TPP中的儿茶酚基团氧化成醌式结构(该结构不仅是交联反应的活性位点,也是微凝胶后续实现近红外光热效应的关键基础)。这些醌式结构随后与明胶分子链上的氨基发生共价交联反应(主要通过席夫碱反应和迈克尔加成反应),从而形成最终稳定的、具有三维网络结构的GTP微凝胶。
后处理
交联反应完成后,用水冲洗微凝胶以去除残留的化学物质,然后进行空气干燥,得到最终产物。
整个过程巧妙地模拟了微流控技术精准生成液滴的核心优势,但通过简化的往复注射和批量收集,克服了传统微流控设备复杂、产量低的缺点,实现了单分散性良好、尺寸可控且可规模化制备的多功能微凝胶。
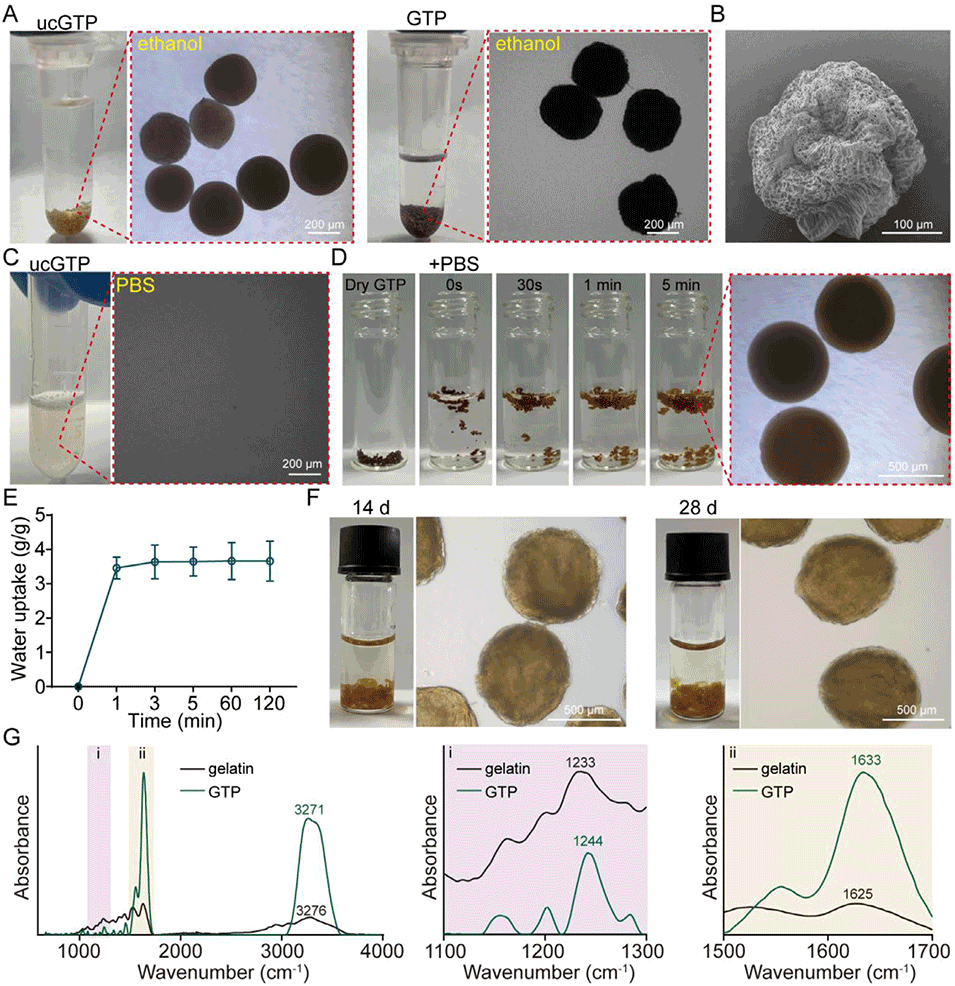
图2:明胶-茶多酚微凝胶的表征
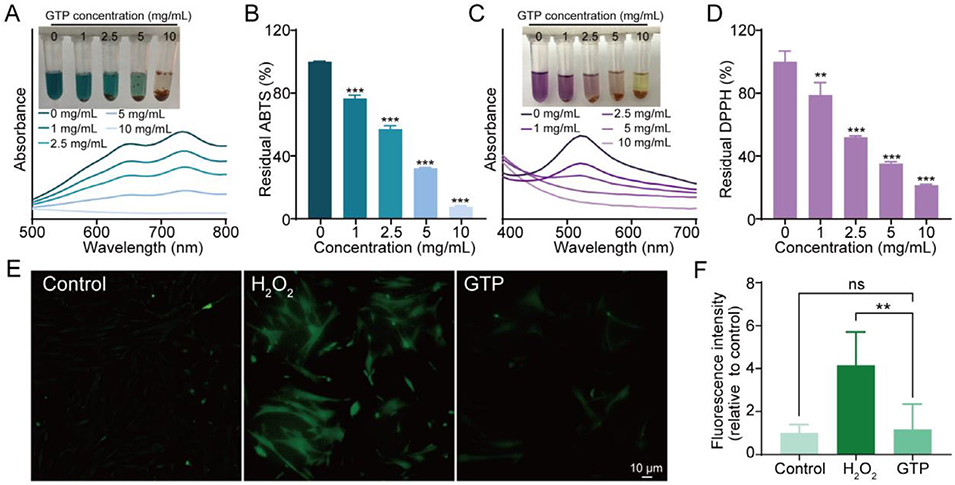
图3:明胶-茶多酚微凝胶的抗氧化能力
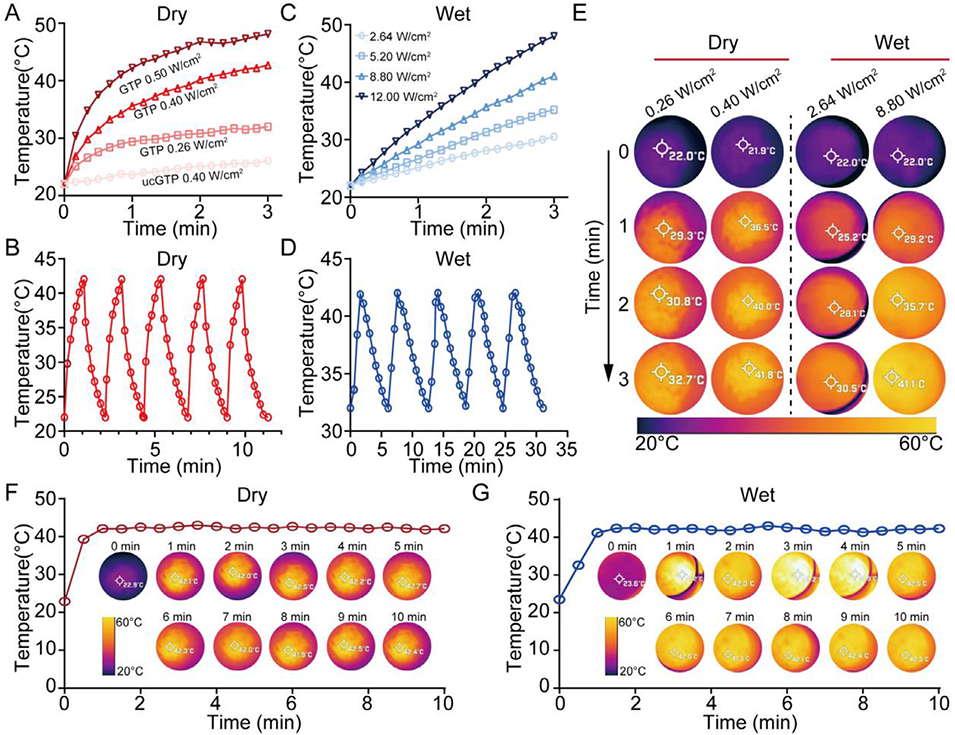
图4:明胶-茶多酚微凝胶的光热性能
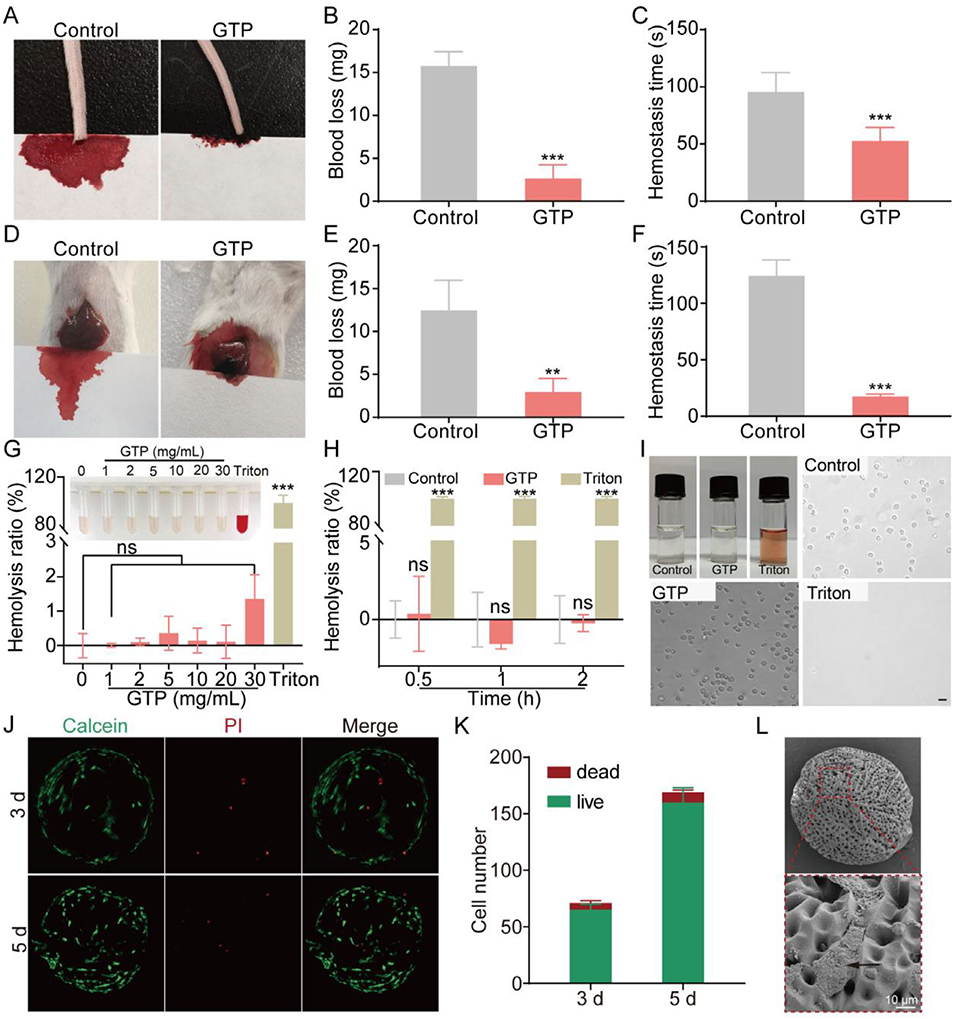
图5:明胶-茶多酚微凝胶的止血性能与细胞相容性
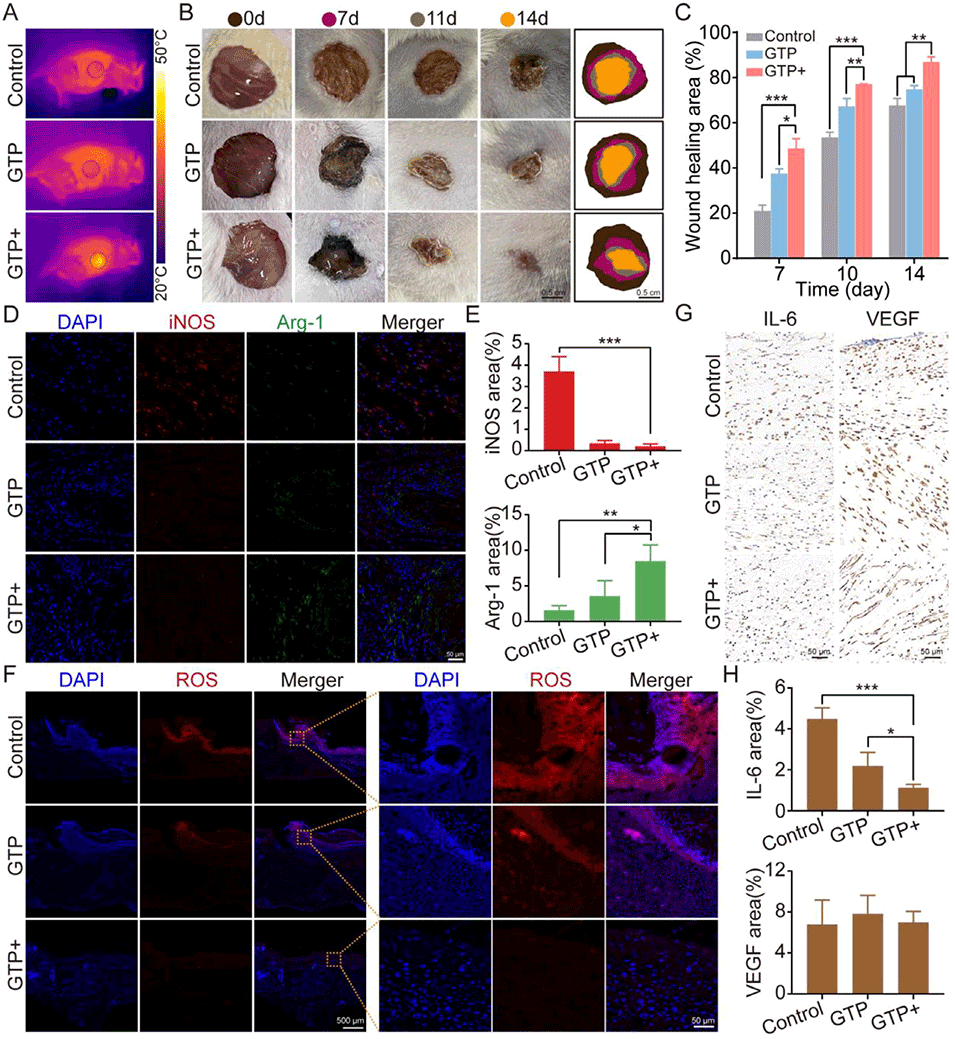
图6:明胶-茶多酚微凝胶在小鼠全层创面模型中的体内评价
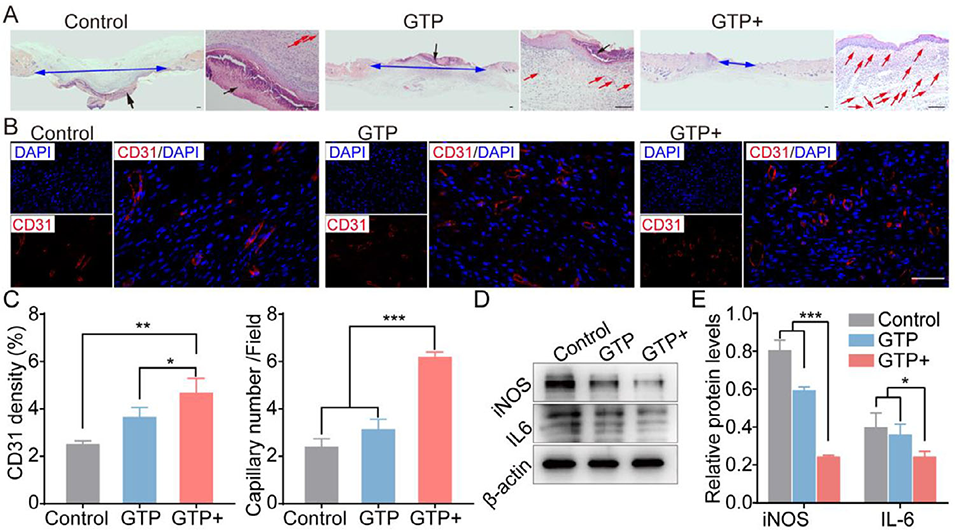
图7:明胶-茶多酚微凝胶治疗创面的组织学与分子生物学分析
论文链接:https://doi.org/10.1002/adhm.202502477
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














