免疫治疗虽在癌症和自身免疫病治疗中成效显著,但免疫系统、肿瘤微环境等存在的细胞异质性,使传统批量检测难以精准解析疾病机制,而微流控技术能实现单细胞水平的转录组、蛋白质组分析,为免疫治疗新生物标志物发现提供关键支持。

导读:
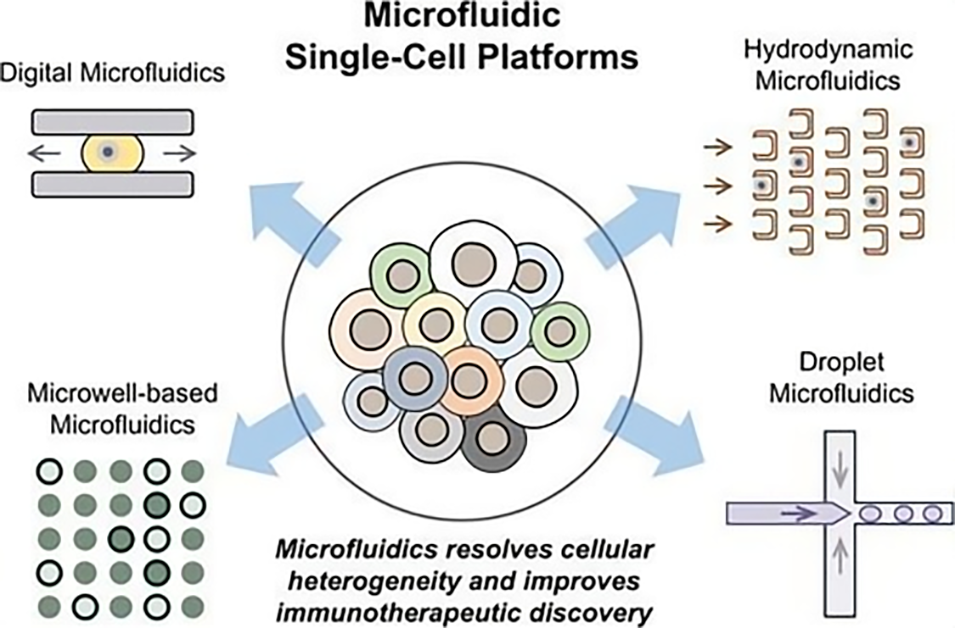
近期,北京理工大学陈康富教授联合美国西北大学王宗杰研究员发表综述,系统梳理了数字微流控、流体动力控制装置、微孔系统、液滴微流控四大类微流控单细胞技术的设计原理与性能特点,深入阐述其在癌症免疫治疗与自身免疫性疾病临床前靶点发现中的应用价值,并展望了技术优化与产业转化的未来方向。相关研究成果以“Microfluidic single-cell technologies for immunotherapeutic target discovery: From design concepts to preclinical applications”为题目,发表在期刊《VIEW》上。
本文要点:
1、本综述探讨了用于单细胞分析流程(涵盖单细胞基因组学、单细胞转录组学、单细胞蛋白质组学及单细胞多组学)的微流控装置的设计、功能与局限性。
2、详细阐述了四类广泛应用的微流控技术——数字微流控、流体动力控制系统、微孔系统及液滴微流控平台,以及它们与单细胞分离、下一代测序(NGS)、微型化免疫分析、质谱(MS)等前沿技术的整合方式。
3、此外,还简要介绍了这些已开发装置在识别免疫治疗各类靶点中的应用,并就微流控技术的未来发展、技术整合及其向免疫治疗靶点发现流程的转化提供了具体见解。
一张图读懂全文
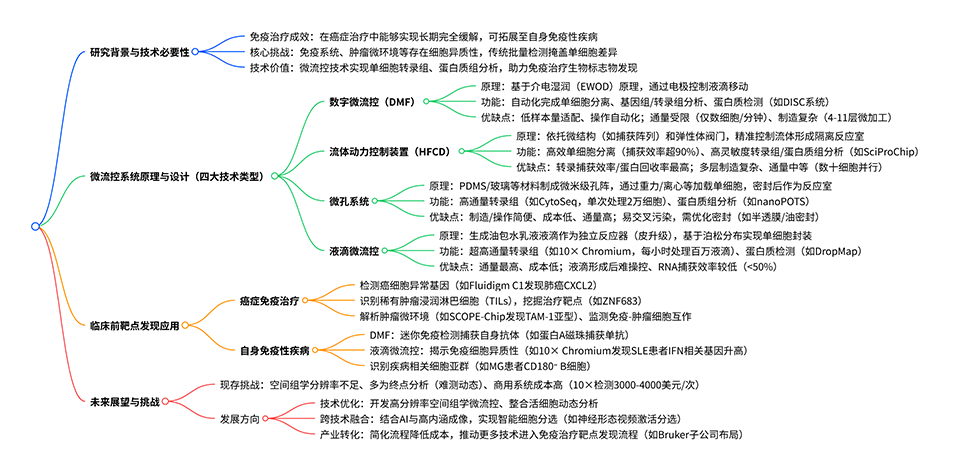
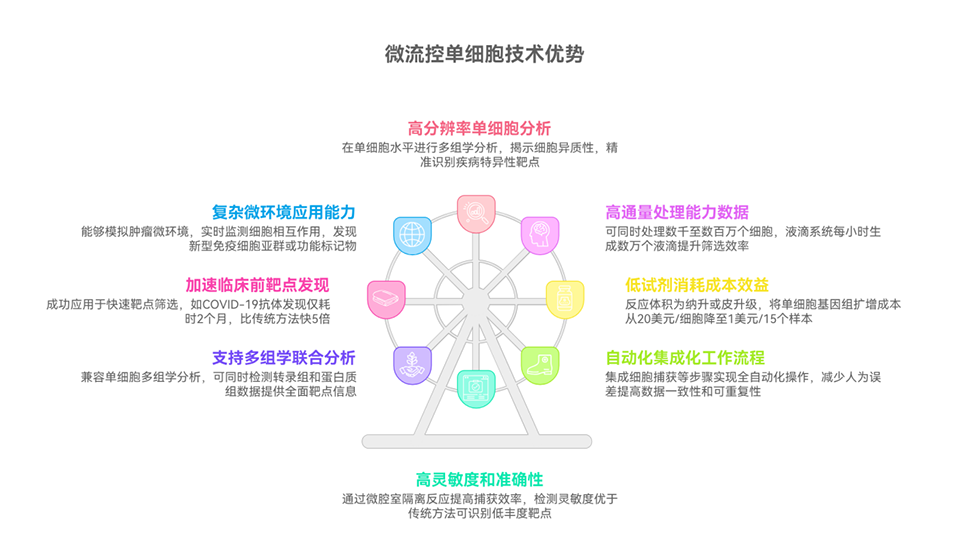
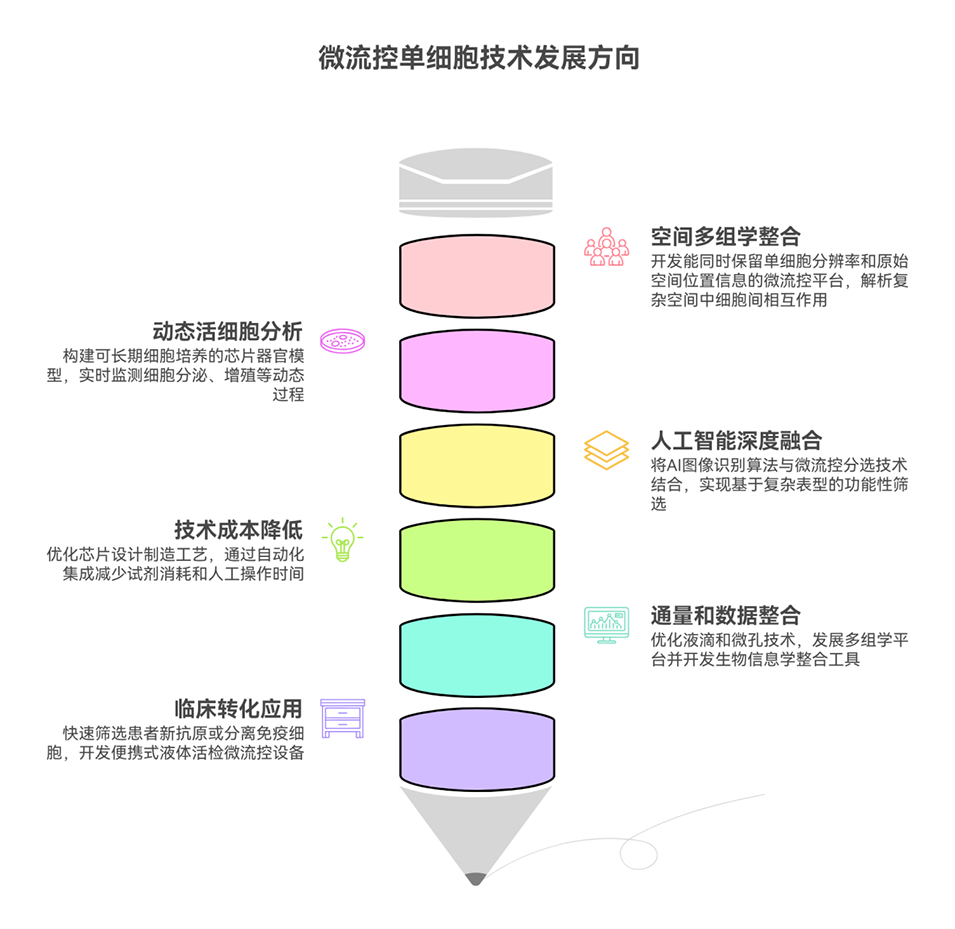
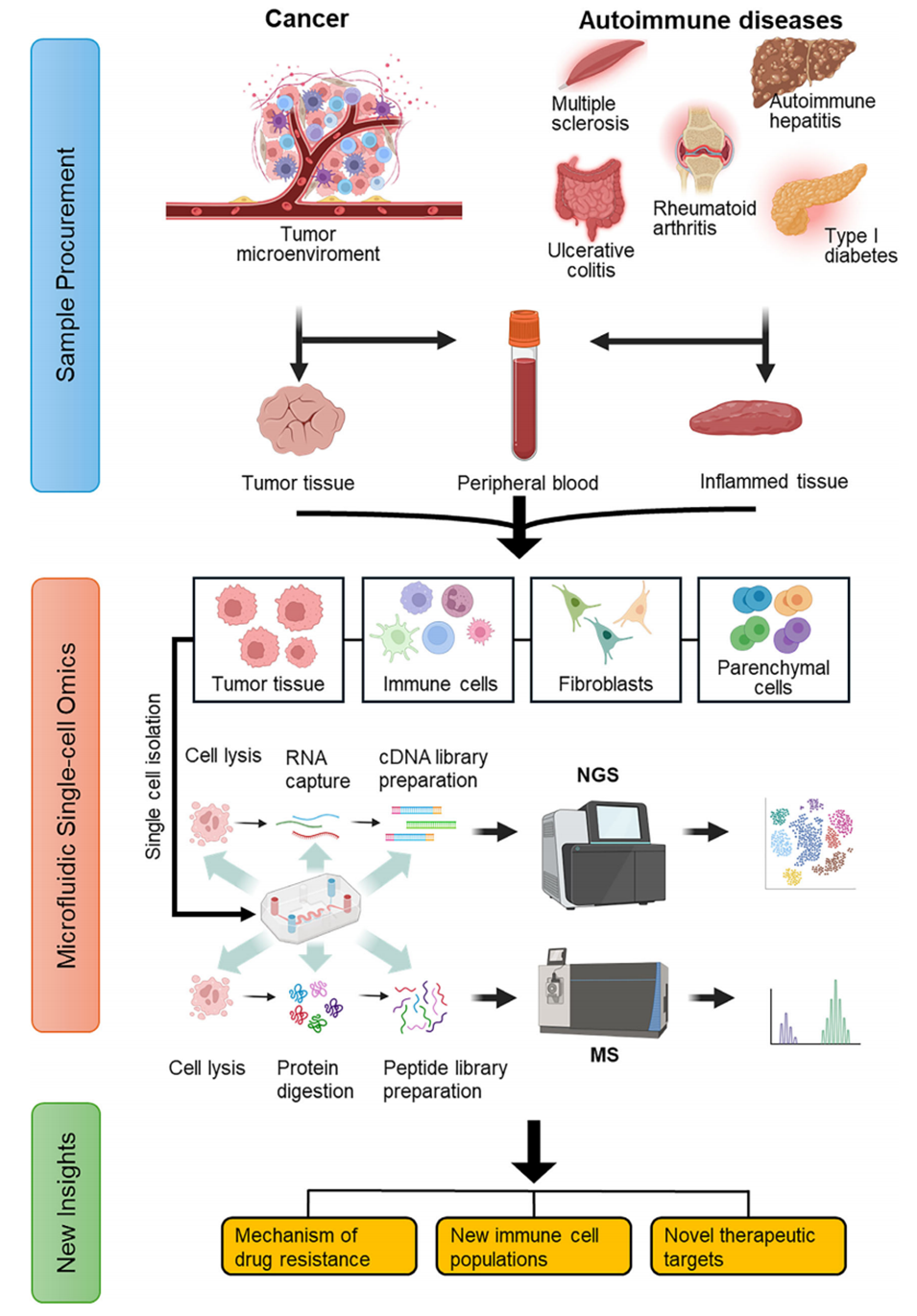
图1. 微流控介导的单细胞组学在癌症与自身免疫性疾病免疫治疗中的应用。首先从患者体内采集病变组织或血液样本;随后通过组织解离或血液处理试剂盒获得单细胞悬液;单细胞转录组、蛋白质组及分泌组的提取可在微流控平台上完成;借助最先进的下一代测序(NGS)和质谱(MS)技术,可进一步开展多组学分析。这一流程有助于更深入地揭示疾病病理机制、识别新型免疫细胞群体,并发现新的治疗靶点。
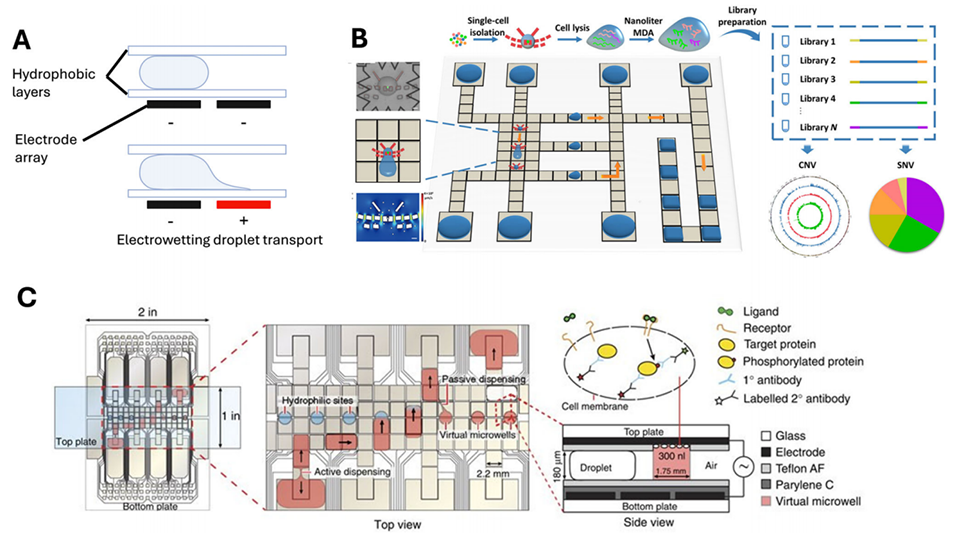
图2. 用于单细胞组学研究的数字微流控(DMF)技术。(A)介电湿润与液滴传输示意图:液滴被两层内嵌电极阵列的疏水表面包裹;当向邻近电极网格施加正电压时,表面局部亲水性发生改变,从而牵引液滴向带电网格移动。(B)数字微流控用于单细胞全基因组测序的示意图:单细胞分离、细胞裂解及 DNA 捕获等步骤均可在 DMF 平台上完成。(C)数字微流控用于单细胞蛋白质检测的示意图:该技术依托微型化荧光免疫分析方法,实现对蛋白质磷酸化水平的监测。
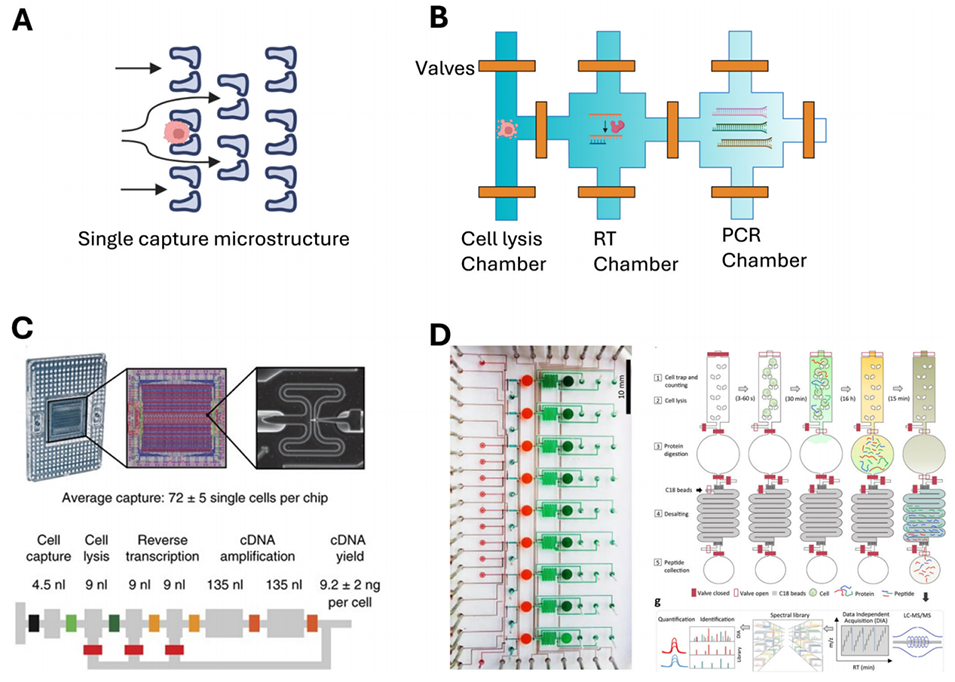
图3. 用于单细胞组学研究的流体动力控制装置。(A)用于单细胞捕获与分离的微结构示意图。(B)由微型阀门构建的隔离反应室示意图:在阀门系统的精准控制下,细胞裂解、逆转录及聚合酶链式反应(PCR)可在隔离反应室内依次进行。(C)商用流体动力控制装置(HFCD)——Fluidigm C1:该装置可用于高灵敏度单细胞转录组研究,通过单细胞捕获结构与阀门系统,实现单细胞裂解、逆转录、扩增及 cDNA 文库构建。(D)用于单细胞蛋白质组研究的流体动力控制装置:该装置可实现全自动操作,包括细胞分离、计数、成像、芯片上细胞裂解、蛋白质消化、肽段制备,以及微量蛋白质的鉴定与定量。
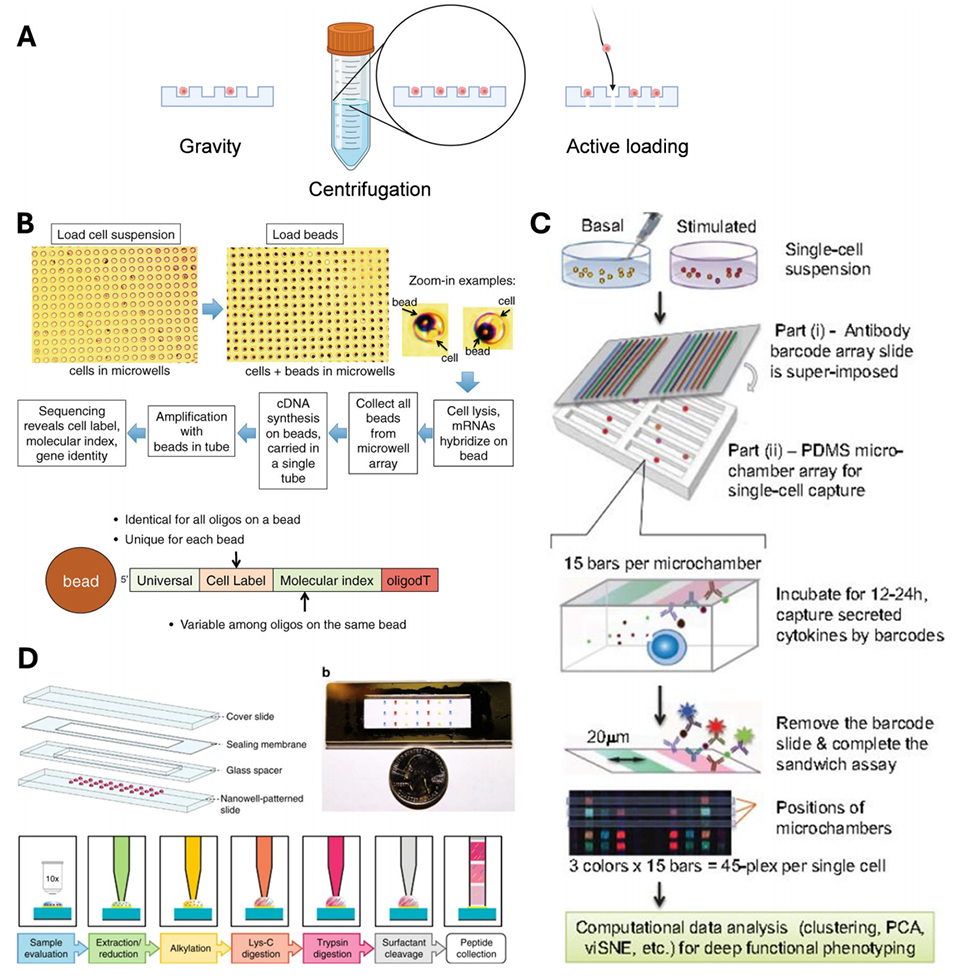
图4. 用于单细胞组学研究的微孔系统。(A)微孔中单细胞加载方式示意图:包括重力介导的单细胞加载、离心介导的单细胞加载,以及流体流动引导的主动式单细胞加载。(B)CytoSeq 技术用于单细胞 RNA 测序的示意图:该系统包含一个微加工制备的表面,其上布满与单细胞尺寸匹配的微孔阵列;通过重力作用完成单细胞加载后,引入带有独特细胞条形码和独特分子标识符(UMI)的微珠,可实现聚合酶链式反应(PCR)偏差校正与基因表达绝对定量分析。(C)基于荧光检测的微孔系统单细胞蛋白质组研究示意图:将抗体条形码阵列玻片与加载了单细胞的微孔贴合,进行孵育与蛋白质分泌反应;目标蛋白质被玻片捕获后,通过荧光标记的二抗实现检测。(D)用于单细胞质谱(MS)分析的微孔阵列:nanoPOTS 技术可在纳米级微孔内完成细胞裂解、蛋白质消化及肽段制备;与传统管级样本制备方法相比,该技术可减少 99.5% 的试剂消耗。
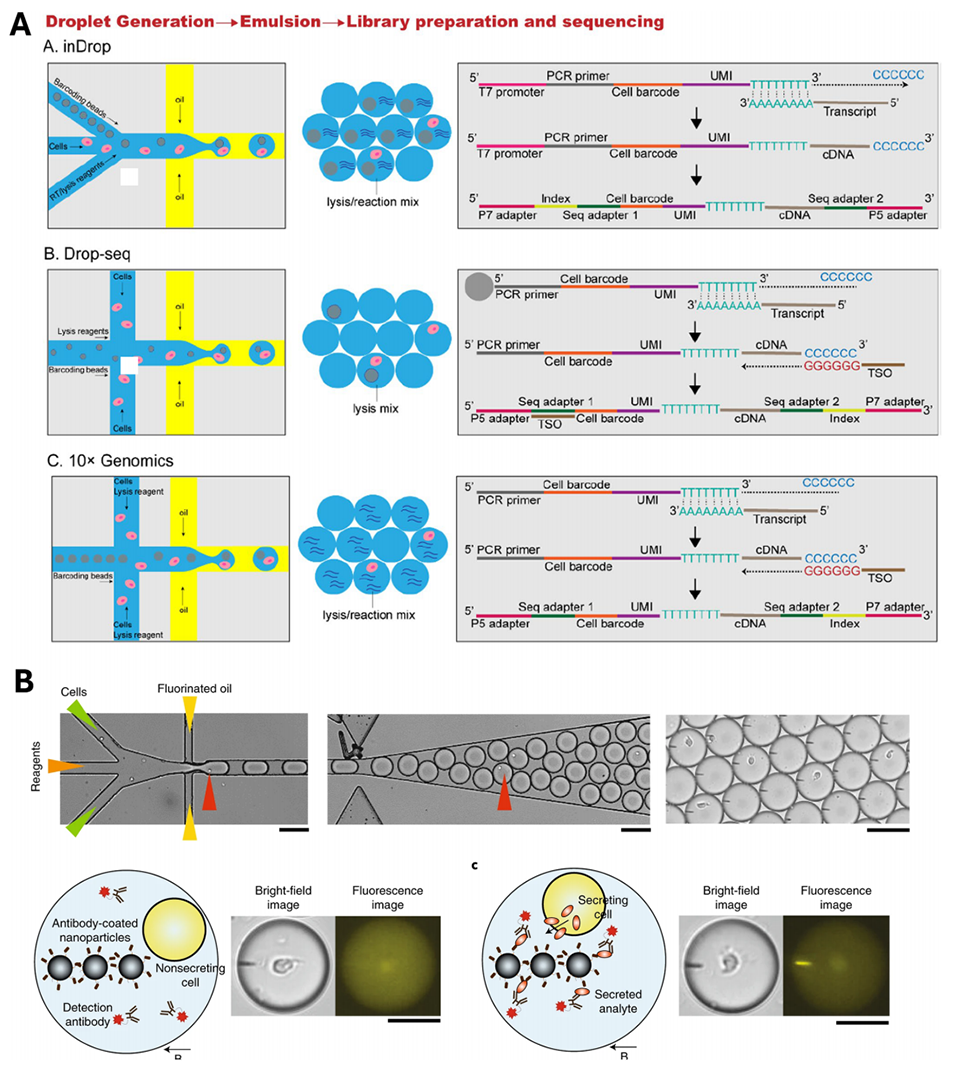
图5. 用于单细胞组学研究的液滴微流控平台。(A)InDrop、Drop-Seq 及 10× Genomics 技术用于单细胞 RNA 测序的工作原理示意图。(B)DropMap 技术用于单细胞分泌分析的示意图:该技术可实现对细胞抗体分泌过程的实时动态监测。
论文链接:https://doi.org/10.1002/VIW.20250065
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














