
导读:
骨关节炎(OA)是慢性疼痛的最常见原因之一。然而,目前的OA疼痛疗法往往无法取得令人满意的结果。为了有效缓解OA疼痛,重庆医科大学第一临床学院白定群教授、韩晓宇博士与上海交通大学护理学院陈亮等人合作,开发了一种超声响应性压电镇痛微球(BaTiO3-RVG@GA/HA),该微球在超声作用下可产生电脉冲,通过调节电压门控钠通道Nav1.7阻断疼痛信号传递,有效缓解骨关节炎疼痛并改善关节病理损伤。相关研究以“Ultrasound-responsive piezoelectric analgesic microspheres alleviate osteoarthritis pain”为题发表于期刊《Journal of Controlled Release》。
本文要点:
1、本研究开发了一种超声响应性压电镇痛微球(BaTiO3-RVG@GA/HA),旨在有效缓解骨关节炎(OA)疼痛。
2、该微球通过微流控技术先构建甲基丙烯酰化明胶(GelMA)和甲基丙烯酰化透明质酸(HAMA)复合水凝胶微球(GA/HA),再将经狂犬病病毒糖蛋白(RVG)修饰的钛酸钡(BaTiO₃)压电纳米颗粒负载其上而形成。
3、在超声作用下,这种镇痛微球能产生电脉冲,通过调节电压门控钠通道(VGSCs)Nav1.7来阻断疼痛信号传递,从而缓解OA疼痛。
4、体外研究证实其能有效降低疼痛相关分子表达,体内研究显示其可显著减少大鼠疼痛相关行为及关节病理损伤,实现OA疼痛改善与关节损伤管理的双重效果。
这种超声响应压电镇痛微球(BaTiO3-RVG@GA/HA)的作用机制主要基于超声介导的压电效应及靶向调控疼痛信号传递,具体如下:
在超声作用下,微球中的钛酸钡(BaTiO3)压电纳米颗粒通过压电效应将机械能转化为电脉冲。由于纳米颗粒经狂犬病病毒糖蛋白(RVG)修饰,可特异性靶向背根神经节(DRG)神经元的烟碱型乙酰胆碱受体(nAChR),精准作用于DRG神经元末端。
电脉冲会导致电压门控钠通道(VGSCs)Nav1.7缓慢失活,减少DRG神经元内的钠离子(Na+)流入,从而阻断疼痛信号向中枢神经系统的传递。同时,该过程还能降低疼痛相关分子(如瞬时受体电位香草酸亚型1(TRPV1)、降钙素基因相关肽(CGRP))的表达,进一步抑制疼痛信号传导,实现骨关节炎疼痛的缓解。
此外,这种调控还能改善关节病理损伤,通过增加软骨合成代谢蛋白COL2的表达,降低基质降解代谢蛋白MMP13的表达,促进关节软骨的修复。
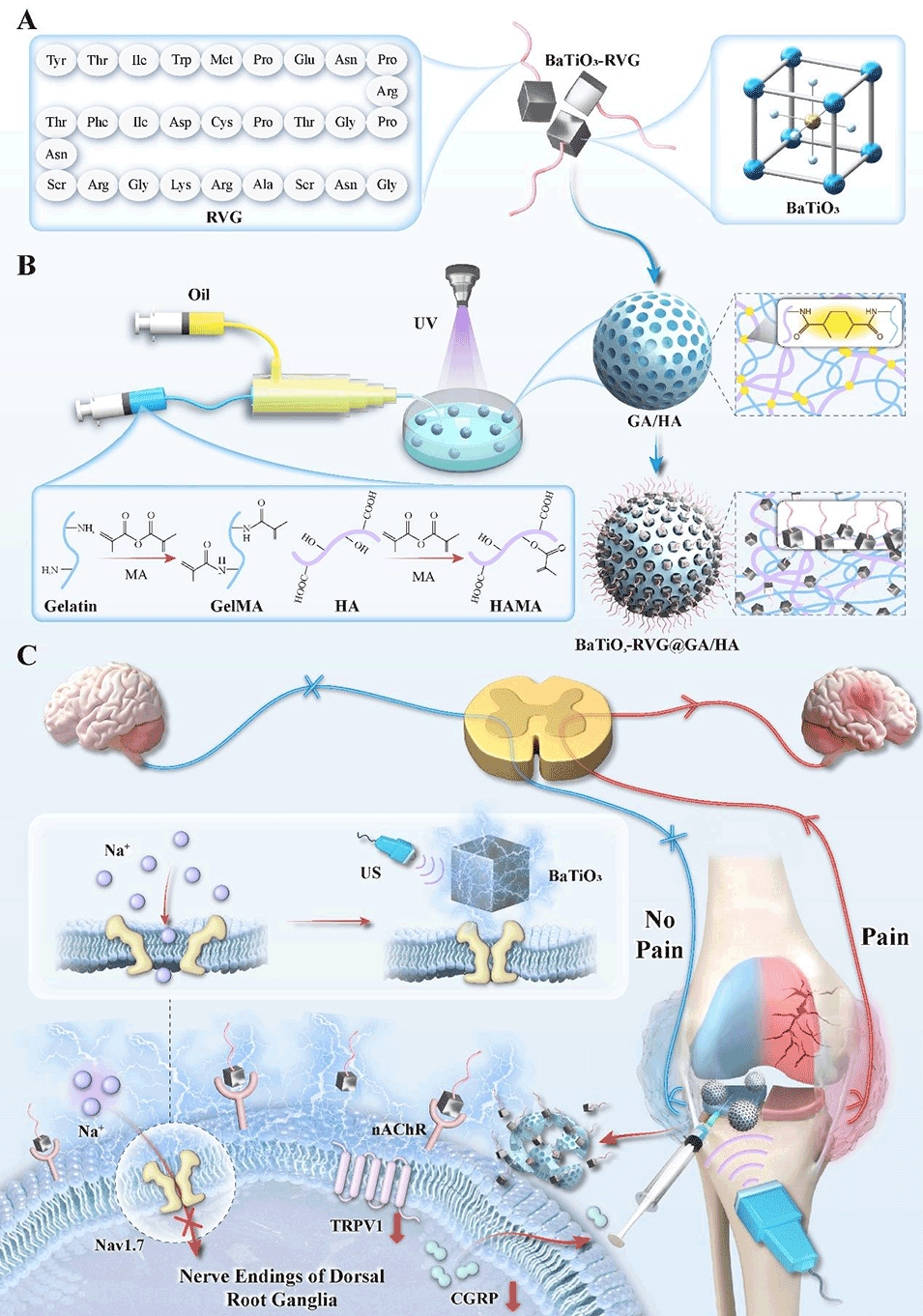
Scheme1:镇痛微球通过超声介导的压电效应缓解骨关节炎疼痛的示意图
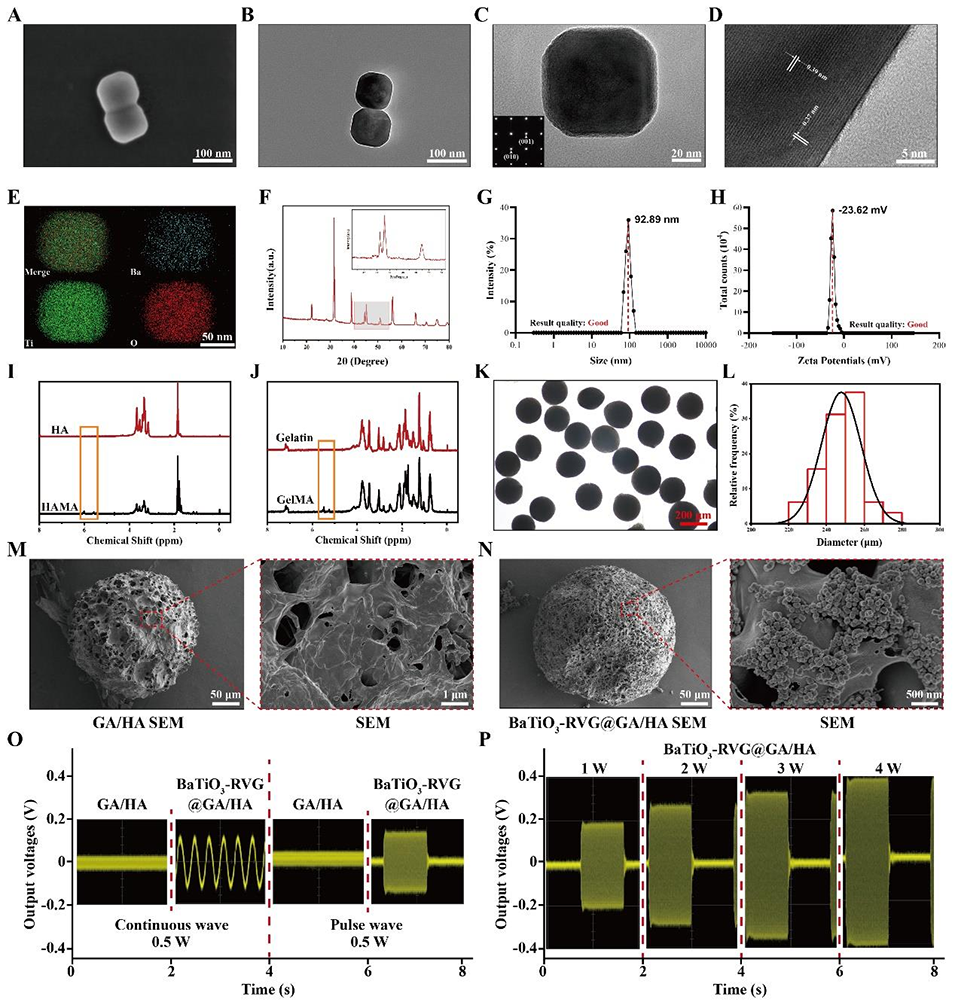
图1:镇痛微球的表征
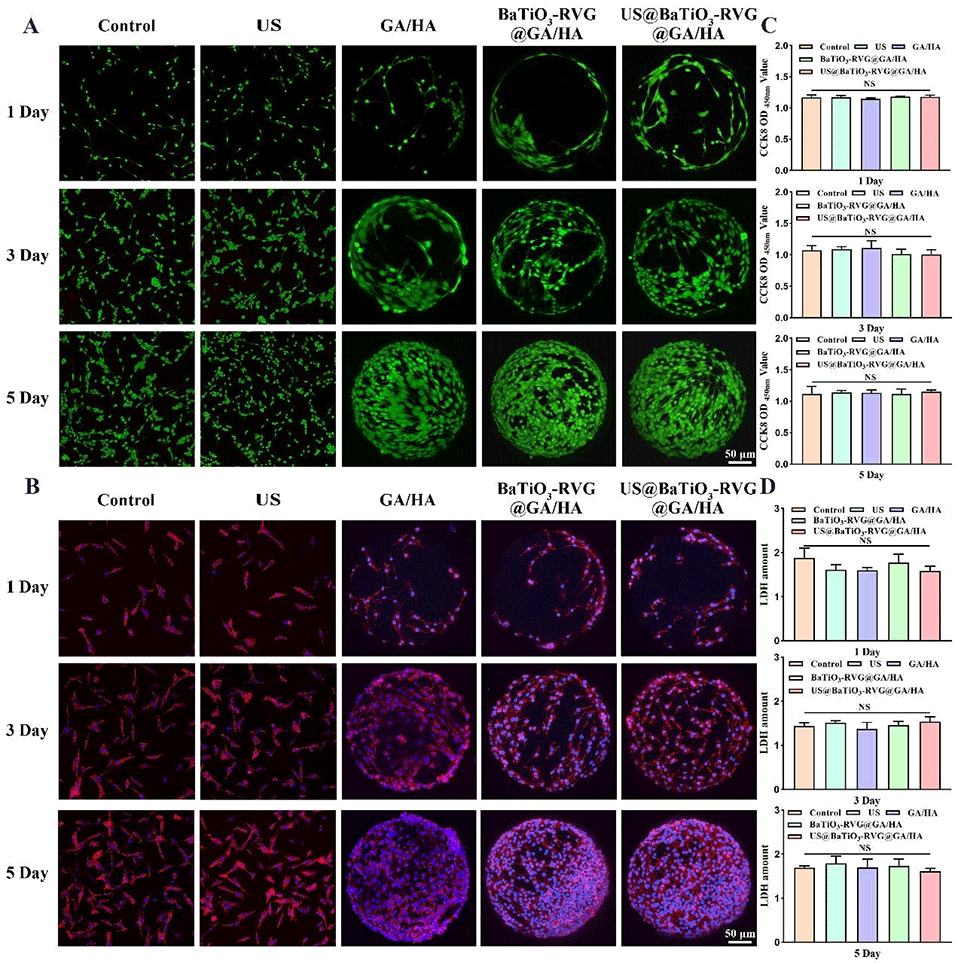
图2:镇痛微球的生物相容性
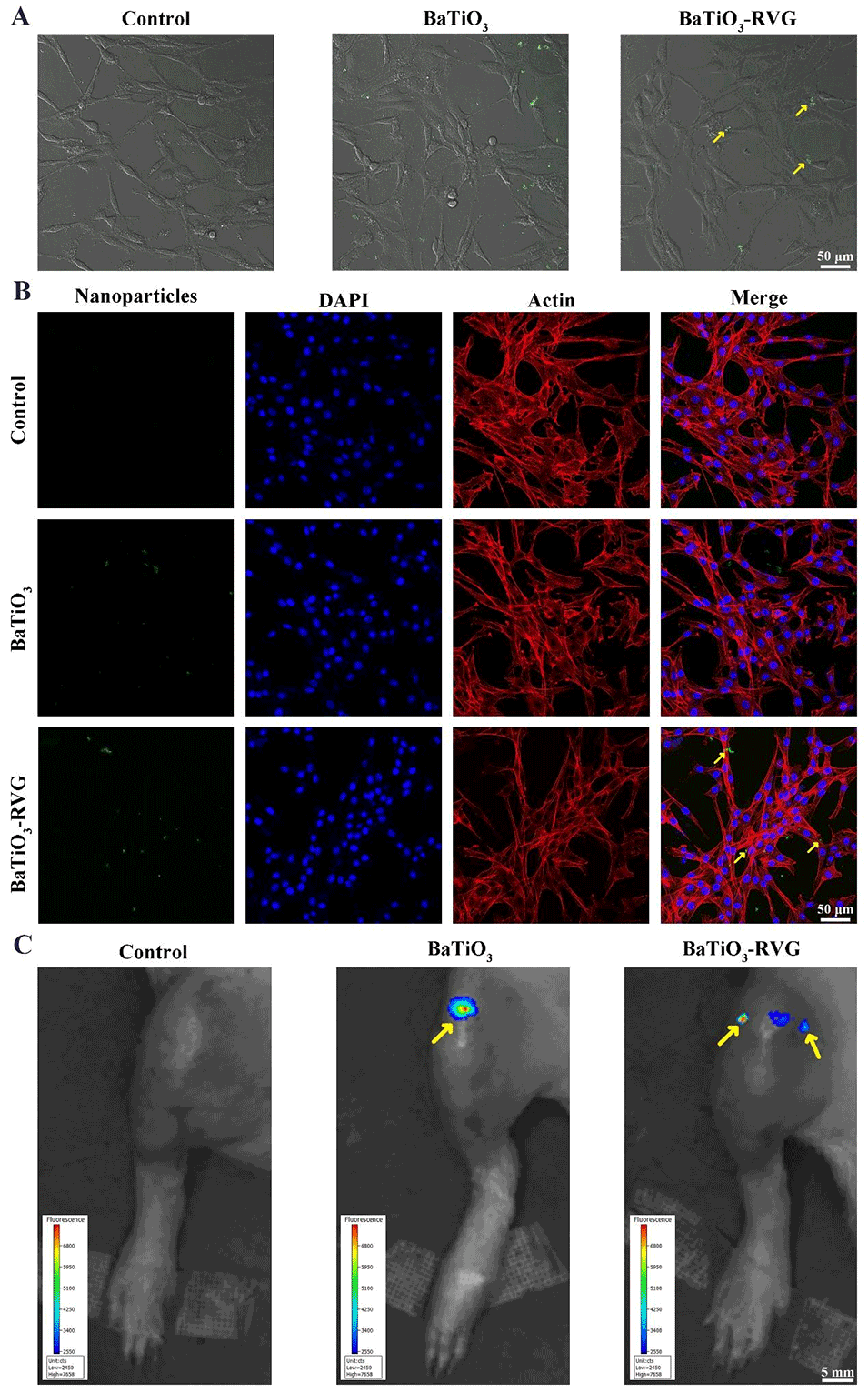
图3:镇痛微球的靶向能力
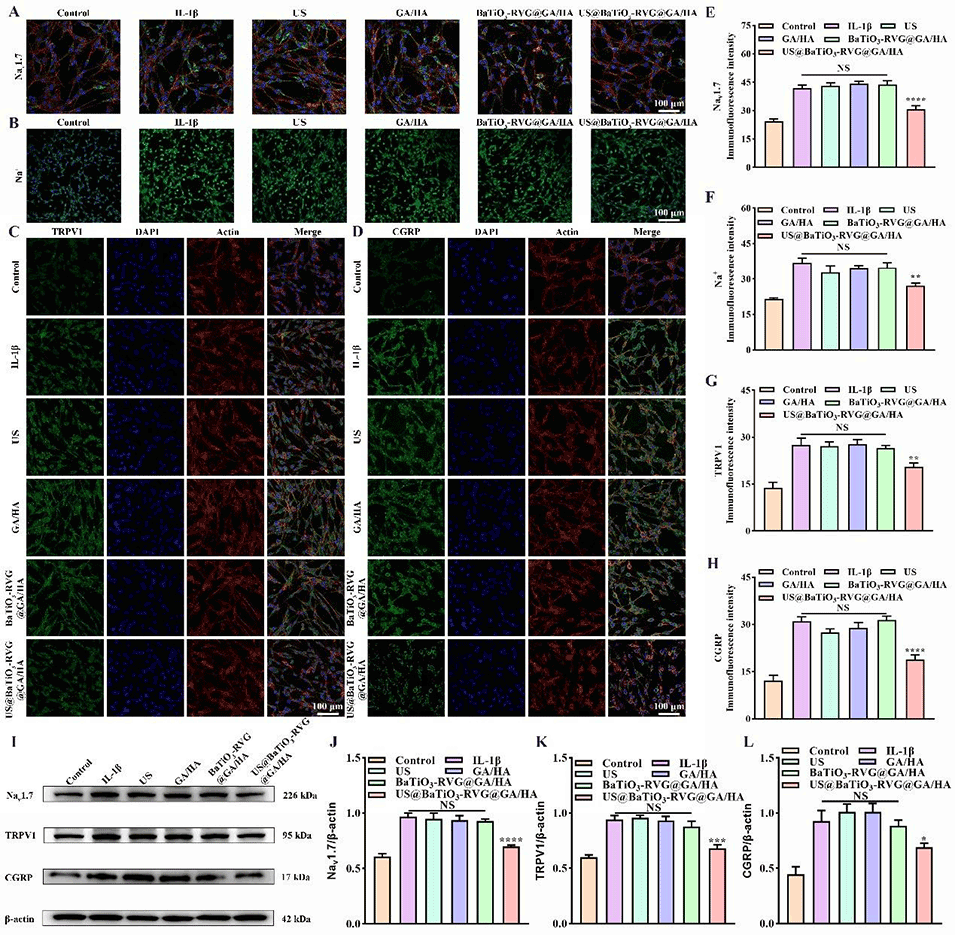
图4:镇痛微球的体外镇痛效果
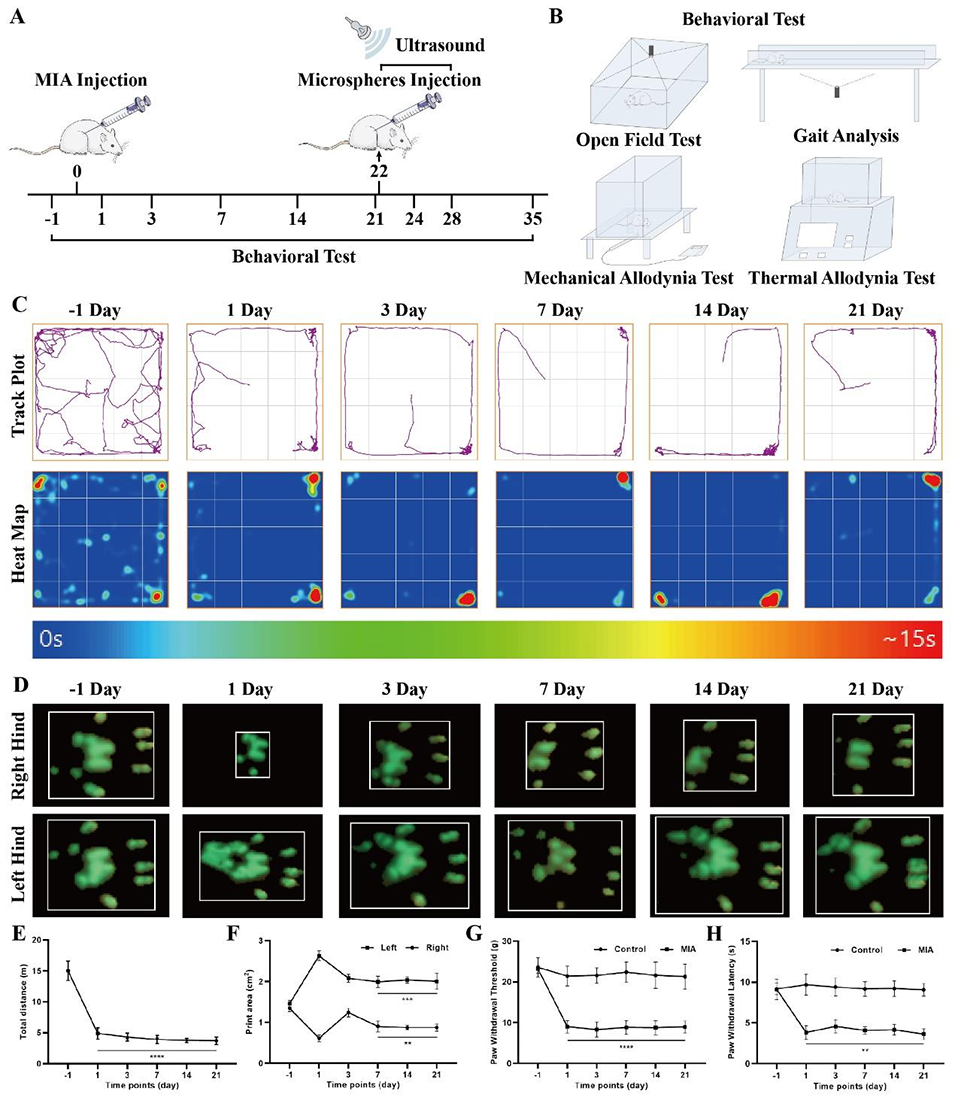
图5:体内实验设计,用于评估镇痛微球对大鼠骨关节炎疼痛的缓解效果
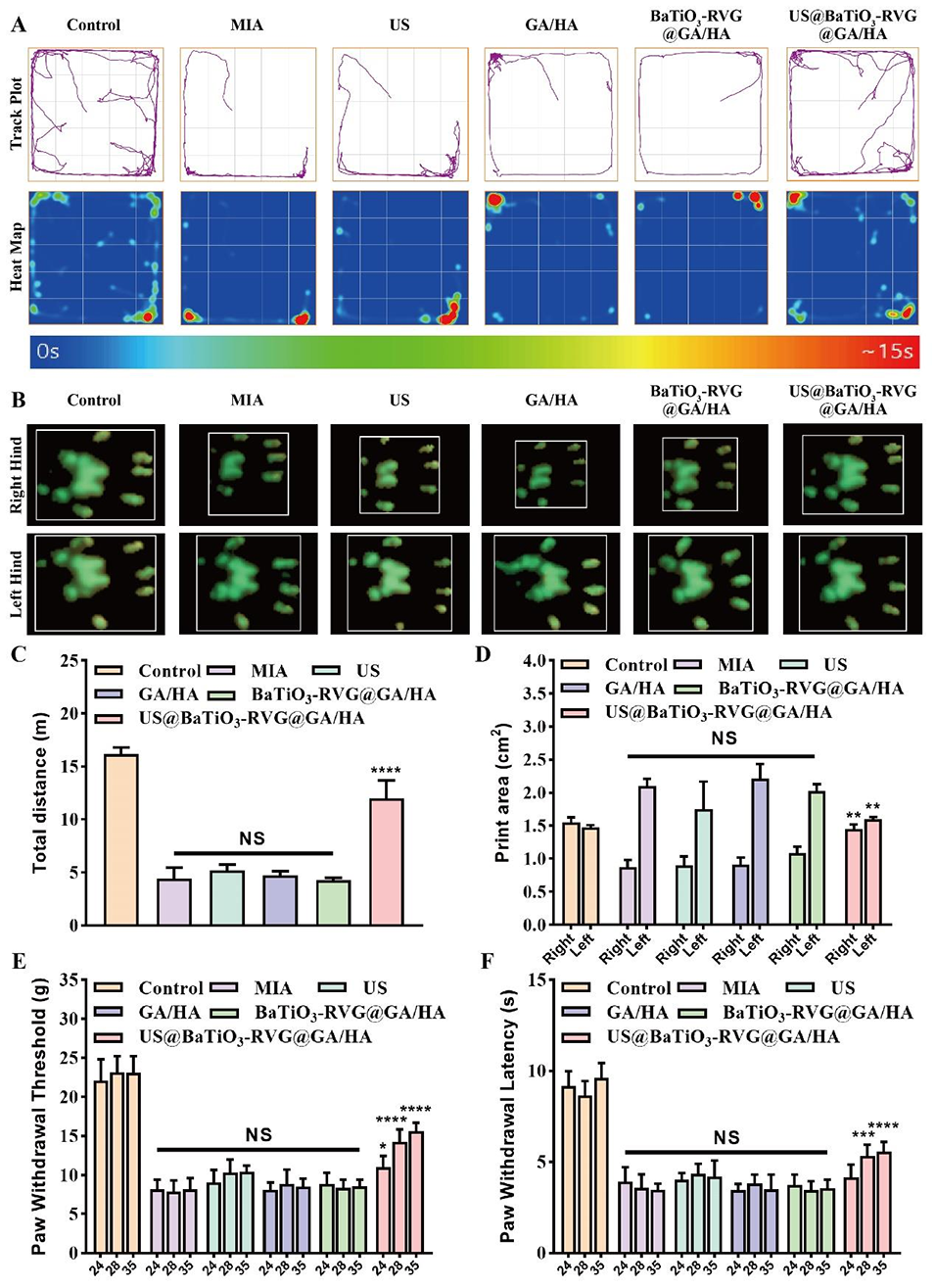
图6:不同处理组大鼠的开放场试验、步态分析及痛觉测试结果,体现镇痛微球的体内镇痛效果
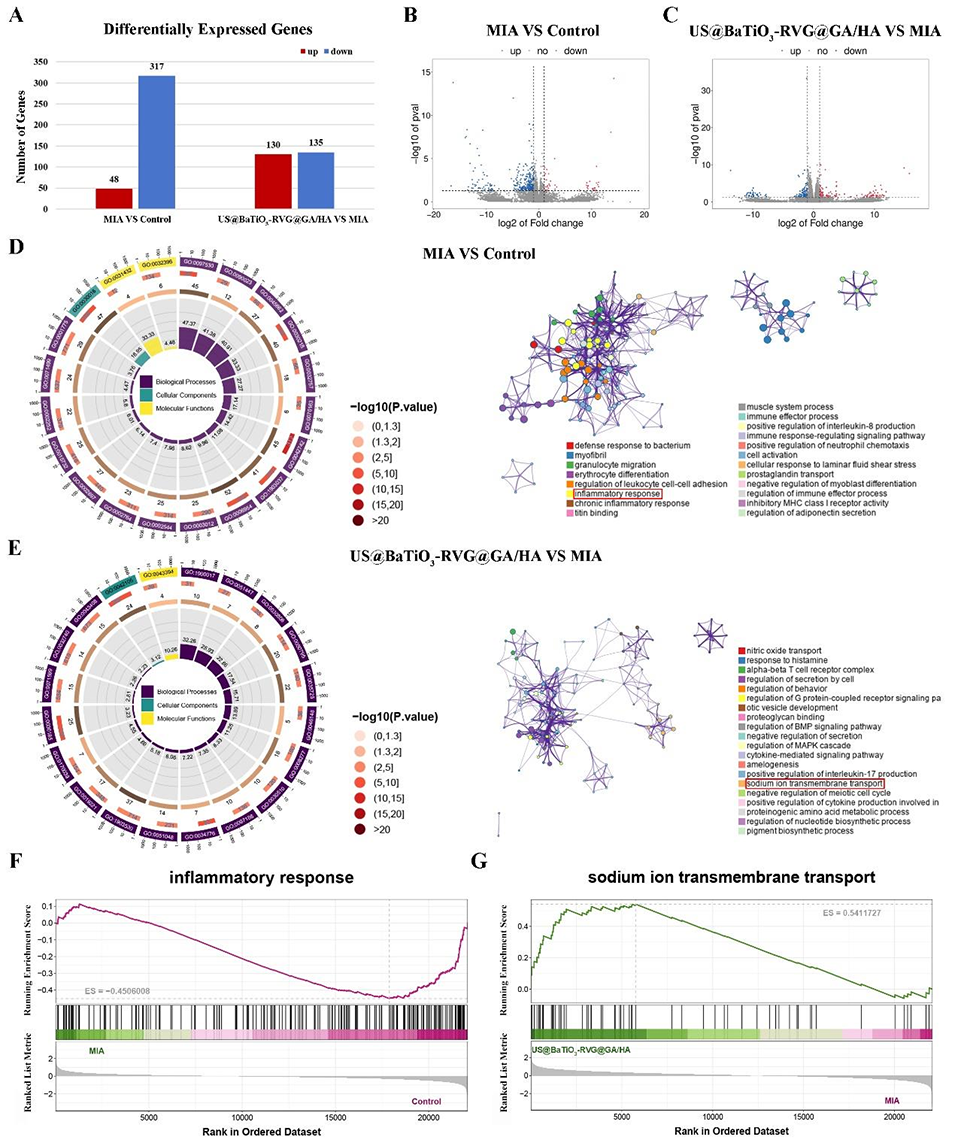
图7:镇痛微球的镇痛机制
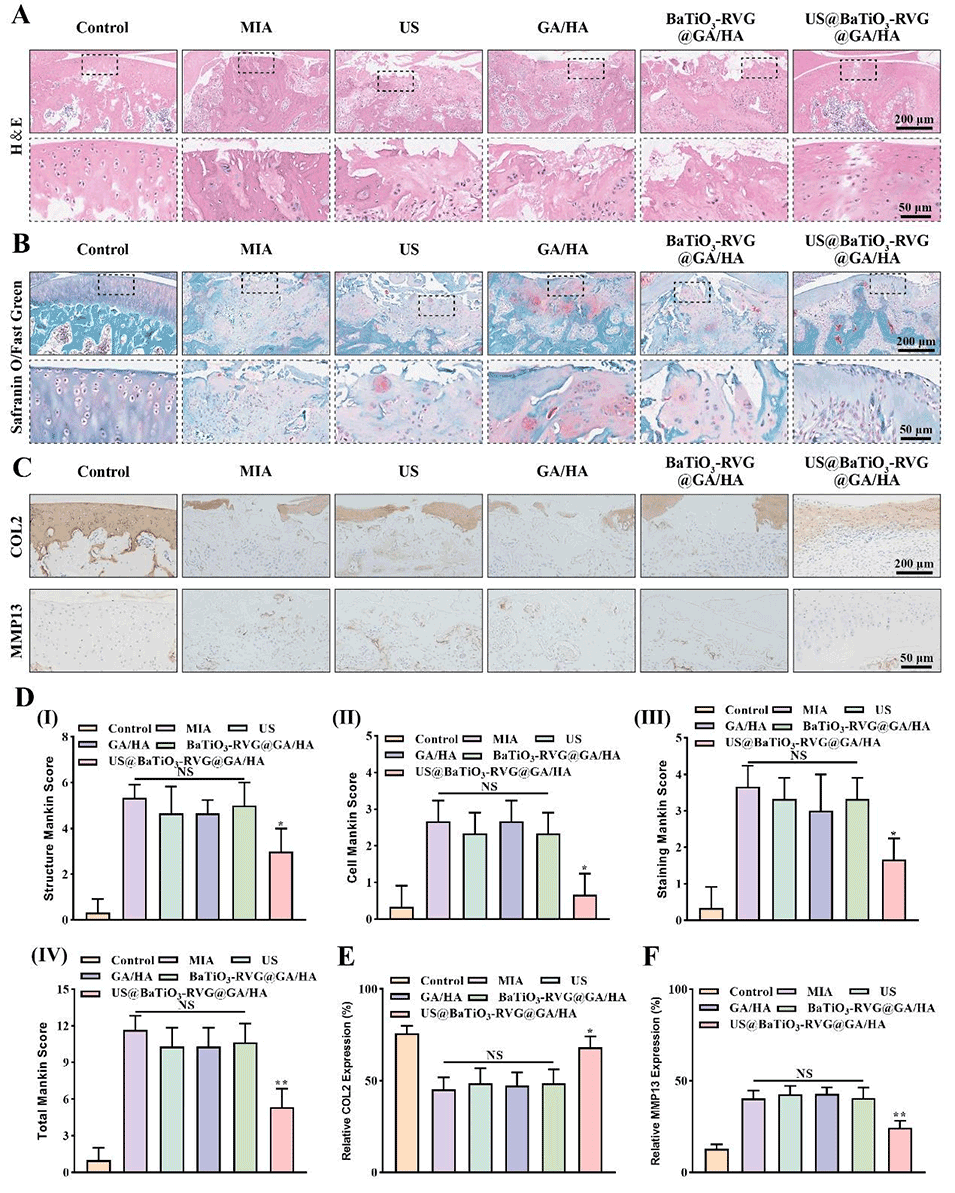
图8:镇痛微球对大鼠膝关节组织病理学分析的影响
论文链接:https://doi.org/10.1016/j.jconrel.2025.114049














