牙周炎是一种常见的口腔炎症性疾病,会导致牙槽骨吸收和牙齿脱落,难以控制且易复发。当前治疗方法因深部弯曲的牙周袋和耐药菌(如具核梭杆菌)的存在而效果有限,且无法同时实现强效抗菌、抗炎和牙周组织再生这三个关键目标。

近期,重庆医科大学附属口腔医院张红梅教授团队受莲花结构的启发,精心设计了一种纳米/微米复合水凝胶微球。该微球将聚多巴胺/黄连素纳米粒子、骨形成蛋白9转染的牙周膜干细胞巧妙封装其中,在抗菌、抗炎及促进牙周组织再生等方面展现出卓越性能,为牙周炎治疗开拓了全新路径。相关研究以“Bioinspired nano-micron hydrogel microspheres for periodontitis therapy through synergistic multi-targeted remodeling of microenvironment”为题目,发表在期刊《Theranostics》上。
本文要点:
1、本研究针对牙周炎治疗难题,通过微流控技术开发了一种仿莲花结构的纳米/微米复合水凝胶微球(PDA/BBR@Gel@BMP9-PDLSC)。
2、这种微球封装负载黄连素(BBR)的聚多巴胺(PDA)纳米粒子和骨形态发生蛋白9重组腺病毒(Ad-BMP9)感染的牙周韧带干细胞(PDLSCs),展现出优异的生物相容性、持续药物释放能力,以及显著的抗菌、抗炎和骨组织再生效果。
3、体内外实验表明,该微球能有效治疗由具核梭杆菌(F. nucleatum)持续感染引发的颅骨缺陷和牙周炎,促进新骨形成并具备抗炎效果,且无器官毒性。
4、RNA测序和Western blot分析显示,黄连素与骨形态发生蛋白9通过调控转化生长因子-β(TGF-β)、肿瘤坏死因子(TNF)及过氧化物酶体增殖物激活受体(PPAR)信号通路中的关键基因,协同发挥抗炎和成骨作用。
5、PDA/BBR@Gel@BMP9-PDLSC微球将现代生物材料技术与中药成分、传统药物(黄连素和骨形态发生蛋白9)相结合,开发了兼具有效性和安全性的新型牙周炎治疗策略,为口腔医学研究开辟了新方向。
纳米微米复合水凝胶微球组成与设计

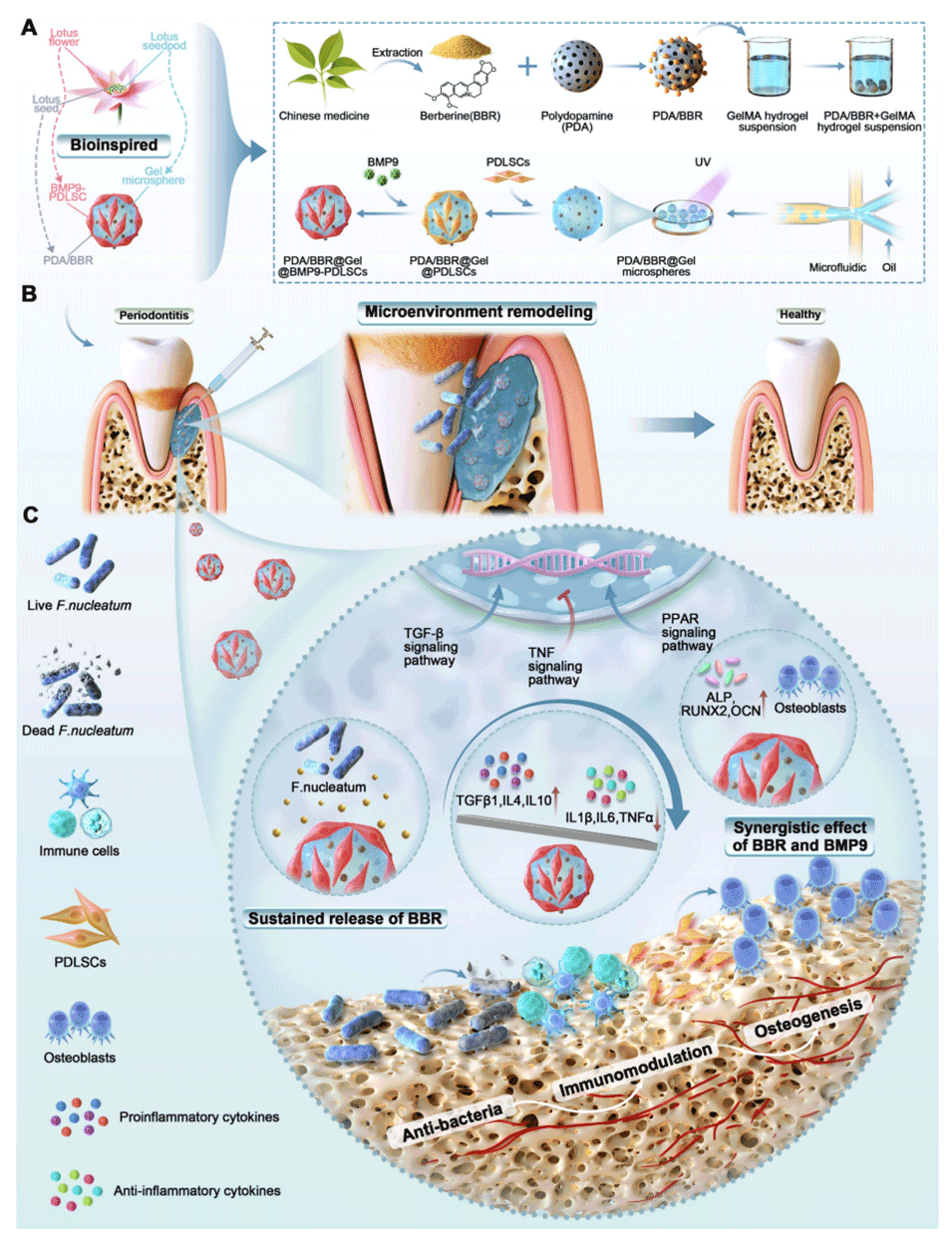
Scheme 1:PDA/BBR@Gel@BMP9-PDLSC微球的形成及其在治疗牙周炎中的多功能作用示意图。(A)受莲花启发的PDA/BBR@Gel@BMP9-PDLSC微球制备过程。(B)PDA/BBR@Gel@BMP9-PDLSC微球原位注射用于牙周炎治疗。(C)PDA/BBR@Gel@BMP9-PDLSC微球对重塑牙周微环境的多功能作用(抗菌、免疫调节和成骨)及机制。
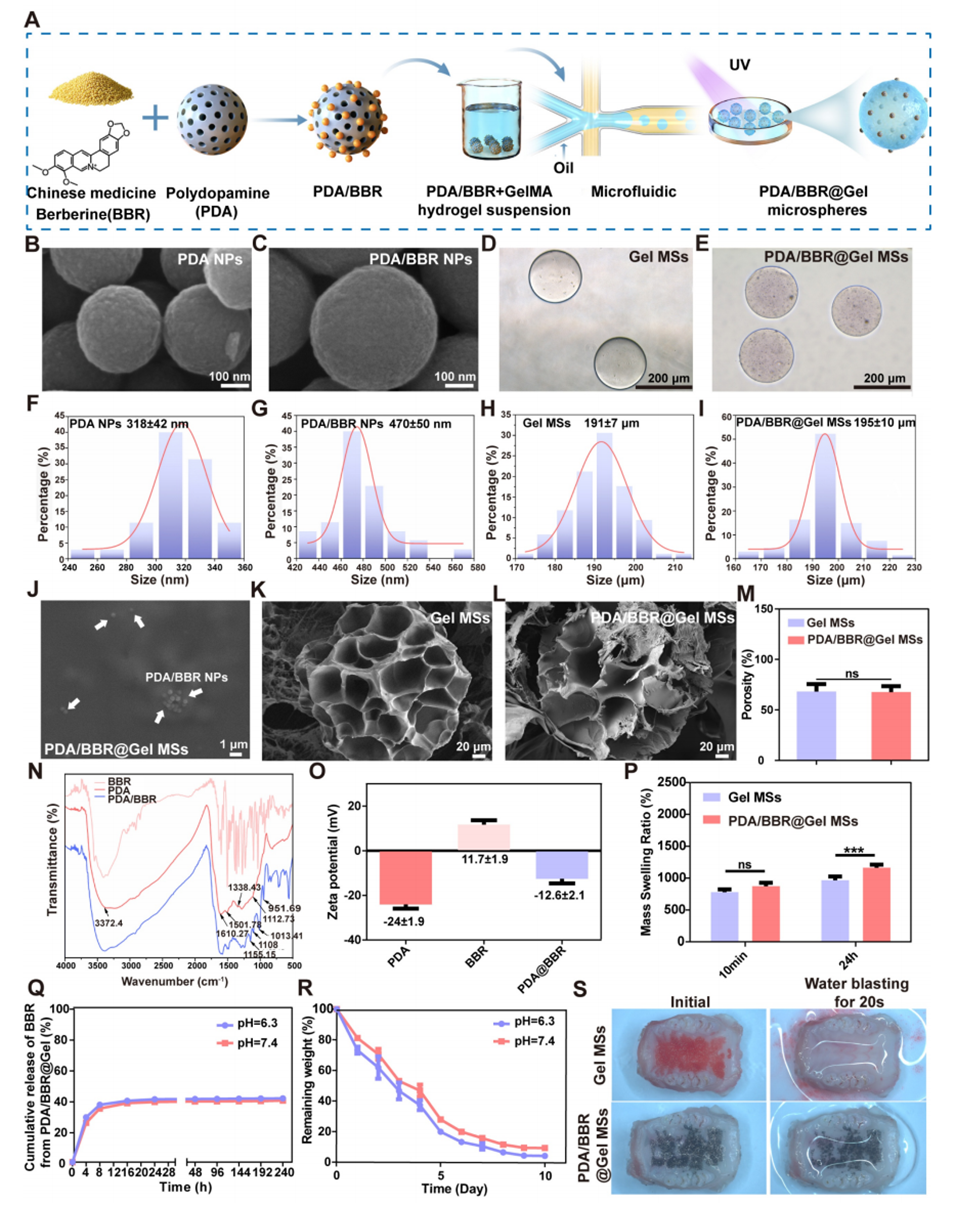
图1:PDA/BBR纳米粒子和PDA/BBR@Gel微球的物理特性
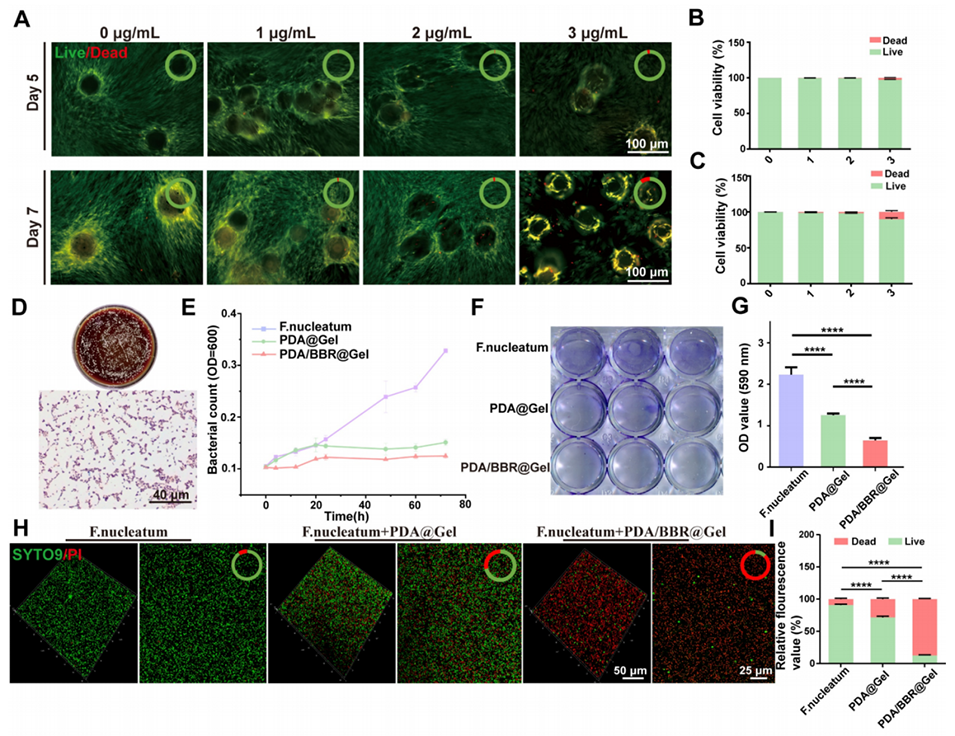
图2:PDA/BBR@Gel微球的生物相容性和抗菌性能
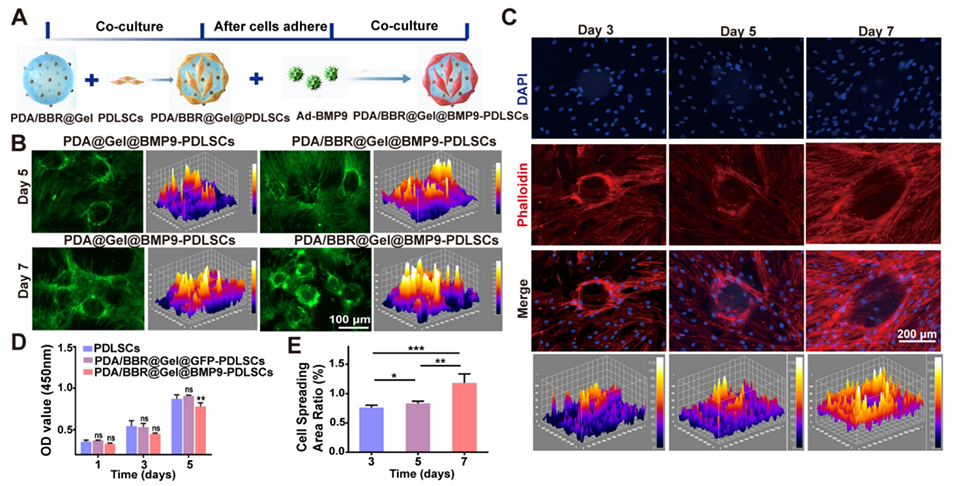
图3:PDA/BBR@Gel@BMP9-PDLSC微球的构建
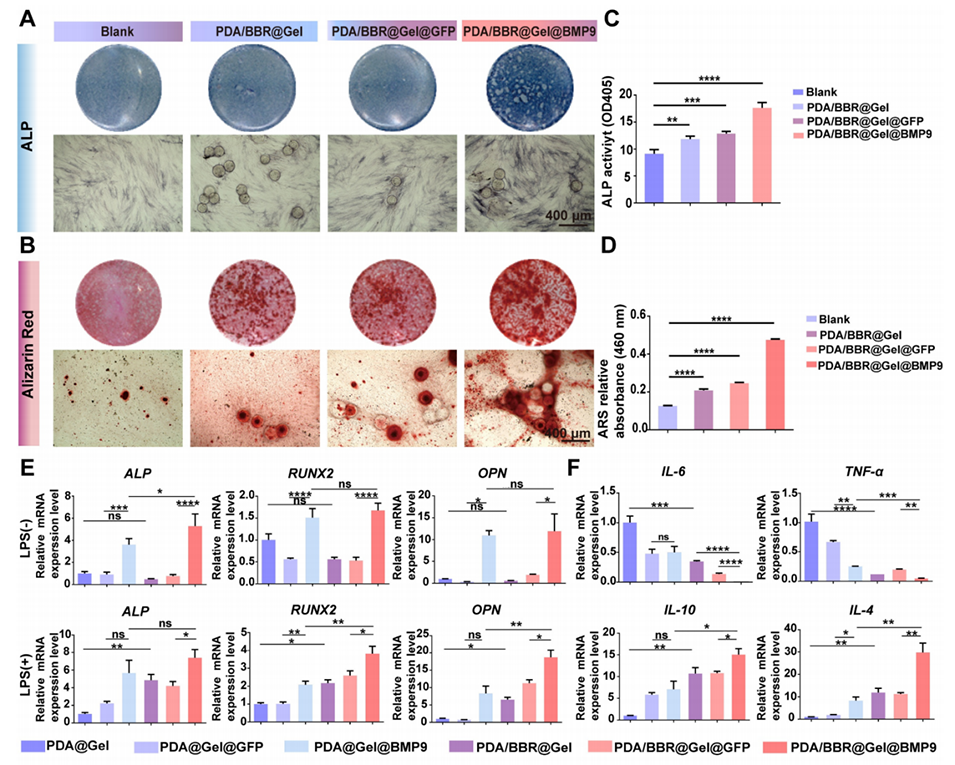
图4:PDA/BBR@Gel@BMP9-PDLSC微球在体外炎症环境中诱导成骨分化和抗炎作用

图5:PDA/BBR@Gel@BMP9-PDLSC微球修复颅骨缺损

图6:PDA/BBR@Gel@BMP9-PDLSC微球对持续性具核梭杆菌感染后牙周炎的影响
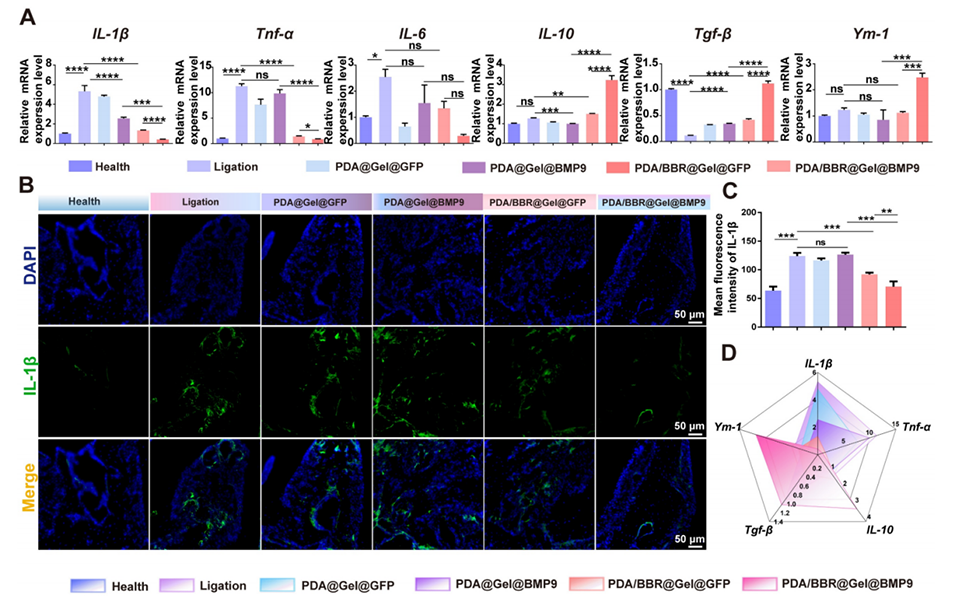
图7:PDA/BBR@Gel@BMP9-PDLSC微球对持续性具核梭杆菌感染牙周炎的影响
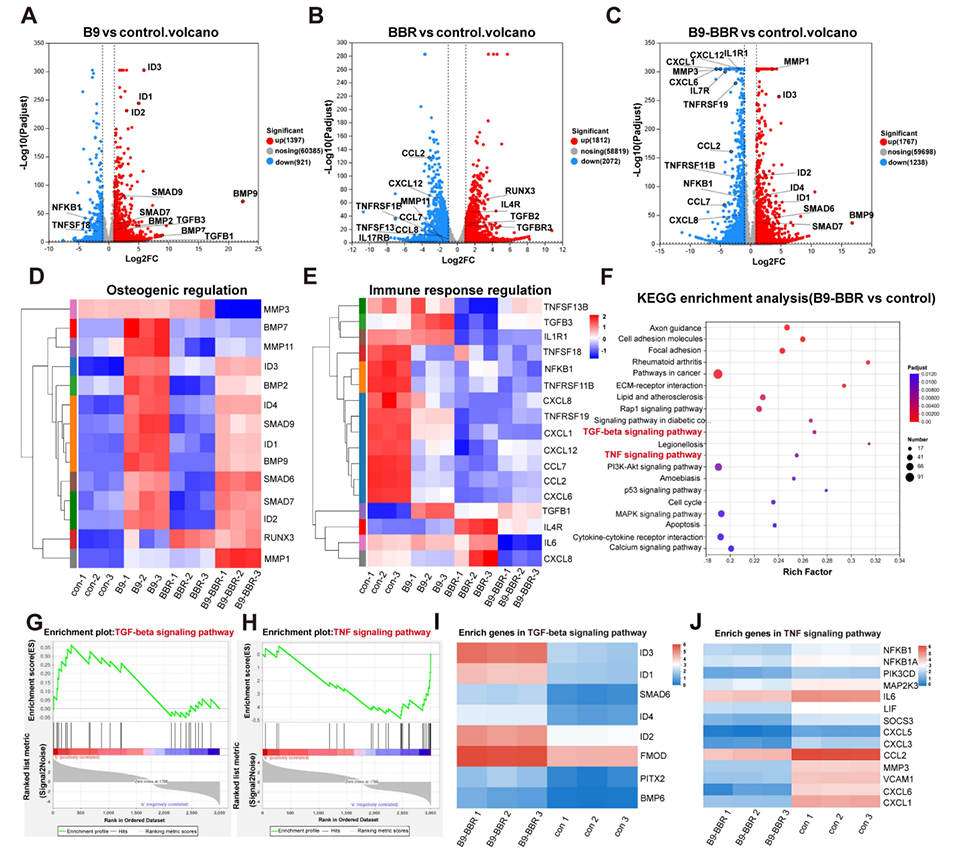
图8:RNA测序差异分析
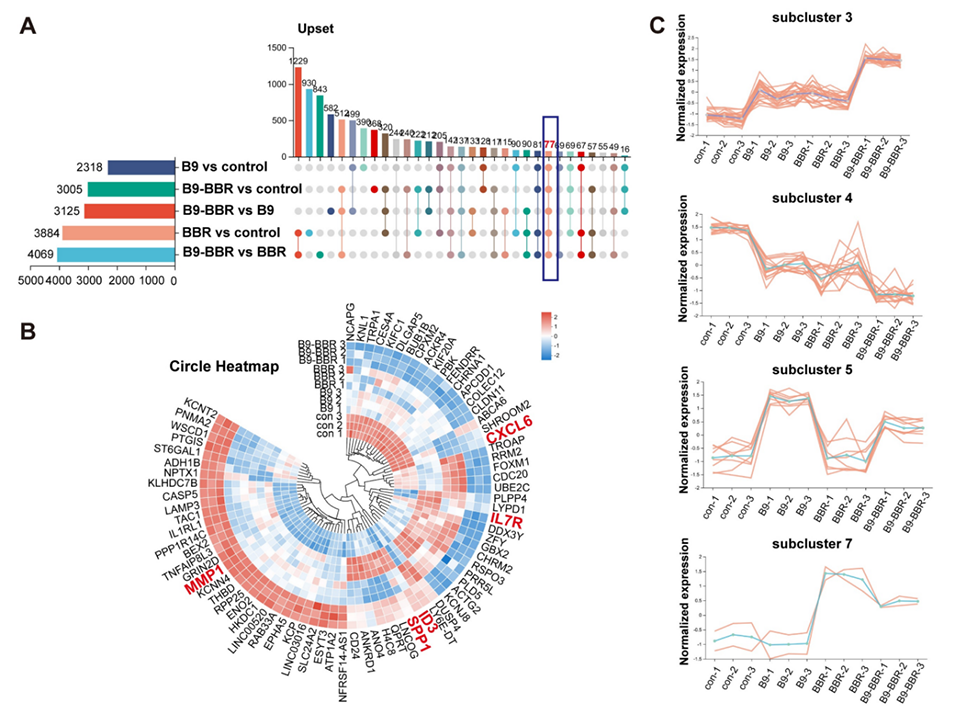
图9:组间差异表达基因和亚簇分析
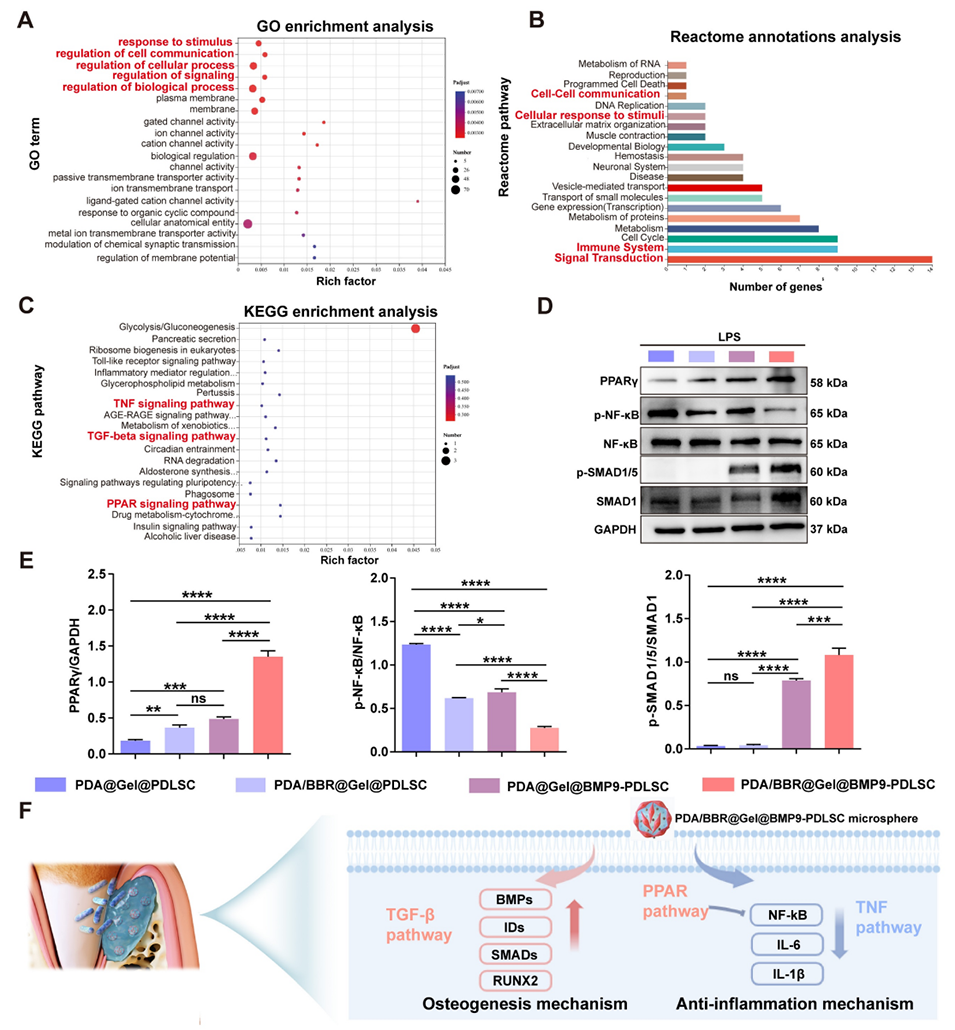
图10:参与调控BMP9和BBR协同作用的基因及通路
文献:doi:10.7150/thno.112782














