
文献导读:
近日,德国慕尼黑工业大学(TUM)Friedrich C. Simmel团队在国际知名期刊《Nature Communications》上发表了题为“Quantifying phage-host dynamics using droplet microfluidics”的研究成果。该研究介绍了一种利用液滴微流控技术量化噬菌体与宿主相互作用的高通量新方法。研究人员通过将单个噬菌体和细菌共同包裹在微米级液滴中,实现了对个体感染事件及裂解动力学的精确监测。
该平台克服了传统双层平板计数法(DLA)无法实时监控且耗时长的局限性,能够提供更准确的有效滴度分析。通过调节液滴大小和组分混合比例,该技术扩展了实验的动态范围与统计可靠性。这种数字化分析框架为理解病毒生物学提供了新视角,并有助于开发应对抗生素耐药性的新型抗菌策略。这一创新工具能够以单事件分辨率并行处理成千上万个独立实验,具有极高的科研应用价值。
本文要点:
1. 研究背景与挑战
传统方法的局限性:传统的双层琼脂平板法(DLA)虽是金标准,但存在实验设置固定、重复性差、无法实时监测感染动力学以及仅能在群体层面反映信息等缺点。
临床需求:随着抗生素耐药性危机加剧,噬菌体疗法重新受到重视,急需能够精确量化噬菌体感染动态的工具。
2. 核心技术平台:液滴微流控
高通量数字化检测:平台通过将单个噬菌体和细菌共封装在微米级液滴中,实现对成千上万个独立感染事件的并行观测,每秒可分析数千个液滴。
双共流封装(Dual Co-flow):噬菌体和细菌在封装瞬间才接触,确保了暴露时间的精确同步,消除了预混合带来的动力学偏差。
荧光数字化识别:使用不透膜的DNA荧光染料(YOYO-1)检测细菌裂解。当细菌裂解释放DNA时,液滴荧光显著增强。利用高斯混合模型(GMM)实现自动化的液滴分类(阳性 vs 阴性)。
3. 数学模型与统计优化
统计学指导:采用泊松分布模型处理噬菌体和细菌的封装随机性,通过实验观察到的阳性液滴比例计算出准确的“数字滴度”。
动态范围扩展:通过在同一实验中系统性地改变液滴大小和混合比例(α),显著扩大了该方法能检测的噬菌体滴度范围。
4. 主要发现与成果
高度一致性:该平台测得的“数字滴度”与传统DLA方法获得的结果高度吻合,验证了其准确性。
识别有效宿主浓度:研究发现,液滴实验揭示的“有效细菌密度”仅为体相吸光度(OD)测得密度的约6%,这反映了群体中仅有一部分细胞处于易受感染的代谢活跃状态。
单事件动力学研究:不同于群体培养中后代噬菌体会干扰后续感染过程,该平台能够观察初始噬菌体引起的独立裂解动态,揭示了噬菌体群体的感染力多样性。
5. 应用前景
该技术具有通用性,适用于各种裂解性噬菌体-宿主系统。
它为噬菌体生物学研究、抗微生物策略开发以及噬菌体工程化改造(如通过液滴分选优化治疗性噬菌体)提供了强大且准确的框架。
该平台通过双共流封装(dual co-flow encapsulation)方案,从物理机制和实验流程两个方面确保了噬菌体暴露时间的精确同步:
物理隔离与瞬时接触:在封装之前,含有噬菌体的溶液和含有细菌的溶液是通过不同的入口单独引入的。这两者仅在封装的一瞬间(即液滴形成的时刻)才会相遇。
协同注射机制:悬浮液被共同注射进一个流动聚焦(flow-focusing)微流控芯片中。在芯片的交汇处,连续相(油相)将两种水相溶液切割成微米级液滴,迫使噬菌体和细菌在微小的空间内开始接触。
消除预混合偏差:这种设计避免了在封装前噬菌体与宿主发生任何相互作用。如果采用传统的预混合方法,对于像 T7 这样裂解周期短的噬菌体,在实验开始前就可能发生感染和裂解,从而导致感染动力学或滴度定量出现偏差。
通过这种方式,研究人员可以精确控制暴露时间(exposure time),确保数以万计的液滴中每一个感染事件的“计时器”几乎是同时启动的,从而实现对单事件动力学的准确监测。
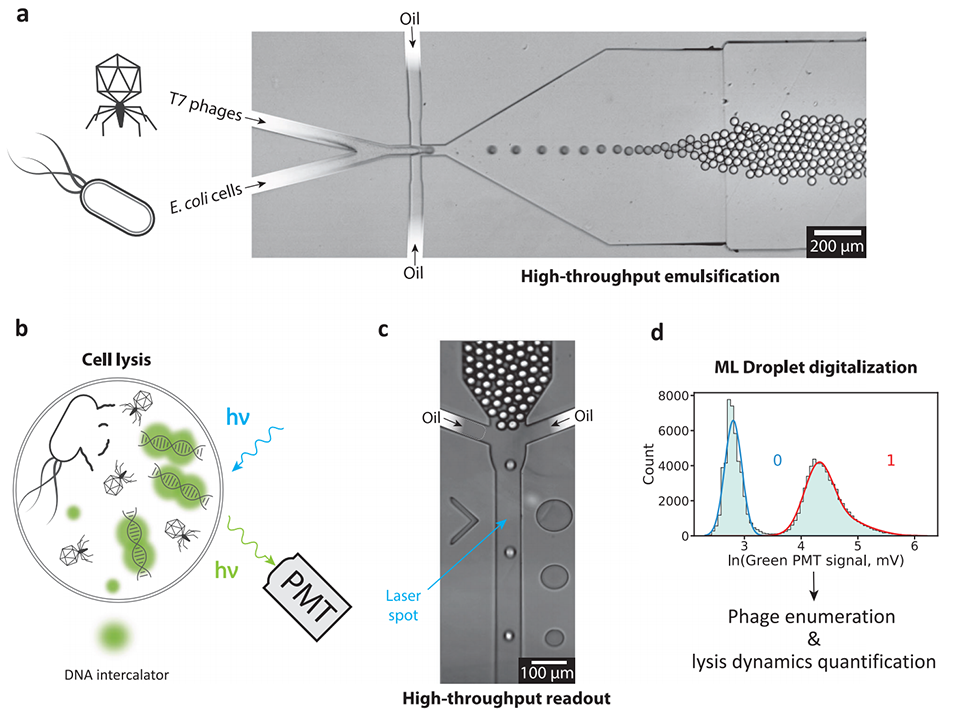
图1 实验流程。a 明场显微镜图像显示了噬菌体和细菌的共封装。乳液在采集前于 37℃ 下孵育。该乳化方案重复了 20 次独立实验。b 液滴内裂解的放大示意图。一种 DNA 嵌入染料(YOYO-1)在裂解发生时会导致绿色荧光发射增强。PMT:光电倍增管。c 高通量液滴采集的明场显微镜图像。间隔油确保液滴被良好分离并依次由激光激发。该采集方案重复了 20 次独立实验。d 绿色荧光信号允许使用高斯混合模型(GMM)对液滴进行数字化处理,以计算数字噬菌体滴度和其他参数。计算考虑了各种因素,如噬菌体和细菌悬浮液之间的混合比例、液滴体积、孵育时间以及细菌细胞密度。
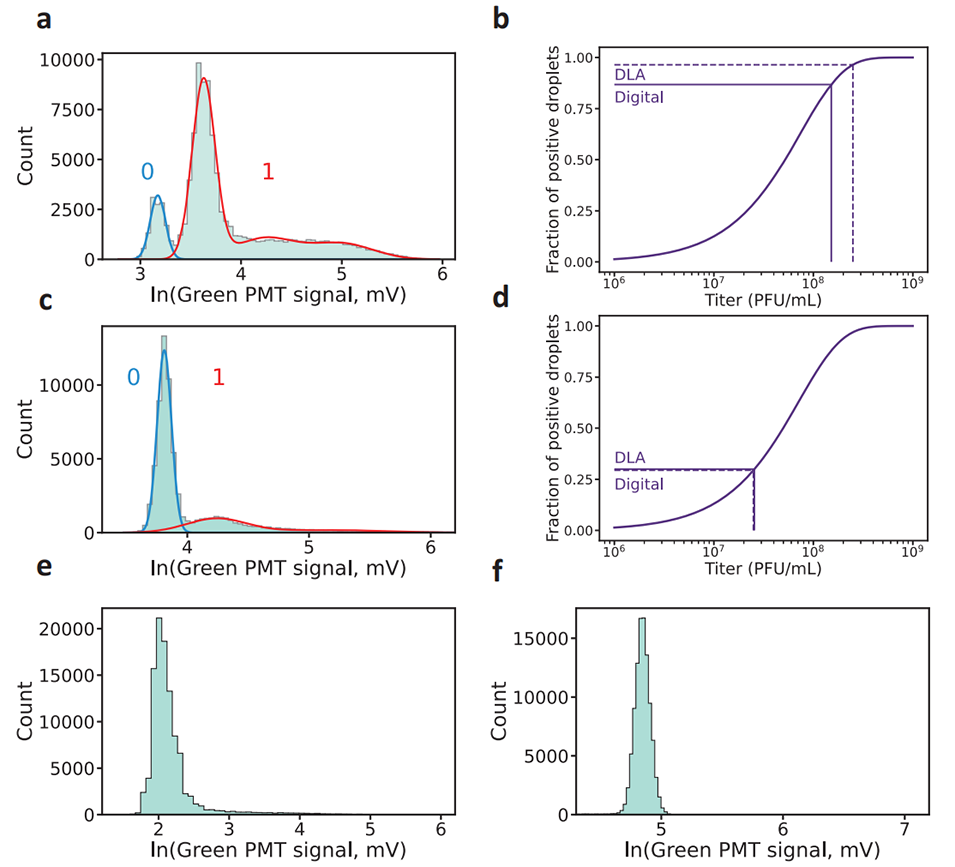
图2 液滴数字化与数字滴度测定。图 a 和 c 分别显示了含有细菌和具有 (a) 高和 (c) 低 DLA 噬菌体滴度的噬菌体液滴的对数转换绿色荧光信号分布(浅蓝色柱状图)。由高斯混合模型检测到的模式分别由蓝色曲线(0,阴性液滴)和红色曲线(1,阳性液滴)表示。PL 通过计算归一化后的所有高阶模式贡献总和相对于总计数的比例来确定。b、d 显示了噬菌体滴度与观测到的阳性液滴比例 PL 之间的理论关系。垂直虚线表示通过 DLA 测定的滴度,水平虚线表示基于 DLA 滴度的预期 PL。相反,数字滴度(垂直实线)是根据实验确定的 PL(水平实线)计算得出的。其计算出的数字滴度分别为 (b) 1.516 × 108 PFU/mL(n= 1.01 × 105 个液滴)和 (d) 2.553 × 107 PFU/mL(n= 6.69 × 104 个液滴),非常接近通过 DLA 测定的滴度,分别为 2.50 × 108 PFU/mL 和 2.50 × 107 PFU/mL。e 无噬菌体时的对数转换绿色荧光信号分布,n= 1.031 × 105 个液滴。f 仅含有红色参考染料的液滴的对数转换绿色荧光信号分布,n= 1.001 × 105 个液滴。该空白检测的光电倍增管增益高于其他子图。
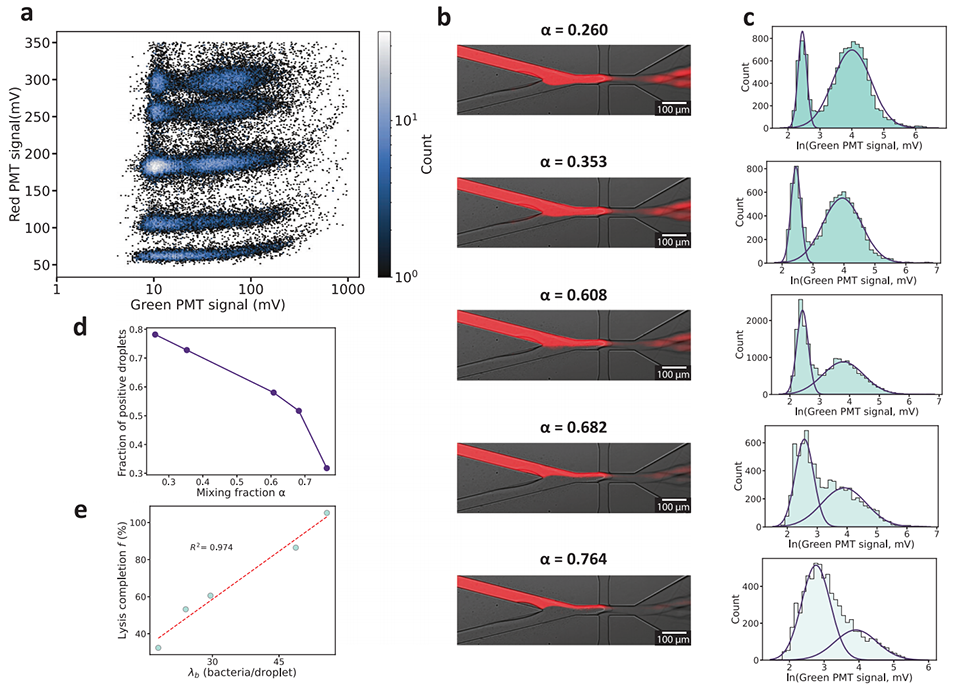
图3 离散混合比例的筛选。a 红色和绿色荧光信号的二维直方图,n= 6.40 × 104 个液滴。b 液滴生成过程中流向聚焦交汇处的荧光与明场显微镜叠加图像。为每个亚群指出了确定的混合比例 α 平均值。该液滴制备方案重复了 4 次独立实验。c 每个亚群的对数转换绿色荧光信号分布(浅蓝色柱状图)。紫色曲线代表由 GMM 预测的阳性和阴性液滴模式,对应的轮廓系数(silhouette scores)分别为 0.616、0.609、0.612、0.605 和 0.609;对于 α 分别为 0.260、0.353、0.608、0.682、0.764 的亚群,液滴数 n 分别为 1.09 × 104、9.30 × 103、2.01 × 104、7.59 × 103 和 6.86 × 103。d 阳性液滴比例 PL 随混合比例 α 的变化函数。e 裂解完成度随预期液滴细菌占有率 λb 的变化函数。100% 裂解完成时的阳性液滴比例是根据 DLA 滴度和溶液中的细菌细胞密度计算出的 λb 得出的。虚线:线性拟合。
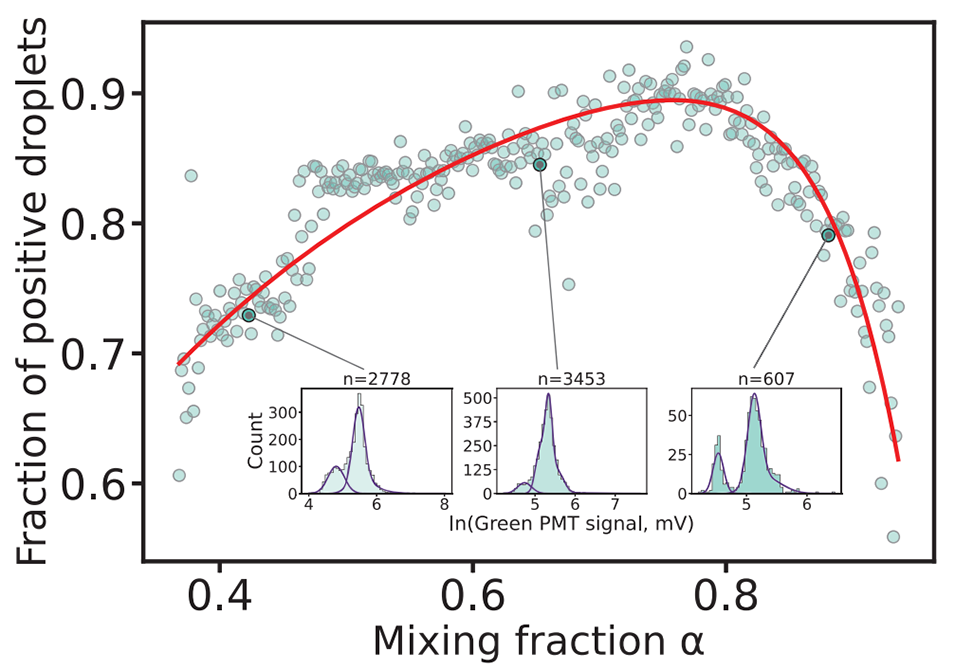
图4 混合比例的连续筛选。蓝色圆点代表红色荧光信号的分组,每组平均包含约 2400 个液滴。分析的总液滴群体为 n=7.20 × 105。每个分组根据其平均红色荧光信号被分配一个 α 值,其阳性液滴比例 PL 由 GMM 确定。此处作为示例的插图展示了 α 值范围内三个分组的对数转换绿色荧光信号分布(蓝色柱状图)以及由 GMM 确定的模式(紫色曲线),n 是该分组中的液滴数量。红色曲线代表方程 (1) 的拟合函数(R2 = 0.784),由此得出的噬菌体滴度为 1.205 × 108 PFU/mL,OD 值为 0.773。
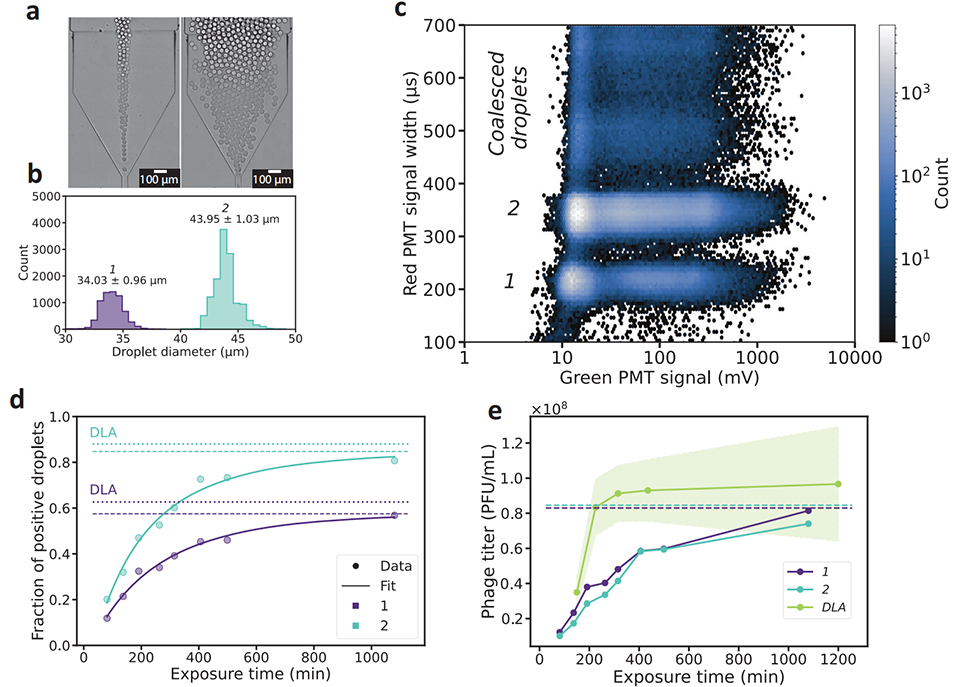
图5 具有双峰大小分布的乳液分析。a 通过明场显微镜监测液滴生成。这种具有两种尺寸模式的乳化方案重复了 4 次独立实验。b 液滴尺寸测量。尺寸模式 1 和 2 的液滴数分别为 n=6.70 × 103 和 n=1.28 × 104。c 孵育 191 分钟后绿色荧光信号与红色荧光信号宽度的二维直方图,n=6.85 × 105 个液滴。d 两种尺寸模式下,细菌暴露于噬菌体不同时间后的阳性液滴比例。圆点:液滴数字化数据。尺寸模式 1 和 2 对应的液滴样本数 n 在图中详述。曲线:方程 (2) 的拟合函数。虚线:来自拟合的极限值。点线:基于从 DLA 获得的滴度计算出的预期阳性液滴比例。e 针对每种尺寸模式从不同暴露时间计算出的数字噬菌体滴度以及来自 DLA 的噬菌体滴度。蓝色和紫色曲线显示了各尺寸模式的数字滴度。绿色曲线代表 DLA 滴度的平均值(n=3,技术重复),绿色阴影区域表示重复实验间的 ±标准差。虚线:基于两种尺寸模式拟合得出的噬菌体滴度。
论文链接:https://doi.org/10.1038/s41467-026-72427-3
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
上一篇:全水相微流控技术实现微凝胶无油量产,细胞存活率超 99%
下一篇:暂无














