研究背景
微凝胶因其高含水量、优异的生物相容性和可调的物理化学性质,在组织工程、再生医学及药物递送领域展现出显著优势。传统的液滴微流控技术虽能生产单分散微凝胶,但大多基于油包水(W/O)体系,制备后需通过繁琐的洗涤步骤去除油相和表面活性剂,这往往会损害封装细胞的活性。
为了解决上述问题,双水相系统(ATPS)作为一种“水包水”策略受到关注,它完全无需油相,能提供更接近生理微环境的条件。然而,ATPS 面临两大核心挑战:
1、稳定性难题:由于水-水界面张力极低,液滴形成不稳定,通常需要复杂的外部阀门控制装置,这增加了操作难度并限制了规模化生产。
2、材料局限性:现有 ATPS 技术高度依赖海藻酸盐(Alg),但其固有的刚性会限制细胞的粘附、铺展与增殖。
因此,临床转化急需一种无需辅助控制、生物相容性更高且具备材料通用性的微凝胶制备新方法,以实现对微米级结构和形貌的精准定制。

导读:
近期,广州医科大学药学院唐国胜教授团队开发了一种全水相微流控技术,用于制造具有高度一致性的单分散微凝胶。该方法通过使用双水相系统 (ATPS),彻底摒弃了传统工艺中对有机油类和表面活性剂的依赖,从而显著提升了材料的生物相容性。研究人员通过精准调节流体参数与光固化位置,实现了对微凝胶尺寸、孔隙率及几何形状(如球形或纤维状)的灵活定制。
这种平台展现了极强的材料适配性,能够处理包括GelMA和透明质酸在内的多种生物聚合物。实验证明,载有壳寡糖的多孔微凝胶能有效延长药物在体内的停留时间,并成功用于霍乱弧菌感染的预防与治疗。这一创新方案为组织工程、精准药物递送及再生医学领域提供了更安全、高效且可扩展的制造策略。相关研究以“Scalable and oil-free fabrication of monodisperse microgels via all-aqueous microfluidics”为题目,发表于期刊《Cell Reports Physical Science》。
本文要点:
1. 技术创新:全水相微流体系统 (ATPS)
无油无表面活性剂:开发了一种基于水-水(W/W)型双水相系统(ATPS)的一步法策略,利用其极低的界面张力,在无需添加油相或表面活性剂的情况下实现微凝胶的规模化生产。
无需复杂控制:与以往依赖外部阀门控制或振荡辅助的全水相系统不同,该方法通过精确调节相流速、前体组成和同轴喷嘴配置,即可稳定形成液滴,简化了设备设计并提高了操作稳定性。
2. 形态与尺寸的高度可调性
形貌定制:通过空间调节紫外(UV)固化的位置,可以实现形貌的灵活控制——在上游固化可产生纤维状微凝胶,在下游固化则产生球形微凝胶。
复杂结构:通过引入致孔剂(如PEO)可制备多孔微凝胶,利用多通道喷嘴则能制备具有物理分隔性质的Janus微凝胶。
精确控径:通过调节流速比、凝胶浓度和喷嘴直径,微凝胶的直径可在 77 至 710 μm之间精确控制,且具有极低的组内偏差(CV < 10%)。
3. 广泛的材料兼容性与生物相容性
材料普适性:该平台证明了对多种生物材料的兼容性,包括 GelMA、HAMA、丝素蛋白(SS)和 F127-DA。
卓越的细胞相容性:由于不含有机溶剂,该过程确保了极高的细胞存活率(>99.8%)。实验表明,封装在 GelMA 微凝胶中的 HUVEC 细胞表现出比传统海藻酸钠(Na-Alg)微凝胶更好的细胞铺展和骨架发育能力。
4. 生物医学应用:霍乱预防与治疗
载药应用:研究者制备了负载壳寡糖(COS)的多孔球形 GelMA 微凝胶(CPGM)。
长效性能:相比于海藻酸盐载体,GelMA 微凝胶展现出更强的耐酸性,能有效保护药物通过胃部并在肠道内显著延长留存时间(达48小时)。
疗效验证:动物实验证明,CPGM 能显著降低小鼠肠道内的霍乱弧菌( cholerae)定植量,抑制毒力基因表达,并减轻肠道炎症及组织损伤。
总结:该研究克服了传统油包水(W/O)系统需繁琐洗涤以及传统全水相系统依赖阀门控制的局限,为组织工程、细胞递送及精准医疗提供了一种高效、通用且生物友好的微加工工具。
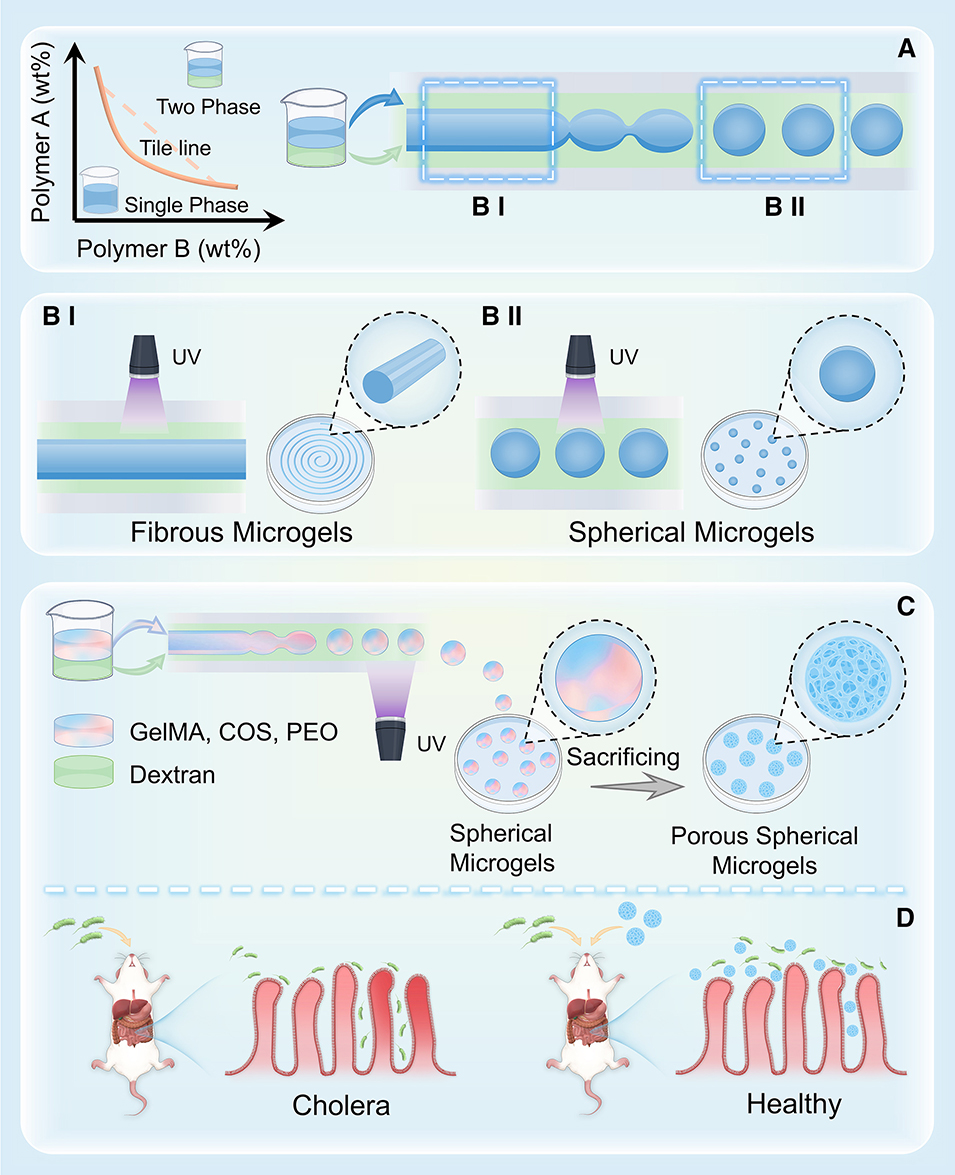
图1. ATPS 液滴微流控策略的开发及其在霍乱治疗和预防中的应用。(A) ATPS 相图以及利用基于 ATPS 的微流控策略制备微凝胶的示意图。(B) 通过调节微流控通道内紫外线(UV)固化的位置,基于 ATPS 的微流控平台能够实现对微凝胶形貌(BI,纤维状;BII,球形)和结构的精确时空控制。(C 和 D) 负载壳寡糖(COS)的多孔球形 GelMA 微凝胶的制备示意图 (C) 及其在霍乱治疗和预防中的应用 (D)。
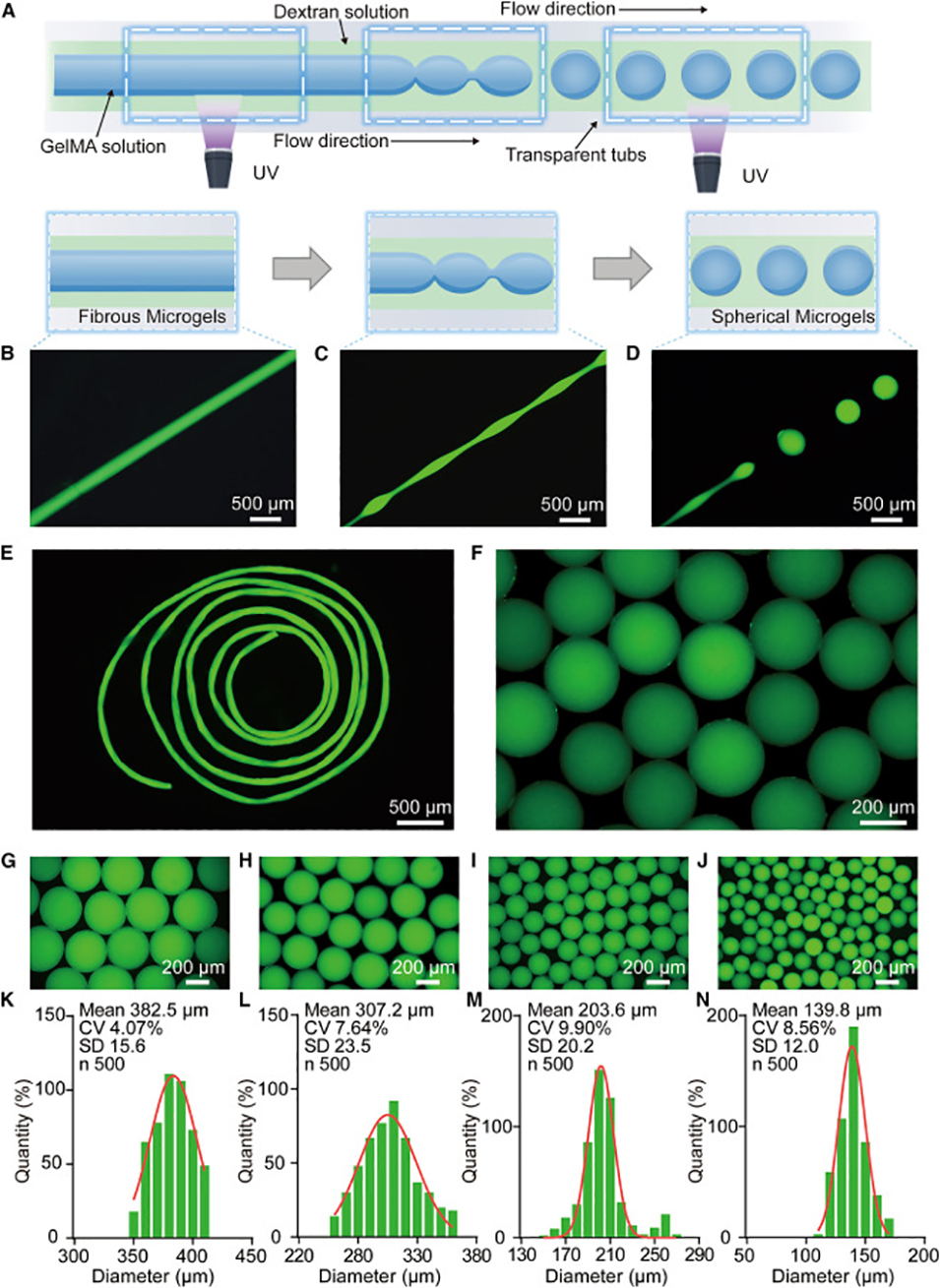
图2. ATPS 液滴微流控系统。(A) 用于制备 GelMA 微凝胶的 ATPS 液滴微流控系统示意图。(B–D) 与示意图相对应的微通道内 GelMA 微凝胶形成的实时荧光图像。比例尺:200 μm。(E 和 F) 纤维状微凝胶 (E) 和球形微凝胶 (F) 的选择性制备。比例尺:500 μm。(F) 通过调节微通道内的不同固化位置制备而成。比例尺:200 μm。(G–N) 具有宽粒径范围(从 130 到 400 μm)且低多分散性的球形 GelMA 微凝胶 (G–J)。比例尺:200 μm。(K–N) 中的微凝胶可通过 ATPS 液滴微流控策略生产。连续相(右旋糖酐)的流速分别为 10、20、30 和 50 μL/min,而分散相(GelMA)的流速始终为 1 μL/min。数据以落在每个直径范围内的微凝胶百分比表示。

图3. ATPS 液滴微流控策略实现微凝胶形貌的精确定制。(A–F) 通过基于 ATPS 的微流控策略生产的均质型 (A 和 B)、多孔型 (C 和 D) 以及 Janus 型 (E 和 F) 球形微凝胶的显微镜和扫描电镜(SEM)图像。均质微球使用纯 GelMA 溶液作为分散相获得,而多孔微球使用 GelMA/PEO 混合溶液生产,其中 PEO 作为牺牲组分。Janus 多孔微球通过引入不同颜色的荧光染料进一步区分。比例尺:(A)、(C)、(E) 为 200 μm,(B)、(D)、(F) 为 30 μm。(G–R) 展示通过调节各种参数实现微纤维直径可调性的代表性图像:连续相(右旋糖酐)流速分别为 1,000、400、80 和 50 μL/min (G–J);分散相(GelMA)流速分别为 3、5、7 和 9 μL/min (K–N);以及分散相 GelMA 浓度分别为 5、10、15 和 20 wt% (O–R)。比例尺:200 μm。(S–U) 相应微纤维直径的定量分析。显著性通过单因素方差分析(one-way ANOVA)确定,并以 p 值表示。****p < 0.0001。数据以平均值 ± 标准差(SD)表示。
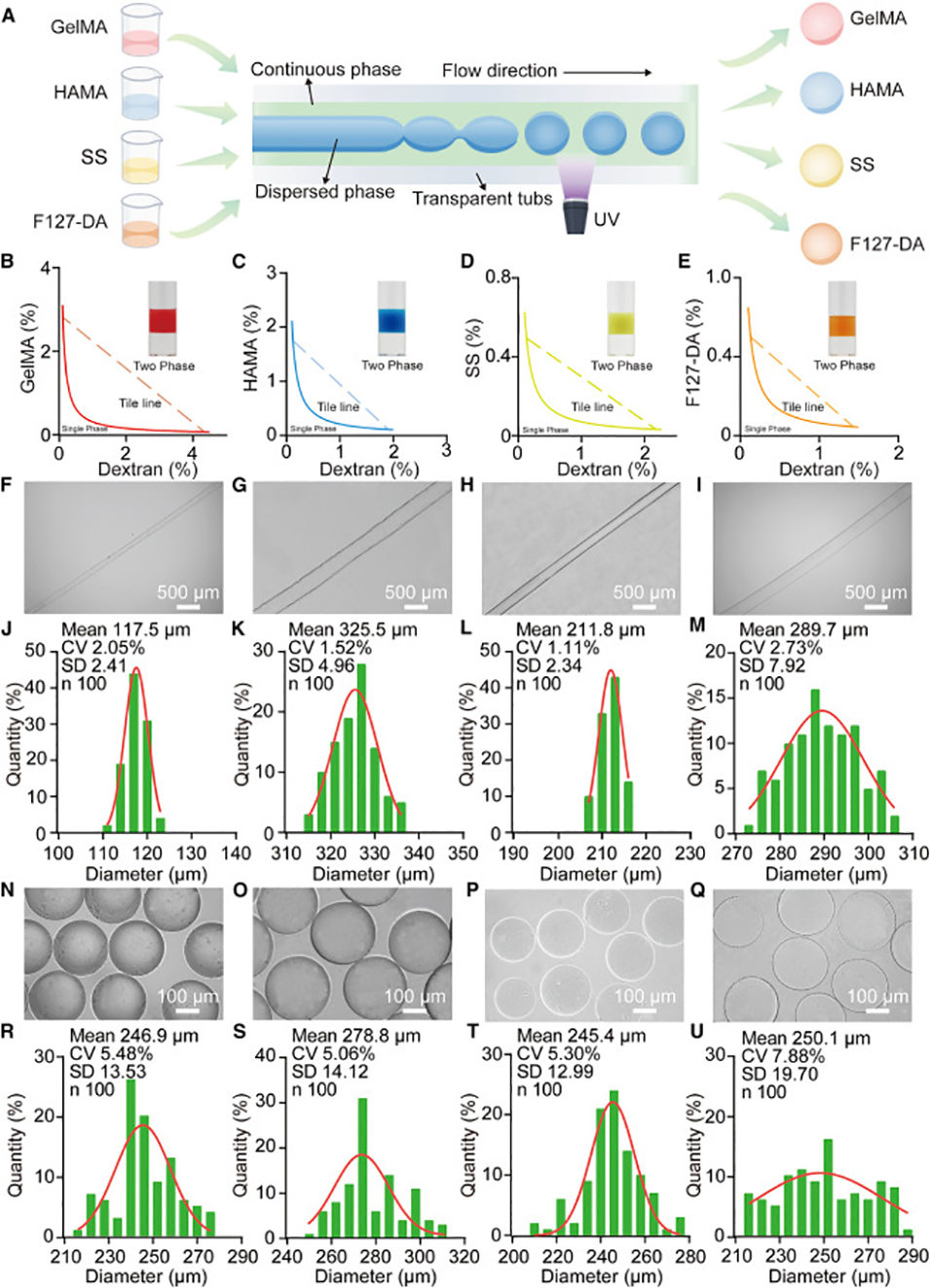
图4. 基于 ATPS 的微流控策略具有广泛的材料适应性。(A) ATPS 制备策略的广泛材料适应性。(B–E) 由右旋糖酐与 GelMA (B)、HAMA (C)、SS (D) 以及 F127-DA (E) 组成的 ATPS 相图。双节线(binodal curve)被划定为单相区和两相区之间的临界边界。两相区中的初始点根据系线(tie line)分离成两个热力学平衡的水相:富含右旋糖酐相和另一相。(F–U) 由相应的 ATPS 组合制备的微纤维 (F–I) 和微球 (N–Q) 及其尺寸分布 (J–M 和 R–U)。比例尺:(F–I) 为 500 μm,(N–Q) 为 100 μm。数据以落在每个直径范围内的微凝胶百分比表示。
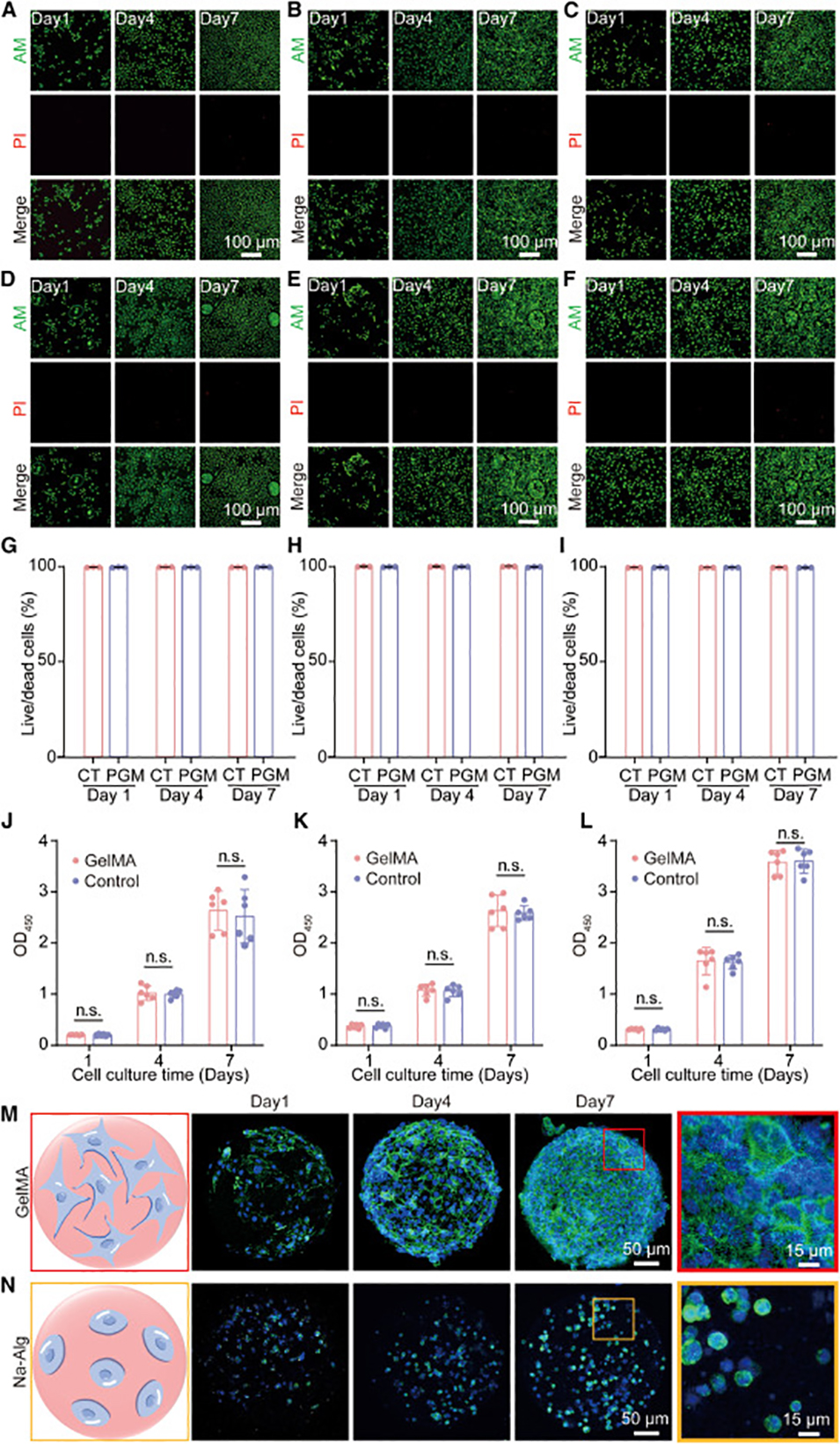
图5. 通过 ATPS 液滴微流控策略制备的微凝胶的生物相容性。(A–C) 通过 CCK-8 实验评估对照组(A549 细胞、HeLa 细胞和 HUVEC 细胞)在培养 1、4 和 7 天后的细胞增殖定量分析。(D–F) 通过 CCK-8 实验评估 PGM 组(A549 细胞、HeLa 细胞和 HUVEC 细胞)在培养 1、4 和 7 天后的细胞增殖定量分析。比例尺:100 μm。(G–L) 不同细胞系与 GelMA 微球共培养 1、4 和 7 天后的活/死染色图像 (G–I) 及其相应的细胞活力定量分析 (J–L)。(M 和 N) 通过共聚焦激光扫描显微镜(CLSM)观察在 GelMA (M) 和海藻酸钠 (Na-Alg) (N) 微球上培养 1、4 和 7 天后的 HUVEC 细胞的纽带蛋白(Vinculin)免疫荧光染色。比例尺为 50 μm,框选区域为 15 μm。显著性通过双因素方差分析(two-way ANOVA)确定,并以 p 值表示。n.s.,p > 0.05。数据以平均值 ± 标准差(SD)表示。
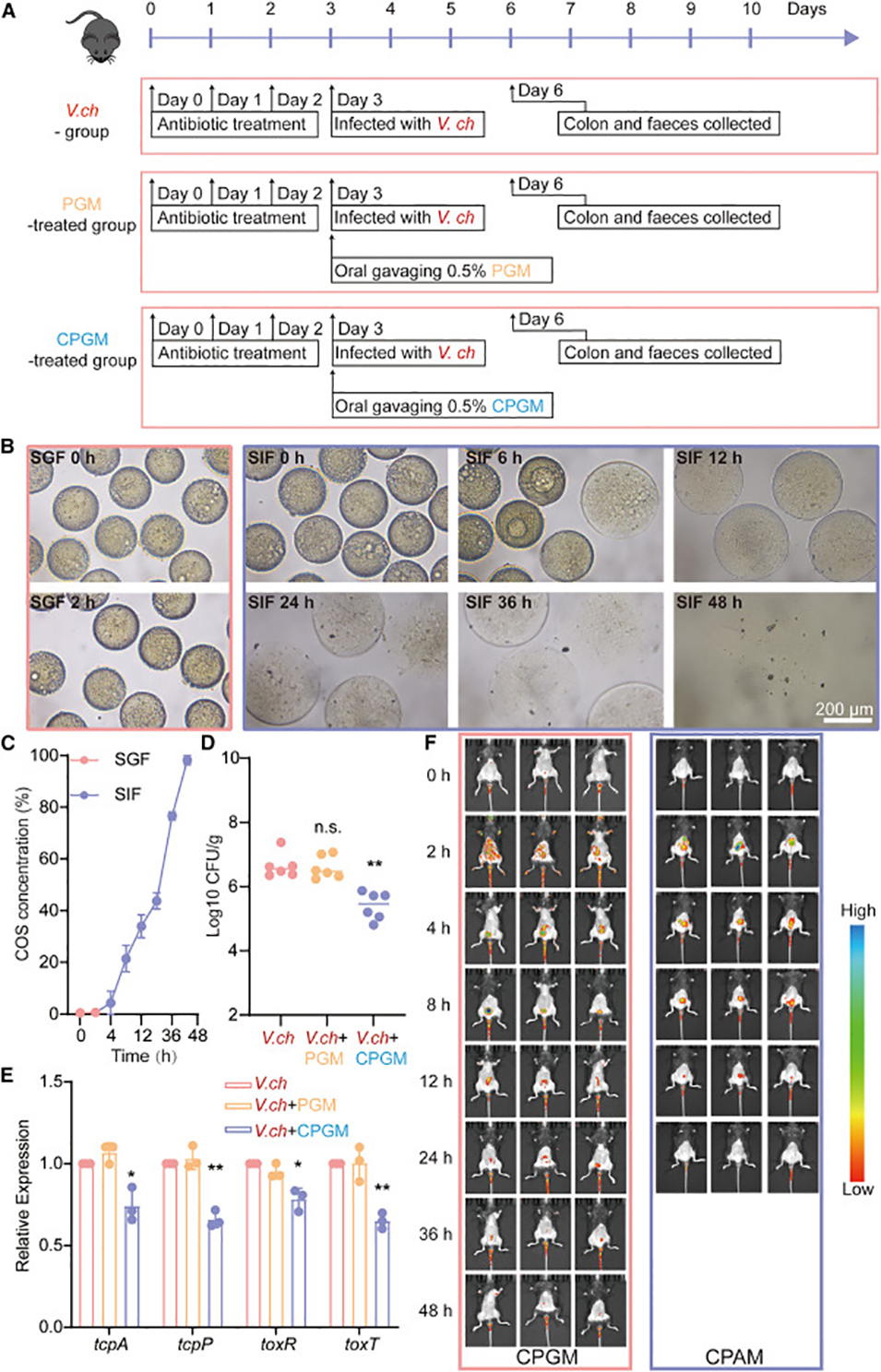
图6. 负载壳寡糖(COS)的 GelMA 微球用于控制霍乱弧菌定植。(A) 霍乱弧菌定植感染模型示意图。(B) 负载 COS 的 GelMA 微球在模拟胃液(SGF)和模拟肠液(SIF)中的溶解情况。比例尺:200 μm。(C) 通过紫外分光光度计检测 COS 在 SGF 和 SIF 中的释放情况。(D) 评估在细菌口服挑战时给予 PGM 和 CPGM 的成年小鼠,在感染 3 天后肠道内霍乱弧菌的定植能力(n = 7)。(E) 感染 24 小时后,给予 0.5% PGM 或 CPGM 的成年小鼠小肠中霍乱弧菌毒力基因(tcpP、toxT、ctxA 和 tcpA)的 RT-qPCR 表达水平(n = 3)。(F) 通过活体成像系统(IVIS)检测 CPGM 和 CPAM(负载 COS 的多孔海藻酸盐微球)在小鼠体内的滞留时间。比例尺为 500 μm,框选区域为 100 μm。显著性通过双侧曼-惠特尼 U 检验(Mann-Whitney U test)或双尾非配对 Student's t 检验确定,并以 p 值表示。*p < 0.05,**p < 0.01,***p < 0.001。数据以平均值 ± 标准差(SD)表示。
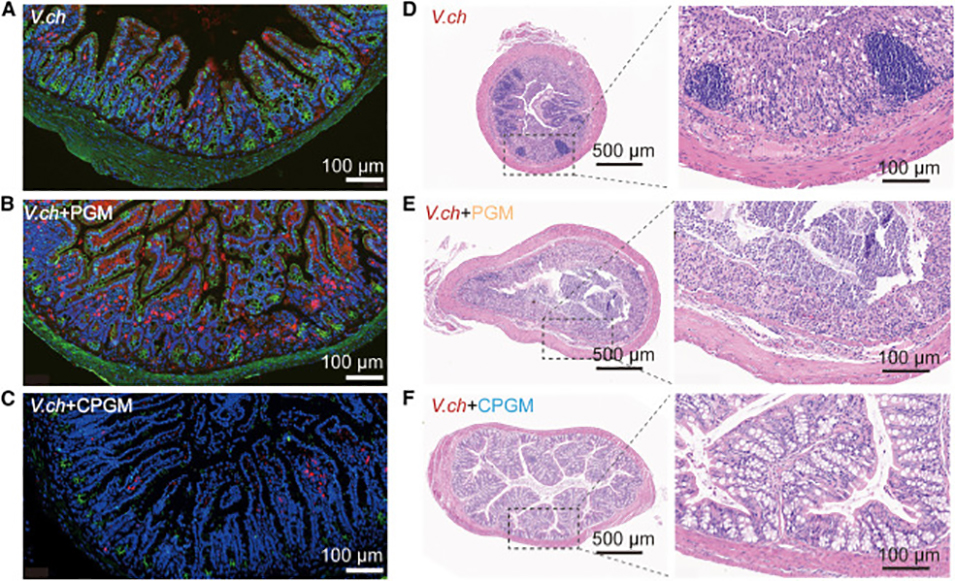
图7. CPGM 减轻霍乱相关的肠道炎症。(A–C) 对照组、PGM 组和 CPGM 组小肠的免疫荧光双染色,显示了肿瘤坏死因子-α(TNF-α,绿色)、白细胞介素-1β(IL-1β,红色)和细胞核(蓝色)。比例尺:100 μm。(D–F) 给予 0.5% PGM 或 CPGM 的成年小鼠小肠中霍乱弧菌的 H&E 染色。所有分析均在感染后 3 天进行。比例尺为 500 μm,框选区域为 100 μm。
论文链接:https://doi.org/10.1016/j.xcrp.2026.103253
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
下一篇:暂无














