研究背景与研究意义
1、HCC与TARE疗法:肝细胞癌(HCC)是全球高发致死的恶性肿瘤,经动脉放射栓塞(TARE)治疗作为微创姑息治疗手段,通过将载治疗性核素的栓塞剂注入肿瘤供血动脉,结合动脉栓塞与局部放疗,相比全身治疗具有全身毒性低、患者依从性高的优势,是不可切除HCC的标准治疗方案。
2、现有 TARE 微球的缺陷
FDA批准的⁹⁰Y玻璃/树脂微球:不可降解,肿瘤复发后无法重复治疗;玻璃微球密度高注射难,树脂微球比活度低需大剂量给药,易反流至非靶血管。
欧洲获批的¹⁶⁶Ho-PLA微球:虽可降解、能SPECT成像,但¹⁶⁶Ho半衰期短,储存运输难、成本高。
核素标记技术:现有聚多巴胺、膦酸功能化硅胶标记法步骤复杂,易造成微球损伤。
3、研究切入点
选择¹⁷⁷Lu:半衰期7天,理化性质优异,可发射γ射线实现SPECT成像,成本低、物流便利,适合TARE治疗。
选择P204(二 - 2 - 乙基己基磷酸):阳离子交换萃取剂,能高效络合稀土金属离子,不溶于水,络合物稳定性高,且可实现核素按需标记,避免传统预加载的辐射损伤。
选择微流控技术:可制备单分散、粒径可控的微球,解决传统方法粒径分布宽的问题。

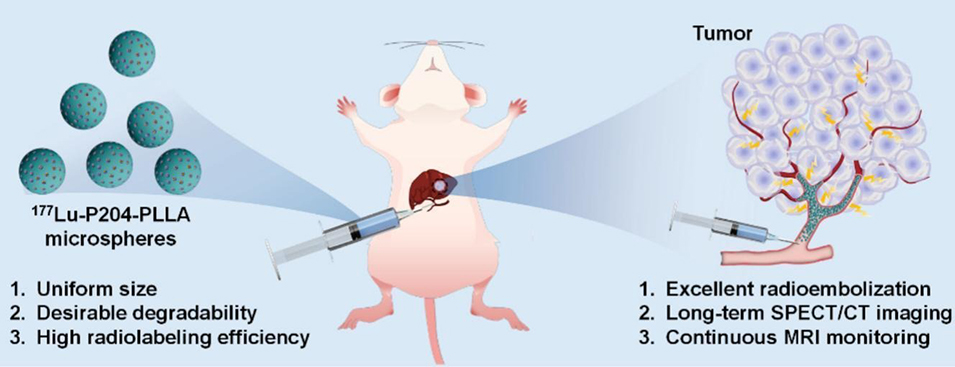
该研究以“Monodisperse lutetium-177-labeled poly(lactic acid) microspheres for radioembolization therapy of hepatocellular carcinoma”为题发表于期刊《Chemical Engineering Journal》,由四川大学褚良银教授、巨晓洁教授团队完成,旨在开发适用于肝细胞癌经动脉放射栓塞(TARE)治疗的新型可降解单分散微球,解决现有微球不可降解、粒径分布宽、无在体追踪能力的临床局限。
本文要点:
1、该研究通过微流控乳化结合真空浸渍法,制备出掺杂二 (2 - 乙基己基) 磷酸(P204)的聚 L - 乳酸(PLLA)微球,再经阳离子交换实现镥 - 177(¹⁷⁷Lu)标记,得到 ¹⁷⁷Lu-P204-PLLA 微球。
2、该微球可通过调控 PLLA 浓度和外相流速精准控制粒径(20-50μm),具备良好的可注射性、可降解性和生物相容性,¹⁷⁷Lu 标记效率达 97.45%,在 PBS 和大鼠血清中 28 天放射化学纯度仍超 91.23%。
3、在大鼠肝癌模型中,经肝动脉输注该微球后,SPECT/CT 成像显示其能长期稳定栓塞肿瘤供血动脉,无明显脱靶蓄积;肿瘤体积仅扩增 5 倍(未处理组达 172 倍),大鼠中位生存期从 53 天延长至 99 天以上,且对肝、肾等正常组织无显著毒性,血液指标和组织病理均无异常。
4、研究证实,¹⁷⁷Lu-P204-PLLA 微球兼具在体追踪、高效抑瘤、良好生物安全性的优势,克服了现有 TARE 微球的诸多缺陷,成为肝细胞癌放射性栓塞治疗的极具潜力的新型制剂。
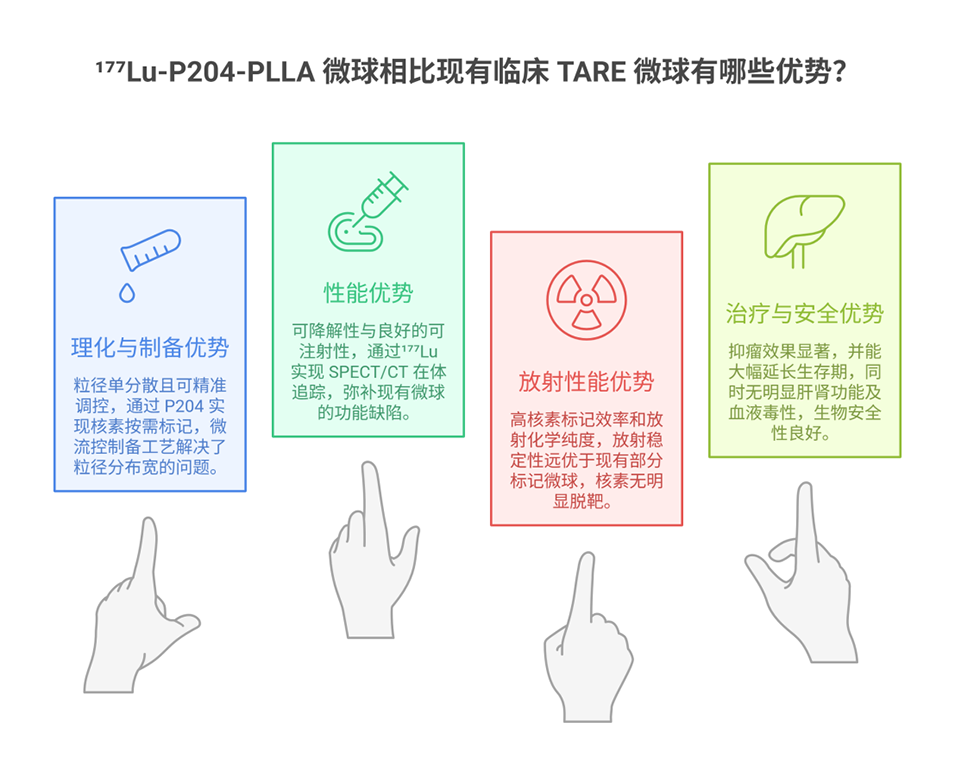
P204 在 ¹⁷⁷Lu-P204-PLLA 微球的制备与功能实现中,起到了哪些不可替代的作用?
P204 是该微球的核心功能组分,具体作用体现在:
1、核素标记的关键:PLLA 微球自身仅通过末端羧基络合金属离子,稳定性差,无法有效结合 Lu³⁺,而 P204 作为阳离子交换萃取剂,能高效、稳定络合 ¹⁷⁷Lu³⁺,实现 97.45% 的高标记效率,是微球能成功负载 ¹⁷⁷Lu 的前提;
2、提升放射稳定性:P204 与 ¹⁷⁷Lu 形成的络合物化学稳定性高,使微球在 PBS 和大鼠血清中 28 天放射化学纯度仍超 91.23%,避免核素脱落造成的非靶组织毒性;
3、实现核素按需标记:P204 的络合特性使微球可在制备完成后根据需求进行核素标记,完全避免了传统预加载、中子活化体系中辐射对微球的损伤,提升了微球的制备与应用灵活性。
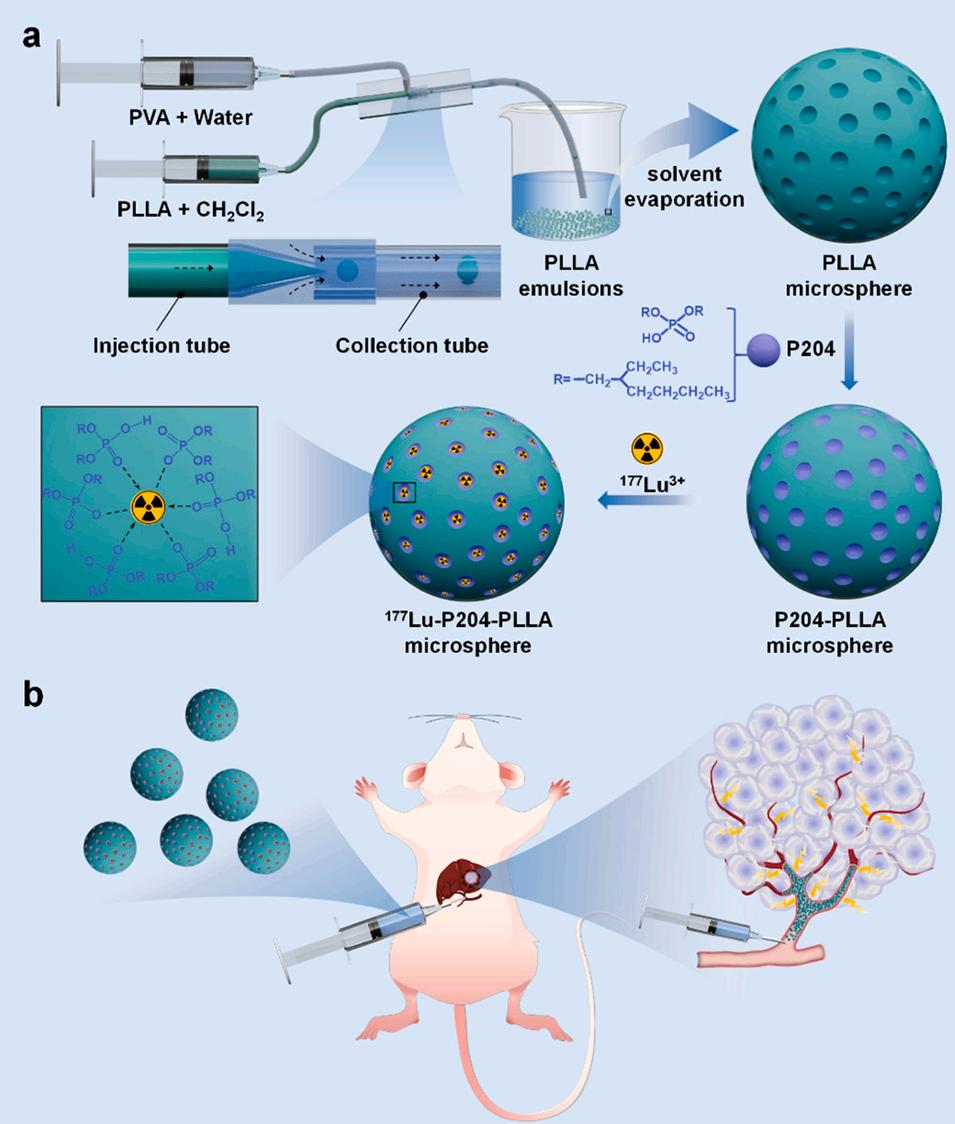
图1. ¹⁷⁷Lu 标记 P204 掺杂聚 L - 乳酸微球(¹⁷⁷Lu-P204-PLLA)的制备流程(a)及治疗过程示意图(b)
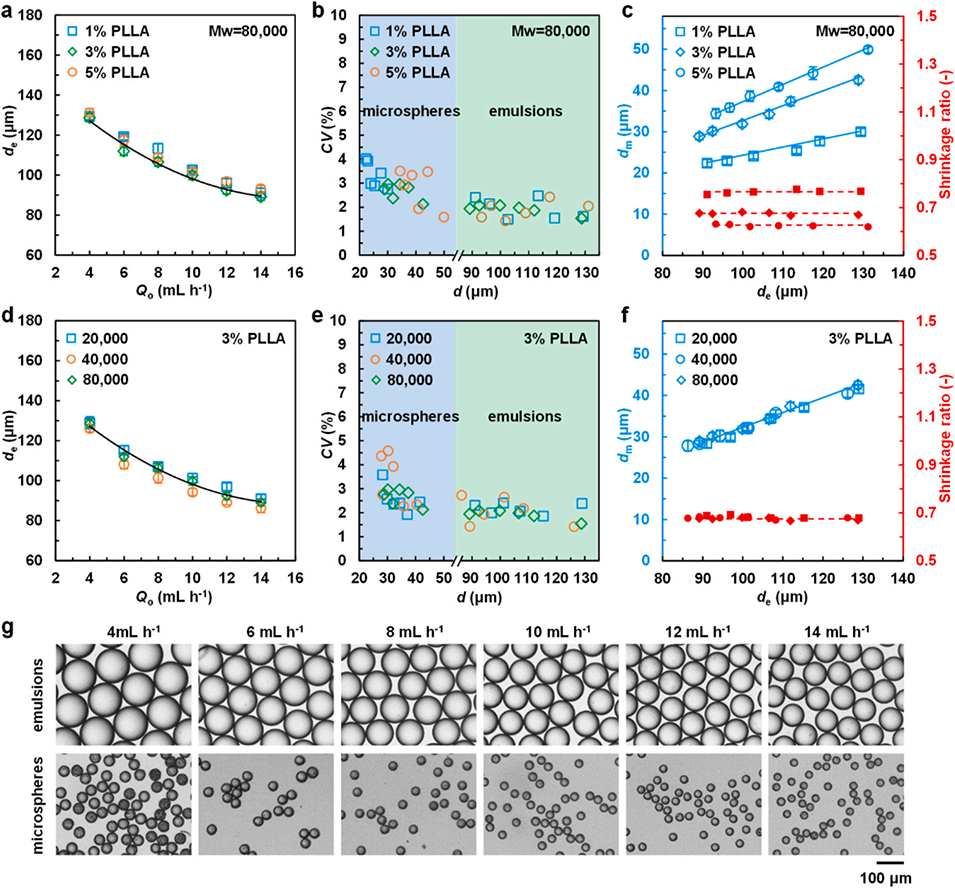
图2. 外相流速、聚 L - 乳酸浓度和分子量对乳液模板及所得微球的粒径和单分散性的影响。(a-c):外相流速和聚 L - 乳酸浓度对乳液模板粒径(a)、乳液模板及对应微球的变异系数(b)、微球粒径与乳液模板粒径的关系及粒径收缩率(c)的影响;(d-f):外相流速和聚 L - 乳酸分子量对乳液模板粒径(d)、乳液模板及对应微球的变异系数(e)、微球粒径与乳液模板粒径的关系及粒径收缩率(f)的影响;(g)以分子量 80000、浓度 3%(质量体积比)的聚 L - 乳酸为内相,在不同外相流速下制备的乳液模板和微球的光学显微镜图像(内相流速为 1 mL・h⁻¹)
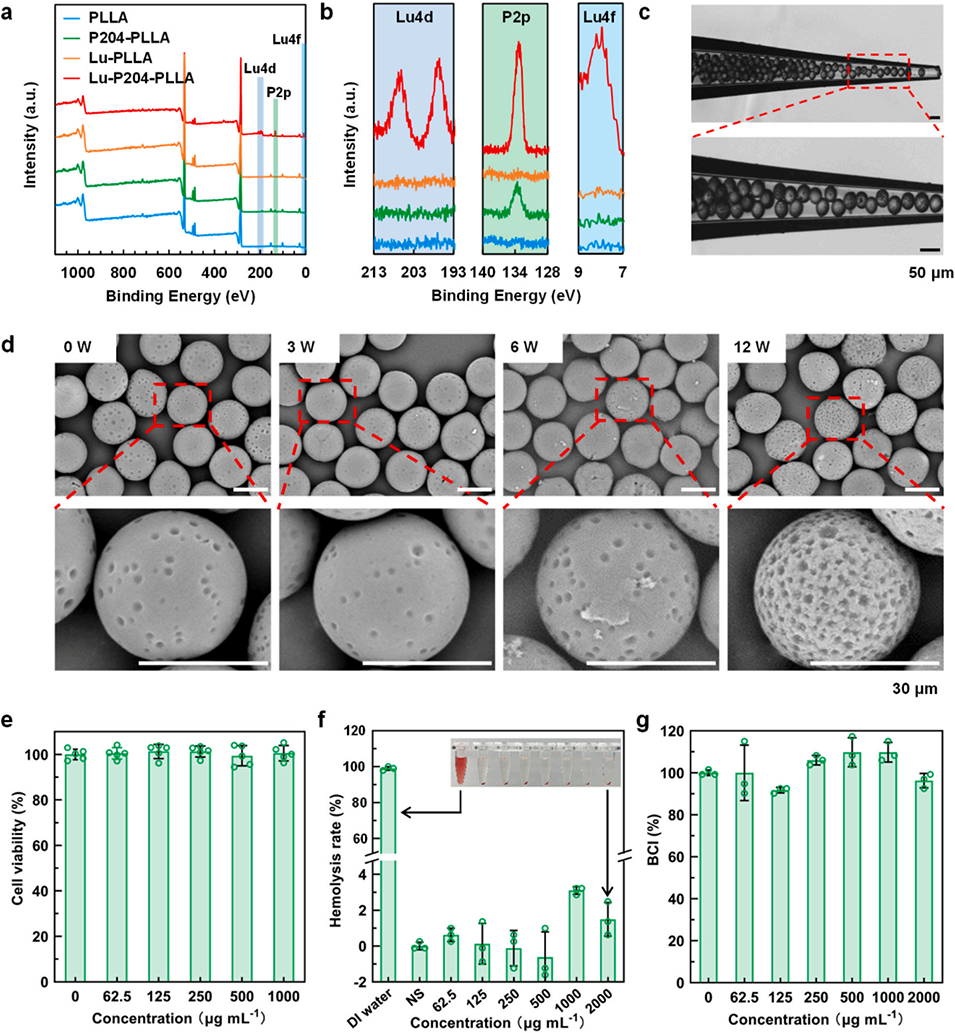
图3. P204-PLLA 微球的材料表征、体外栓塞行为、降解特性及生物相容性。(a)微球的 X 射线光电子能谱图;(b)Lu 4d、P 2p 和 Lu 4f 能谱区的高分辨率 X 射线光电子能谱图;(c)P204-PLLA 微球栓塞玻璃毛细管的光学显微镜图像;(d)P204-PLLA 微球在大鼠血清中孵育 0、3、6、12 周后的扫描电子显微镜图像;(e-g)P204-PLLA 微球的体外生物相容性评价:细胞活力(e)、溶血率(f)、血液凝固指数(g)
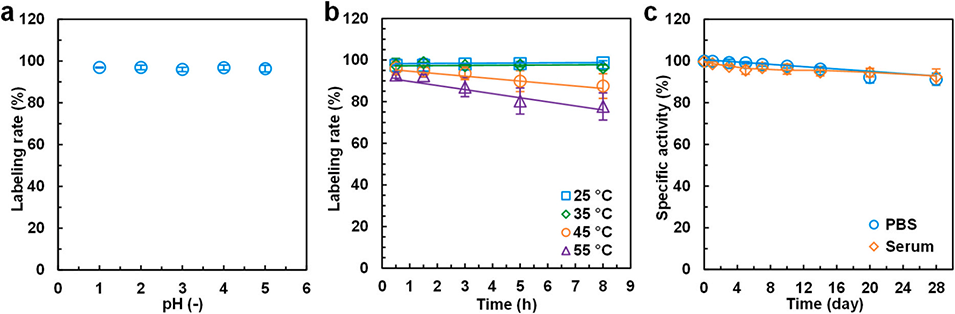
图4. 放射性标记效率与稳定性评价。(a、b)pH 值(a)、温度和反应时间(b)对放射性标记效率的影响;(c)¹⁷⁷Lu-P204-PLLA 微球在磷酸盐缓冲液和大鼠血清中的放射性稳定性随时间的变化
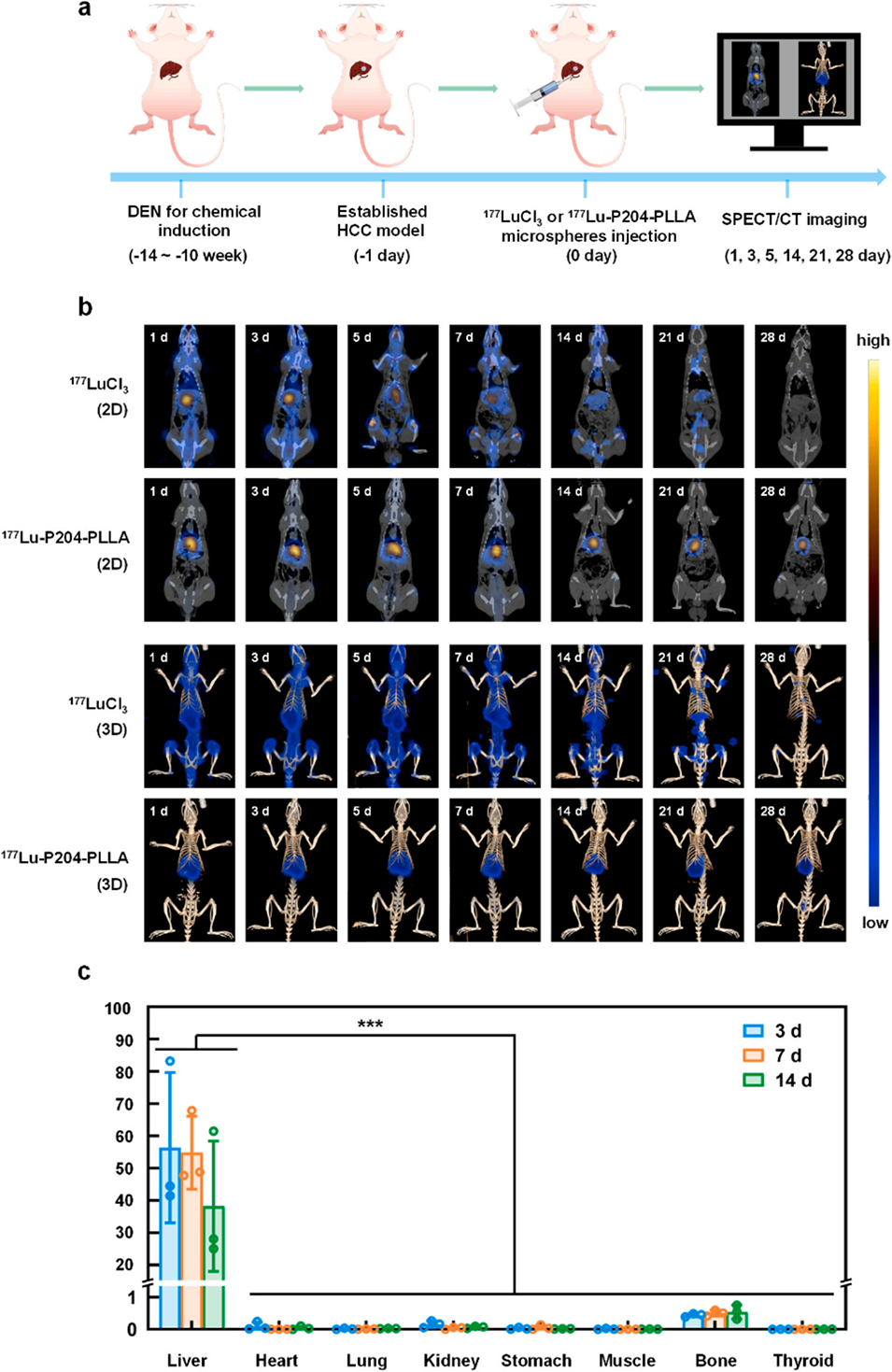
图5. 经动脉注射后,¹⁷⁷LuCl₃ 和 ¹⁷⁷Lu-P204-PLLA 在大鼠体内的分布及稳定性(全身单光子发射计算机断层扫描/计算机断层扫描成像检测)。(a)实验时间线;(b)代表性的单光子发射计算机断层扫描/计算机断层扫描图像;(c)¹⁷⁷Lu-P204-PLLA 在大鼠主要脏器中于注射后 3、7、14 天的体内分布情况(n=3,采用单因素方差分析结合杜凯氏多重比较检验计算 P 值,***P<0.001)
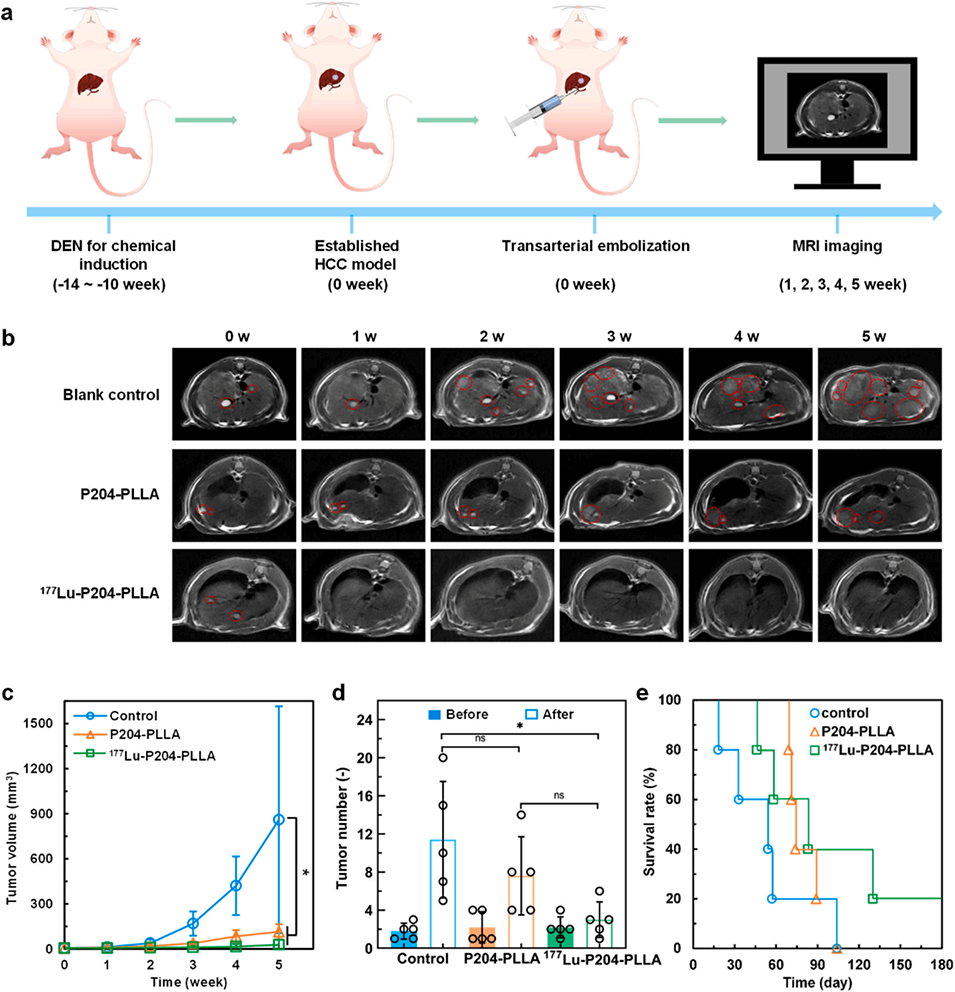
图6. ¹⁷⁷Lu-P204-PLLA 微球在大鼠肝癌模型中的体内治疗效果。(a)实验时间线;(b)大鼠肝脏治疗前后的代表性磁共振成像图像;(c)各组大鼠的肿瘤生长曲线(n=5);(d)治疗前(0 周)和治疗后(5 周)大鼠肿瘤数量的定量分析(n=5);(e)不同实验组大鼠的生存曲线(采用单因素方差分析结合杜凯氏多重比较检验计算 P 值,*P<0.05)
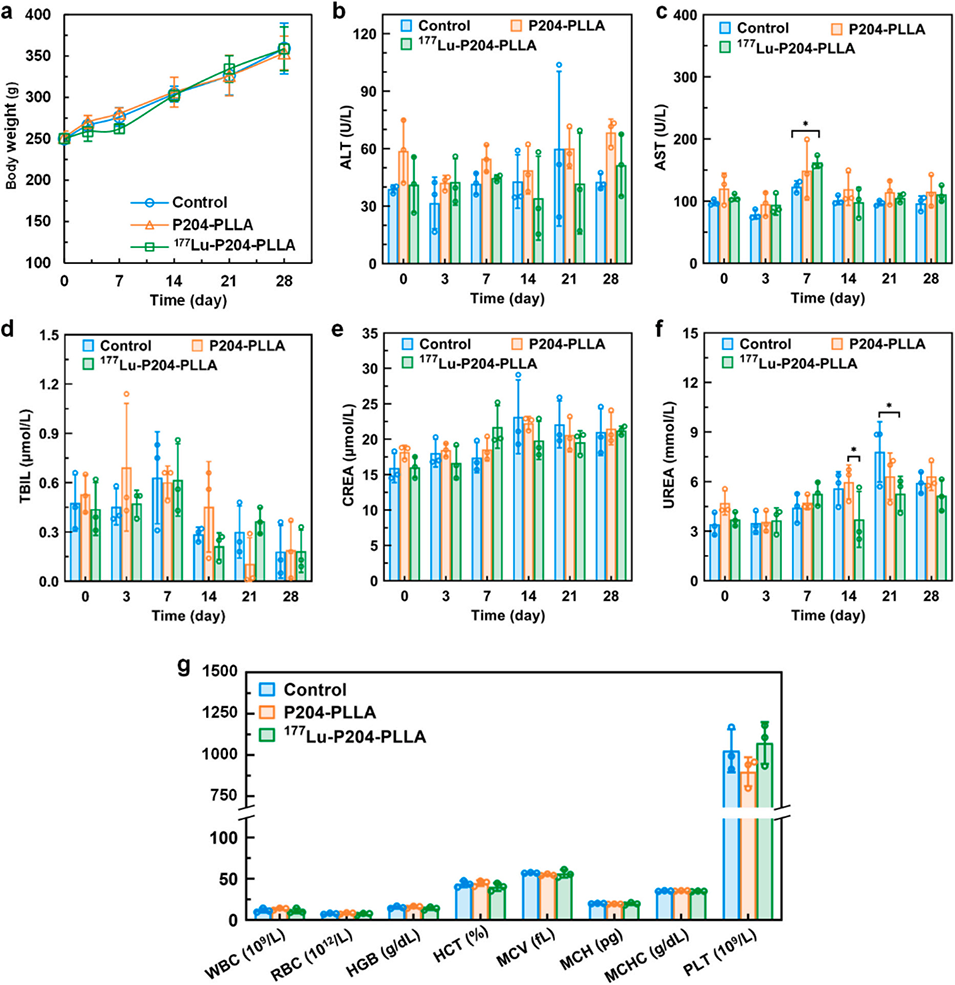
图7. P204-PLLA 和 ¹⁷⁷Lu-P204-PLLA 微球经肝动脉注射后在大鼠体内的生物安全性评价(n=3)。(a)不同实验组大鼠的体质量变化;(b-f)各组大鼠血清中的谷丙转氨酶(b)、谷草转氨酶(c)、总胆红素(d)、肌酐(e)和尿素(f)水平;(g)注射后 28 天各组大鼠的血常规检测结果(采用双因素方差分析结合杜凯氏多重比较检验计算 P 值,*P<0.05)
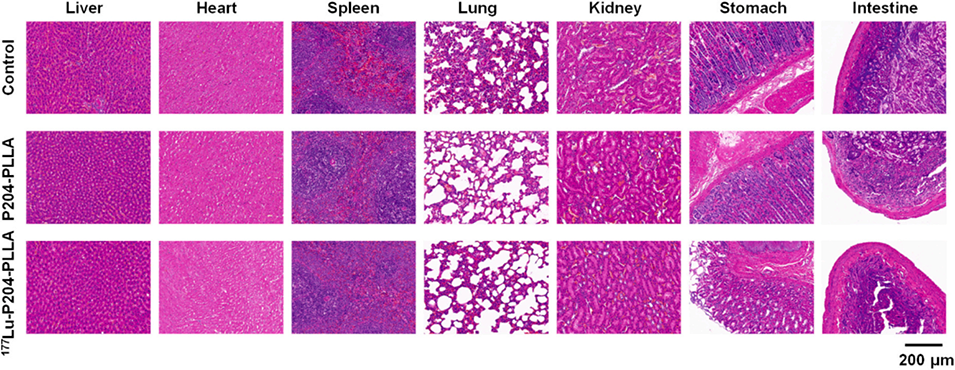
图8. 注射后 28 天,不同实验组大鼠的肝、心、脾、肺、肾、胃和肠组织经苏木精-伊红染色后的组织病理学分析图像(标尺为 200 μm)
论文链接:https://doi.org/10.1016/j.cej.2026.174448
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














