
导读:
肿瘤球体是3D细胞培养的重要模型,广泛应用于药物反应评估,但高通量生成均一、功能性球体仍具挑战。近期,澳大利亚多所高校团队合作开发了一种流动聚焦式液滴微流控平台,实现肿瘤球状体的高通量、均一化生成,并将其应用于siRNA纳米药物的疗效评估,填补了液滴微流控生成的肿瘤球状体在纳米药物蛋白水平高通量功能评价中的研究空白。相关成果以“High-Throughput Generation of Tumor Spheroids via Droplet Microfluidics for siRNA-Loaded Nanomedicine Assessment”为题目,发表在期刊《Advanced Healthcare Materials》上。
本文要点:
1、平台性能:该平台5分钟内可生成超5万个微液滴,每个液滴作为独立生物反应器用于肿瘤球状体形成,可通过调节细胞浓度、水油流速比精准调控球状体初始尺寸,释放后的球状体可在液体环境或3D胶原基质中继续生长,直径超300μm,且MCF-7、U87 MG两种细胞生成的球状体均保持高存活率(分别约94.29%、98.78%),并展现出各自的表型特征(如U87 MG球状体具有侵袭性,MCF-7则无)。
2、纳米药物制备与验证:构建了以氟化低分子量聚乙烯亚胺(PEI-F)为载体、透明质酸(HA)包被靶向CD44受体的siRNA纳米颗粒,该颗粒粒径均一、包封效率高,在2D细胞实验中证实低细胞毒性、高摄取率和基因沉默能力,且能有效穿透3D肿瘤球状体,穿透效率在U87 MG球状体中更高。
3、纳米药物疗效评估:以靶向STAT3的siRNA纳米药物为验证对象,发现其对肿瘤球状体的生长抑制和细胞杀伤效果显著优于游离siRNA,且对U87 MG球状体的作用更明显;蛋白水平检测证实该纳米药物可显著降低STAT3蛋白表达,呈现浓度依赖性的疗效特征,验证了平台在纳米药物表型和分子水平评价中的有效性。
4、平台优势与局限性:相较于悬滴法、液体覆盖培养等传统肿瘤球状体生成方法,该液滴微流控平台兼具高通量、尺寸均一、微环境可精准调控的优势,提升了药物筛选的可靠性和可重复性;但目前存在球状体尺寸受液滴空间限制、高浓度细胞易沉降、球状体释放后易融合等技术挑战。
5、研究结论与应用价值:该液滴微流控平台为3D肿瘤模型中的纳米药物筛选提供了稳健、可扩展的方法,能更精准地进行临床前药物评估,为理性设计治疗方案、开发个性化医疗策略和先进药物筛选技术奠定了基础。
该研究中MCF-7和U87 MG两种肿瘤球状体在生物学特性及对siRNA纳米药物的响应上存在哪些显著差异?背后的原因是什么?
①生物学特性差异:MCF-7球状体结构致密、边界光滑,无显著侵袭性;U87 MG球状体结构松散、轮廓不规则,在胶原I基质中4h即出现浸润,4天平均侵袭距离达315μm。
②药物响应差异:U87 MG球状体的纳米颗粒穿透效率更高,siSTAT3-NP对其生长抑制和STAT3蛋白下调的效果更显著。
差异原因:一是细胞黏附性,MCF-7高表达E-钙粘蛋白,细胞间黏附性强导致球状体致密,而U87 MG黏附性弱,球状体松散更利于纳米颗粒穿透;二是受体表达,U87 MG高表达CD44受体,增强了HA修饰纳米颗粒的结合与内吞,提升了药物递送效率。
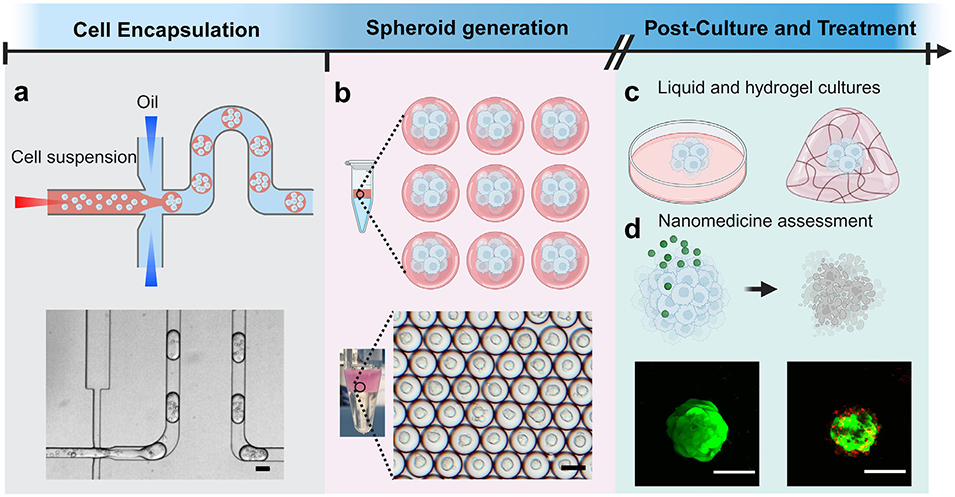
图1. 基于液滴微流控平台的肿瘤球状体制备及纳米药物评价流程示意图。(a)肿瘤细胞在微流控器件的流动聚焦区域包封于微液滴内;(b)肿瘤球状体在微液滴内形成;(c)从微液滴中释放的球状体在液体培养基和水凝胶基质中培养,以支持其进一步生长发育;(d)将制备得到的肿瘤球状体用于siRNA纳米药物的治疗效果评估。比例尺:100μm。
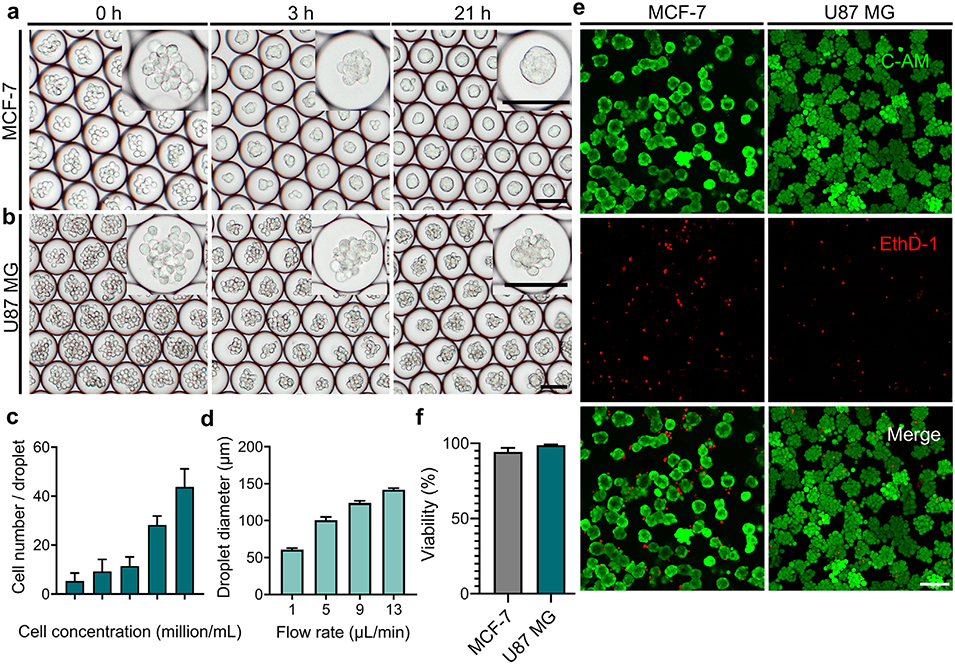
图2. 液滴微流控技术制备的肿瘤球状体的形成与表征。(a)MCF-7细胞在液滴内于0、3、21小时的形态变化延时图像;(b)U87 MG细胞在液滴内于0、3、21小时的形态变化图像;(c)固定流速(水:油= 9:15μL/min)下,初始细胞浓度与每个液滴中平均包封细胞数的关系(每种条件下n=50);(d)恒定油相流速(15μL/min)下,水相流速与液滴直径的相关性(每种条件下n=50);(e)钙黄绿素-AM/乙锭同源二聚体-1染色的球状体荧光代表图像,绿色为活细胞,红色为死细胞;(f)从液滴中释放的球状体的细胞活力定量分析(n=3)。比例尺:100μm。数据以平均值±标准差表示。
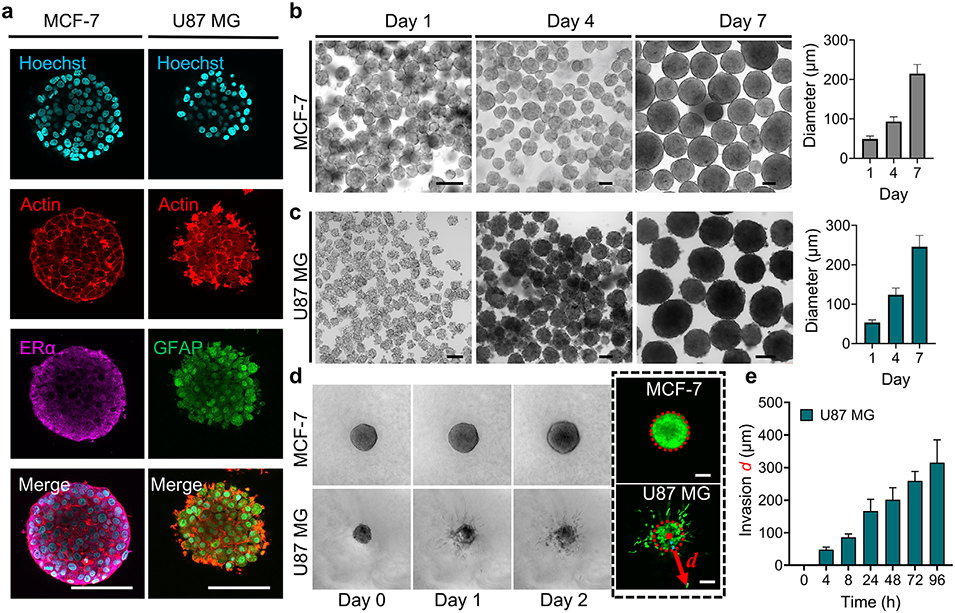
图3. 从微液滴中释放后肿瘤球状体的表征与生长情况。(a)MCF-7和U87 MG肿瘤球状体的免疫荧光染色结果;(b、c)MCF-7和U87 MG球状体在培养1、4、7天时的形态演变及直径变化(每种条件下n=45);(d)MCF-7球状体和U87 MG球状体在I型胶原中培养第0天(初始包埋)、第1天、第2天的形态变化显微代表图像;(e)包埋于I型胶原中的U87 MG球状体的侵袭距离随时间的变化(n=3)。比例尺:100μm。所有数据以平均值±标准差表示。
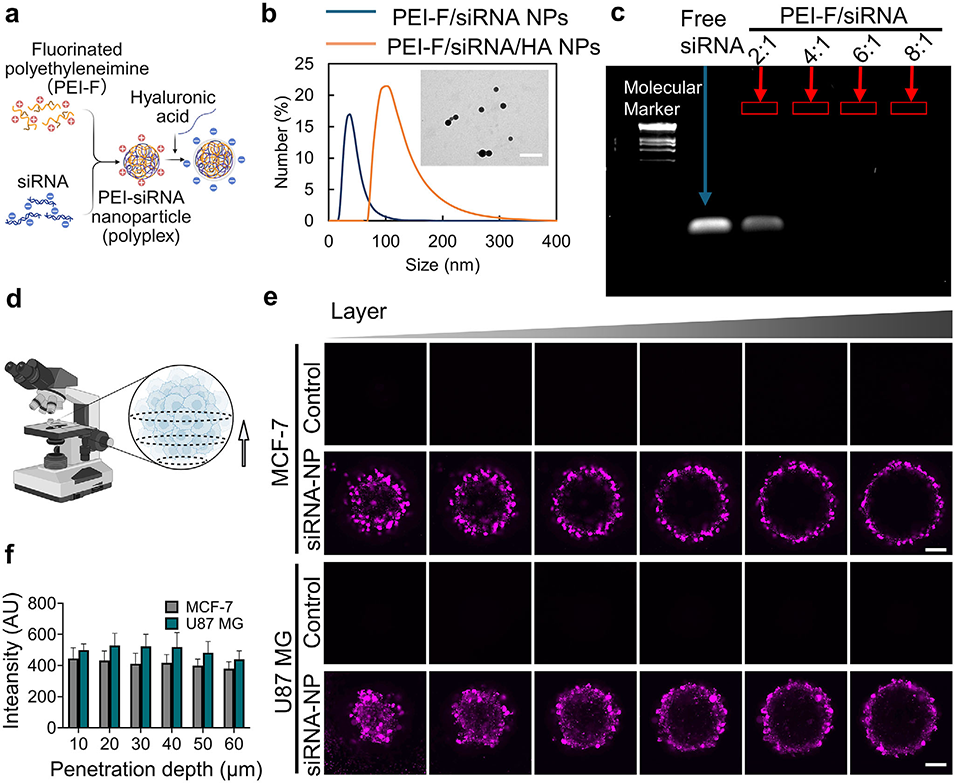
图4. 纳米颗粒向3D肿瘤球状体的穿透性评价。(a)PEI-F/siRNA/HA纳米颗粒的结构示意图;(b)PEI-F/siRNA纳米颗粒和PEI-F/siRNA/HA纳米颗粒的粒径分布,以及PEI-F/siRNA/HA纳米颗粒的透射电镜图像(插图),比例尺:500 nm;(c)不同PEI-F与siRNA质量比下,siRNA的包封效率凝胶电泳结果;(d)肿瘤球状体共聚焦成像示意图,从球状体底部扫描至中心;(e)Cy5标记的siRNA纳米颗粒从球状体底部向中心穿透的Z轴堆叠共聚焦荧光代表图像,比例尺:100μm;(f)MCF-7和U87 MG球状体孵育6小时后Cy5荧光强度的定量分析(n=3个生物学重复)。数据以平均值±标准差表示。对照组:经游离Cy5标记siRNA处理的球状体;siRNA-NP组:经PEI-F/Cy5标记siRNA/HA纳米颗粒处理的球状体。
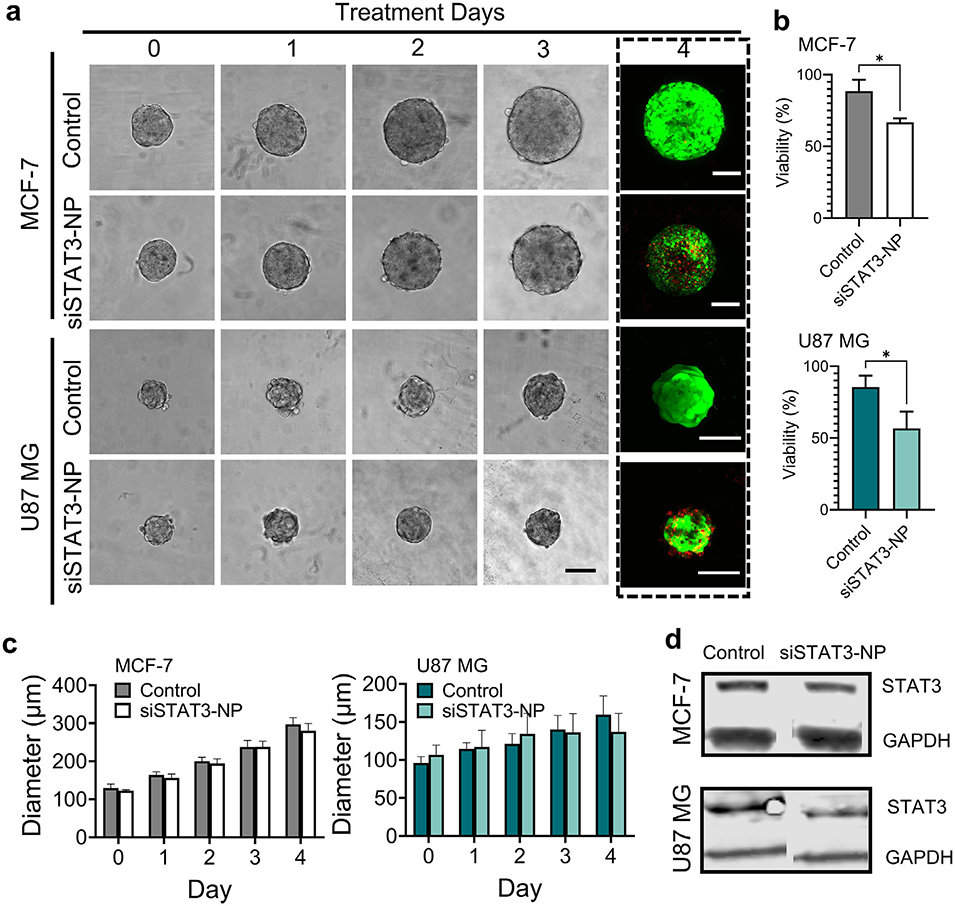
图5. 利用3D肿瘤球状体评价纳米药物的治疗效果。(a)MCF-7和U87 MG球状体经游离 siSTAT3(对照组)或siSTAT3载药纳米颗粒(siSTAT3-NP 组)处理后,在第0、1、2、3天的形态变化明场代表图像;第4天的活/死细胞荧光图像(虚线框标注)显示不同处理组的细胞活力差异,比例尺:100μm;(b)MCF-7和U87 MG球状体经处理后的细胞活力定量分析(平均值±标准差,n=3),采用双尾非配对t检验计算P值,*p<0.05,**p<0.01,***p<0.001,****p<0.0001,无标记为无统计学差异;(c)对照组和siSTAT3-NP组中,MCF-7和U87 MG肿瘤球状体在治疗期间的平均直径变化(平均值±标准差,n=3);(d)对照组和siSTAT3-NP组球状体中STAT3蛋白表达水平的蛋白质印迹代表图像。
论文链接:https://doi.org/10.1002/adhm.202503604
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














