研究背景
1、CKD现状:慢性肾病(CKD)是全球性健康挑战,影响数百万人,早期无症状易忽视,晚期不可逆,需大规模筛查和持续监测。
2、核心标志物:尿白蛋白/肌酐比值(uACR)是CKD早期筛查和监测的关键指标,其阈值标准为:<30 mg/g(正常)、30-300 mg/g(微量白蛋白尿,可治愈)、>300 mg/g(大量白蛋白尿,不可治愈)。
3、现有方法局限:
传统定量方法(ELISA、放射免疫法、Jaffe反应):准确性高,但依赖中心化实验室、昂贵仪器和专业人员,难以大规模应用。
简易方法(试纸条、横向免疫测定):操作简单,但颜色变化模糊、非定量,无法准确计算uACR,且难以识别糖尿病肾病。

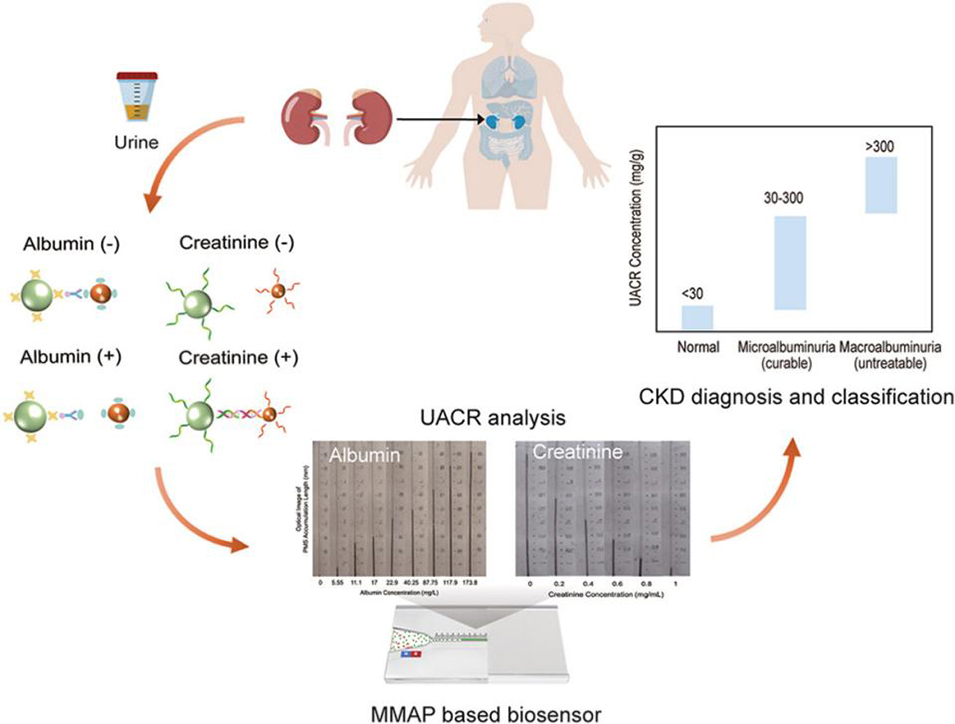
鉴于此,香港城市大学陈定璿教授团队开发了一种去中心化、无需仪器的微流控微球累积平台(MMAP),通过整合竞争性免疫测定与适配体识别技术,实现了尿白蛋白和肌酐的同步可视化定量。该平台借助微球累积长度直观反映标志物浓度并计算uACR,在临床样本检测中展现出与医院标准方法高度一致的准确性,且成本低廉、操作便捷。相关研究以“A Microfluidic Microspheres Accumulation Platform for Direct Visualization of Urine Albumin-to-Creatinine Ratio in Patients with Chronic Kidney Disease”为题目,发表在期刊《Biosensors and Bioelectronics》上。
本文要点:
1、该研究开发了一种去中心化、无需仪器的微流控微球聚集平台(MMAP),用于直接可视化慢性肾病(CKD)患者的尿白蛋白/肌酐比值(uACR)。
2、平台原理方面,白蛋白通过竞争性免疫分析抑制磁性微球(MMSs)与聚合物微球(PMSs)的结合,肌酐则通过抗肌酐适体识别释放DNA阻断链,促进MMSs与PMSs的连接;微流控芯片入口的磁分离器会吸附结合后的微球复合物,游离PMSs在滤纸毛细作用下聚集,其聚集长度可实现uACR的视觉定量。
3、实验优化了PMSs浓度、抗体用量、反应时间等条件,该平台对白蛋白和肌酐检测的检出限分别为4.2811mg/L和0.218mg/mL,具有良好的选择性、pH耐受性和重复性。
4、临床测试中,对17份尿液样本的检测结果与医院标准检测方法(放射免疫分析法、Jaffe反应法)高度相关,且能准确区分正常、微量白蛋白尿和大量白蛋白尿对应的CKD分期,相比尿试纸法准确性更高。
5、该平台成本低(约1美元/次)、操作简便,为CKD的大规模筛查和自我监测提供了可靠工具。
MMAP平台之所以能实现白蛋白与肌酐的同步、可视化定量检测,原因在于其整合了两种特异性检测机制并优化了微流控芯片结构。为实现白蛋白检测,研究团队将白蛋白固定于磁性微球(MMSs)表面,并将生物素化抗白蛋白抗体与链霉亲和素修饰的聚苯乙烯微球(PMSs)相结合。如此一来,尿液中存在的白蛋白会通过竞争性免疫反应,抑制磁性微球与聚合物微球之间的免疫亲和结合。
针对肌酐检测,采用抗肌酐适配体——当尿液中存在肌酐时,肌酐与抗肌酐适配体特异性结合,使预先与适配体杂交的单链阻断 DNA(阻断剂)解离释放;该阻断剂随后分别与固定在磁性微球(MMSs)表面的DNA探针P1、聚合物微球(PMSs)表面的DNA探针P2杂交,形成“聚合物微球-阻断剂-磁性微球”的三明治结构。
为可视化这种微球结合状态的变化,将微球反应液加载到微流控芯片中。该芯片在入口处设有磁分离器,内部含亲水微通道,末端则装配滤纸。磁分离器可截留游离的磁性微球及结合态的微球复合物,仅游离的聚合物微球会在滤纸的毛细管引力作用下继续流动,直至被滤纸捕获并在其前端累积。因此,通过视觉观察芯片上聚合物微球的累积长度,即可解读尿液中白蛋白与肌酐的浓度,无需借助任何外部读取设备。
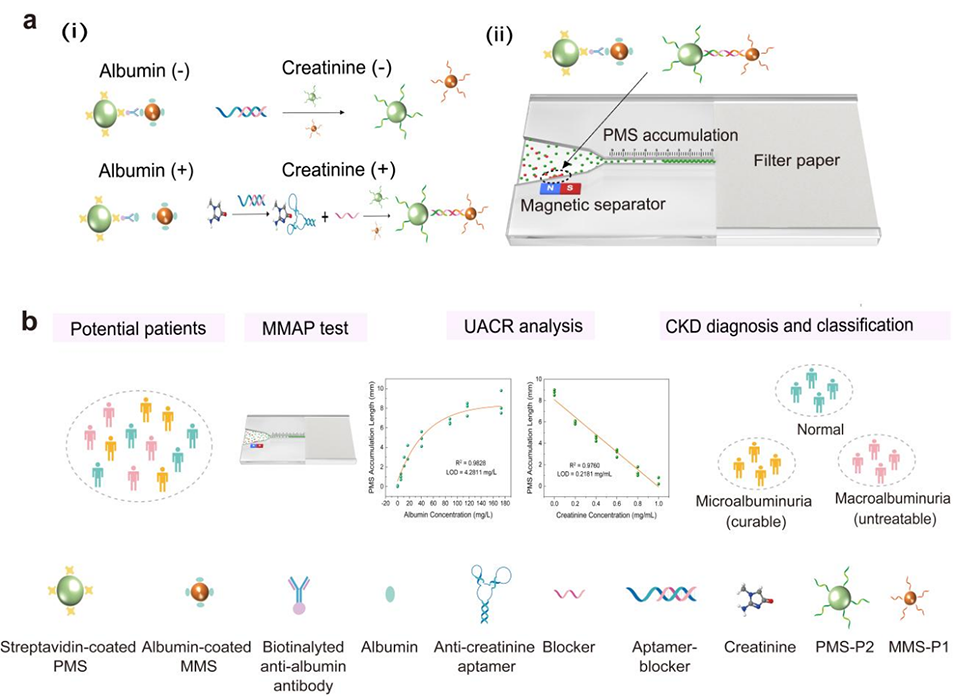
图1. 用于尿白蛋白/肌酐比值(uACR)检测的微流控微球累积平台(MMAP)生物传感器概述
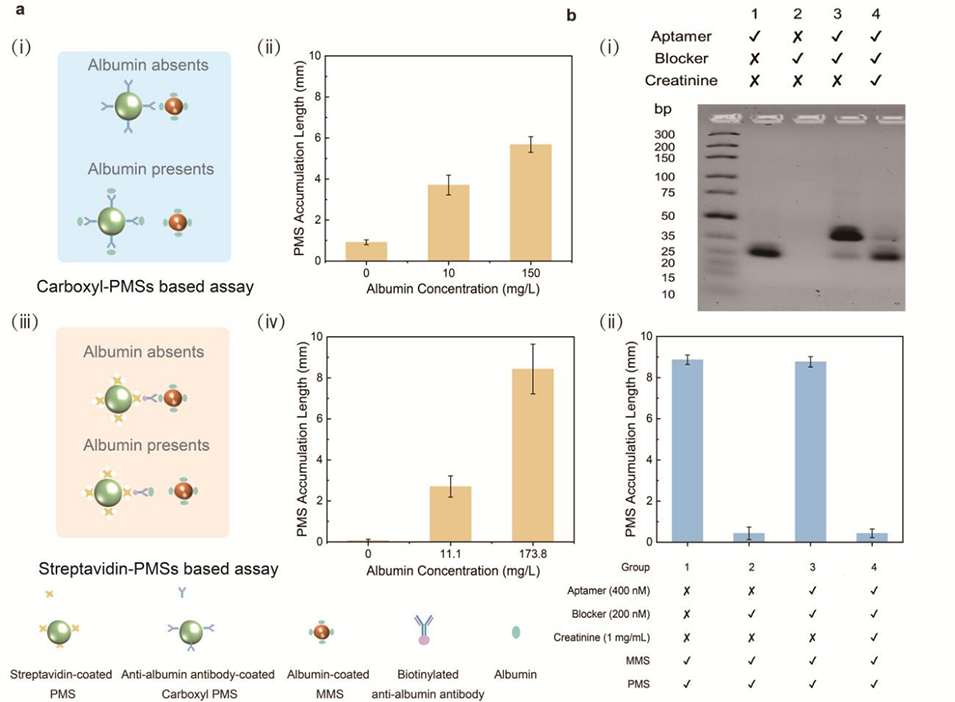
图2. 白蛋白与肌酐检测的可行性分析
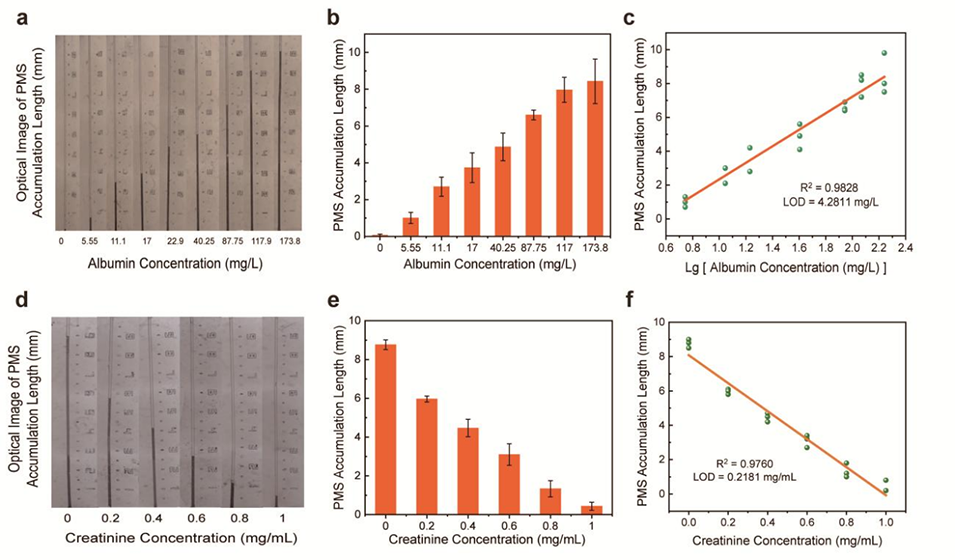
图3. 白蛋白与肌酐的可视化定量检测
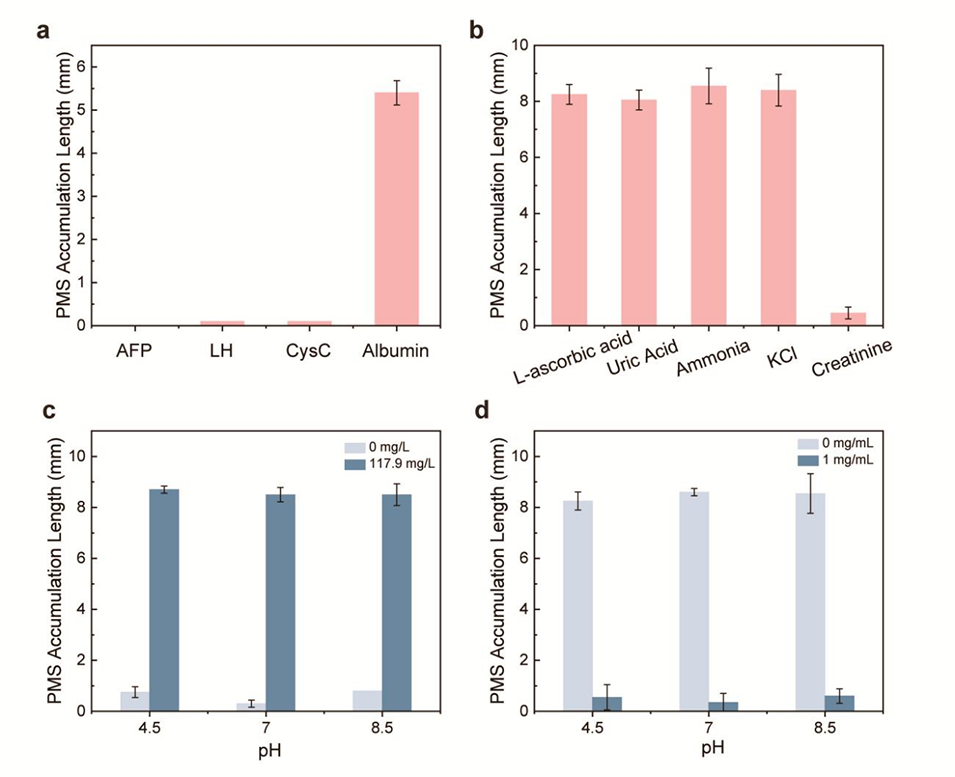
图4. 尿液样本中干扰因素对白蛋白和肌酐检测的影响分析
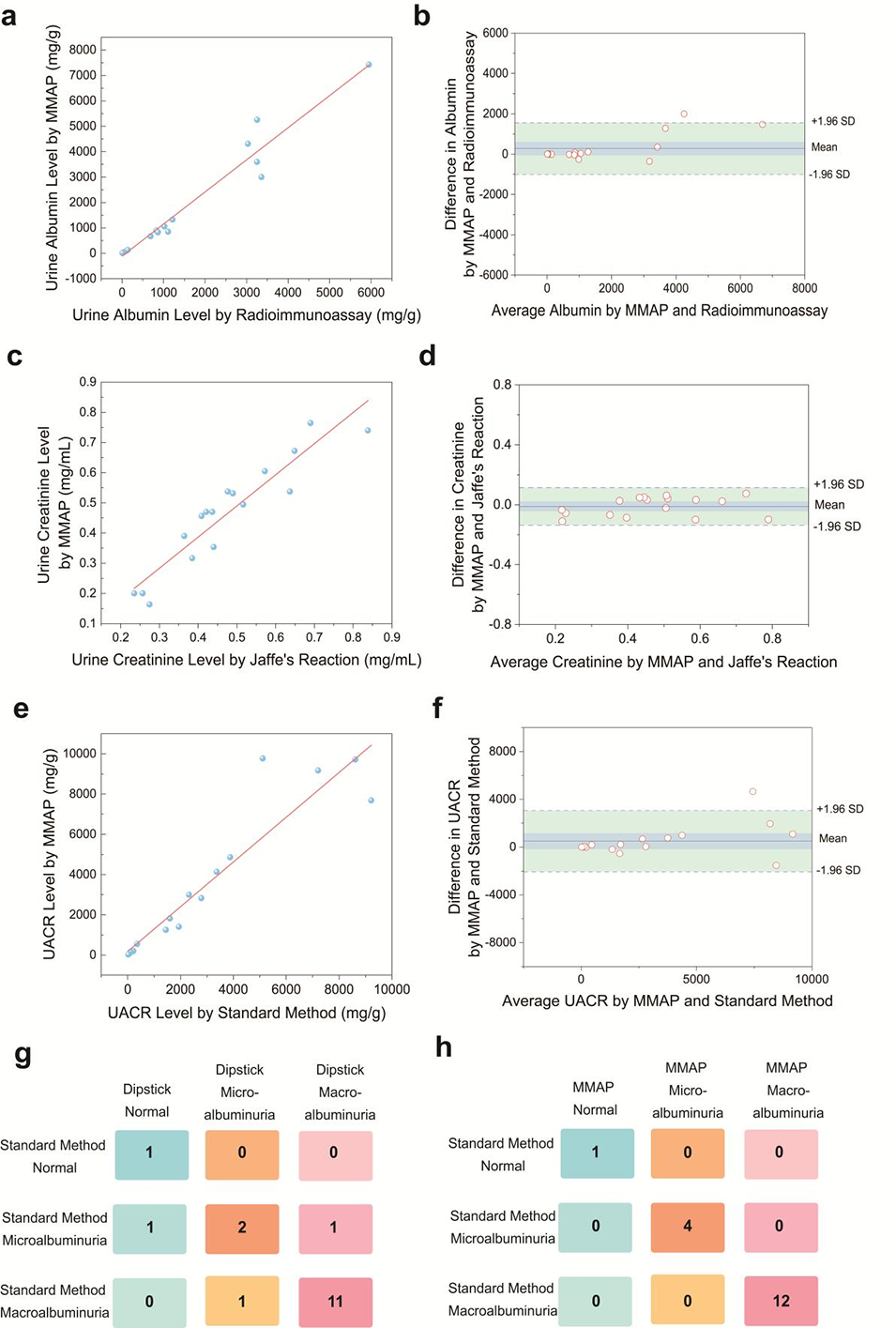
图5. 临床样本检测实验
论文链接:https://doi.org/10.1016/j.bios.2026.118400
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














