各向异性微粒凭借明确的形态特征,突破了普通球形微粒的应用局限,在传感、药物递送、细胞治疗、组织工程等多个领域具有广泛应用。人体中肌肉、血管、神经等组织均由各向异性纤维状重复单元构成,因此封装细胞的纤维状水凝胶微粒可作为体外重建天然器官复杂结构的基础单元,且其几何形态会影响注射性能、组装行为及细胞活性等关键特性。
微流控技术为各向异性微粒的制备提供了高效平台,相较于模塑、乳化、光刻等传统技术,能更精准地独立调控微粒的形态、尺寸和单分散性。但传统微流控系统中,流体在T型结、流动聚焦等装置内的不稳定性易导致产物多为球形;而微流控与光刻结合的方法虽能制备复杂形态微凝胶,却存在工艺条件苛刻、生物相容性材料受限等问题,难以保障细胞活性。因此,在生物相容性条件下高通量制备几何形态可控的纤维状微粒,仍是软物质物理、材料科学及生物医学工程领域的核心挑战。

近期,北京航空航天大学樊瑜波教授/刘肖副教授团队开发了一种基于多相液-液界面动力学的可编程被动数字快门机制,能够在微流控平台上精确制造多种形态的水凝胶微纤维。该研究通过调控液体桥的稳定与断裂,实现了对微纤维几何形状的确定性控制,并成功制备出载细胞微纤维与磁响应微纤维,展现了其在组织工程与软体机器人等领域的应用潜力。相关研究以“A Microfluidic Digital Shutter of Liquid–Liquid Interface for Fabrication of Multifaceted Hydrogel Microfiber Structure”为题目,发表于期刊《Advanced Science》。
本文要点:
1、该研究提出一种基于多相液-液界面动力学的可编程被动数字快门机制,在微流控平台实现水凝胶微纤维的精准制备。
2、研究设计了集成T型结与共流装置的微流控芯片,采用石蜡油、氯化钙溶液和海藻酸钠溶液三相流体系统:两互不相溶相形成数字快门,两水相用于水凝胶成型。其核心是利用液-液界面处水凝胶溶液的液桥存在临界稳定长度,通过切换液桥维持与断裂状态实现数字快门功能。
3、通过调控该快门,可精确控制微纤维的长度、长径比、曲率和扭转度等几何参数,制备出线性、螺旋形、蝌蚪形、球形等多种形态的微纤维。研究还验证了该平台的应用潜力,成功制备出高分辨率、高细胞活性的载细胞微纤维,以及磁响应性微纤维。
4、该方法无需外部驱动,凭借毛细管不稳定性实现流体逻辑控制,具有无模板、可重构、低能耗等优势,在组织工程、软机器人、药物递送等生物医学领域具有广阔应用前景,但目前在制备多组分各向异性微纤维、优化流变学特性影响及实现高通量生产等方面仍有改进空间。
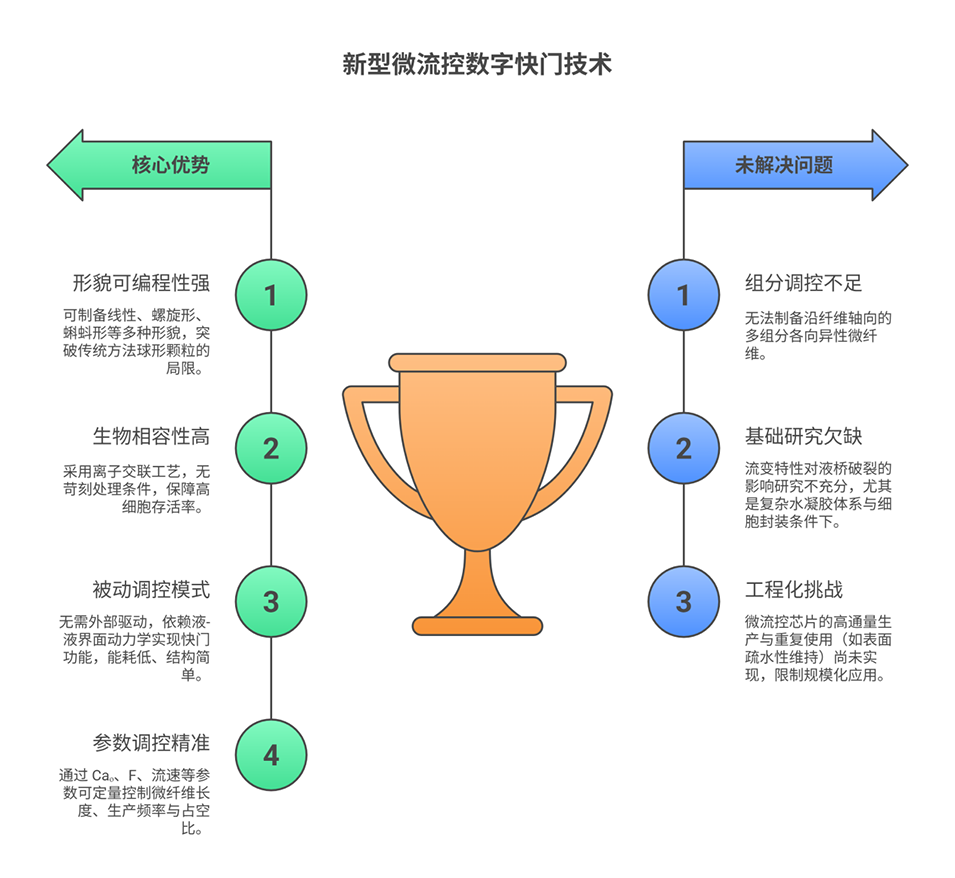
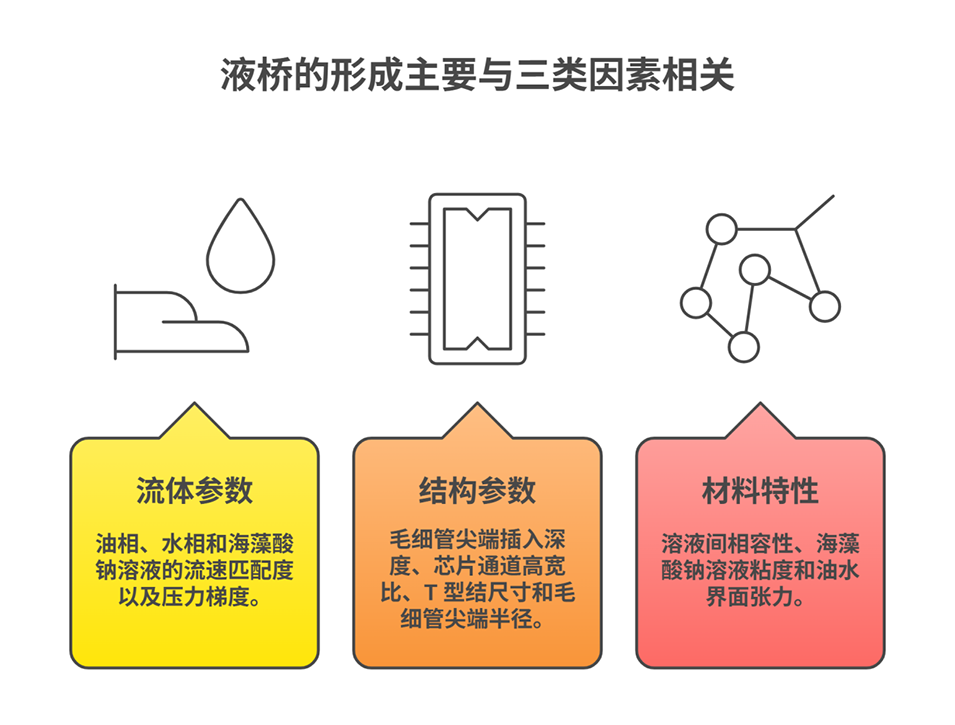
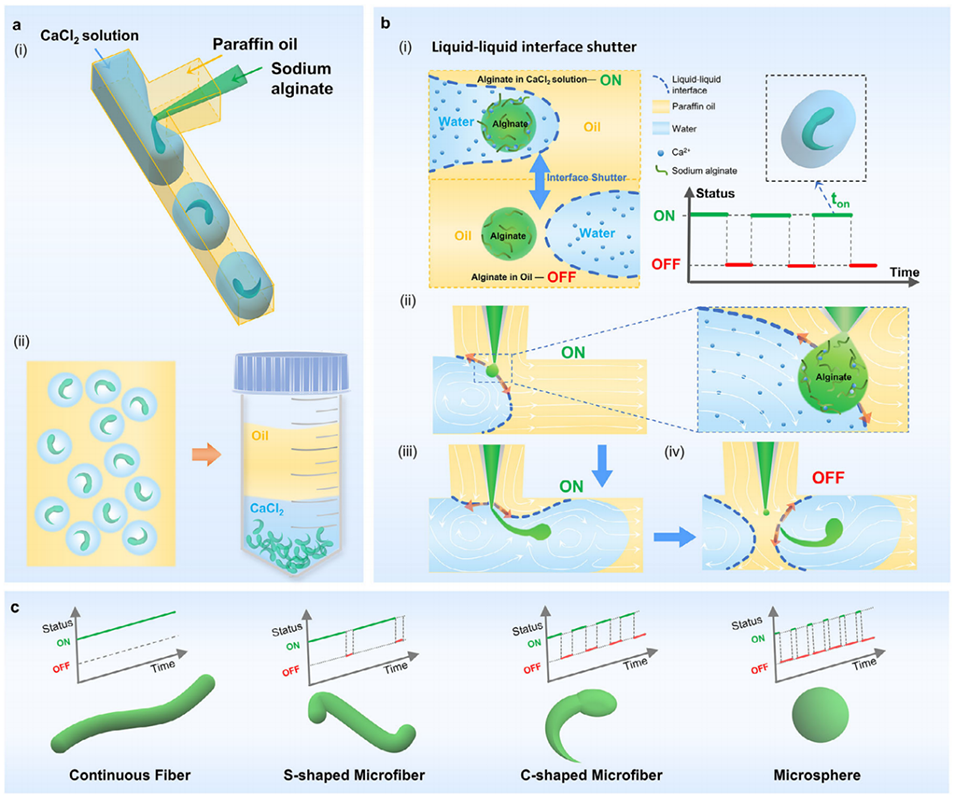
图1. 基于微流控液-液界面快门的水凝胶微纤维可编程制备
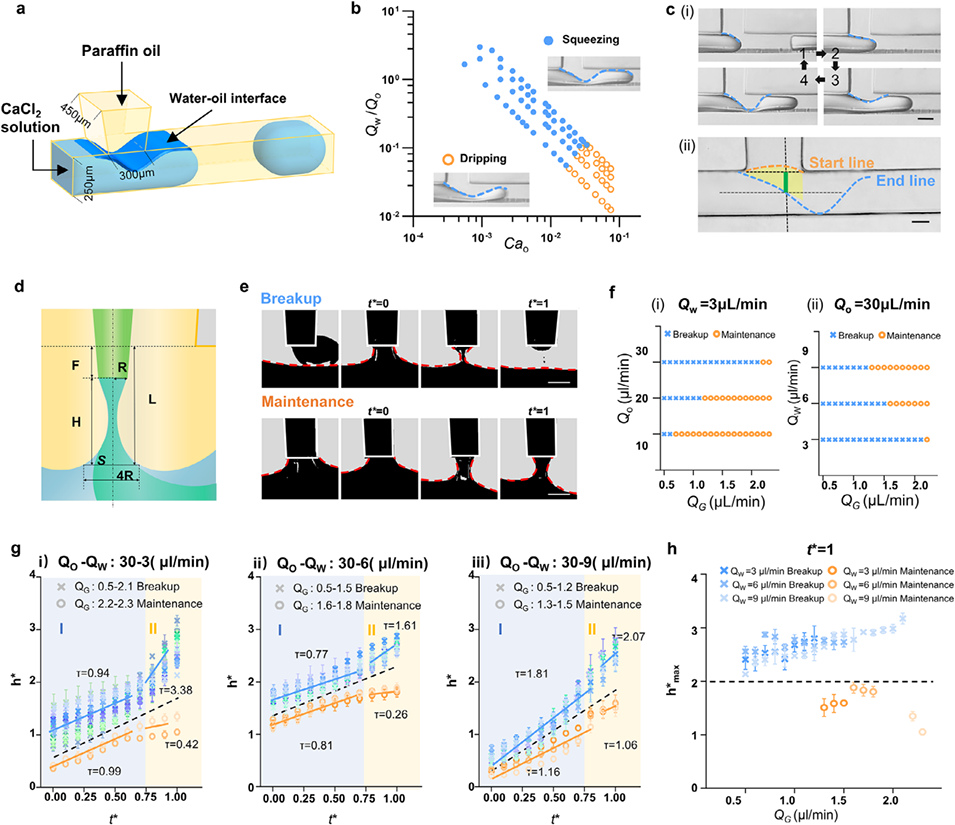
图2. 基于液-液界面调控的被动式数字快门设计与形成机制
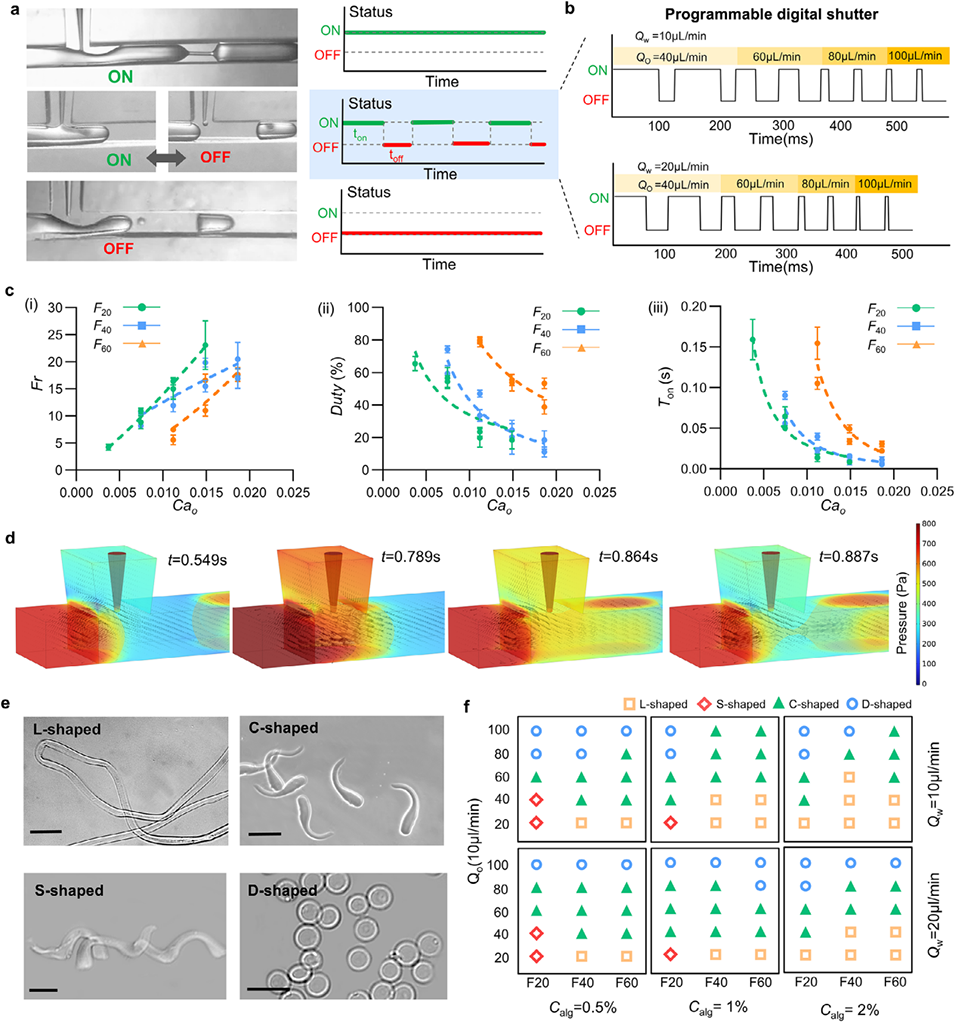
图3. 基于流量调控被动式数字快门的水凝胶微纤维形态可编程调控
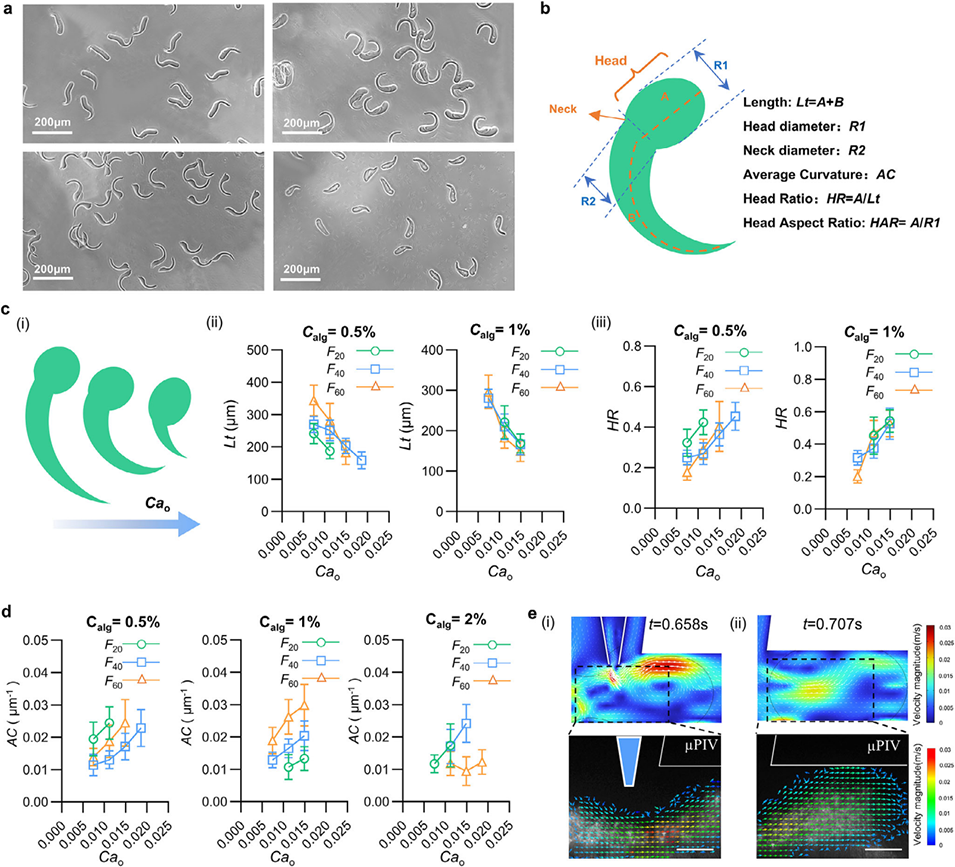
图4. C形微纤维的几何结构调控
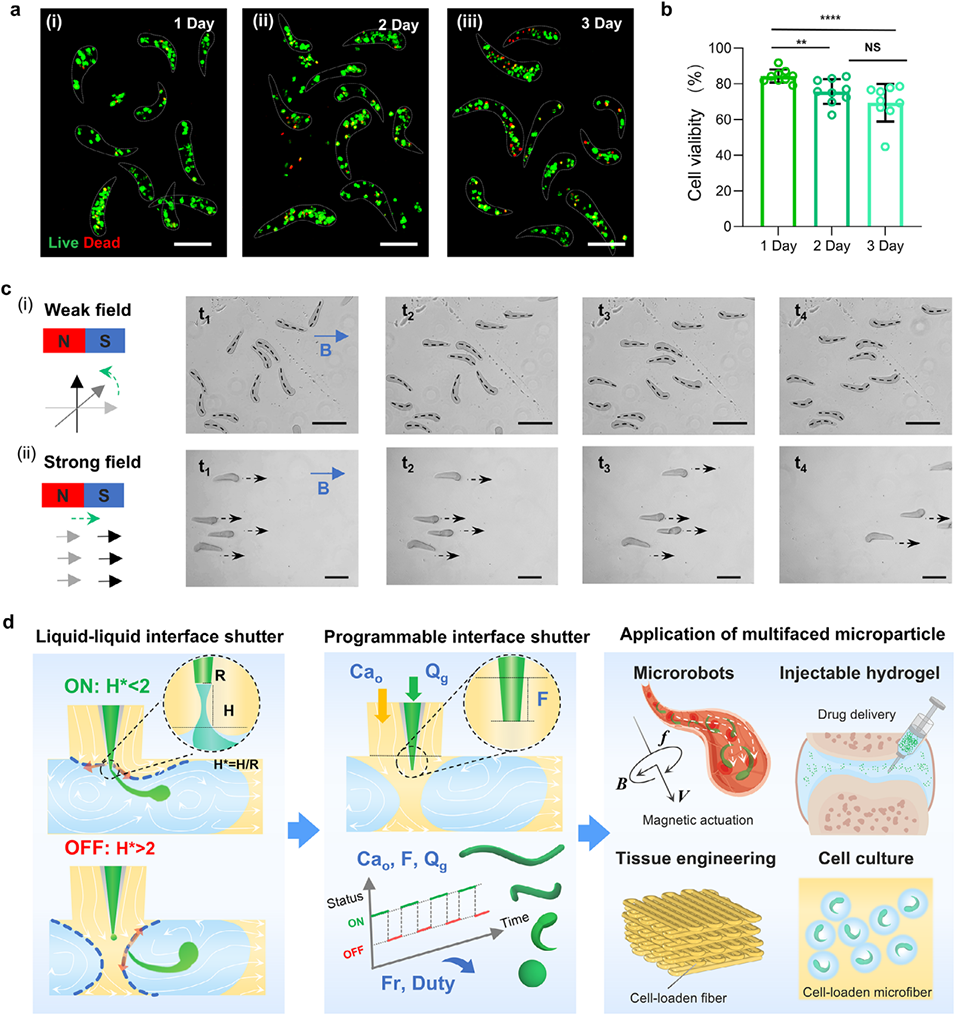
图5. 载细胞及磁响应性C形微纤维的制备与性能评估
论文链接:https://doi.org/10.1002/advs.202510989
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














