多孔微针作为一种微创工具,在间质液采样和生物标志物分析领域备受关注。然而,现有多孔微针的制备方法普遍存在提取效率低的问题,这主要是由于提高孔隙率与维持足够机械强度之间存在固有的权衡关系。

鉴于此,东京大学工学部研究人员提出了一种基于微流控技术制备单分散聚乳酸微球、经热键合工艺制造多孔微针的新方法。通过调控微球尺寸优化孔径、亲水性聚乙二醇(PEG)表面处理提升亲水性,同时优化键合条件平衡孔隙率与机械强度,最终实现了迄今最高的间质液体外提取速率,并成功集成于比色纸基传感器实现葡萄糖的精准检测。相关研究以“Controllable-pore porous microneedles for high-speed extraction and biomarker detection of interstitial fluid”为题目,发表在期刊《Microsystems & Nanoengineering》上。
本文要点:
1、本文提出了一种新型制备方法,可制造出孔径可控、提取性能优异的多孔微针。通过微流控技术制备单分散聚乳酸微球,经热键合后形成多孔微针——其内部相互连通的孔隙网络源自微球之间的间隙。
2、通过精确调节微球直径,在保证结构完整性的同时优化孔径,以实现高提取效率。
3、经过亲水性聚乙二醇(PEG)表面处理和键合参数优化,所制备的多孔微针具备足够的机械强度,可穿透人体皮肤,且体外提取速率达到0.95μL/min/针,为目前已报道的最高值。
4、将多孔微针与扩散层键合,并集成到比色纸基传感器中,用于葡萄糖检测。在人工皮肤模型上的测试证实,葡萄糖浓度与纸基传感器的颜色变化呈线性相关。
5、该研究为高速间质液提取提供了一种极具前景的工具,并拓展了生物传感应用中多孔结构的制造策略。
该研究制备的多孔微针通过以下三重关键设计协同,解决了传统多孔微针“提取效率低”的核心问题。具体如下:
1、孔径可控:采用微流控技术制备单分散PLA微球,通过调节微球尺寸(最终选定10μm)控制微球间通道宽度(孔径1.75μm),最大化毛细管力;
2、孔隙连通性:热键合工艺保留微球间的连续空隙,形成互通通道,避免传统方法中孔隙随机分布、连通性差的问题,开放孔隙率接近总孔隙率;
3、亲水性优化:采用PEG表面处理,将多孔PLA表面接触角从95.3°降至41.5°,显著提升毛细管力,最终实现0.95μL/min/针的迄今报道的最高提取速率。
该研究在平衡多孔微针“机械强度”与“提取性能”方面采取了哪些措施,效果如何?
① 结构设计:采用金字塔形微针结构,相比圆锥形、六边形等结构,机械强度更高、皮肤穿透应力更小;
② 键合条件优化:将键合温度从140 ℃提升至170 ℃(增强微球间键合界面),压力从15 kPa降至3 kPa(避免微球过度变形导致孔隙堵塞),使微针破坏力从180.8 mN提升至404.4 mN,远超皮肤穿透所需力(58 mN);
③ 孔隙保留:优化后总孔隙率仅从41%降至38%,仍维持良好的孔隙连通性,确保提取性能不受显著影响,最终微针可穿透猪皮无断裂,且提取速率达迄今最高。
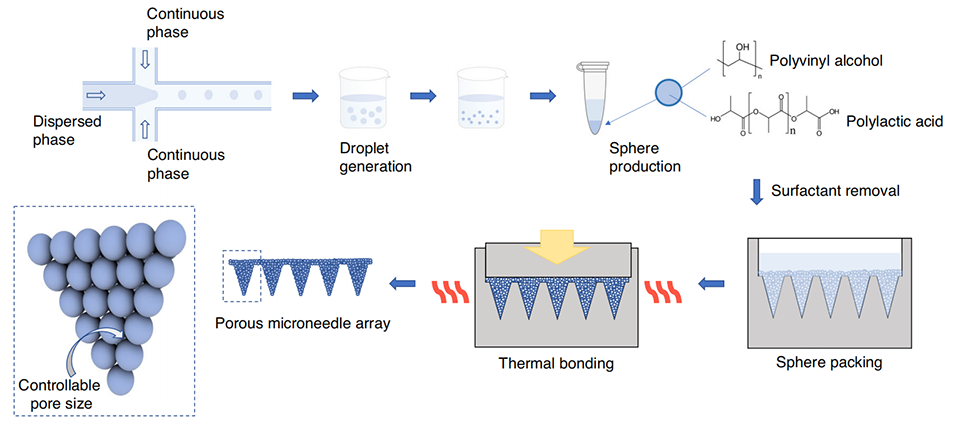
图1 基于微流控技术制备微球,并以此构建可控孔径多孔微针的流程示意图
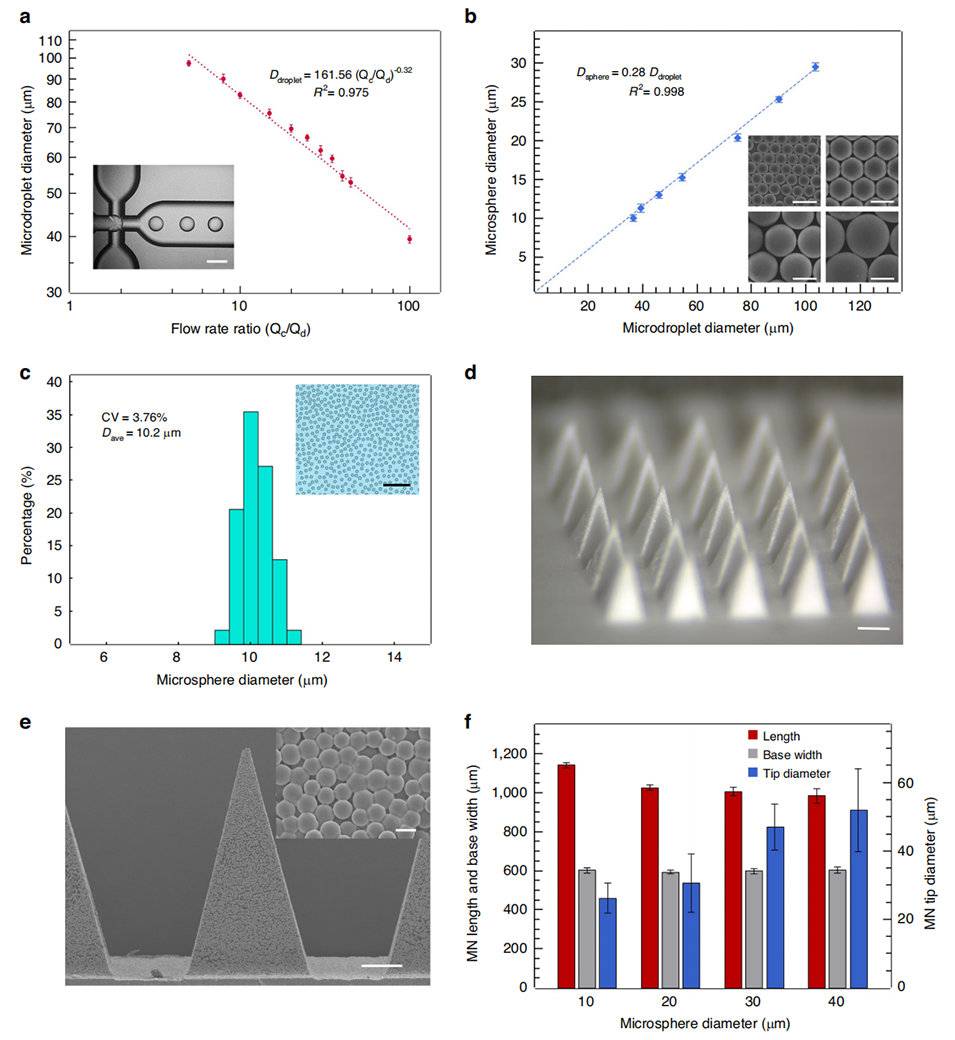
图2 可控尺寸微滴生成与微球制备用于多孔微针构建
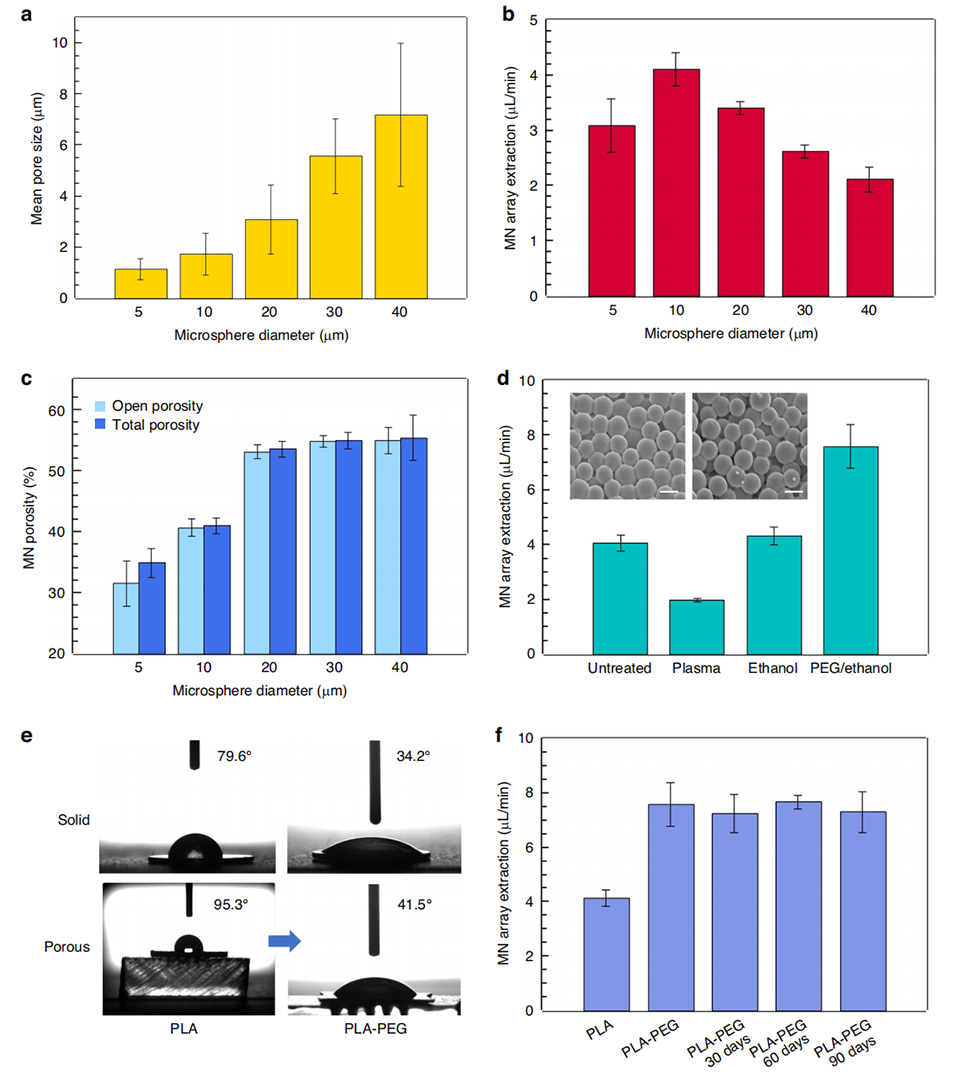
图3 多孔微针提取性能的提升
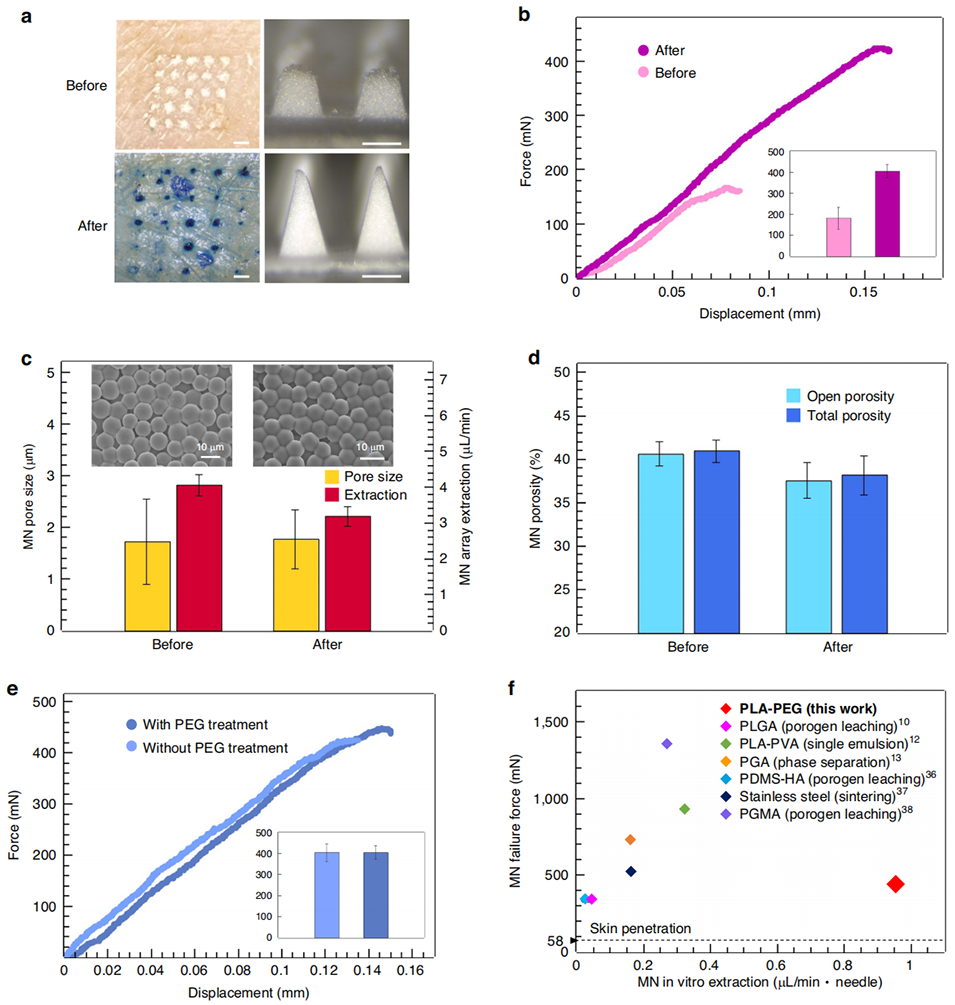
图4 多孔微针机械强度的提升
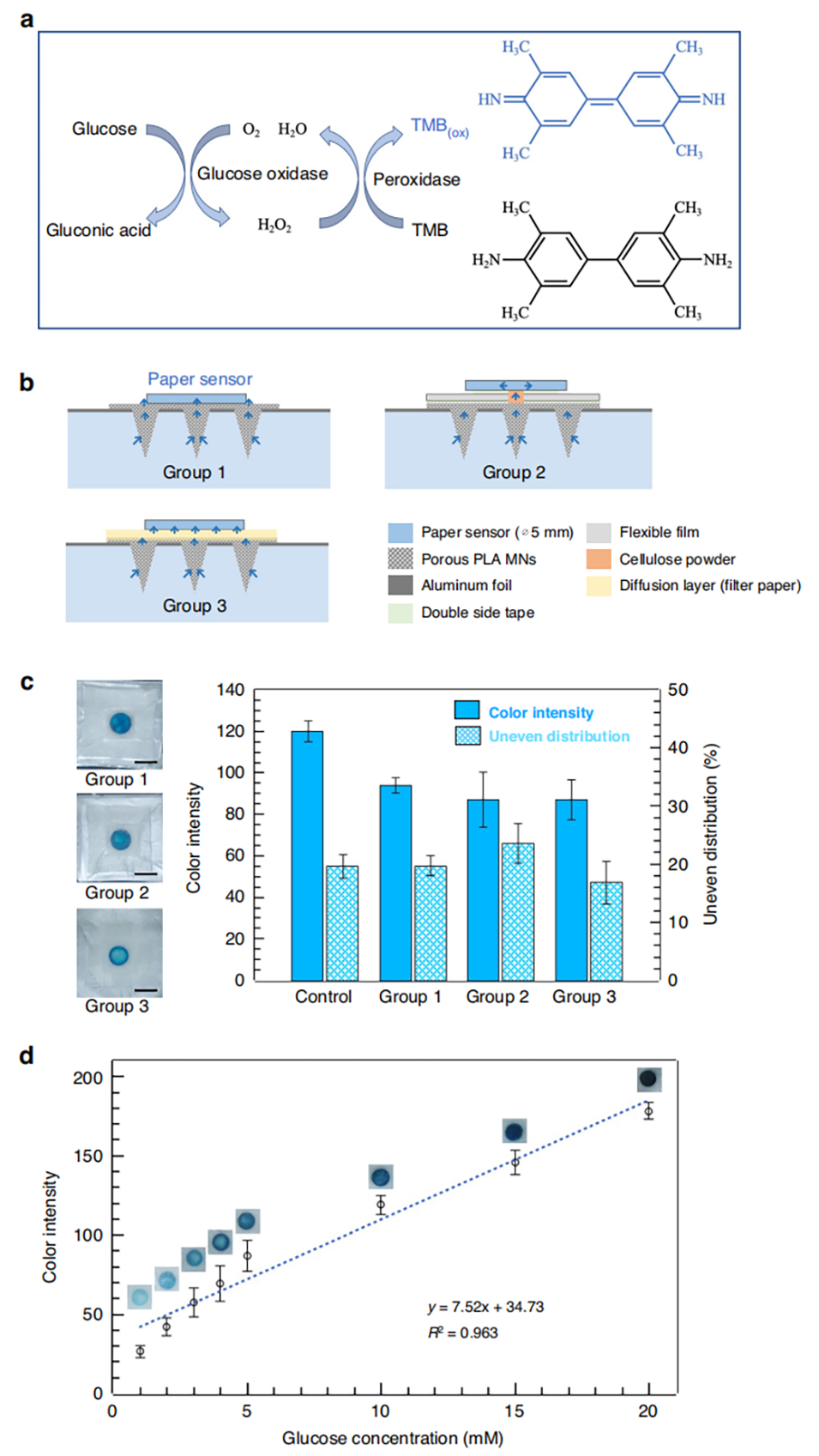
图5 使用多孔微针集成纸基传感器进行葡萄糖检测
论文链接:https://doi.org/10.1038/s41378-025-01103-1
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














