以细菌定植、伤口微环境破坏和形状复杂性为特征的不愈合感染性伤口是临床实践中一个棘手的问题。

近期,青岛大学附属医院王培戈、南京医科大学附属金陵医院黄金健等人受乐高积木(可以组装成所需形状的积木玩具)的启发,开发了一种基于电喷雾技术的纳微米复合海藻酸钠微球。这种微球能够适应不规则感染伤口的形状,通过协同抗菌和促血管生成作用加速愈合,展现出重要的临床应用潜力。相关研究以“Electrospray Nano-Micro Composite Sodium Alginate Microspheres with Shape-Adaptive, Antibacterial, and Angiogenic Abilities for Infected Wound Healing”为题目,发表在期刊《ACS Applied Materials & Interfaces》上。
本文要点:
1、本研究受乐高积木启发,提出利用电喷雾制备的纳微米复合海藻酸钠(SA)微球,快速填充不规则伤口并促进愈合。
2、通过水包油包水双乳液法制备包封碱性成纤维细胞生长因子(bFGF)的多孔PLGA微球(MSs),并与含ZIF-8纳米颗粒的SA溶液混合,电喷雾生成bFGF@MS/ZIF-8@SAMSs复合微球。
3、复合MS的尺寸可以通过PLGA-MS质量比和电喷雾电压来调节。
4、bFGF(有效的血管生成剂)和ZIF-8(杀菌纳米颗粒)以受控和可持续的方式从bFGF@MS/ZIF-8@SAMSs中释放,促进细胞增殖、迁移和管形成并杀死细菌。
5、动物实验表明,该微球可适应伤口形状,协同抗菌与促血管生成,加速感染伤口愈合。
6、本研究为感染性伤口的治疗提供了可行的解决方案,利用生物活性微球作为构建块填充不规则形状的感染伤口并促进愈合,具有重要的临床应用潜力。
复合微球(bFGF@MS/ZIF-8@SAMSs)的具体制备过程如下:
1、ZIF-8的制备
将17 g Zn(NO3)2·6H2O和22.70 g 2-甲基咪唑分别溶于40 mL纯水中,超声处理10分钟以确保完全溶解。
将金属溶液加入配制好的配体溶液中,在30°C下搅拌10小时。
通过离心(10,000 rpm,12分钟)收集生成的白色胶体,用纯水和甲醇交替清洗三次后,于60°C下干燥,得到ZIF-8粉末。
2、使用水包油包水(w/o/w)双乳液法制备bFGF@PLGA微球
将150 mg PLGA溶于3 mL二氯甲烷中,同时将10 μg bFGF溶于0.8 mL纯水中,并加入BSA作为渗透剂。
两种溶液在8000 rpm下乳化60秒,形成初乳(w/o)。
初乳倒入15 mL 4% PVA水溶液中,在1000 rpm下搅拌5分钟,形成复乳(w/o/w)。
将复乳倒入300 mL 4% PVA水溶液中,在1000 rpm下搅拌4小时以蒸发有机溶剂。
最终通过离心(3000 rpm,5分钟)收集微球,用PBS清洗三次后冷冻干燥,得到bFGF@PLGA微球。
3、复合微球(bFGF@MS/ZIF-8@SAMSs)的制备
将bFGF@PLGA微球(0.5、1.0或1.5 mg/mL)和ZIF-8(1.0、2.5或5.0 mg/mL)溶于纯水中,超声均质后与20 mg/mL的海藻酸钠(SA)溶液混合。
将混合溶液装入10 mL注射器,通过24G金属喷嘴进行电喷雾。
施加7-9 kV电压,正极连接喷嘴,负极连接含1 wt% CaCl2溶液的收集板。
溶液以5 mm/min的速度挤出,形成泰勒锥后喷射生成复合微球。
收集微球后冷冻干燥(-50°C),并用SEM观察其形貌。
通过上述步骤,成功制备了具有抗菌、促血管生成和形状适应性的复合微球。
在复合微球中使用ZIF-8具有以下优势:
1、优异的抗菌性能:ZIF-8具有较低的最小杀菌浓度(250 mg/L),相比其他含锌纳米颗粒(如ZnO的600 mg/L)表现出更强的抗菌效果,能够有效抑制和杀灭细菌,减少感染风险。
2、可控释放:ZIF-8的引入防止了药物的突释现象,实现了缓慢、可控的释放,从而降低了细胞毒性并延长了抗菌作用时间。
3、良好的生物相容性:ZIF-8由锌离子和2-甲基咪唑组成,具有良好的生物相容性,适用于生物医学领域。
4、高比表面积和多孔性:ZIF-8具有较大的比表面积和多孔结构,有助于药物的负载和释放,同时增强了材料的抗菌性能。
5、易于制备和分散:ZIF-8的制备工艺简单,易于分散在复合材料中,与其他成分(如海藻酸钠和PLGA微球)结合良好。
综上,ZIF-8的使用不仅赋予复合微球优异的抗菌性能,还通过可控释放和生物相容性提升了材料的安全性和治疗效果。
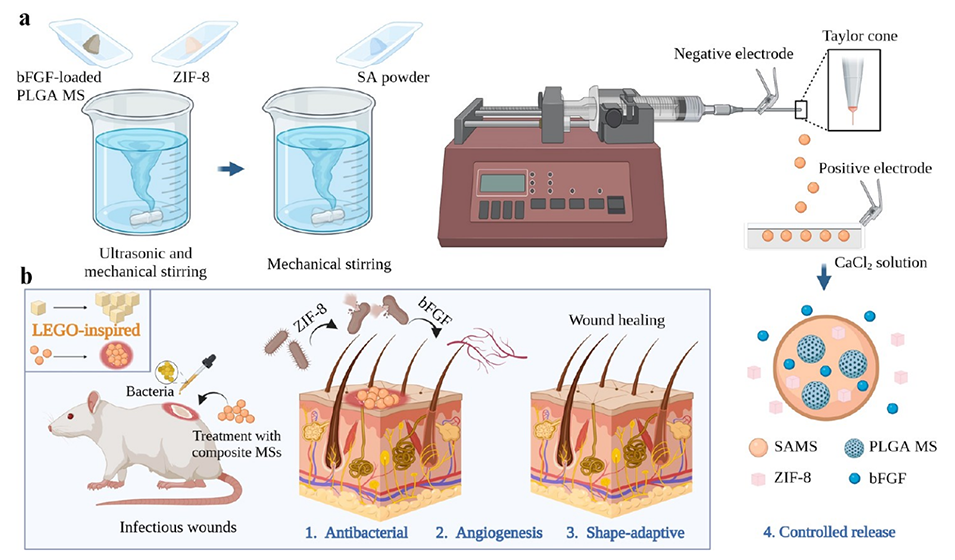
图1.使用纳微米复合bFGF@MS/ZIF-8@SAMSs治疗感染伤口的示意图。
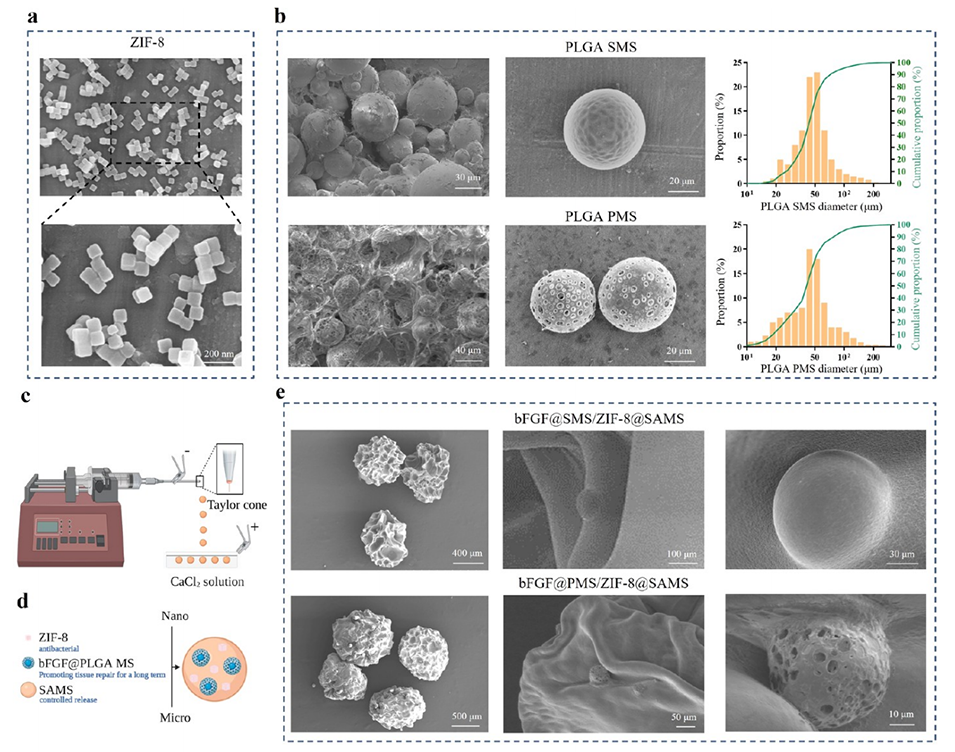
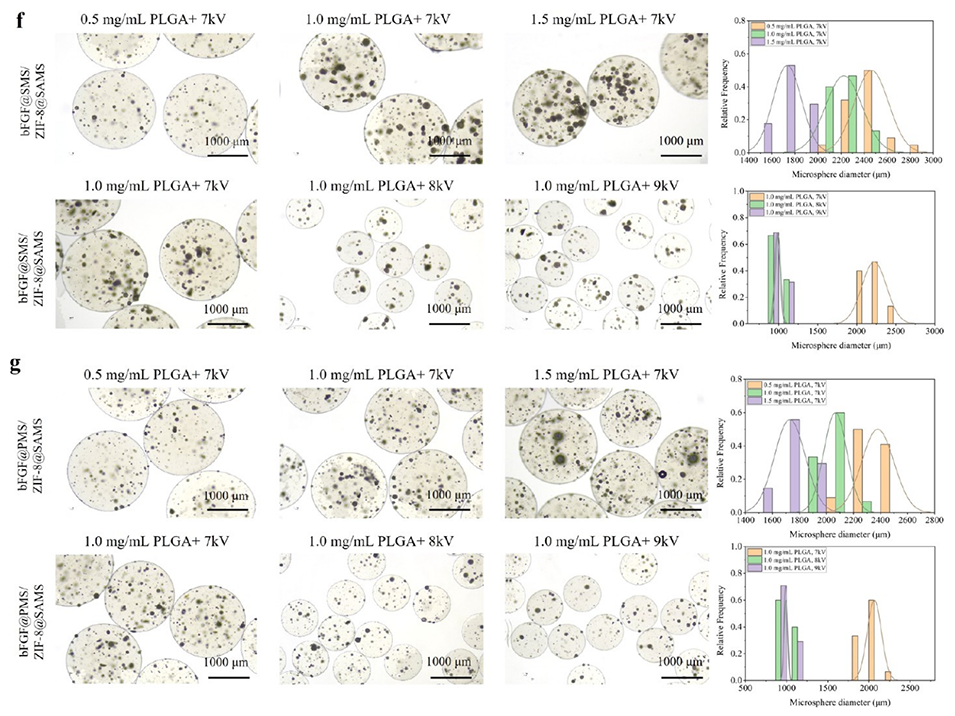
图2.纳微米复合bFGF@MS/ZIF-8@SAMS的制备与调控。
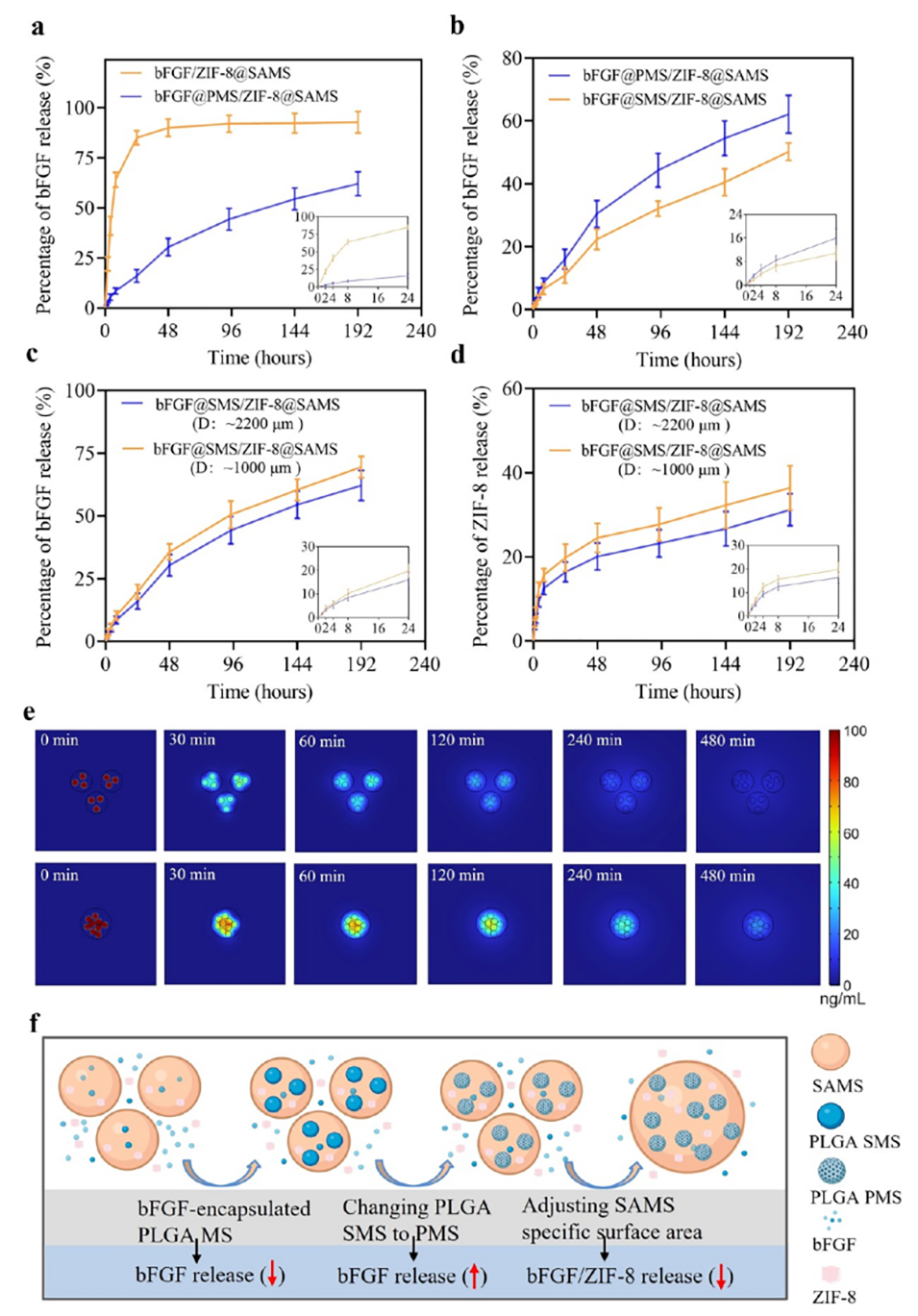
图3.bFGF@MS/ZIF-8@SAMS调控bFGF和ZIF-8释放特性。
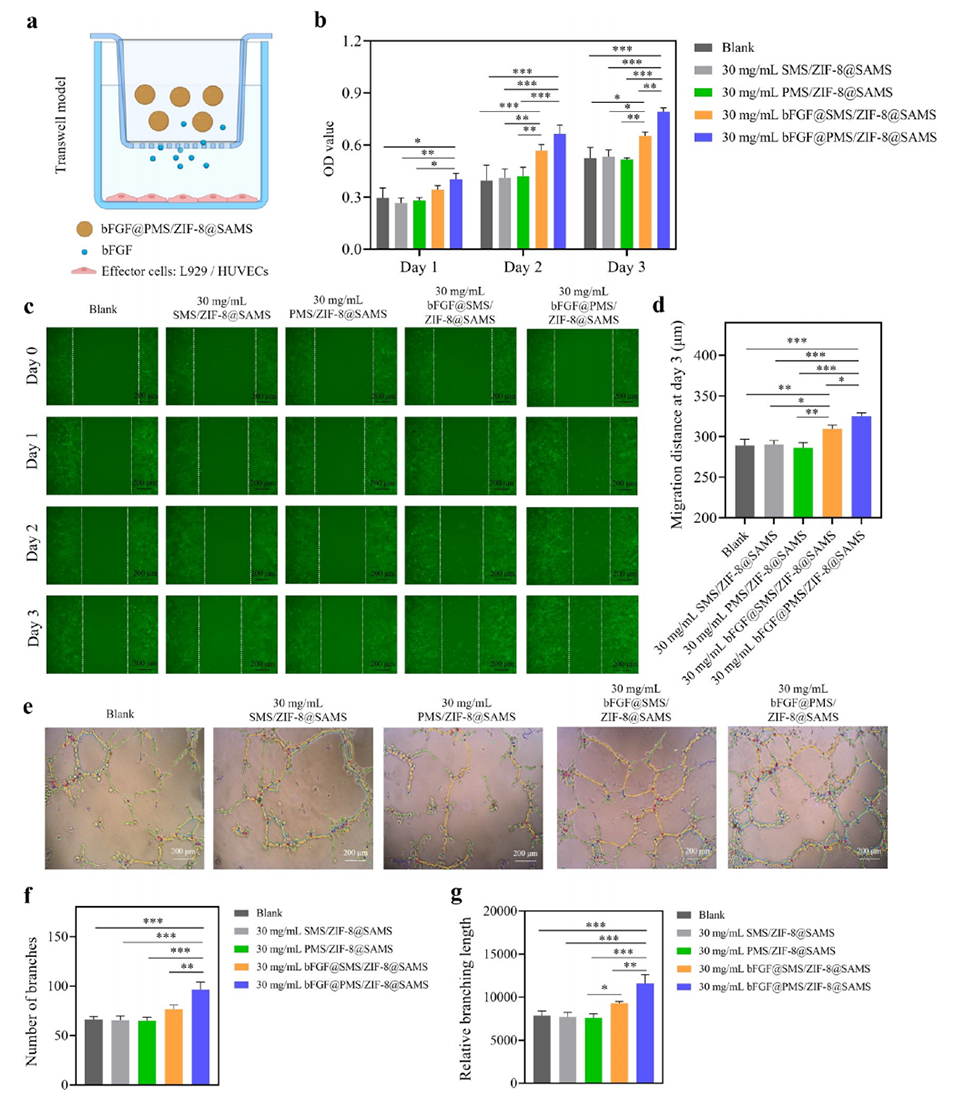
图4.bFGF@MS/ZIF-8@SAMS对细胞的生物学功能。
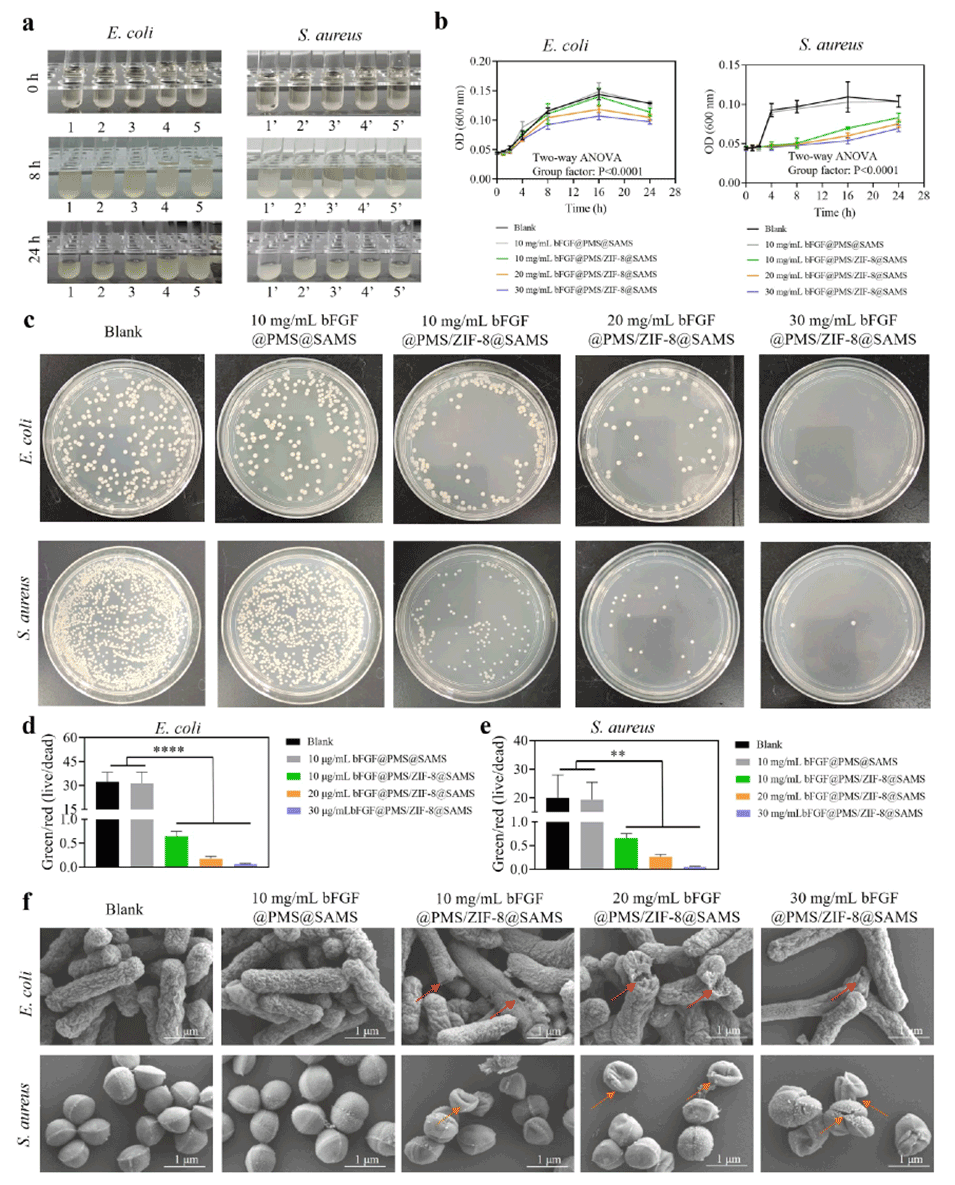
图5.bFGF@MS/ZIF-8@SAMS的抗菌作用。
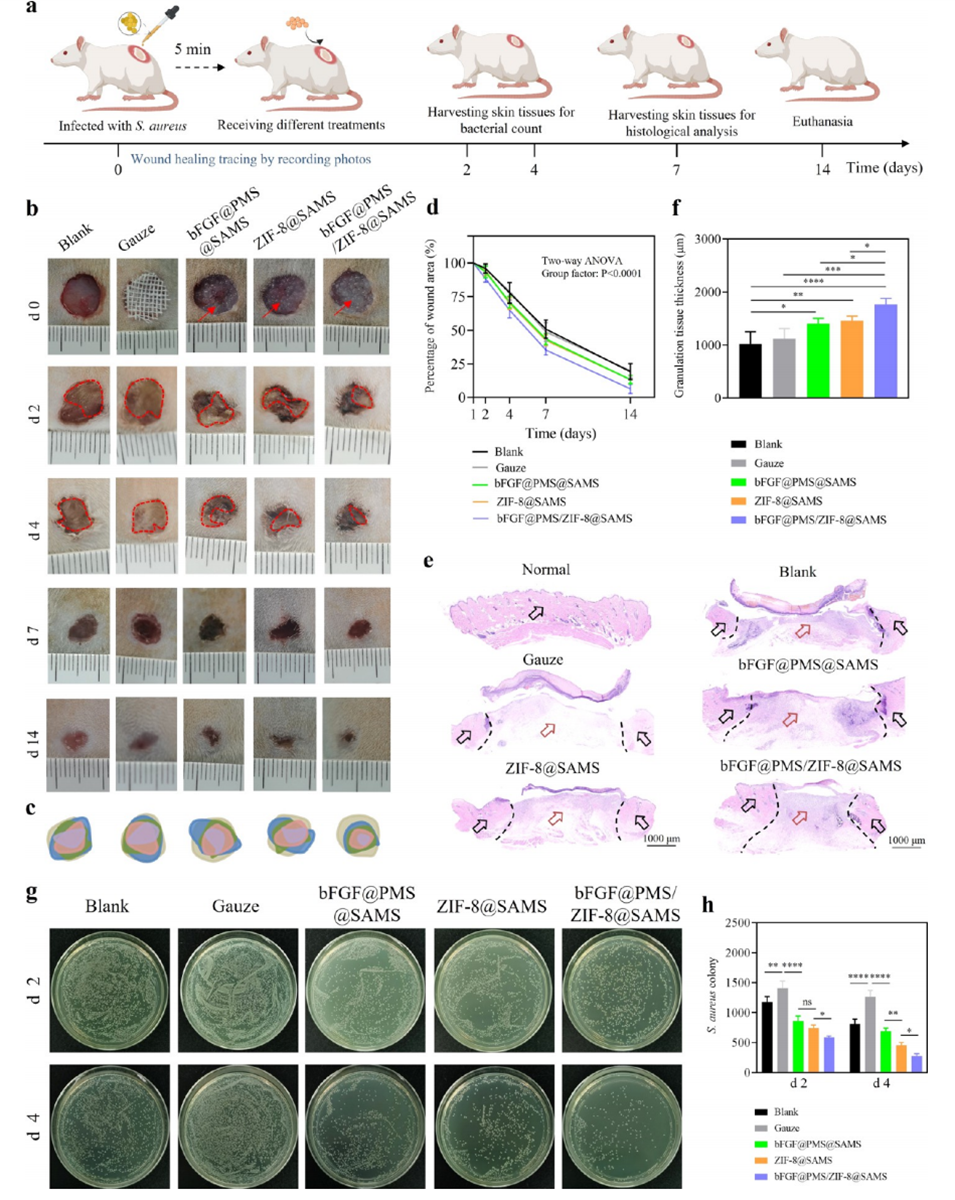
图6.bFGF@MS/ZIF-8@SAMS治疗大鼠感染创面。
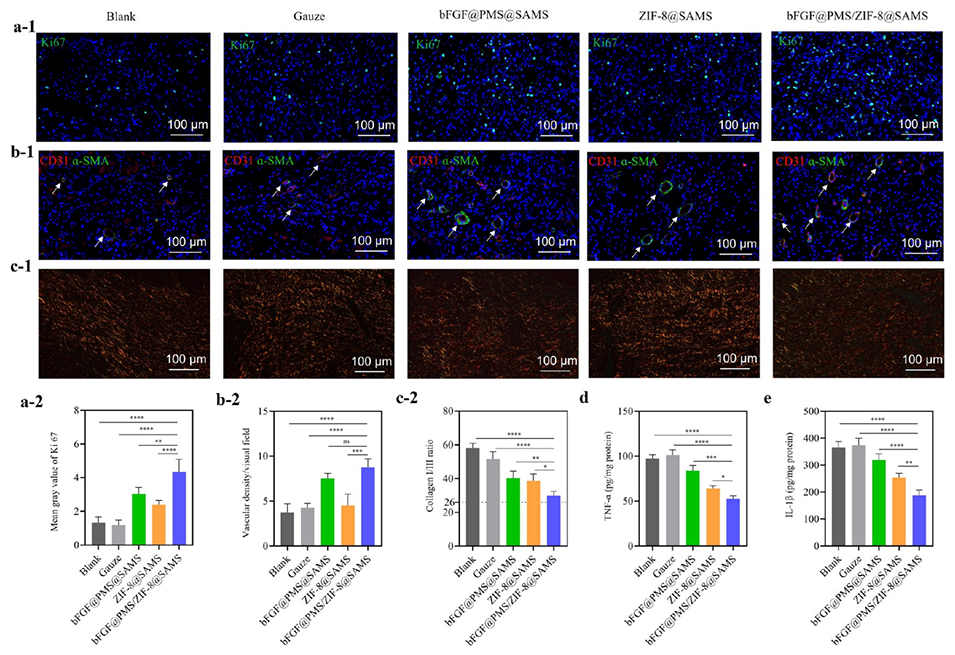
图7.不同处理后再生肉芽组织的组织学和分子分析。
论文链接:https://doi.org/10.1021/acsami.4c03655














