小内体衍生的脂质纳米囊泡(30-200nm)由活细胞主动分泌,可作为早期癌症诊断的关键生物标志物。然而,研究细胞外囊泡(EV)需要从各种体液中对其进行分离和纯化。传统的EV分离检测技术虽然日趋成熟,但通常样本量大、耗时长、通量相对较低。如何高通量地从体液中高效分离、纯化和检测这些结构特异性的EV仍然是体外诊断和临床研究中的巨大挑战。

近期,山东大学晶体材料国家重点实验室刘宏教授、海洋研究院韩琳教授和山东大学齐鲁医院神经外科李刚教授团队合作开发了一种基于氧化铝纳米通道阵列膜的微流控装置,用于高效、经济地过滤EV。相关研究以“Efficient EVs separation and detection by an alumina-nanochannel-array-membrane integrated microfluidic chip and an antibody barcode biochip”为题目,发表在期刊《Analytica Chimica Acta》上。
本文要点:
1、本研究提出了一种基于氧化铝纳米通道阵列膜的微流体装置,可实现高效、经济的EV分离。
2、评估了不同直径氧化铝膜的过滤性能,发现经过亲水处理的通道直径为90nm的优化腔室阵列可以实现高达82%的过滤效率,而无需任何化学或物理分离方法的辅助。
3、重要的是,通过集成精心设计的多通道微流控生物芯片,可以原位捕获EV并通过抗体条形码生物芯片进行监测。
4、该分离芯片结合高通量检测芯片能够过滤几十微升的样本并识别不同的表型。对临床样本中EV的实际过滤和检测证明了该设备的高性能。
5、总之,这项工作提供了一种经济、高效、自动化的EV过滤和检测双功能集成芯片平台,可直接从血清或脑脊液中分离EV,并进行原位检测。
6、这种小型流体装置为高效识别和分析EV提供了强大的工具,在临床检测中具有巨大的应用潜力。
全文总结/概括:
微流控芯片在提高EV分离效率方面有哪些关键优势?
1、高过滤效率:该微流控芯片采用氧化铝纳米通道阵列膜,通过优化设计,可实现高达82%的EV过滤效率。
2、快速分离:该芯片能够在1小时内完成1mL样品的富集,显著减少了传统技术如超速离心所需的时间。
3、低成本和操作简便:与需要昂贵设备和复杂操作的传统方法相比,微流控芯片的制造和运行成本更低,操作更为简便。
4、可集成化:可与检测芯片集成,从而在同一平台上实现EV的分离和检测,提高实验的效率和便捷性。
所开发的集成式微流控芯片平台在以下领域展现出巨大的应用潜力:
1、临床诊断:该集成式微流控芯片平台能够快速从生物体液中分离和检测EV,为癌症等疾病的早期诊断提供有效工具。
2、生物标志物分析:该平台有助于在生物样本中发现和验证新的疾病相关生物标志物,推动个性化医疗和精准医疗的发展。
3、药物筛选与开发:通过分析EV在药物作用下的变化,该微流控芯片平台可用于药物效果的初步筛选和药代动力学研究。
4、疾病机理研究:该平台能够提供对疾病发展过程中EV变化的深入理解,为病理机制的探究提供重要工具。
5、生物医学研究:这种集成式微流控芯片平台可用于模拟和研究细胞间通讯,特别是在细胞外囊泡介导的信号传递方面。
6、微量样本检测:对于难以获取的珍贵样本,该平台能够在微量水平上实现高效的分析,适用于需要最小化样本量的临床研究。
7、高通量筛选:该集成式平台能够处理大量样本,适用于大规模的生物医学研究和疾病筛查项目。
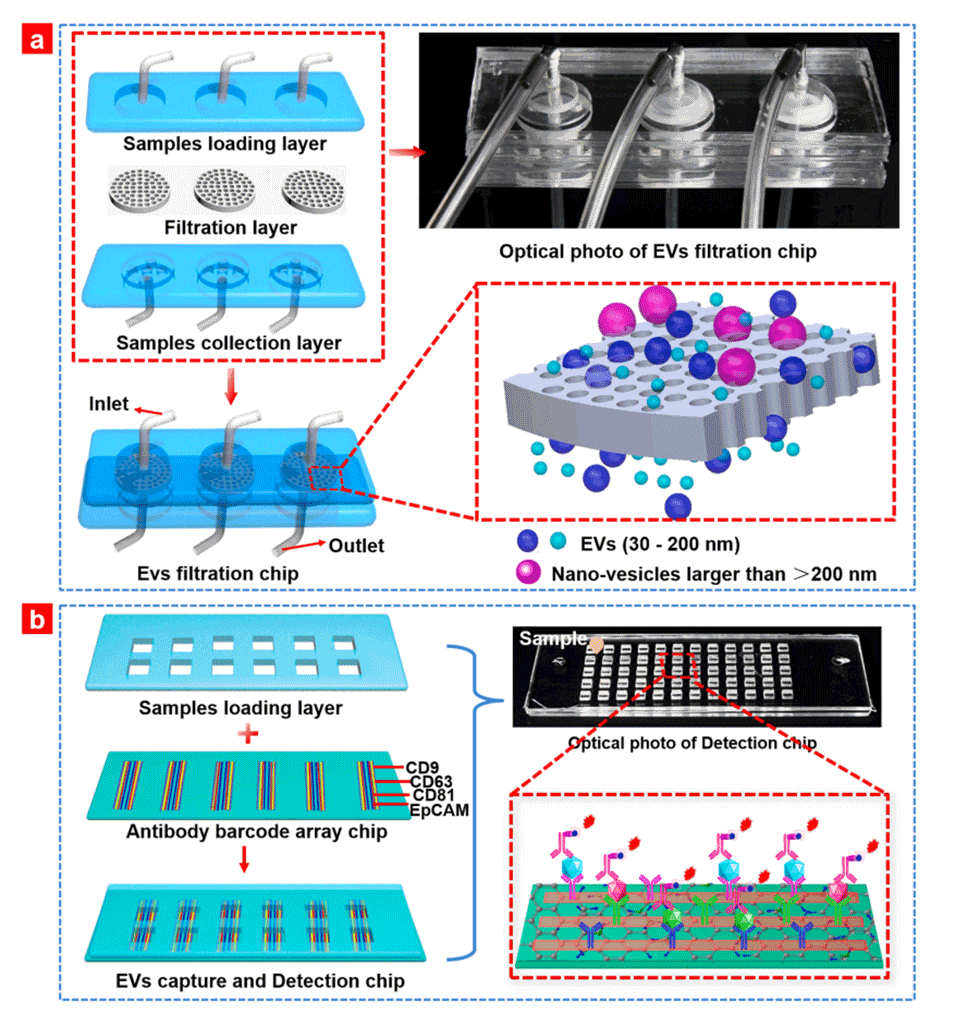
图1.(a)EV过滤芯片和(b)检测芯片的结构示意图和光学照片

图2.具有不同纳米通道直径的过滤膜和EV的表征
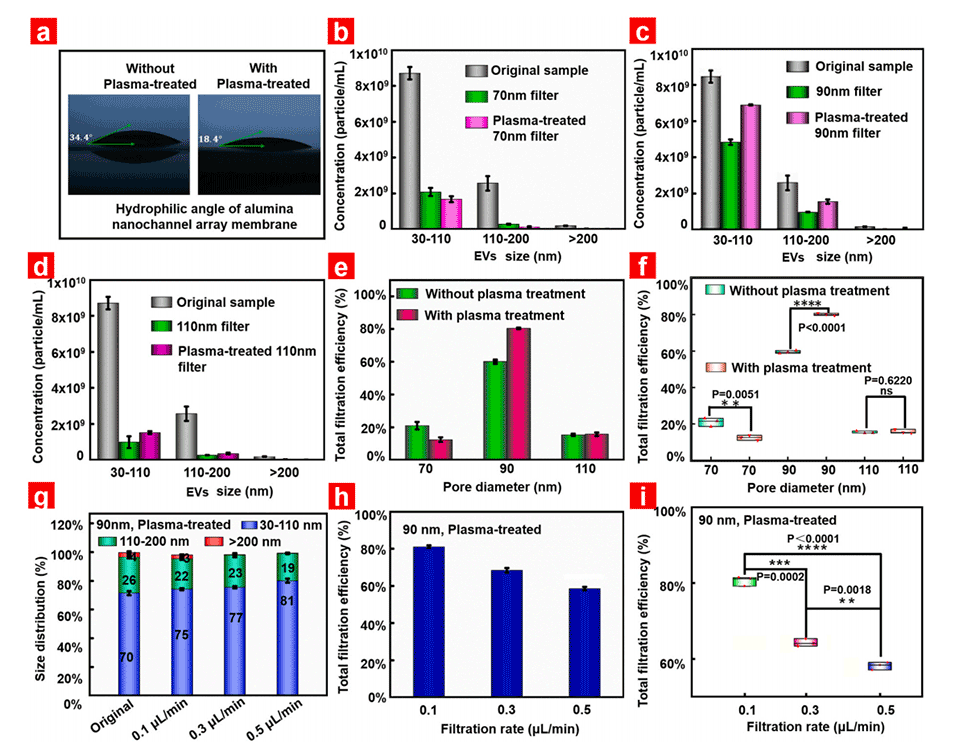
图3.实验参数的优化
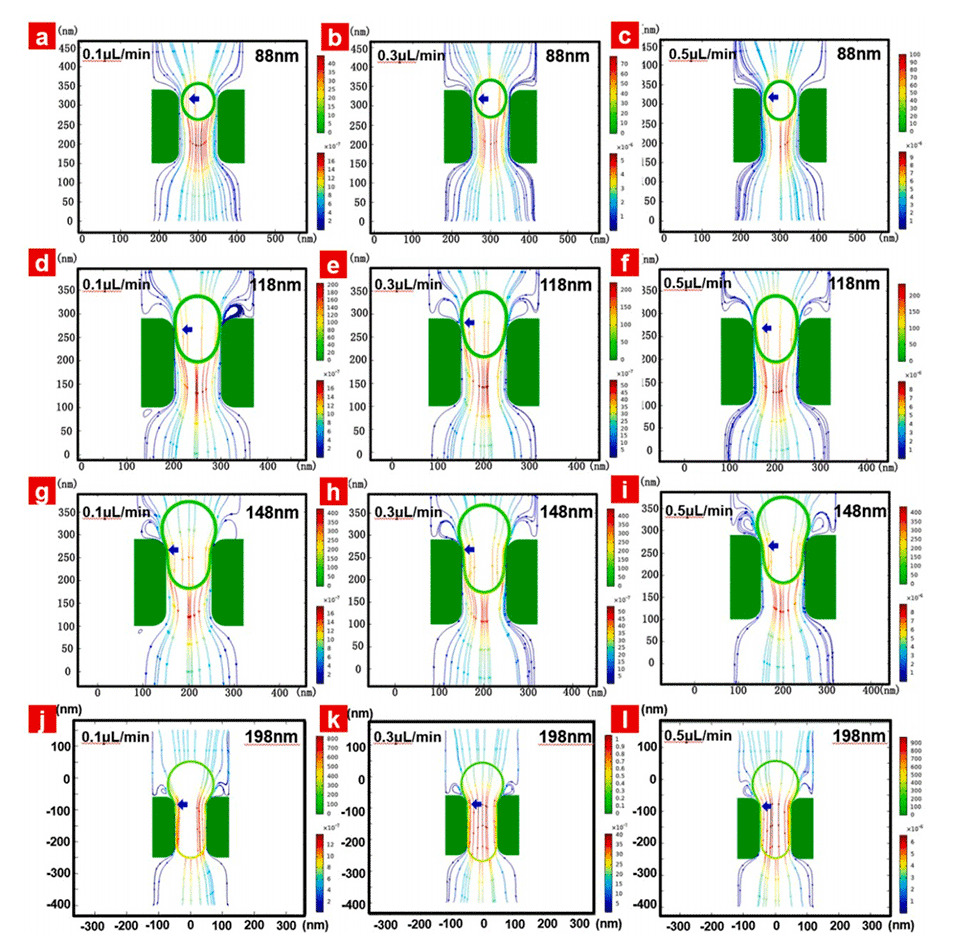
图4.不同加载速率下不同直径氧化铝纳米通道阵列膜的应力场和速度场分布的COMSOL仿真
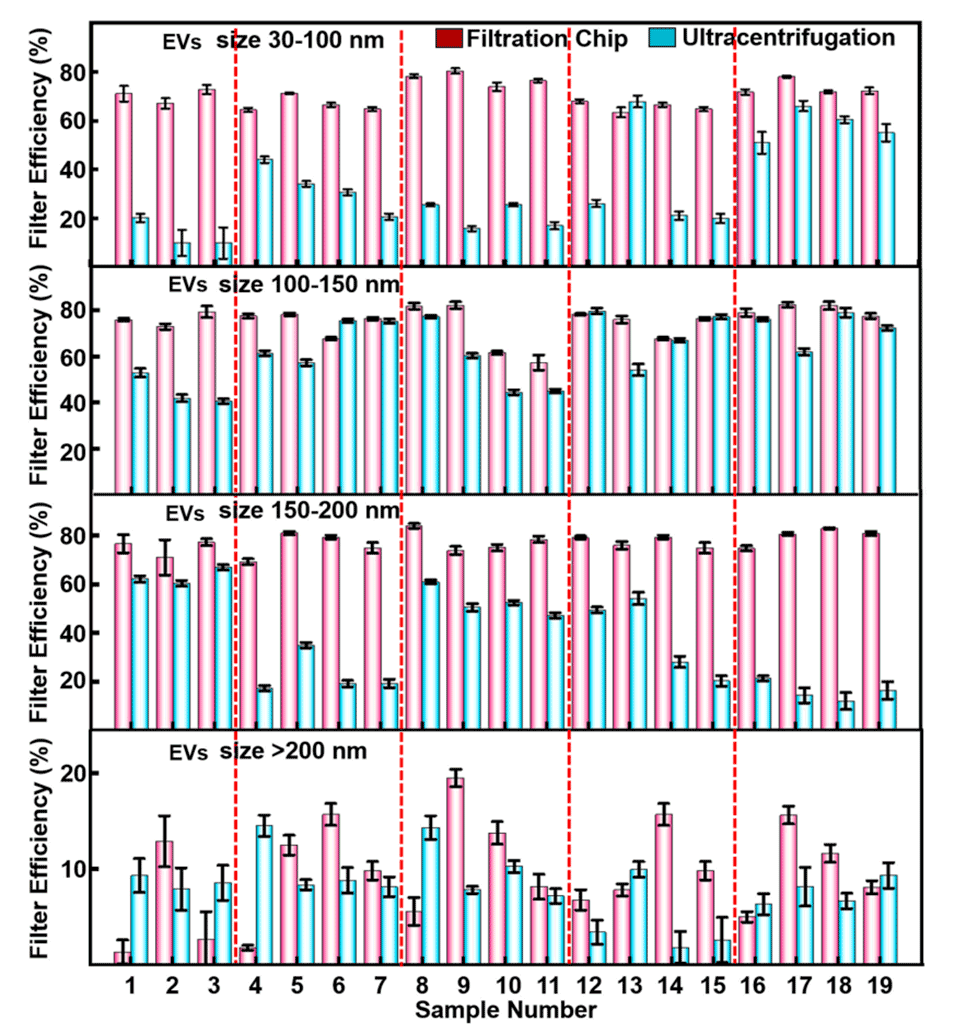
图5.微流控芯片过滤样品与金标准超离心法过滤效率的比较
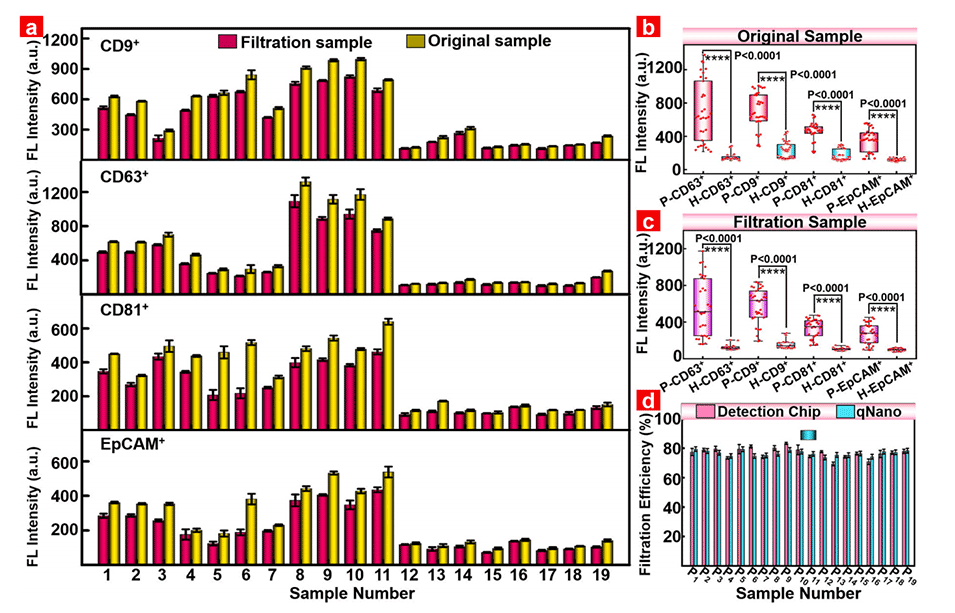
图6.纳流控芯片富集前后不同表型EV的荧光强度
原文链接:https://doi.org/10.1016/j.aca.2024.342576














