
导读:
该研究介绍了一种名为 PlasDroplex 的新型数字等离子体检测平台,旨在通过液滴微流控技术实现肿瘤衍生细胞外囊泡(EVs)的免清洗快速定量。该系统利用表面修饰了特定抗体的金纳米颗粒,在微小液滴中与目标囊泡结合并产生聚集效应,从而通过暗场显微成像将生物信号转化为可计数的“开/关”光学信号。这种方法仅需 10 微升血浆样本,即可在 1 小时内完成检测,显著提升了液体活检的效率与便捷性。临床验证显示,该技术在前列腺癌和肺癌的诊断中表现优异,其受试者工作特征曲线下面积(AUC)最高可达 0.998。通过消除复杂的洗涤步骤,该平台解决了传统 EV 检测中灵敏度低和操作繁琐的难题,为癌症早期诊断和免疫治疗监测提供了先进的数字检测方案。相关研究以“Wash-Free Digital Detection of Tumor Extracellular Vesicles via Plasmonic Droplet Microfluidics”为题目,发表在期刊《ACS Sensors》上。
本文要点:
1. 技术原理与核心突破
液滴限制性结合:将 10 μL 患者血清与抗体功能化的金纳米颗粒(Ab-AuNPs)共同封装在皮升(pL)级别的微液滴中。
等离激元耦合效应:当特定的 EV 与金纳米颗粒结合时,会诱导纳米颗粒在 EV 表面聚集形成网络,产生强烈的等离激元耦合,使液滴在暗场显微镜下呈现明亮的“开(On)”状态;未结合的液滴则保持“关(Off)”状态。
数字化定量:利用泊松分布统计原理,通过对“开/关”液滴进行自动化计数,实现对特定 EV 亚群的绝对定量,分辨率可达单颗粒水平。
2. 主要技术优势
免清洗(Wash-free):传统的 EV 检测通常需要繁琐的洗涤步骤以降低背景噪声,而 PlasDroplex 通过液滴微流控技术消除了洗涤和多步标记过程,避免了样本损失。
快速且微量:整个检测流程在 1 小时内即可完成,且仅需 10 μL的微量血浆样本。
高灵敏度与重复性:检测限(LOD)低至 2500–6700 EVs/mL,且具有极高的重复性(变异系数 CV < 3%)。
3. 临床应用与验证
研究团队通过 63 份临床样本验证了该平台在癌症诊断中的卓越表现:
前列腺癌诊断:针对 PSA 和 PSMA 阳性 EV 的检测,其受试者工作特征曲线下面积(AUC)分别达到 926和 0.932。
肺癌诊断:针对 PD-L1 阳性 EV 的检测,AUC 高达 998,展现了在免疫检查点监控方面的巨大潜力。
4. 材料工程创新
采用了单宁酸(Tannic Acid)辅助的表面工程策略,在金纳米颗粒表面构建了高密度的抗体层。
相比传统的柠檬酸钠稳定法,这种方法显著提高了抗体的负载效率和 EV 结合的亲和力,从而增强了光学信号。
总结而言,PlasDroplex 为液态活检提供了一种低成本、高效率且易于操作的数字化检测方案,克服了传统 EV 分析中操作复杂、耗时长和灵敏度不足等挑战。
该研究仍存在一些局限性:
首先,尽管 TEM 图像证实了金纳米颗粒在 EV 表面的密集聚集,但单颗粒水平上的标记化学计量比尚未得到定量解析。
其次,虽然泊松统计降低了多个 EV 占据同一液滴的概率,但极高浓度的 EV 样本可能会增加共封装(co-encapsulation)的风险。
第三,未来需要规模更大、更多样化的患者队列(包括早期、转移期和治疗后的病例)来全面评估其临床性能
液滴微流控技术之所以能够消除繁琐的洗涤步骤,主要归功于其独特的物理空间限制和等离激元信号增强机制。具体原因如下:
液滴的微反应器效应:该技术将样本分割成数以百万计的皮升(pL)级微液滴,每个液滴都作为一个独立的微反应器。这种数字化分割实现了单颗粒水平的分辨率,避免了在大体积溶液中常见的非特异性信号叠加,从而无需通过洗涤来降低背景噪声。
抑制非特异性聚集:在宏观溶液中,抗体功能化的金纳米颗粒(Ab-AuNPs)容易发生随机的、不受控制的聚集,导致信号不稳定。液滴的物理边界限制了纳米颗粒的运动空间,有效抑制了预限制阶段的非特异性聚集。在液滴内部,AuNPs 只会在目标细胞外囊泡(EV)表面特异性地聚集,形成均匀且局域化的组装体。
高对比度的“等离激元开关”机制:这是实现“免清洗”检测的核心物理原理。
“关(Off)”状态:单个直径 10 nm 的金纳米颗粒在暗场显微镜下的散射信号极弱,几乎不可见。因此,未结合目标 EV 的液滴保持黑暗。
“开(On)”状态:当多个 AuNPs 结合在同一个 EV 表面时,它们之间的距离缩短(通常在 6-10 nm 范围内),产生强烈的近场电磁耦合。
信号放大:这种耦合效应会使散射截面增加两个数量级以上,并产生明显的红移,使含有目标 EV 的液滴在显微镜下呈现明亮的信号。 由于未反应的游离纳米颗粒不产生可察觉的信号,因此无需物理洗涤来去除它们,直接通过光学对比即可区分。
无需表面固定化:传统的检测平台通常需要将 EV 固定在固相表面上,这一过程必然涉及多次洗涤以去除未结合的杂质。而 PlasDroplex 是在液滴的液相环境中完成结合的,避免了复杂的表面化学处理和随后的洗涤步骤,同时也减少了样本在洗涤过程中的损失。
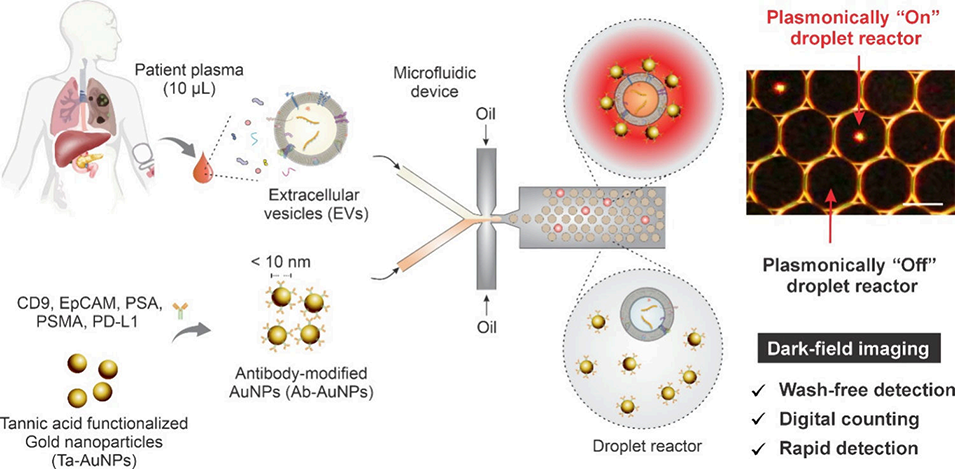
图1. 用于免清洗细胞外囊泡(EV)检测的 PlasDroplex 分析示意图。 将患者血浆(10 μL)与抗体功能化的金纳米颗粒混合,并分割封装至约 9 pL 的液滴(直径约 27 μm)中。EV 与金纳米颗粒(AuNP)的结合诱导了等离激元聚集,产生明亮的“开(On)”液滴,而无 EV 的液滴则保持黑暗,从而能够通过暗场成像实现快速、免清洗的数字化检测。
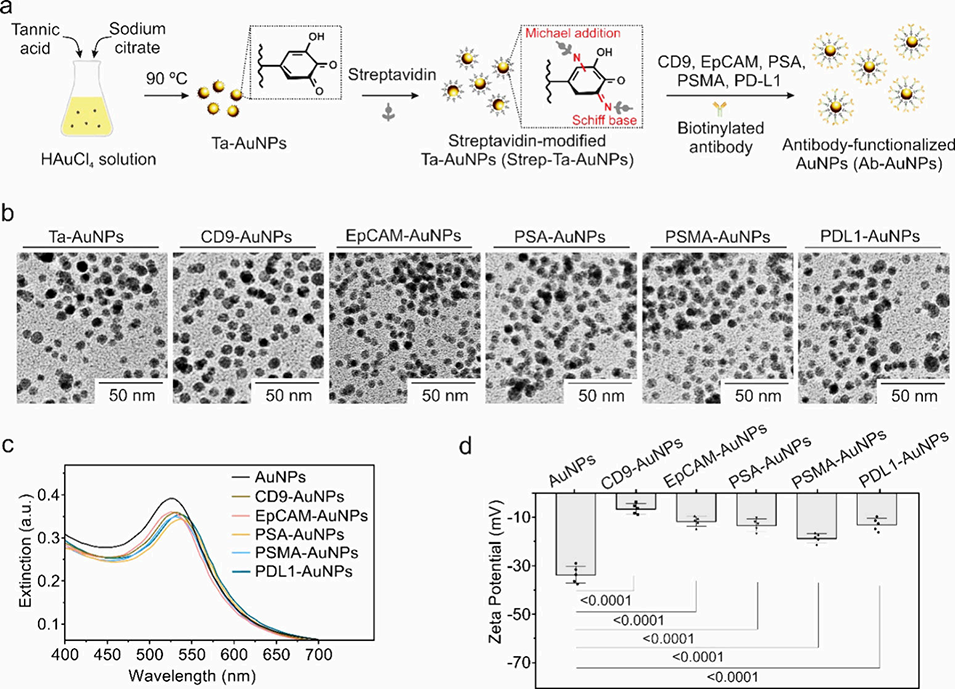
图2. 抗体功能化的金纳米颗粒(AuNPs)和细胞外囊泡(EVs)的制备与表征。 (a) 单宁酸还原的 AuNP 合成、链霉亲和素修饰以及与生物素化抗体(CD9、EpCAM、PSA、PSMA、PD-L1)偶联的示意图。 (b) 抗体功能化 AuNPs 的透射电子显微镜(TEM)图像。比例尺:50 nm。 (c) 紫外-可见(UV-vis)光谱显示抗体偶联后特征性的表面等离激元共振(LSPR)红移。 (d) Zeta 电位变化证实了表面功能化的成功。数据为平均值 ± 标准差 (n = 5);统计分析采用单因素方差分析(one-way ANOVA)及 Tukey 多重比较检验。
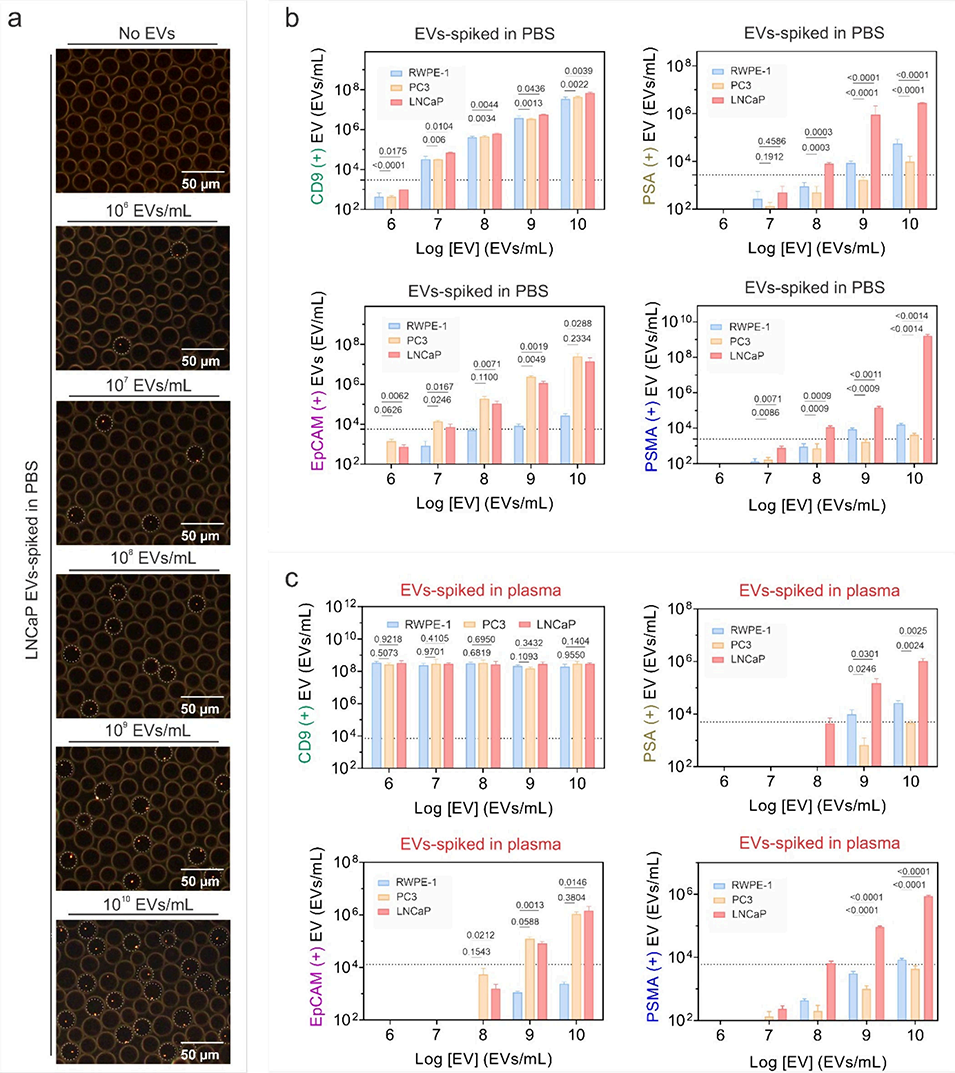
图3. 使用 PlasDroplex 分析对 PBS 和血浆中的 EV 生物标志物进行数字化检测。 (a) 暗场图像显示,随着掺入 PBS 中的 LNCaP 来源 EV 浓度升高(106–1010 EVs/mL),等离激元“开”液滴(圆圈标记)的数量随之增加。比例尺:50 μm。 (b) 对掺入 PBS 中的 CD9(+)、EpCAM(+)、PSA(+) 和 PSMA(+) EVs 的定量分析。CD9 作为广谱 EV 标志物,而相对于正常对照(RWPE-1),EpCAM、PSA 和 PSMA 在前列腺癌来源的 EVs(PC3、LNCaP)中富集。 (c) 对掺入血浆中的 EV 生物标志物的定量分析,基质效应降低了信号强度,但仍保留了标志物特异性的辨别能力。数据为平均值 ± 标准差 (n = 3);统计分析采用单因素方差分析及 Tukey 多重比较检验。
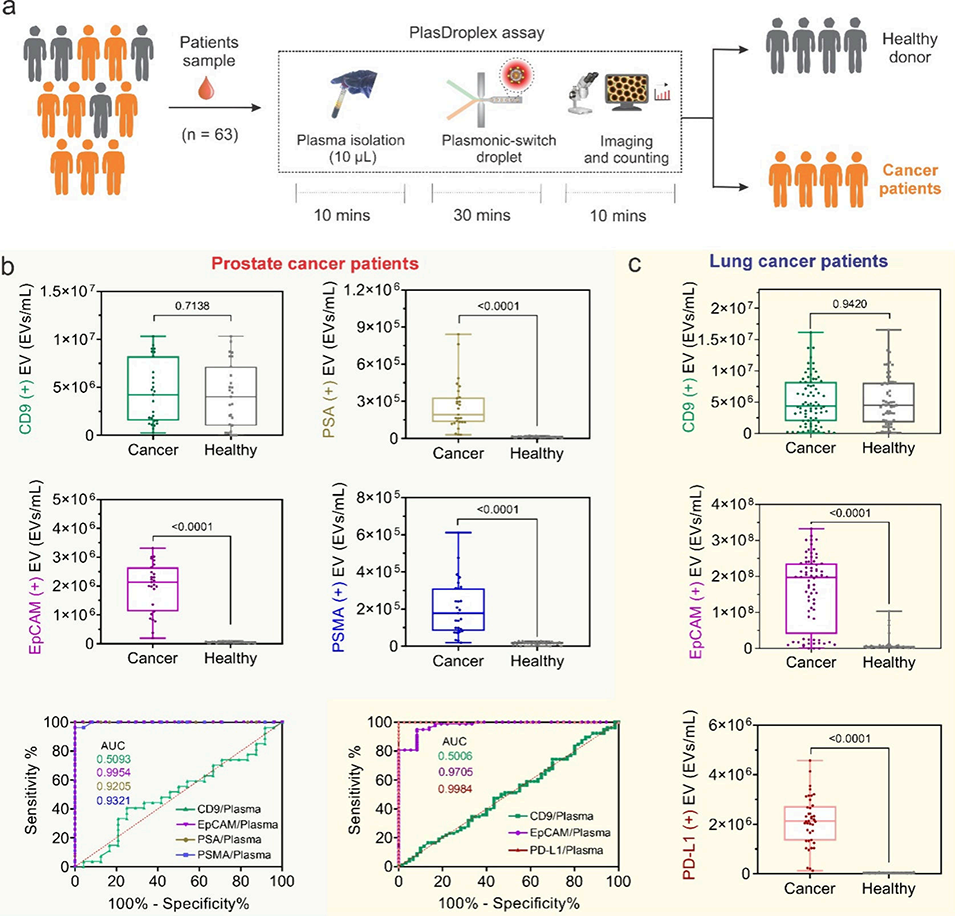
图4. 使用人类血浆样本(n = 63)对 PlasDroplex 分析进行临床验证。 (a) 临床验证的 PlasDroplex 工作流程,包括血浆处理、基于液滴的等离激元检测、成像和 1 小时内的数字化 EV 计数。 (b) 前列腺癌患者和健康捐赠者血浆中 CD9(+)、EpCAM(+)、PSA(+) 和 PSMA(+) EVs 的定量。CD9 水平相当,而 EpCAM、PSA 和 PSMA 在患者中显著升高。ROC 分析得出的 AUC 值分别为 0.926 (PSA) 和 0.932 (PSMA)。 (c) 来自肺癌患者(n = 26)和健康捐赠者(n = 20)血浆样本中 CD9(+)、EpCAM(+) 和 PD-L1(+) EVs 的定量,其中 PD-L1 的 AUC 达到 0.998。数据为平均值 ± 标准差;显著性通过双尾非配对 Student t 检验确定。
论文链接:https://doi.org/10.1021/acssensors.5c03705
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














