微流控机械穿孔技术作为一种细胞内递送外源物质的新兴方法,在免疫细胞工程和细胞治疗领域展现出巨大潜力。与传统的病毒载体和非病毒载体相比,机械穿孔技术能够高效且无载体地实现核酸、蛋白质、纳米颗粒等多种生物大分子的细胞内传递,同时最大限度地保持细胞活力和功能。该综述深入分析了三类主要的微流控机械穿孔技术平台:纳米结构介导的膜穿刺、基于收缩通道的细胞挤压、以及剪切力驱动的水力穿孔。每种策略的原理、设备设计及其在不同免疫细胞中的递送性能均被详尽探讨。相关研究成果以“Microfluidic-based mechanoporation for immune cell engineering: Principles, design, and applications in cell therapy”为题目,发表在期刊《Materials Today Advances》上。

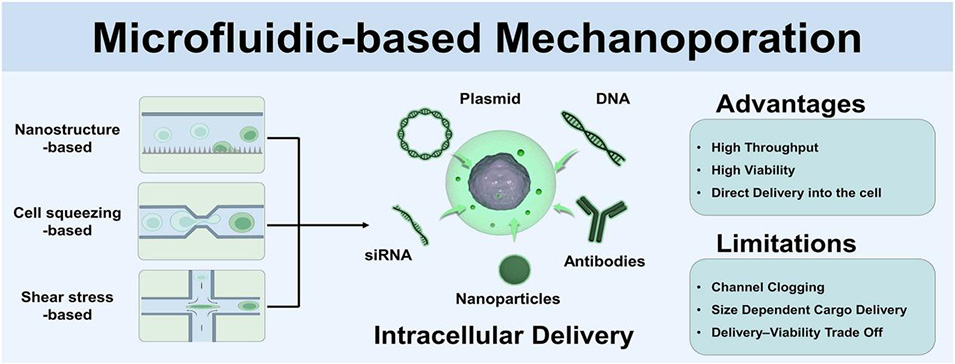
纳米结构介导的穿刺利用垂直排列的尖锐纳米针、纳米稻草等结构,直接穿透细胞膜形成短暂通道,实现外源物质的直接胞质递送。此类平台如纳米稻草阵列不仅支持重复且时序控制的递送,还能够实现高效的DNA、siRNA和蛋白质传递,且对细胞活力和基因表达干扰最小。然而,该技术受限于细胞附着性、纳米结构制备复杂及透膜效率不稳定,尚需结合电场等辅助策略提升递送效率。
基于细胞挤压的机械穿孔技术则通过微流控通道中的狭窄构造对细胞施加机械变形,诱导细胞膜产生瞬时孔洞,允许外源分子扩散进入胞内。该类方法具有高通量和无载体的优势,已实现对多种难转染免疫细胞的有效转染和CRISPR基因编辑。通过优化通道几何结构(如钻石形障碍物、曲面通道、纳米刀片)和引入粘弹性介质,进一步提升了递送效率与细胞存活率。尽管存在通道堵塞和对细胞尺寸敏感等挑战,基于细胞挤压的微流控设备在临床制造中显示出良好的应用前景。
剪切应力诱导的机械穿孔技术则利用微流控中的流体动力学现象,如惯性聚焦、拉伸剪切及涡流产生,非接触式地诱导细胞膜形成短暂孔洞。该类平台避免了物理通道狭窄带来的堵塞问题,兼容细胞尺寸多样性,且能实现高达每秒百万级的细胞处理速率。典型设计包括T形、Y形及十字形流道结构,以及基于涡流剪切的柱阵列。通过流体剪切力的精确调控,实现了多种载体的高效递送和基因组编辑,且细胞功能及表型保持良好。该方向的挑战在于需保证流体稳定性、聚焦精度及均匀的应力分布,未来有望通过多通道并行化和实时监测实现大规模临床应用。
总体而言,微流控机械穿孔技术以其高效、安全、无载体的细胞递送优势,正逐步克服传统基因转染方法的瓶颈。尽管设备复杂性、工艺稳定性及跨细胞类型的普适性仍待提升,结合纳米材料设计、流场工程及辅助物理刺激的多模态策略,将进一步推动其临床转化。随着制造工艺的优化和GMP兼容流程的开发,机械穿孔技术有望成为下一代细胞与基因治疗的核心工具。
本文亮点
全面概述了用于细胞工程的微流控机械穿孔技术。
对比分析了纳米结构介导型、收缩通道与剪切力驱动型三类平台。
探讨了不同细胞类型下的递送效率、细胞活性及技术可扩展性。
综述了该技术与细胞治疗和基因治疗临床流程的集成应用。
梳理了新一代机械穿孔技术面临的挑战与未来发展方向。
一张图读懂全文
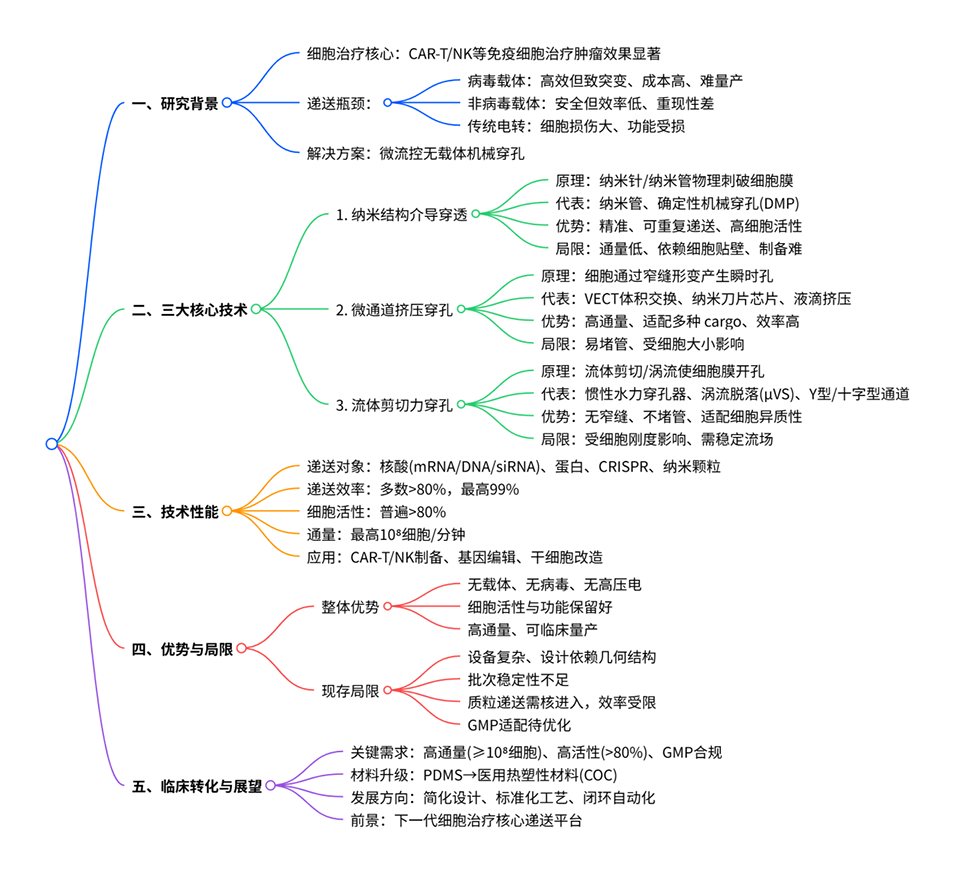
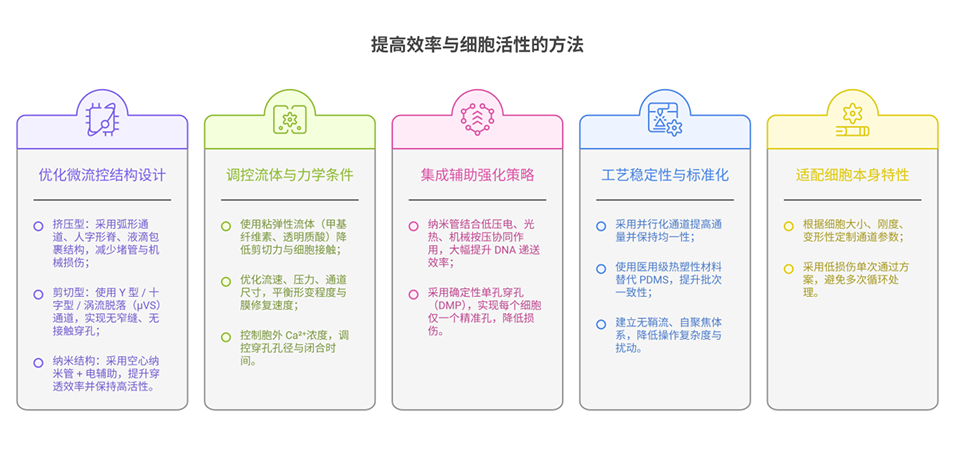
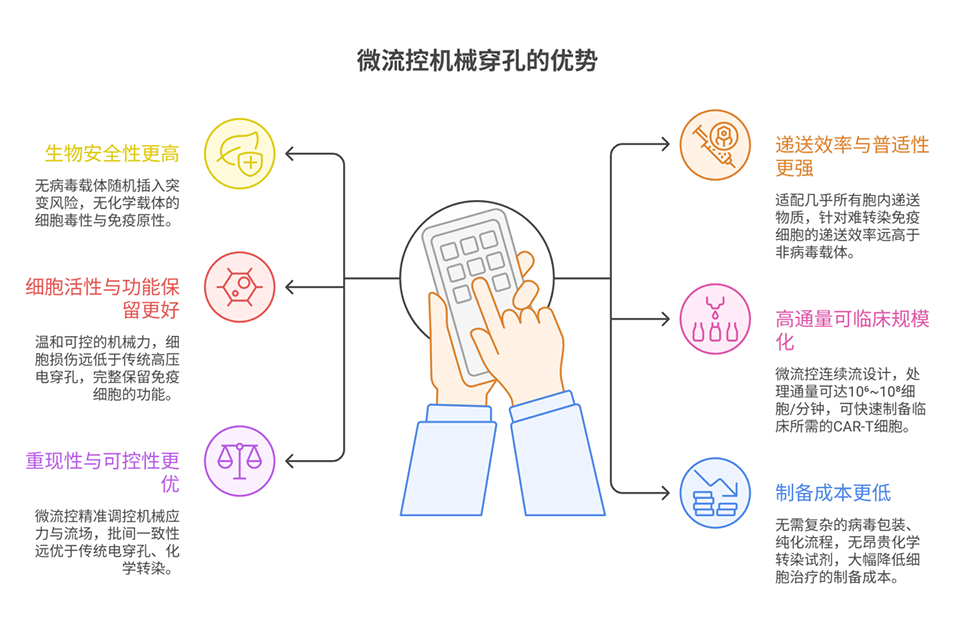
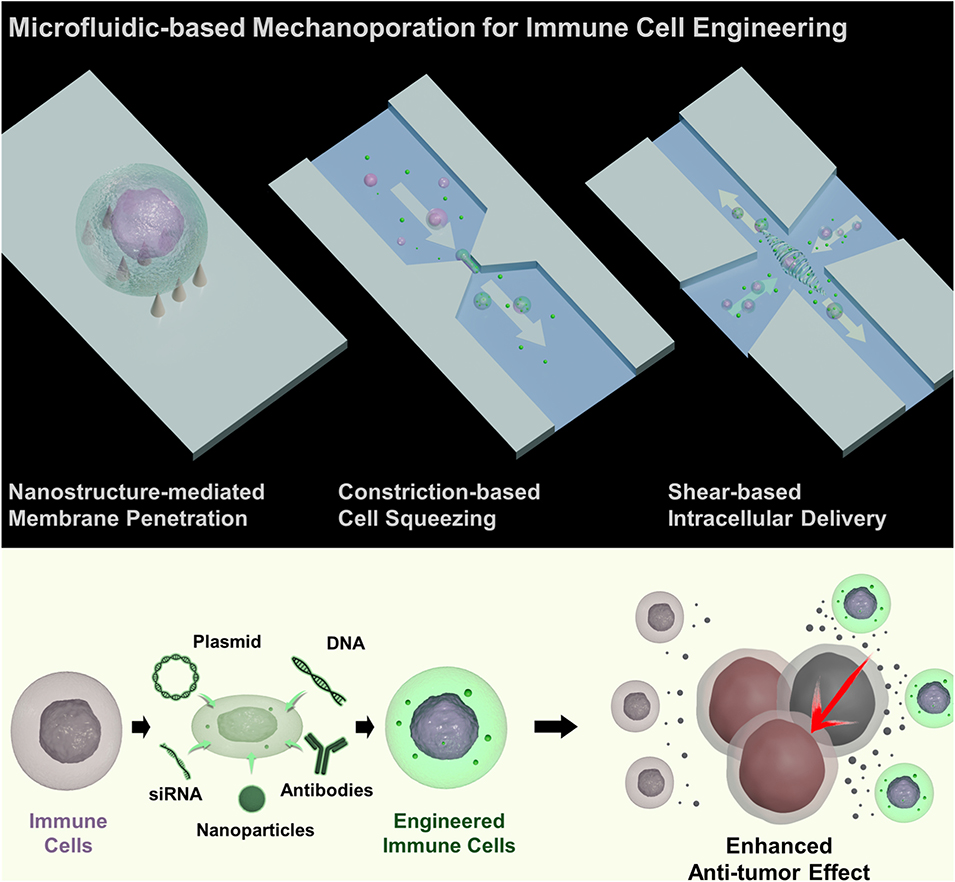
图1 三种代表性微流控机械穿孔策略用于胞内递送的示意图。纳米结构介导的细胞膜穿透利用垂直排列的尖锐纳米材料瞬时破坏细胞膜,实现多种生物分子直接进入胞质。基于收缩的细胞挤压通过使细胞在微通道收缩区变形来递送外源载荷,而基于剪切力的胞内递送则利用拉伸或惯性剪切等流体动力产生瞬时膜孔,无需物理收缩。这些方法可将核酸、蛋白质、抗体和纳米颗粒递送至免疫细胞,实现细胞工程化以增强抗肿瘤活性。
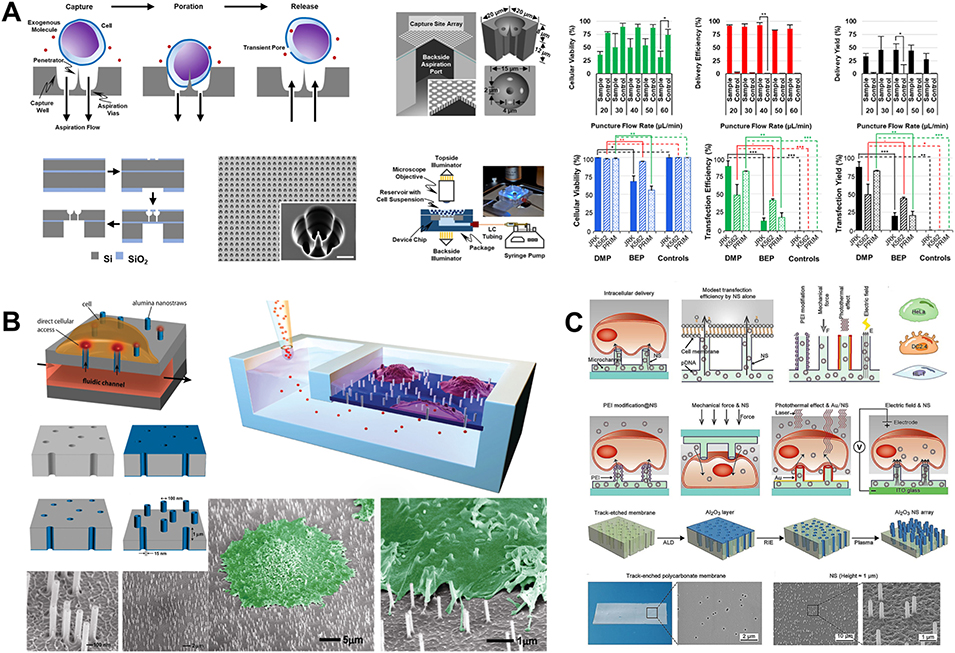
图2 利用纳米结构介导穿透实现外源物质胞内递送的微流控装置。(A) 确定性机械穿孔微流控芯片通过可控的机械膜穿透在每个细胞上诱导单个瞬时膜孔,可在多种细胞类型中实现高重现性与高效胞内递送。(B) 垂直排列的中空纳米管自发穿透细胞膜,建立直接的胞质通路,实现对膜不通透性分子的稳定、微创递送。(C) 纳米管阵列采用多种物理化学策略(如表面修饰、机械压缩、光热刺激、局部电场),证明电耦合(纳米电穿孔)最有效提升多种细胞的 DNA 转染效率,同时维持高细胞活性。
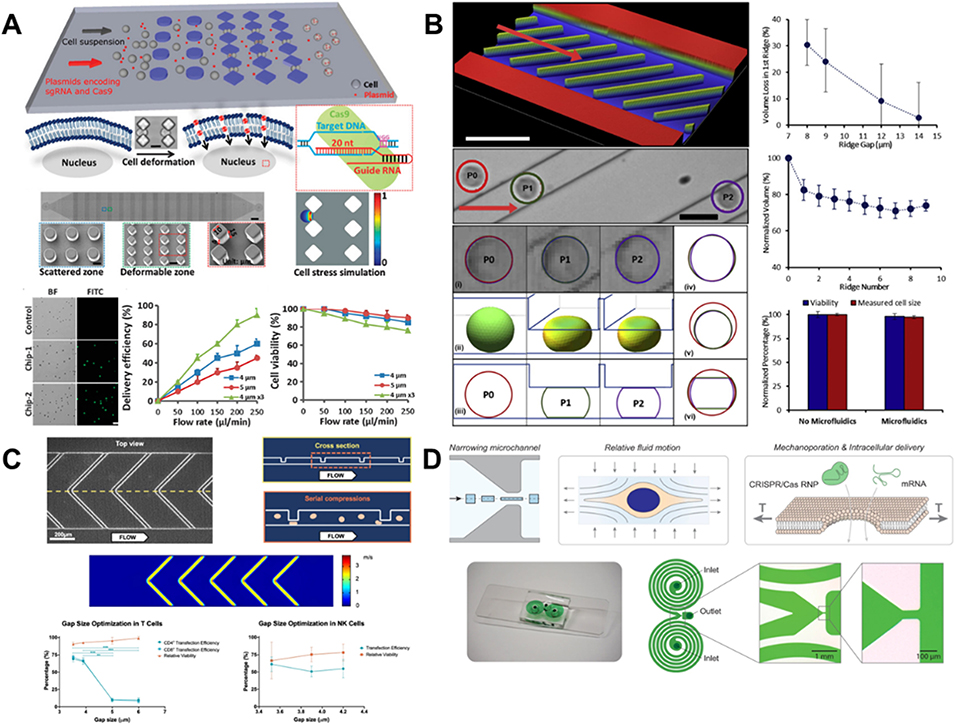
图3 利用收缩型细胞挤压实现外源物质胞内递送的微流控装置。(A) 集成菱形障碍物的微流控芯片,通过诱导反复机械变形,实现将核酸与蛋白质高效递送至多种细胞。(B) 矩形脊结构实现对流传递体积交换(VECT),反复压缩–松弛循环促进各种外源物质以尺寸无关的方式进入细胞。(C) 优化的人字形脊结构增强 VECT 性能,在可规模化制备条件下实现原代 T 细胞与 NK 细胞的高效 mRNA 转染与 CRISPR 介导编辑。(D) 基于透明质酸溶液的粘弹性聚焦平台,在大于细胞直径的收缩通道中实现无接触机械穿孔,在保持高递送效率与存活率的同时将机械损伤降至最低。
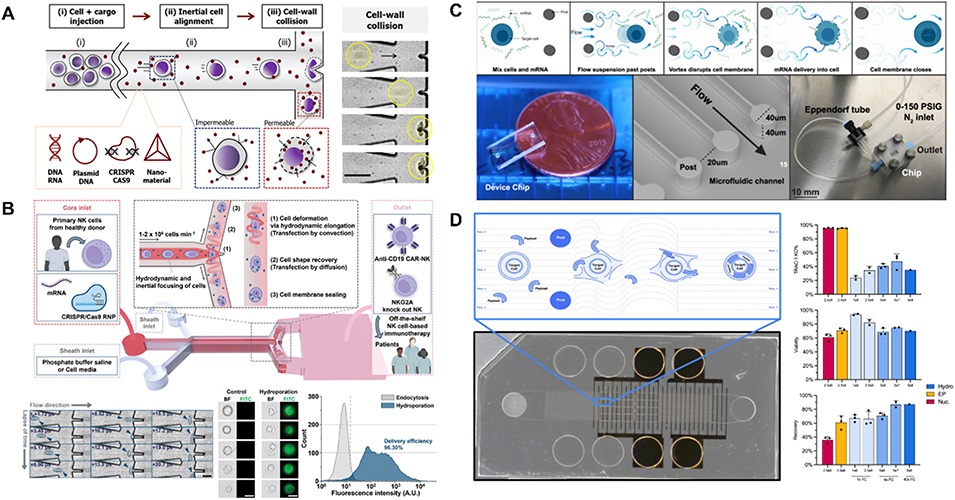
图4 利用流体剪切力实现外源物质胞内递送的微流控装置。(A) 惯性微流控细胞水力穿孔器(iMCH)作为用于纳米材料胞内递送的流体动力机械穿孔平台,展示了装置结构与工作原理:惯性聚焦将细胞导向带尖锐尖端的 T 型接头,引发可控的细胞–壁碰撞与流体剪切,产生瞬时膜纳米孔以实现载荷进入。(B) 200° 夹角的 Y 型接头水力穿孔器,采用三个入口实现鞘流辅助聚焦。细胞在驻点快速拉伸,形成瞬时纳米孔,可高效递送多种载荷。(C) 微流控涡流脱落(μVS)平台采用圆柱柱阵列,在高通量、防堵塞条件下利用持续涡流使细胞膜通透。(D) μVS 适用于 CRISPR–Cas9 核糖核蛋白与 AAV 模板的共递送,可在原代 T 细胞中实现靶向 CAR 敲入,同时保持高存活率与得率。
论文链接:https://doi.org/10.1016/j.mtadv.2026.100725
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














