细胞治疗、组织工程等领域的规模化推进,迫切需要能高效扩增高质量细胞的技术支撑。微载体作为贴壁细胞动态培养的核心载体,凭借高比表面积、节省培养基用量的突出优势,已成为实现细胞高密度培养的关键选择。但传统微载体仍存在诸多亟待解决的局限:合成聚合物基微载体初始细胞附着率偏低,高细胞汇合度下脱附效率不佳,往往需要额外修饰蛋白或细胞外基质才能满足使用需求;天然聚合物基微载体如明胶类,虽生物相容性更优,但机械稳定性不足,在动态培养环境中易提前降解,产生破碎颗粒,影响规模化应用。
更为关键的是,现有微载体的细胞脱附过程高度依赖胰蛋白酶等高蛋白水解酶,高浓度酶不仅会损伤细胞膜、破坏细胞骨架与细胞间连接,还可能降解细胞外基质蛋白,显著降低收获细胞的质量与功能。尽管温度响应型微载体为无酶脱附提供了新思路,如聚苯乙烯基PNIPAM涂层微载体,但其刚度较高,无法模拟软组织的天然柔韧性,容易对细胞增殖、分化等行为产生不利影响;而明胶基PNIPAM涂层微载体则延续了明胶机械性能弱的短板,在动态生物反应器中难以稳定应用,限制了其规模化推广。

近期,维多利亚大学机械工程系微工程创新实验室团队研发出一种温度响应型BrushGel微载体,通过微流控技术制备并经PNIPAM聚合物刷共价接枝功能化,实现了人真皮成纤维细胞与临床级间充质干细胞的高效扩增。该载体结合4℃低温与低浓度酶即可完成温和脱附,酶用量减少10倍且细胞存活率保持高位,适配规模化动态培养需求。相关研究以“Thermoresponsive BrushGel Microcarriers for Efficient Cell Expansion and Enzyme-Reduced Harvesting”为题目,发表于期刊《Advanced Healthcare Materials》。
本文要点:
1、本研究开发了一种温度响应型微载体BrushGel,其核心是通过微流控技术制备甲基丙烯酰化明胶(GelMA)水凝胶颗粒,并经EDC-NHS化学接枝聚(N-异丙基丙烯酰胺)(PNIPAM)聚合物刷,实现高效细胞扩增与低酶收获。
2、通过调节GelMA的甲基丙烯酰化程度(DOM)和PNIPAM浓度,精准调控微载体表面的PNIPAM接枝密度,确保单分散性和温度响应性能。
3、在动态培养条件下,人真皮成纤维细胞(HNDF)密度提升4.9倍,COL1A1基因表达上调12倍,胶原蛋白分泌增加;临床级间充质干细胞(MSCs)5天内扩增5.3倍,且均保持良好表型。
4、4℃低温处理可实现65%的细胞脱附效率,结合低浓度酶(用量减少10倍)时,脱附效率最高达90%以上,细胞存活率超80%。
5、在搅拌式生物反应器中可稳定培养10天,30rpm搅拌速率下细胞活性和代谢水平最优,适用于贴壁依赖型细胞的大规模工业化生产。
6、BrushGel通过减少酶的使用、降低细胞损伤、提升扩增效率,为再生医学、细胞治疗及生物制药领域提供了更安全、经济且可规模化的细胞培养平台。
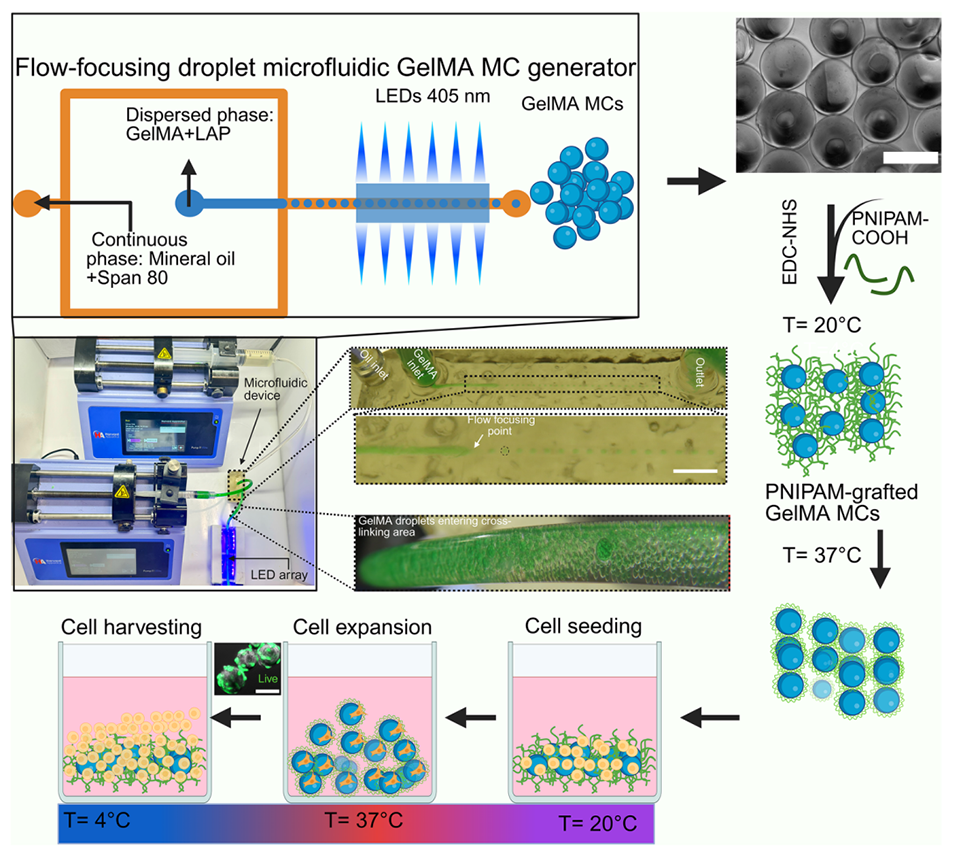
图1. 表面修饰甲基丙烯酰化明胶微载体(GelMA MCs)的制备流程及其在细胞生长与收获中的应用示意图
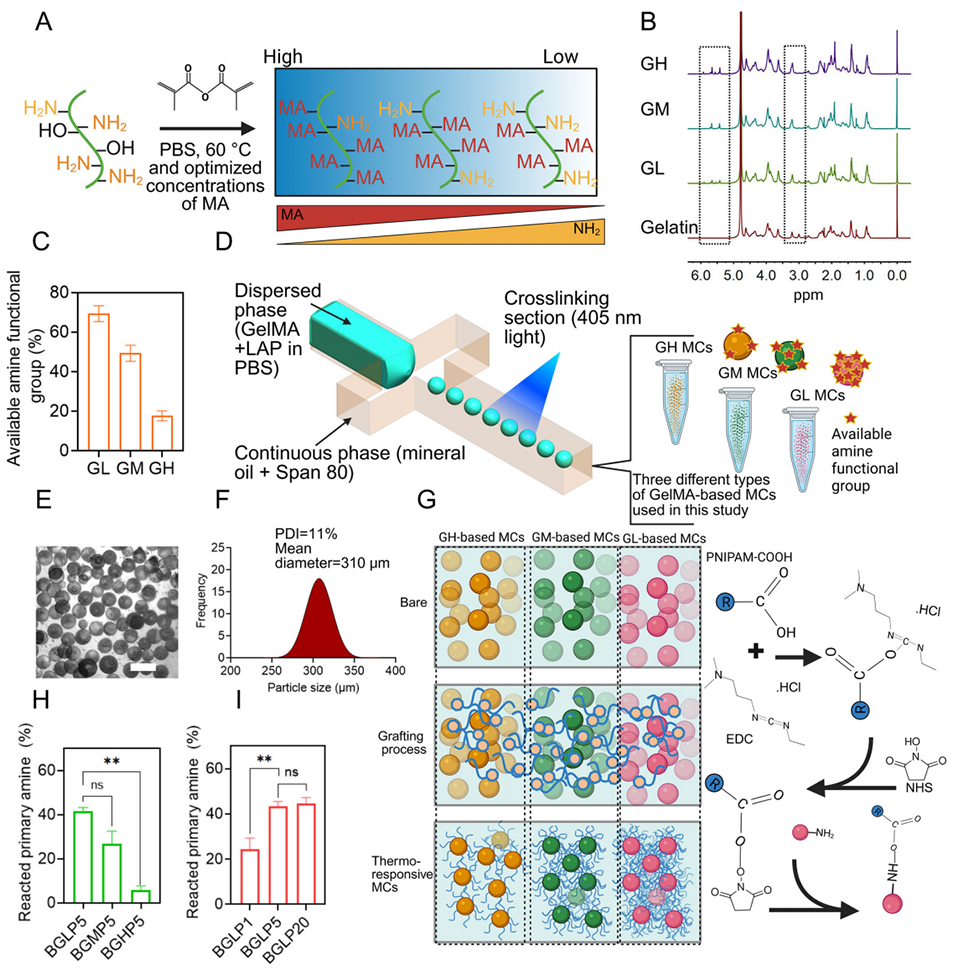
图2. 具有可调PNIPAM密度的PNIPAM接枝GelMA微载体的制备流程示意图
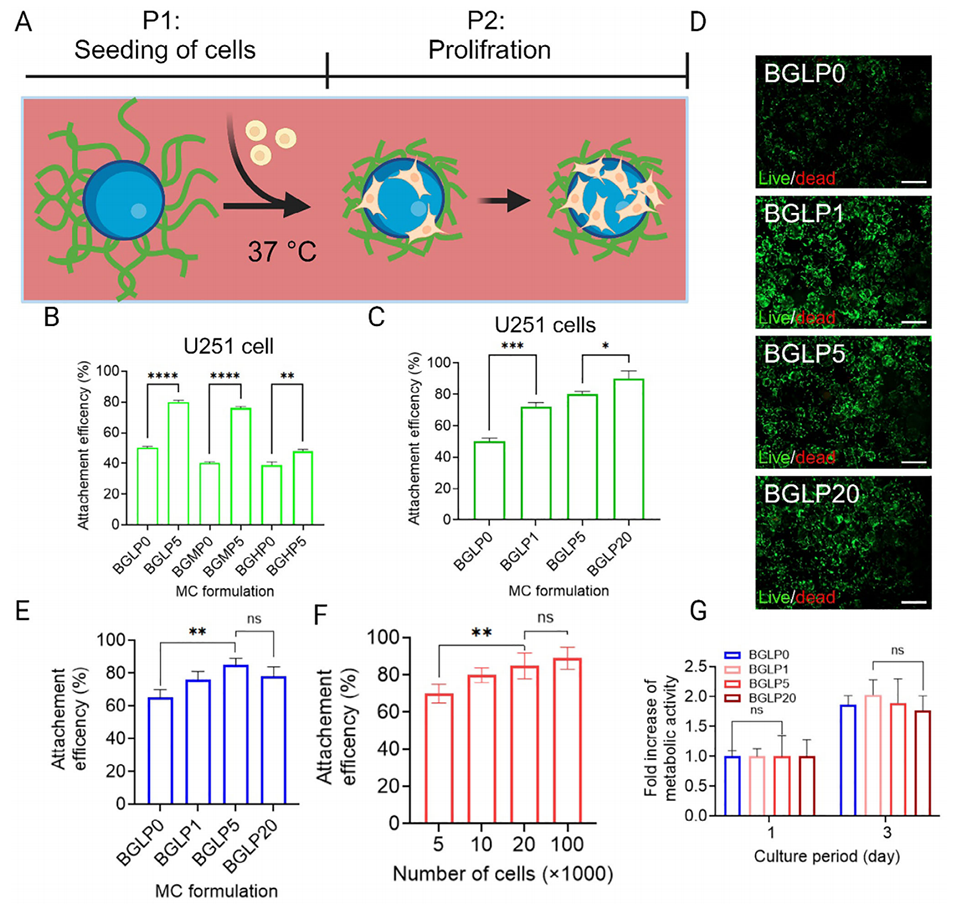
图3. PNIPAM接枝GelMA微载体上的细胞黏附与增殖情况
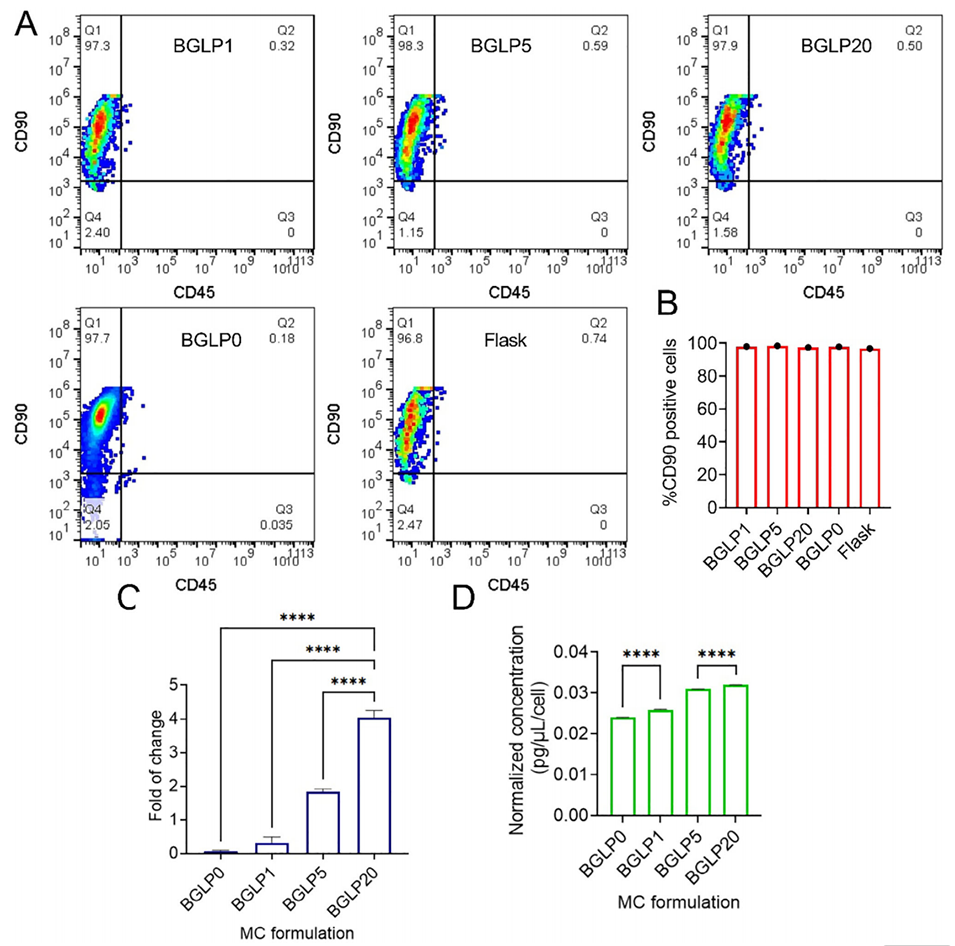
图4. 不同配方BrushGel微载体培养下HNDF细胞的表型、基因表达及蛋白分泌特性表征
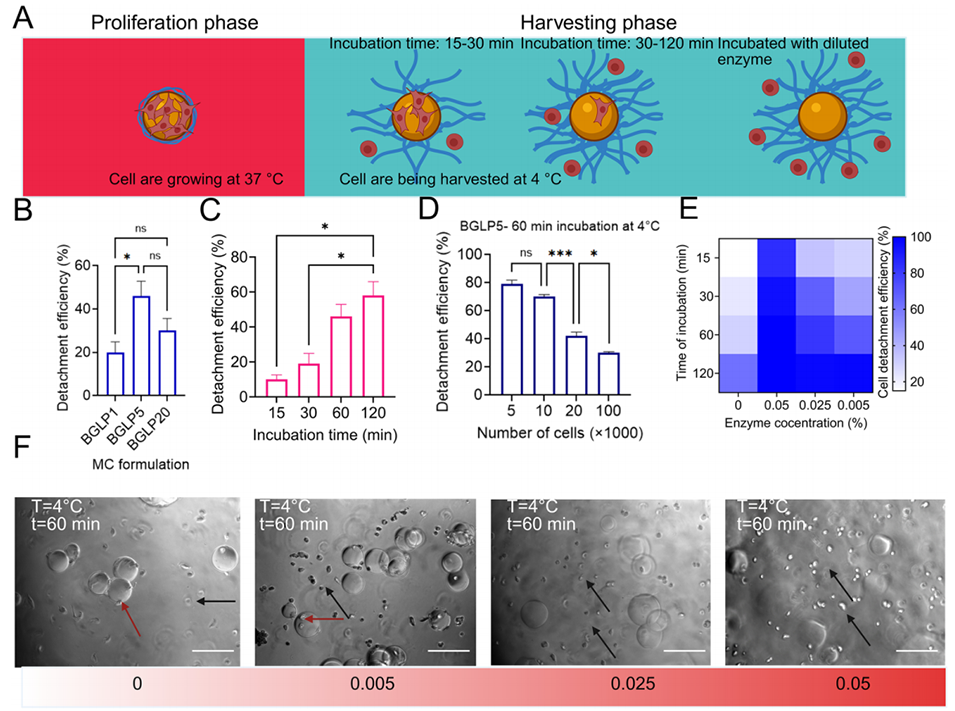
图5. 从BrushGel微载体收获HNDF细胞的相关特性研究

图6. 从BrushGel微载体收获间充质干细胞的相关特性研究
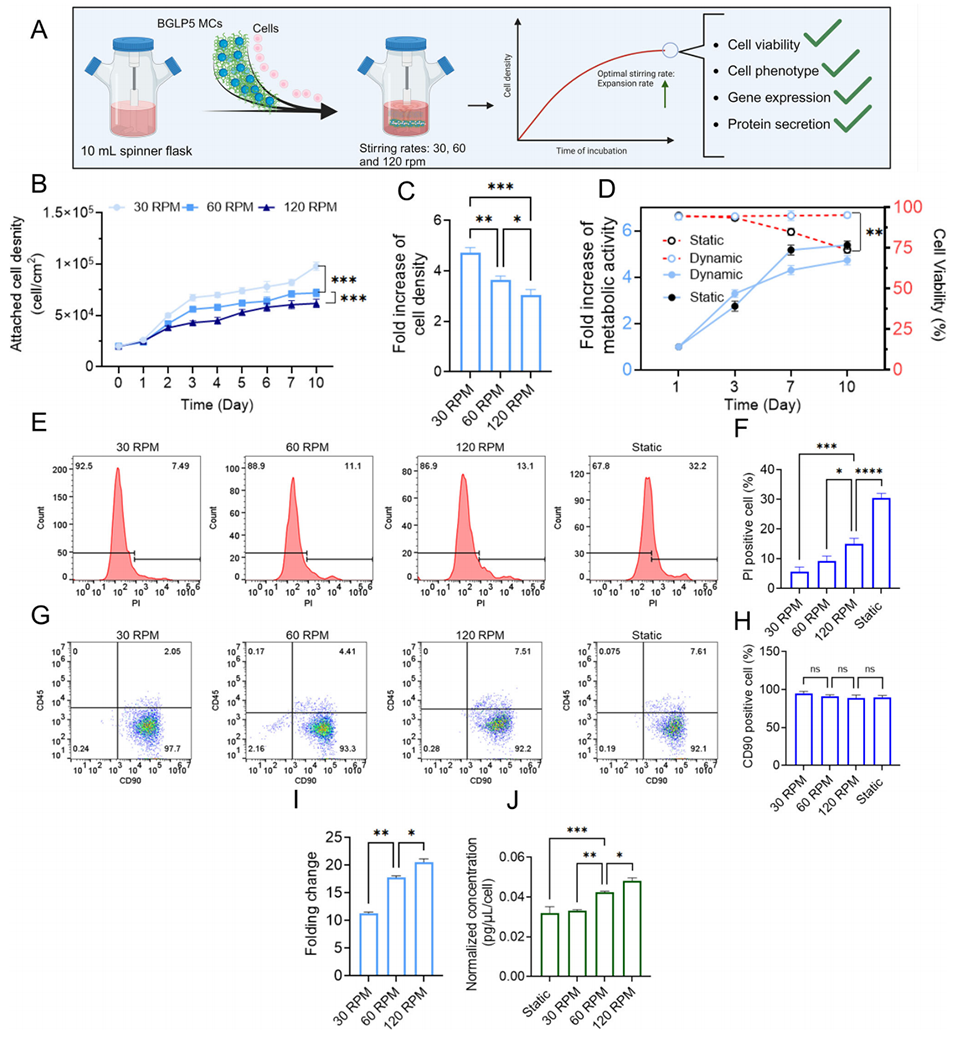
图7. BrushGel微载体在HNDF细胞动态培养环境中的应用特性
论文链接:https://doi.org/10.1002/adhm.202404538
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














