糖尿病,尤其是2型糖尿病(T2DM),已成为全球日益严重的健康问题,影响着约4.51亿人,预计到2045年这一数字将上升至6.93亿。尽管现有的口服降糖药物种类繁多,但它们在控制血糖方面往往效果不佳,尤其是对于T2DM患者。
维达列汀(VLG)作为一种DPP-4抑制剂,因其在调节与血糖相关的激素(如GIP和GLP-1)方面的作用而受到关注。然而,现有的维达列汀制剂存在频繁给药、血药浓度波动及胃肠道不适等问题,导致患者依从性差。

为了解决这些挑战,有研究人员开发了一种通过微反应器辅助的离子凝胶化技术制备的VLG负载壳聚糖-硫酸葡聚糖纳米粒子(VLG-CDNPs),旨在实现药物的持续释放,以提高其在糖尿病管理中的疗效和生物利用度。相关研究以“Engineered vildagliptin-loaded polymeric nanoparticles via microfluidic and spray drying for enhanced antidiabetic activity”为题目,发表在期刊《Future Journal of Pharmaceutical Sciences》上。
本文要点:
1、本研究使用微反应器开发了一种负载维达列汀(VLG)的交联壳聚糖-硫酸葡聚糖纳米颗粒(VLG-CDNPs),用于增强抗糖尿病药物VLG的治疗效果。
2、通过实验设计方法系统优化了制备过程,优化后的VLG-CDNPs平均粒径为217.4 ± 12.3 nm,包封效率为78.25 ± 3.0%。
3、体外研究显示,VLG在12小时内持续释放,在酸性和碱性条件下分别释放了约58%和83%的药物。
4、即使在100 μg/mL的浓度下,细胞存活率仍保持在80%,与纯VLG相比,VLG-CDNPs显著提高了L6细胞的葡萄糖摄取(78.34% vs. 60.91%),并对α-淀粉酶和α-葡萄糖苷酶表现出中等抑制活性。
5、该研究结果表明,优化的VLG-CDNPs有望成为治疗糖尿病的有效且有前途的纳米制剂。
在糖尿病治疗中使用纳米颗粒给药有什么优势?
1、增强生物利用度:纳米颗粒能够改善药物的溶解性和吸收,特别是对于水溶性差的药物,如维达列汀(VLG)。通过包裹在生物相容性聚合物中,纳米颗粒可以提高药物在体内的生物利用度。
2、持续释放:纳米颗粒可以设计为实现药物的持续释放,减少给药频率,从而提高患者的依从性。这种释放机制有助于维持稳定的血药浓度,改善糖尿病的管理。
3、靶向递送:纳米颗粒可以通过表面修饰实现靶向递送,增强药物在特定组织或细胞中的积累,减少对健康组织的影响,降低副作用。
4、减少副作用:通过靶向递送和控制释放,纳米颗粒可以减少药物的系统性副作用,尤其是胃肠道不适等常见问题。
5、提高药物稳定性:纳米颗粒的制备和固化过程(如喷雾干燥)可以提高药物的化学稳定性,延长其储存寿命。
6、改善药物的细胞摄取:研究表明,纳米颗粒能够有效地被细胞摄取,增强药物在细胞内的作用,特别是在肌肉细胞中,提高葡萄糖摄取能力。
7、可扩展性和可重复性:微反应器技术的应用使得纳米颗粒的生产过程更加可控、可扩展,确保了制备的一致性和质量。
综上所述,纳米颗粒在糖尿病药物递送中展现出显著优势,能够改善治疗效果并提高患者的生活质量。
维达列汀(VLG)负载壳聚糖-硫酸葡聚糖纳米粒子(VLG-CDNPs)的制备过程主要包括以下几个步骤:
1、材料准备:首先,准备所需的材料,包括低分子量壳聚糖(CS)、硫酸葡聚糖(DEX)、维达列汀(VLG)以及稳定剂(如Tween 80)。
2、溶液制备:
将50 mg的壳聚糖溶解在0.5%的醋酸溶液中,并加入0.5%的Tween 80作为稳定剂,搅拌均匀。
将25 mg的维达列汀溶解在蒸馏水中,并逐滴加入到壳聚糖溶液中。
另制备一溶液,将1%(w/v)的硫酸葡聚糖溶解在蒸馏水中。
3、微反应器辅助制备:
使用微反应器进行纳米粒子的制备。将上述两种溶液通过注射器以恒定流速注入微反应器中,进行混合反应。
在反应过程中,保持600 rpm的搅拌以确保均匀混合。
4、纳米粒子形成:通过离心分离和过滤,获得的纳米悬浮液即为VLG-CDNPs。
5、优化制备参数:采用Box-Behnken设计(BBD)对制备过程进行优化,调整聚合物浓度、流速和稳定剂类型,以获得理想的粒径、分散性和包封效率。
6、喷雾干燥:将制备好的纳米粒子进行喷雾干燥,以提高其稳定性和再分散性,最终得到干燥的VLG-CDNPs粉末。
7、表征与评估:对制备的VLG-CDNPs进行物理化学特性表征,包括粒径、聚合度分散指数、包封效率、形态学分析等。同时,进行体外药物释放、细胞毒性和抗糖尿病活性等生物学评估。
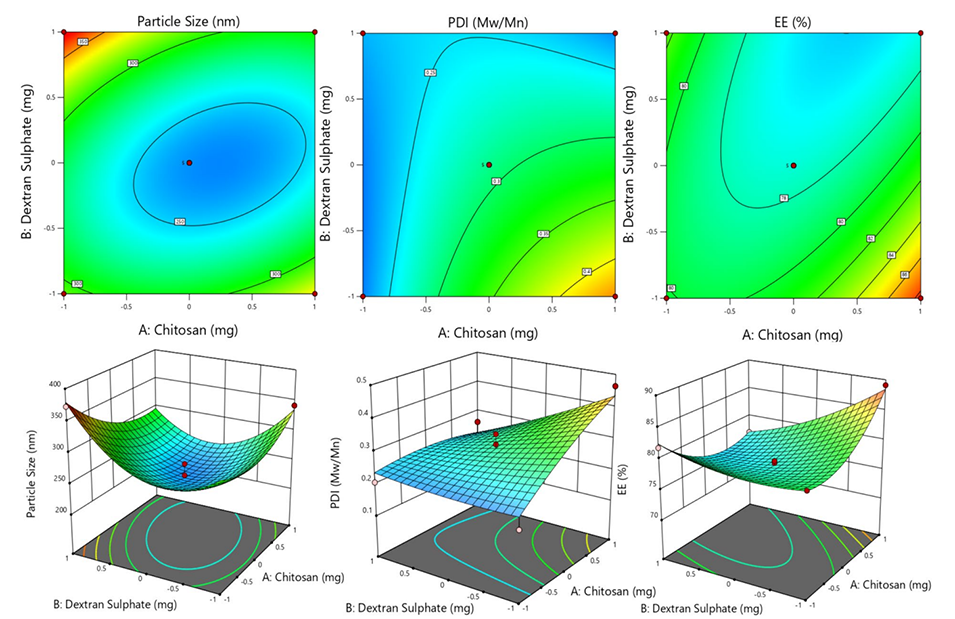
图1.使用Box-Behnken设计(BBD)优化VLG-CDNPs制剂,包含3D响应面图和2D轮廓图。这些图描绘了变量对粒径(A,A')、PDI(B,B')和包封率(C,C')的影响
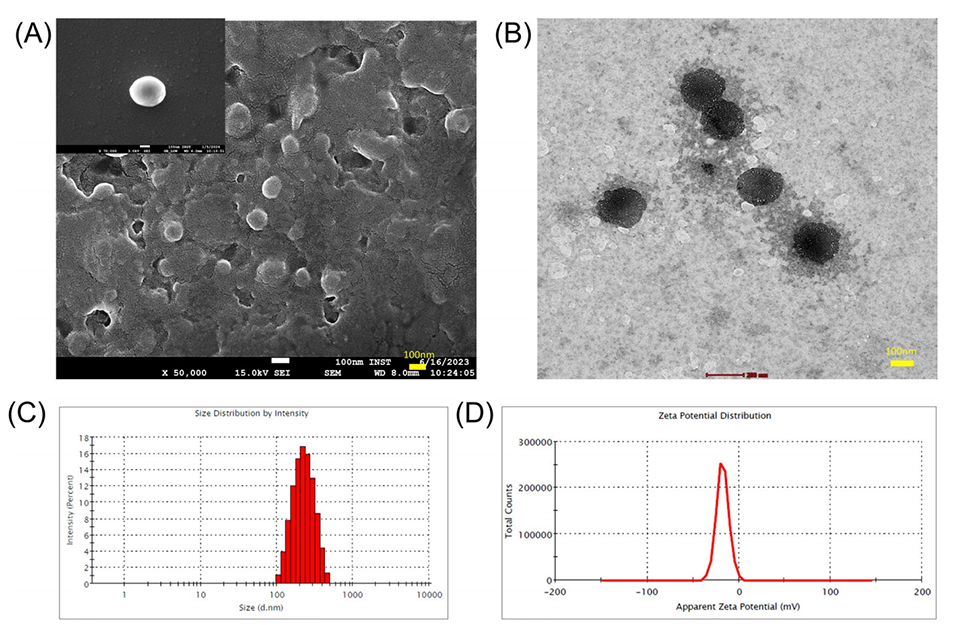
图2.VLG-CDNP制剂的制备和理化特性

图3.VLG-CDNPs干燥粉末的扫描电子显微镜(SEM)图像
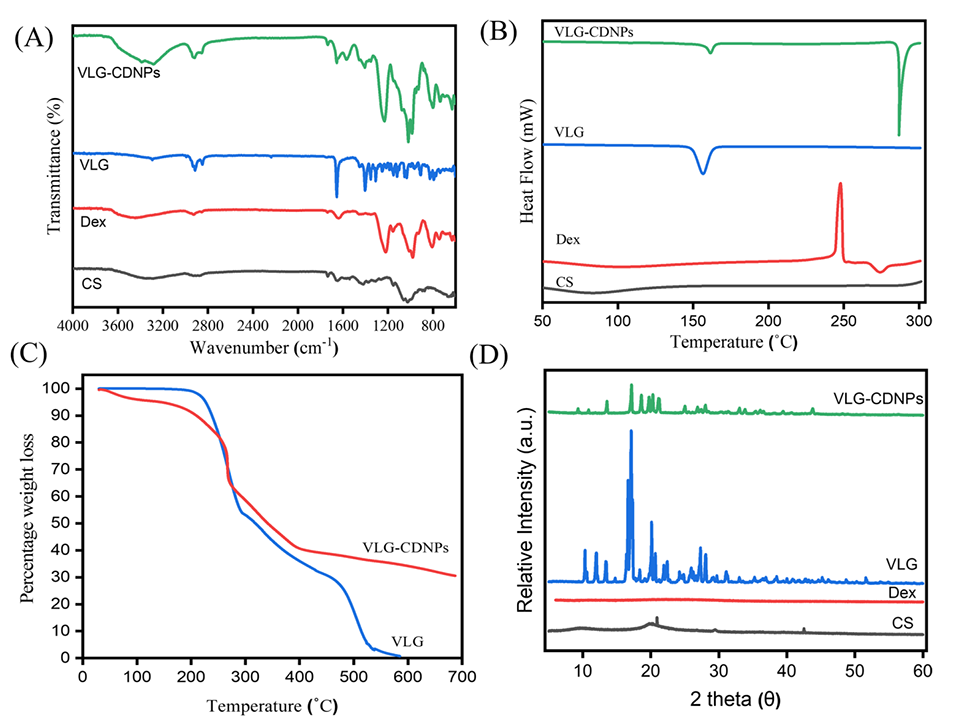
图4.纯VLG、CS、DEX和VLG-CDNPs制剂的固态表征。A)FTIR光谱、B)DSC热图、C)TGA热图和D)XRD图
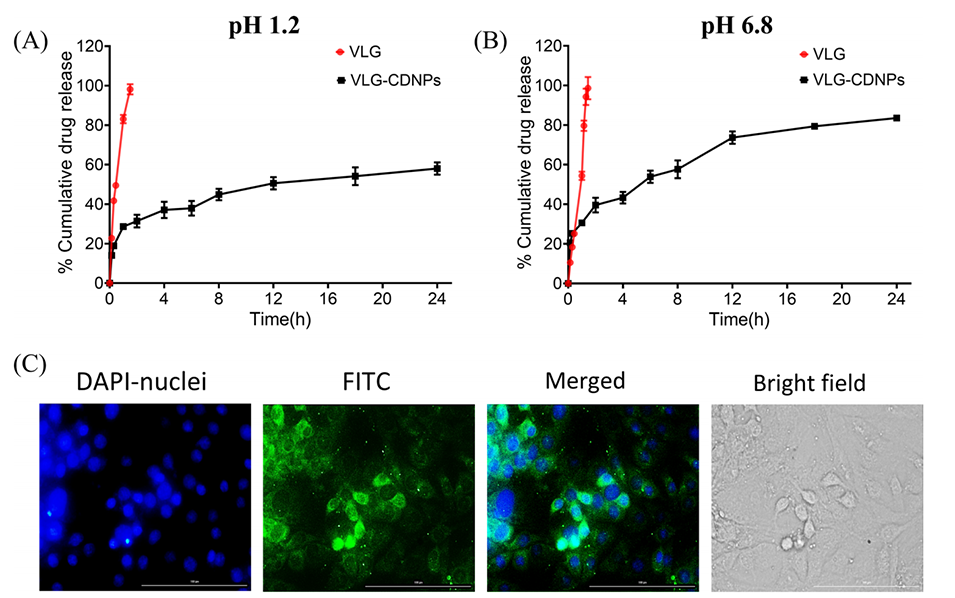
图5.(A,B)纯VLG和VLG-CDNPs制剂的体外药物释放曲线,(C)纳米颗粒的细胞摄取
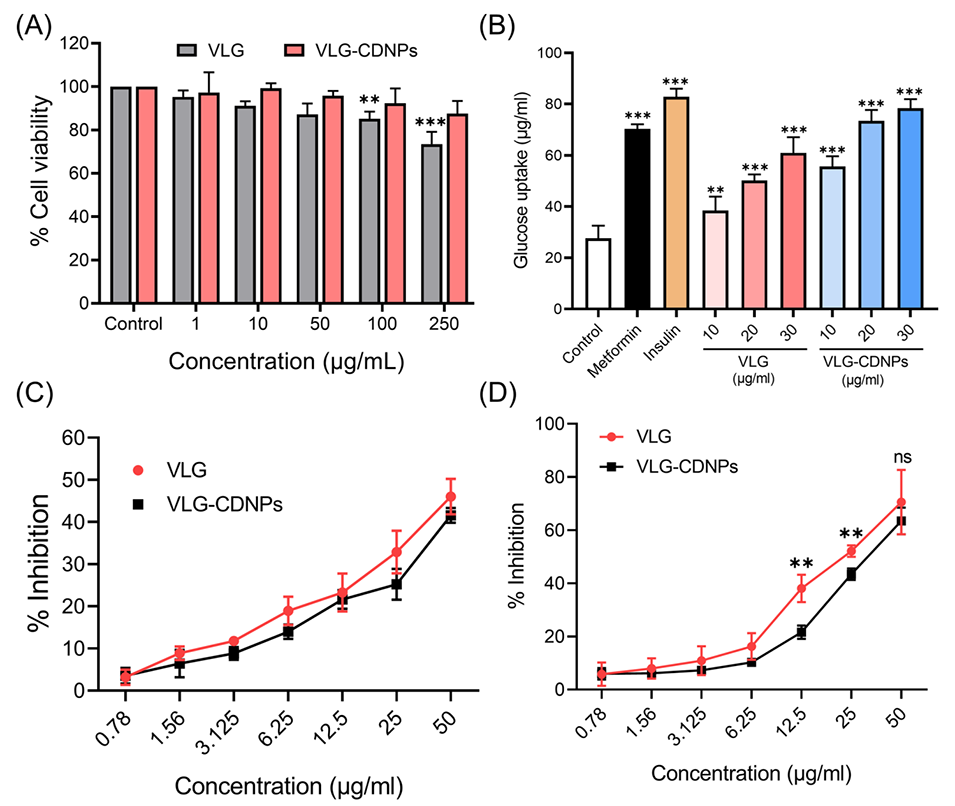
图6.A)用不同浓度的VLG及其制剂(VLG-CDNPs)处理24小时后的细胞存活率。B)L6细胞系的体外葡萄糖摄取研究。不同浓度的VLG和VLG-CDNPs对α-淀粉酶(C)和α-葡萄糖苷酶(D)酶活性的抑制百分比。数据以平均值±标准差表示(n=3)
论文链接:https://doi.org/10.1186/s43094-024-00736-9














